冷热水循环管管径流速
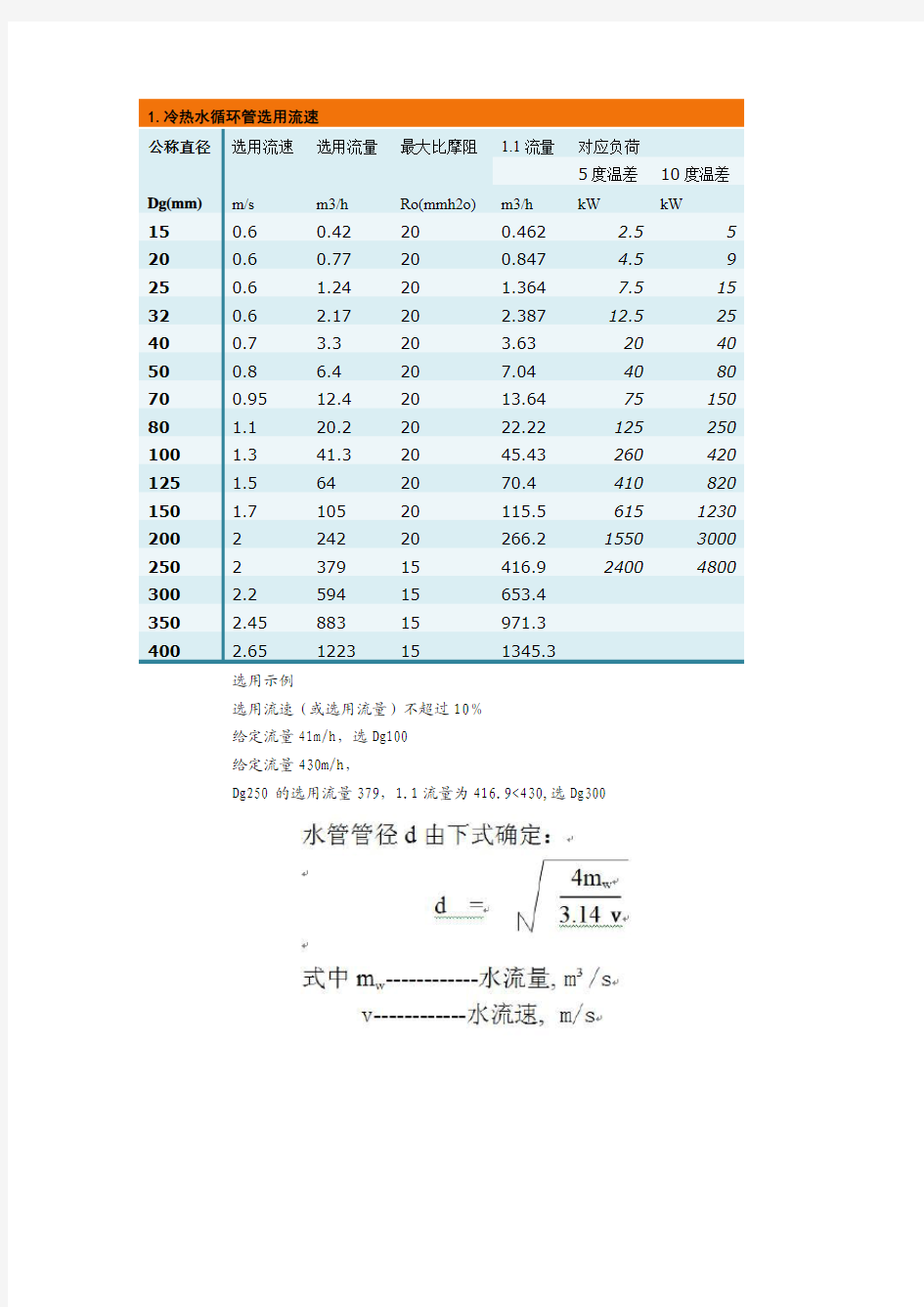
1.冷热水循环管选用流速
公称直径选用流速选用流量最大比摩阻 1.1流量对应负荷
5度温差10度温差Dg(mm)m/s m3/h Ro(mmh2o)m3/h kW kW 150.60.42200.462 2.55 200.60.77200.847 4.59 250.6 1.2420 1.3647.515 320.6 2.1720 2.38712.525 400.7 3.320 3.632040 500.8 6.4207.044080 700.9512.42013.6475150 80 1.120.22022.22125250 100 1.341.32045.43260420 125 1.5642070.4410820 150 1.710520115.56151230 200224220266.215503000 250237915416.924004800 300 2.259415653.4
350 2.4588315971.3
400 2.651223151345.3
选用示例
选用流速(或选用流量)不超过10%
给定流量41m/h,选Dg100
给定流量430m/h,
Dg250的选用流量379,1.1流量为416.9<430,选Dg300
循环水控制指标及解释
循环水水质控制指标及注释 1、PH:7。0—9.2 在25℃时pH=7.0得水为中性,故pH=7.0-9.2得水大体上属于中性或微碱性得范围;冷却水得腐蚀性随pH值得上升而下降;循环水得pH值低于这一范围时,水得腐蚀性将增加,造成设备得腐蚀;循环水得pH值高于这一范围时,则水得结垢倾向增大,容易引起换热器得结垢。 2、悬浮物:≤10mg/L 悬浮物会吸附水中得锌离子,降低锌离子在水中得浓度;一般情况下,循环冷却水得悬浮物浓度或浊度不应大于20mg/L,当使用板式、翅片管式或螺旋板式换热器时,悬浮物浓度或浊度不宜大于10mg/L。 3、含盐量:≤2500mg/L 含盐量也可通过电导率来间接表示,天然淡水得电导率通常在50-500μS/cm;电导率与含盐量大致成正比关系,其比值1μS/cm得电导率相当于0。55-0。90mg/L得含盐量;在含盐量高得水中,Cl-与SO42-得含量往往较高,因而水得腐蚀性较强;含盐量高得水中,如果Ca2+、Mg2+与HCO3-得含量较高,则水得结垢倾向较大;投加缓蚀剂、阻垢剂时,循环冷却水得含盐量一般不宜大于2500mg/L。 4、Ca2+离子:30≤X≤200mg/L 从腐蚀得角度瞧,软水虽不易结垢,但其腐蚀性较强,因此循环水中钙离子浓度不宜小于30mg/L;从结垢得角度瞧,钙离子就是循环水中最主要得成垢阳离子,因此循环水中钙离子浓度也不宜过高;在投加阻垢分散剂得情况下,钙离子浓度得高限不宜大于200mg/L。 5、Mg2+离子: 镁离子也就是冷却水中一种主要得成垢阳离子,循环水中镁离子浓度不宜大于60mg/L或2、5mmol/L(以Mg2+计);由于镁离子易与循环水中得硅酸根生成
工业循环水主要分析报告指标及方法
附页1 工业循环水主要分析方法 一、水质分析中标准溶液的配制和标定 (一)盐酸标准溶液的配制和标定 取9mL市售含HCl为37%、密度为1.19g/mL的分析纯盐酸溶液,用水稀释至1000mL,此溶液的浓度约为0.1mol/L。 准确称取于270~300℃灼烧至恒重的基准无水碳酸钠0.15g (准确至0.2mg),置于250mL锥形瓶中,加水约50mL,使之全部溶解。加1—2滴0.1%甲基橙指示剂,用0.lmol/L盐酸溶液滴定至由黄色变为橙色,剧烈振荡片刻,当橙色不变时,读取盐酸溶液消耗的体积。盐酸溶液的浓度为 c(HCl) = m×1000 / (V×53.00) mol/L 式中 m——碳酸钠的质量,g; V——滴定消耗的盐酸体积,ml; 53.00——1/2 Na2C03的摩尔质量,g/mol。 (二)EDTA标准溶液的配制和标定 称取分析纯EDTA(乙二胺四乙酸二钠)3.7g于250mL烧杯中,加水约150mL和两小片氢氧化钠,微热溶解后,转移至试剂瓶中,用水稀释至1000mL,摇匀。此溶液的浓度约为0.015mol/L。 (1)用碳酸钙标定EDTA溶液的浓度准确称取于110℃干燥至恒重的高纯碳酸钙0.6g(准确至0.2mg),置于250mL烧杯中,加水100mL,盖上表面皿,沿杯嘴加入l+1盐酸溶液10mL。加热煮沸至不再冒小气泡。冷至室温,用水冲洗表面皿和烧杯内壁,定量转移至250mL容量瓶中,用水稀释至刻度,摇匀。 移取上述溶液25.00mL于400mL烧杯中,加水约150mL,在搅拌下加入10mL 20%氢氧化钾溶液。使其pH>l2,加约10mg钙黄绿素—酚酞混合指示剂①,溶液呈现绿色荧光。立即用EDTA标准溶液滴定至绿色荧光消失并突变为紫红色时即为终点。记下消耗的EDTA溶液的体积。 (2)用锌或氧化锌标定EDTA溶液的浓度准确称取纯金属锌0.3g (或已于800℃灼烧至恒重的氧化锌0.38g),称准至0.2mg,放入250mL烧杯中,加水50mL,盖上表面皿,沿杯嘴加入10mL l+1盐酸溶液,微热。待全部溶解后,用水冲洗表面皿与烧杯内壁,冷却。转移入250mL容量瓶中,用水稀释至刻度,摇匀,备用。 用移液管移取上述溶液25.00mL于250mL锥形瓶中,加水100mL,加0.2%二甲酚橙指示剂溶液1~2滴,滴加20%六次甲基四胺溶液至呈现稳定红色,再过量5mL,加热至60℃左右,用EDTA溶液滴定至由红色突变为黄色时即为终点。记下EDTA溶液消耗的体积。 EDTA溶液的浓度用下式计算: c(EDTA) = m×1000 / (M×V×10) mol/L 式中 m——基准物质的质量,mg; M——基准物质的摩尔质量,g/mol,选用碳酸钙时为100.08,选用金属锌(或氧化锌)时为65.39(或81.39); V——滴定消耗的EDTA溶液体积,mL。 用EDTA滴定法测定水硬度时,习惯使用c (1/2 EDTA),这时 c(1/2 EDTA)=2c (EDTA) (三)硝酸银标准溶液的配制和标定 称取1.6g分析纯硝酸银,加水溶解并稀释至1000mL,贮于棕色瓶中。此溶液的浓度约为0.01mol/L。 准确称取0.6g已于500~600℃灼烧至恒重的优级纯氯化钠(准确至0.2mg)。加水溶解后,移至250mL 容量瓶中并稀释至刻度,摇匀。用移液管移取氯化钠溶液10.00mL于250mL锥形瓶中加水约100mL5%铬酸钾溶液lmL,用硝酸银溶液滴定至砖红色出现时即为终点。 记下硝酸银溶液的体积。 用100mL水作空白,记录空白消耗硝酸银溶液的体积。硝酸银溶液的浓度为 c(AgNO3) = m×1000 / [58.44×(V—V0 ) ×25] mol/L 式中 m——氯化钠的质量,g; 58.44——NaCl的摩尔质量,g/mol; V——滴定氯化钠溶液时消耗硝酸银的体积,mL; V0——滴定空白时消耗硝酸银的体积,mL。 ①1g钙黄绿素和1g酚酞与50g分析纯干燥的硝酸钾混合,磨细混匀。 (四)硝酸汞标准溶液的配制和标定
循环水控制指标及解释
循环水水质控制指标及注释 1、PH:7.0-9.2 在25℃时pH=7.0的水为中性,故pH=7.0-9.2的水大体上属于中性或微碱性的范围;冷却水的腐蚀性随pH值的上升而下降;循环水的pH值低于这一范围时,水的腐蚀性将增加,造成设备的腐蚀;循环水的pH值高于这一范围时,则水的结垢倾向增大,容易引起换热器的结垢。 2、悬浮物:≤10mg/L 悬浮物会吸附水中的锌离子,降低锌离子在水中的浓度;一般情况下,循环冷却水的悬浮物浓度或浊度不应大于20mg/L,当使用板式、翅片管式或螺旋板式换热器时,悬浮物浓度或浊度不宜大于10mg/L。 3、含盐量:≤2500mg/L 含盐量也可通过电导率来间接表示,天然淡水的电导率通常在50-500μS/cm;电导率与含盐量大致成正比关系,其比值1μS/cm的电导率相当于0.55-0.90mg/L的含盐量;在含盐量高的水中,Cl-和SO42-的含量往往较高,因而水的腐蚀性较强;含盐量高的水中,如果Ca2+、Mg2+和HCO3-的含量较高,则水的结垢倾向较大;投加缓蚀剂、阻垢剂时,循环冷却水的含盐量一般不宜大于2500mg/L。 4、Ca2+离子:30≤X≤200 mg/L 从腐蚀的角度看,软水虽不易结垢,但其腐蚀性较强,因此循环水中钙离子浓度不宜小于30mg/L;从结垢的角度看,钙离子是循环水中最主要的成垢阳离子,因此循环水中钙离子浓度也不宜过高;在投加阻垢分散剂的情况下,钙离子浓度的高限不宜大于200mg/L。 5、Mg2+离子: 镁离子也是冷却水中一种主要的成垢阳离子,循环水中镁离子浓度不宜大于60mg/L或2.5mmol/L(以Mg2+计);由于镁离子易与循环水中的硅酸根生成类似于蛇纹石组成的不易用酸除去的硅酸镁垢,故要求循环水中镁离子浓度遵从以下关系:[Mg2+](mg/L)*[SiO2](mg/L)<15000,式中[Mg2+]以CaCO3计,[SiO2]以SiO2计。
水循环知识点
自然界的水循环 1、水圈的概念:指地球上各种水体共同构成的一个连续但不规则的圈层 2、水的三种存在形式:液态水、气态水、固态水 3、水体分类(课本P54) 4.河流主要补给类型及特点
5、陆地水体间的相互补关系 ①陆地的各种水体最主要的补给来源是大气降水 ②河流水、湖泊水、地下水之间,存在着相互补给关系。相互补给关系主要看各种水位的高低,水位较高的水体可以补给给水位较低的水体。 ③三种水体的变化速度:河流水>湖泊水〉地下水 ④洪水期水位:河流水>湖泊水〉地下水 洪水期的补给关系:河流水补给湖泊水和地下水;湖泊水补给地下水
⑤ 枯水期水位:地下水>湖泊水〉河流水 枯水期的补给关系:地下水补给湖泊水和河流水;湖泊水补给河流水6.河流的特征 项目水文特征 描述方法影响因素 河流流量大小的变化 主要取决于河流补给 量与流域面积的大 对航运的影响 流量流量的大小 小。一般来讲,补给量 与流域面积越大, 河流流量越大;河流流 量的时间变化主要取 决于河流的补给方 水位 汛期 水位高低和季节变 化,汛期的时间及长 短 含沙量含沙量的大小 式。 包括丰水期、枯水期时 间,汛期长短等,主要 与补给方式和河道特征 有关。河流主要的补给 季节处于汛期,水位 高。河流流量相同的情 况下,河道的宽窄、深 浅影响水位的低与高。 与流域内的植被状况、 地形坡度、地面物质疏 松状况、植被覆盖及降 水强度等有关。 取决于冬季气温高 水量大,流量平稳,丰 水期长,无结冰期, 含 沙量少,对航运有利 结冰期结冰期的有无或长短低。有结冰期的河流, 从低纬流向高纬的河
★ 7、水循环类型(课本P55图) ①维持了全球水的动态平衡,使全球各种水体处于不断更新状态 ②使地表各圈层之间、海陆之间实现物质迁移和能量的交换 ③影响全球的气候和生态
循环水控制指标及解释
循环水水质控制指标及注释 1、PH:7、0-9、2 在25℃时pH=7、0的水为中性,故pH=7、0-9、2的水大体上属于中性或微碱性的范围;冷却水的腐蚀性随pH值的上升而下降;循环水的pH值低于这一范围时,水的腐蚀性将增加,造成设备的腐蚀;循环水的pH值高于这一范围时,则水的结垢倾向增大,容易引起换热器的结垢。 2、悬浮物:≤10mg/L 悬浮物会吸附水中的锌离子,降低锌离子在水中的浓度;一般情况下,循环冷却水的悬浮物浓度或浊度不应大于20mg/L,当使用板式、翅片管式或螺旋板式换热器时,悬浮物浓度或浊度不宜大于10mg/L。 3、含盐量:≤2500mg/L 含盐量也可通过电导率来间接表示,天然淡水的电导率通常在50-500μS/cm;电导率与含盐量大致成正比关系,其比值1μS/cm的电导率相当于0、55-0、90mg/L的含盐量;在含盐量高的水中,Cl-与SO42-的含量往往较高,因而水的腐蚀性较强;含盐量高的水中,如果Ca2+、Mg2+与HCO3-的含量较高,则水的结垢倾向较大;投加缓蚀剂、阻垢剂时,循环冷却水的含盐量一般不宜大于2500mg/L。 4、Ca2+离子:30≤X≤200 mg/L 从腐蚀的角度瞧,软水虽不易结垢,但其腐蚀性较强,因此循环水中钙离子浓度不宜小于30mg/L;从结垢的角度瞧,钙离子就是循环水中最主要的成垢阳离子,因此循环水中钙离子浓度也不宜过高;在投加阻垢分散剂的情况下,钙离子浓度的高限不宜大于200mg/L。 5、Mg2+离子: 镁离子也就是冷却水中一种主要的成垢阳离子,循环水中镁离子浓度不宜大于60mg/L或2、5mmol/L(以Mg2+计);由于镁离子易与循环水中的硅酸根生成类似于蛇纹石组成的不易用酸除去的硅酸镁垢,故要求循环水中镁离子浓度遵从以下
水循环教案
自然界的水循环 【教学目标】 一、知识与技能 1.记住水循环的重要环节,记住水循环的类型,通过水循环示意图得出水循环的定义 2.理解水循环的地理意义。 3.运用水循环的原理知识,分析常见的人类活动对水资源的影响。 二、过程与方法 1.通过水循环等知识的学习,使学生学会运用地理基本概念、原理分析评价地理问题。 2.播放水循环动画,让学生自主构建水循环的知识。 三、情感态度与价值观 1.培养学生学习地理兴趣和学习乐趣。 2.帮助学生树立正确认识和利用水循环的自然规律,实现人类与环境的和谐发展。 【教学重点】 水循环的类型、形成过程和地理意义。 【教学难点】 水循环的过程和地理意义。 【教学方法】 启发讲解法、讨论法、分析综合法等等。
【教学过程】 新课导入 展示黄河的图片,引出李白的诗《将进酒》其中有一句“黄河之水天上来,奔流到海不复回??”,指出诗中的错误,请学生跟着我一起学习第三章第一节水循环,一起来找出错误的原因。 新课讲授 板书 水循环 水循环的过程及类型自学探究:阅读课本的内容,思考下列问题:1.水循环联系了哪些圈层?2.水循环发生的空间领域有哪些?3.水循环的类型有哪些? 展示水循环示意图讲解: 请学生阅读后讨论?? 师:请同学们帮忙老师回答第一个问题。 生:水圈、大气圈、岩石圈、生物圈师:对了,水循环就是联系了水圈、大气圈、岩石圈以及生物圈。那么我们就可以知道了水循环的定义。 生:水循环是指自然界的水在水圈、大气圈、岩石圈、生物圈四大圈层中通过各个
环节连续运动的过程。 板书 一、水循环的定义 师:我们继续看水循环示意图回答第二个问题:水循环发生的空间领域有哪些? 生:海洋与陆地之间、陆地与陆地上空之间、海洋与海洋上空之间。师:对了,水循环就是分别在这些领域发生的,那么我们就可以将水循环分为三种类型,那么同学们知道是哪三种吗? 生:海陆间大循环、陆地内循环、海上内循环。 板书 二、水循环的类型 1.海陆间大循环 2.陆地内循环 3.海上内循环师:对了,看来同学们都非常认真地预习了,现在老师将给大家演示这三种循环分别是怎么进行的。 综合分析:通过三组动画分别演示各种水循环的演变过程。 第一组:海陆间大循环 师:海陆间大循环是最重要的一种循环运动,这运动的具体过程是:海洋表面的水在太阳辐射的作用下经过蒸发变成水汽,水汽上升到空中随着气流运行,被输送到大陆上空,其中一部分水汽在适当条件下凝结,形成降水。降落到地面的水,一部分沿地面流动,形成地表径流;一部分渗入地下,形成地下径流。二者经过江河汇集,最后又回到海洋。通过这种循环运动,陆地上的水就不断地得到补充,水资源得以再生。 第二组:陆地内循环
(完整版)高中地理水循环知识点总结
1、水循环的类型 海陆间循环:发生在海洋和陆地之间,是最重要的类型,又称大循环,使陆地水资源得到补充,水资源得以再生; 典型:长江参与了水循环的地表径流;夏季风参与了水循环的水汽输送;陆地内循环:发生在陆地和陆地上空,补给陆地水的水量很小; 典型:塔里木河流域的降水 海上内循环:发生在海洋和海洋上空,降水量很大 典型:未登陆的台风 2、水循环的意义:维持了全球水的动态平衡,使全球各水体处于不断更 新的状态;使地表各圈层之间、海陆之间实现物质迁移和能量的交换;影响全球的气候和生态;塑造了地表形态 3、影响水循环各环节的因素: 3.1、蒸发因素:光照、气温、风速、湿度、水域表面积 3.2、影响水汽输送带的因素:风(风带:信风带、西风带、极地东风带;季风:主要是夏季风);距离海的远近;地形的阻挡 3.3、影响降水的因素:充足的水汽、强烈上升的大气运动以及凝结核会形成降水 3.4、影响地表径流的因素: 3.5、影响下渗的因素3.6、影响地表径流的因素:考虑地表径流、下渗的因素,重点考虑喀斯特地貌:地下溶洞、地下河众多,储存大量地下水 4、人类活动对水循环的影响 4.1、正面的影响: ?修建水库,改变地表径流的季节分配,,减少洪水期径流量,增加枯水期径流量;同时水面面积的扩大和下渗量增大使地下水位提高,可加大蒸发量和降水量。 ?跨流域调水,改变地表径流的空间分布,也可以使蒸发量增加,大气中水汽增多,从而增加降水量 ?植树造林、保护湿地资源,起到涵养水源的作用,使下渗增多,减少地表径流。 ?城市铺设渗水砖,可减少地表径流,增加下渗,增大地下径流。 ?实施人工增雨,加大降水量。 4.2、负向影响 ?滥伐森林,破坏地表植被,会减少蒸腾,使空气中水汽减少,降水量减少;降雨时,下渗减少,大量地表径流汇聚,容易发生洪涝灾害。?围湖造田减少了湖泊自然蓄水量,削弱了其防洪抗旱能力,也减弱了湖泊水体对周围地区气候的调节作用。 ?城市路面硬化,增加地表径流,减少下渗,减小地下径流,地面蒸发量减少,易造成城市内涝。 ?河流上游地区过度引水灌溉,会导致下游水量减少,甚至出现断流; 对地下水的过量开采和使用,导致地下水位下降,会使有泉水出露的
循环水指标名词解释
循环水指标名词解释 浓缩倍数 浓缩倍数(cyclw of concentratin)循环冷却水中,由于蒸发而浓缩的物质含量与补充水中同一物质含量的比值,或指补充水量与排污水量的比值。 什么是浓缩倍数 在循环冷却水中,由于蒸发而浓缩的溶解固体与补充水中溶解固体的比值,或指补充水流量对排污水流量的比值。在实际测量中,通常为循环冷却水的电导率值与补充水的电导率之比。 提高冷却水的浓缩倍数的好处: ?提高冷却水的浓缩倍数,可以降低补充水的用量,节约水资源; ?提高冷却水的浓缩倍数,可以降低排污水量,从而减少对环境的污染和废水的处理量; ?提高冷却水的浓缩倍数,可以节约水处理剂的消耗量,从而降低冷却水处理的成本; 过多地提高冷却水的浓缩倍数的坏处: ?过多地提高冷却水的浓缩倍数,会使冷却水中的硬度、碱度太高,水的结垢倾向增大; ?过多地提高冷却水的浓缩倍数,会使冷却水中的腐蚀性离子的含量增加,水的腐蚀性增强,从而使腐蚀控制的难度增大; 因此,我们要保证冷却水的处理效果,必须控制好冷却水的浓缩倍数,通常,对于中央空调冷却水的浓缩倍数一般控制在4~5 为佳。 循环冷却水浓缩倍数关键是看水质是否结垢型 2006-10-14 08:16 循环冷却水浓缩倍数关键是看水质是否结垢型 作者:杜林琳; 摘要:针对循环水浓缩倍数低于集团公司指标的情况,进行了相关影响因素分析,依此提出了减少系统保有水量、增加热负荷、改造旁虑池、优化工艺管理及操作等改进措施,并对浓缩倍数提高后系统运行可能存在的问题及注意事项进行了讨论。 循环水浓缩倍数是反映和控制循环水系统运行的一个重要综合性指
标。提高循环水浓缩倍数不仅可以降低补充水量、节约水资源;降低排污水量、减少对环境的污染和废水处理量;还可以减少水处理剂及杀生剂的消耗量、降低水处理成本。 循环冷却水系统作为石油化工行业的一个总要组成部分,近几年来随着管理制度的不断完善;生产工艺技术的不断进步;水处理剂的不断改进、开发,集团公司对循环水质管理的要求也越来越高,特别是浓缩倍数N控制指标逐年提高。如下图示: 1 现状分析 我厂现共有五座循环水场,由于系统设计、处理能力、覆盖的生产装置、管理水平各异,因而各水场的水质差异较大。具体反映在浓缩倍数上详见表1。 表1 循环水场浓缩倍数统计表(2003年) 一循环水场 二循环水场 三循环水场 焦化水场 烷基化水场 浓缩倍数 (平均值) 2.88 3.35 2.63 3.24 2.16 浓缩倍数 合格率(%) 40.0 70.3 20.5 62.5 14.0 注:表中合格率统计均是以N≥3.00为计算依据
循环水控制指标及解释
循环水控制指标及解释Last revision on 21 December 2020
循环水水质控制指标及注释 1、PH:在25℃时pH=的水为中性,故pH=的水大体上属于中性或微碱性的范围;冷却水的腐蚀性随pH值的上升而下降;循环水的pH值低于这一范围时,水的腐蚀性将增加,造成设备的腐蚀;循环水的pH值高于这一范围时,则水的结垢倾向增大,容易引起换热器的结垢。 2、悬浮物:≤10mg/L 悬浮物会吸附水中的锌离子,降低锌离子在水中的浓度;一般情况下,循环冷却水的悬浮物浓度或浊度不应大于20mg/L,当使用板式、翅片管式或螺旋板式换热器时,悬浮物浓度或浊度不宜大于10mg/L。 3、含盐量:≤2500mg/L 含盐量也可通过电导率来间接表示,天然淡水的电导率通常在50-500μS/cm;电导率与含盐量大致成正比关系,其比值1μS/cm的电导率相当于的含盐量;在含盐量高的水中,Cl-和SO42-的含量往往较高,因而水的腐蚀性较强;含盐量高的水中,如果Ca2+、Mg2+和HCO3-的含量较高,则水的结垢倾向较大;投加缓蚀剂、阻垢剂时,循环冷却水的含盐量一般不宜大于2500mg/L。 4、Ca2+离子:30≤X≤200mg/L 从腐蚀的角度看,软水虽不易结垢,但其腐蚀性较强,因此循环水中钙离子浓度不宜小于30mg/L;从结垢的角度看,钙离子是循环水中最主要的成垢阳离子,因此循环水中钙离子浓度也不宜过高;在投加阻垢分散剂的情况下,钙离子浓度的高限不宜大于200mg/L。 5、Mg2+离子: 镁离子也是冷却水中一种主要的成垢阳离子,循环水中镁离子浓度不宜大于60mg/L 或L(以Mg2+计);由于镁离子易与循环水中的硅酸根生成类似于蛇纹石组成的不易用酸除去的硅酸镁垢,故要求循环水中镁离子浓度遵从以下关系:[Mg2+](mg/L)*[SiO2](mg/L)<15000,式中[Mg2+]以CaCO3计,[SiO2]以SiO2计。
水循环的过程教学设计
第三章地球上的水 第一节自然界的水循环 水循环的过程 一、教学目标 1.知识与技能 (1)记住水循环的重要环节,记住水循环的类型,通过水循环示意图得出水循环的定义(2)学会从地理图表、地理现象中获取有用信息。 (1)通过水循环等知识的学习,使学生学会使用地理基本概念、原理分析评价地理问题。 (2)播放水循环PPT动画,让学生自主构建水循环的知识。 3.情感态度与价值观 (1)培养学生学习地理兴趣和学习乐趣。 (2)协助学生树立准确理解和利用水循环的自然规律,实现人类与环境的和谐发展。二、教学重点和难点 (1)教学重点:水循环的类型、形成过程和环节。 (2)教学难点:水循环的过程。 三、教学方法 启发讲解法、讨论法、分析综合法、多媒体演示法等等。 四、教具:PPT课件、黑板、教科书 五、教学过程: 【新课导入】 展示黄河的图片,引出李白的诗《将进酒》其中有一句“黄河之水天上来,奔流到海不复回……”,指出诗中的错误,请学生跟着我一起学习第三章第一节自然界的水循环,一起来找出错误的原因。 【新课讲授】 【板书】第一节自然界的水循环 水循环的过程 【自学探究】阅读课本P59的内容,思考下列问题: 1、水循环联系了哪些圈层? 2、水循环发生的空间领域有哪些? 3、水循环的类型有哪些? 展示水循环示意图讲解:
请学生阅读后讨论…… 师:请同学们帮忙老师回答第一个问题。 生:水圈、大气圈、岩石圈、生物圈 师:对了,水循环就是联系了水圈、大气圈、岩石圈以及生物圈。那么我们就能够知道了水循环的定义。 生:水循环是指自然界的水在水圈、大气圈、岩石圈、生物圈四大圈层中通过各个环节连续运动的过程。 【板书】一、水循环的定义 师:我们继续看水循环示意图回答第二个问题:水循环发生的空间领域有哪些? 生:海洋与陆地之间、陆地与陆地上空之间、海洋与海洋上空之间。 师:对了,水循环就是分别在这些领域发生的,那么我们就能够将水循环分为三种类型,那么同学们知道是哪三种吗? 生:海陆间大循环、陆地内循环、海上内循环。 【板书】二、水循环的类型 1、海陆间大循环 2、陆地内循环 3、海上内循环 师:对了,看来同学们都非常认真地预习了,现在老师将给大家演示这三种循环分别是怎么实行的。 【综合分析】通过三组动画分别演示各种水循环的演变过程。 第一组:海陆间大循环 师:海陆间大循环是最重要的一种循环运动,这运动的具体过程是:海洋表面的水在太阳辐射的作用下经过蒸发变成水汽,水汽上升到空中随着气流运行,被输送到大陆上空,其中一部分水汽在适当条件下凝结,形成降水。降落到地面的水,一部分沿地面流动,形成地表径流;一部分渗入地下,形成地下径流。二者经过江河汇集,最后又回到海洋。通过这种循环运动,陆地上的水就持续地得到补充,水资源得以再生。 第二组:陆地内循环 师:陆地内循环就是在陆地和陆地上空之间发生的一种循环运动。降落到大路上的水,其中一部分或全部通过陆面、水面蒸发和植物蒸腾形成水汽,被气流带到上空,冷却凝结形成降水,仍降落到大路上,这就是陆地内循环。由陆地内循环运动而补给陆地水体的水量为数很少。第三组:海上内循环 师:海上内循环就是在海洋和海洋上空之间发生的一种循环运动。海面上的水蒸发形成水汽,
2021版新高考选考地理(湘教版)一轮复习教师用书:第12讲水循环
第12 讲水循环
1.陆地水体的相互补给关系 (1)水体存在有三种类型:海洋水、陆地水和大气水。陆地水体之间具有水源相互补给 的关 系。 (2)由图甲可知,存在相互补给关系的水体是河流水与湖泊水、河流水与地下水、湖泊 水与 地下水。 (3) 结合图甲及所学知识,说明河流的主要补给类型:雨水、季节性积雪融水、冰雪融 水、 地下水、湖泊水。 (4) 图乙中左图表示丰水 (填“丰水”或“枯水” )期河流水与地下水的补给关系, 流水补给地下水。 (5) 图乙中右图表示枯水 (填“丰水”或“枯水” )期河流水与地下水的补给关系, 下水补给河流水。 (6)各类水体的相互补给状况取决于水位高低和流量大小的动态变化。 2.自然界的水循环 (1) 主要环节:①⑧蒸发,②④降水,③水汽输送,⑤地表径流,⑥地下径流,⑦下渗, ⑨蒸腾。 (2) 图中表示海陆间循环的环节有①③④⑤⑥⑦,表示海上内循环的环节有①②,表示 陆地 内循环的环节有④⑧⑨。 (填序号 ) 此时河 此时地
(3)“黄河之水天上来,奔流到海不复回。”此诗句中体现了水循环的降水、地表径流 环节。 (4)人类活动对⑤ (填序号)环节影响最大,主要表现:改变时间分配规律——修建水库,改变空间分布规律——跨流域调水。 (5)简要说明水循环的意义 ①“维持” ——全球水的动态平衡。 ②“缓解” ——不同纬度热量收支不平衡的矛盾。 ③“联系” ——海陆间的主要纽带。 ④“塑造” ——地表形态。 微点1 水循环的动力和根本原因 驱动水循环的动力主要是太阳辐射能和水的重力能,水循环的根本原因是水的三态变化。 微点2 内、外流区的水循环 外流区域发生海陆间循环,又存在陆地内循环,但以海陆间循环为主;内流区域以陆地 内循环为主。 微点3 水循环类型的判定一看发生的领域:位于海洋上、陆地上还是海洋与陆地之间。 二看水循环的环节:海陆间循环的环节最多,陆地内循环比海上内循环多了植物蒸腾这一环节。 三看参与水量的多少:海上内循环参与水量最多,陆地内循环参与水量最少。 微点4 受人类影响最大的水循环环节 受人类活动影响最大的水循环环节是地表径流,主要表现为改变时间分配规律——修建 水库;改变空间分布规律——跨流域调水。 微点5 人类活动对下渗环节的影响 人类活动主要通过对地表的改造影响下渗,这其中包括有利和不利两个方面: (1)有利方面包括农业生产活动中的坡地改梯田、翻耕土壤以及植树造林等均可增加下 渗量。 (2)不利方面主要是毁林开荒、过度放牧等破坏地表植被的行为,使水分下渗量减少。 陆地水体的相互关系
常用流体流速选择
管道内流速常用值/(m/s) 管道内流速常用值/(m/s)流体种类应用场合管道种类平均流速备注水一般给水主压力管道2~3低压管道0.5~1泵进口0.5~2.0泵出口1.0~3.0工业用水离心泵压力管3~4离心泵吸水管DN250 1~2 DN250 1.5~2.5往复泵压力管1.5~2往复泵吸水管1给水管道内流速常用值/(m/s) 流体种类 水应用场合 一般给水 泵进口 泵出口 工业用水管道种类 主压力管道 低压管道 离心泵压力管 离心泵吸水管 往复泵压力管 往复泵吸水管 给水总管 排水管 冷却 凝结冷水管 热水管
凝结水泵吸收管凝结水泵出水管自流xx管 一般液体 高粘度液体低粘度粘度 50mt;">·sDN25 DN50 DN100 DN25 粘度 100 mt;">·sDN50 DN100 DN200 DN25 粘度 1000 mt;">·sDN50 DN100 DN200 气体低压 高压
压缩空气压气机烟道压气机进气管平均流速2~3 0.5~1 0.5~2.0 1.0~3.0 3~4 DN2501~2 DN2501.5~2.5 1.5~2 <1 1.5~3 0.5~1.0 1.5~ 2.5 1~1.5 0.5~1 1~2 0.1~0.3 1.5~3.0 0.5~0.9
1.0~1.6 0.3~0.6 0.5~0.7 0.7~1.0 1.2~1.6 0.1~0.2 0.16~0.25 0.25~0.35 0.35~0.55 10~20 8~15 2~7 ~1020~30MPa 备注 压气机输气管 一般情况 饱和蒸汽DN<50 DN>70 DN<100 锅炉、汽轮机
循环水水质控制指标及注释
序号项目控制指标注释 1 PH 7.0-9.2 在25℃时pH=7.0的水为中性,故pH=7.0-9.2的水大体上属于中性或微碱性的范围;冷却水的腐蚀性随pH 值的上升而下降;循环水的pH值低于这一范围时,水的腐蚀性将增加,造成设备的腐蚀;循环水的pH值高 于这一范围时,则水的结垢倾向增大,容易引起换热器的结垢。 2 悬浮物≤10mg/L 悬浮物会吸附水中的锌离子,降低锌离子在水中的浓度;一般情况下,循环冷却水的悬浮物浓度或浊度不应大 于20mg/L,当使用板式、翅片管式或螺旋板式换热器时,悬浮物浓度或浊度不宜大于10mg/L。 3 含盐量≤2500mg/L 含盐量也可通过电导率来间接表示,天然淡水的电导率通常在50-500μS/cm;电导率与含盐量大致成正比关 系,其比值1μS/cm的电导率相当于0.55-0.90mg/L的 含盐量;在含盐量高的水中,Cl-和SO42-的含量往往较高,因而水的腐蚀性较强;含盐量高的水中,如果Ca2+、 Mg2+和HCO3-的含量较高,则水的结垢倾向较大;投加缓蚀剂、阻垢剂时,循环冷却水的含盐量一般不宜大
于2500mg/L。 4 Ca2+离 子30≤X≤200mg/L 从腐蚀的角度看,软水虽不易结垢,但其腐蚀性较强,因此循环水中钙离子浓度不宜小于30mg/L;从结垢的角度看,钙离子是循环水中最主要的成垢阳离子,因此循环水中钙离子浓度也不宜过高;在投加阻垢分散剂的 情况下,钙离子浓度的高限不宜大于200mg/L。 5 Mg2+离 子镁离子也是冷却水中一种主要的成垢阳离子,循环水中镁离子浓度不宜大于60mg/L或2.5mmol/L(以Mg2+计);由于镁离子易与循环水中的硅酸根生成类似于蛇纹石组成的不易用酸除去的硅酸镁垢,故要求循环水中镁离子浓度遵从以下关 系:[Mg2+](mg/L)*[SiO2](mg/L)<15000式中[Mg2+ ]以CaCO3计,[SiO2]以SiO2计 6 铜离子浓 度 0.1mg/L 循环水中的铜离子会引起钢和铝的局部腐蚀,因此循环水中的铜离子浓度不宜大于0.1mg/L。 7 铝离子浓≤0.5mg/L 天然水中铝离子的含量较低,循环水中的铝离子往往是由于补充水在澄清过程中添加铝盐作混凝剂而带入的;
详细说明游泳池水循环方式—逆流式
莱特莱德泳池景观水处理公司 https://www.360docs.net/doc/0511492162.html, 详细说明游泳池水循环方式—逆流式 游泳池的全部循环水量经设在池底的给水口或给水槽送入游泳池内,池水回水经池壁溢流堰溢流进入设在紧邻池壁外侧的溢流回水槽,溢流回水通过设在槽底的溢流回水口,汇入回水管,重力流入均衡水池;循环水泵从均衡池吸水送入过滤器去除回水中的杂质,降低回水的浑浊度,并对虑后循环水进行加热,水质平衡和消毒等处理后,再由池底给水口或给水槽送回游泳池继续使用的一种水流组织方式。 逆流式游泳池水循环方式特点: ①能有效去除集聚在池水表面脏污杂质,能满足将净化过的水送到游泳池的每个部位和从它的表面排除受污染最严重的表面水75%~80%的水量; ②池底均匀布置给水口能满足池内水流均匀,防止出现涡流、短流和死水区等现象; ③能均匀有效地使被净化处理的洁净水有序交换,更新池内尚未进行再次净化处理的水,提高池水净化处理效果; ④保证不同水层、不同部位的池内水质(洁净度、消毒余量、PH值和水温等)均匀; ⑤池底沉积污染物质极少。 因此,竞赛游泳池、训练游泳池、高档宾馆和俱乐部(会所)游泳池宜采用逆流式游泳池水循环方式。但这种循环方式建设费用较高,管道施工安装和维护较困难。 1. 池底给水口型如图所示。这种泳池水循环处理方式在我国目前采用比较普遍。 池底给水口型循环示意图 2. 池底给水槽如图所示。 池底给水槽型循环示意图 3. 池底端壁给水型如图所示。这种形式是从深水端靠近池底处的端壁上的给水口向池内进水,由浅水端的溢水槽回水,可以适应浅水端游泳人数多、池水受污染较严重的状况,对于尽快去除地面漂浮污染杂质较有效。适宜短池(池长L≦25m)采用。这种形式在国内使用实例较少,据资料介绍,在欧美国家有采用实例。 莱特莱德泳池景观水处理公司 https://www.360docs.net/doc/0511492162.html,
管道流速常用值
1. 生活给水管道流速:摘自《建筑给排水设计规范》GB 50015-2003 3.6.9 生活给水管道的水流速度,宜按表3.6.9采用。。 表3。6。9 生活给水管道的水流速度 (也是参考5.5.8规定。) 表5.5.8 水管道的流速 以下摘自教科书《建筑给水排水工程》,考虑到经济流速因素,设计时给水管道流速应控制在正常范围内: 生活或生产给水管道,不宜大于2.0m/s,当防噪声要求,且管径不大于25mm时,流速可采用0.8~1.0m/s; 消火栓系统,消防给水管道,不宜大于2.5m/s; 自动喷水灭火系统给水管道,不宜大于5.0m/s,但其配水只管在个别情况下,可控制在10 m/s以内。 2. 室外消防给水管流速:摘自《石油化工企业设计防火规范》GB 50160—92 第7.3.14条工艺装置区或罐区的消防给水干管的管径,应经计算确定,但不宜小于200mm。独立的消防给水管道的流速,不宜大于5m/s。 3.自动喷水灭火系统给水管流速: 摘自《自动喷水灭火系统设计规范》GB GB 50084—2001 9. 2 管道水力计算 9. 2. 1 管道内的水流速度宜采用经济流速,必要时可超过5m/s,但不应大于10m/s。9. 2. 1条文说明:采用经济流速是给水系统设计的基础要素,本条在原规范第7.1.3条基础上调整为宜采用经济流速,必要时可采用较高流速的规定。采用较高的管道流速,不利
于均衡系统管道的水力特性并加大能耗;为降低管道摩阻而放大管径、采用低流速的后果,将导致管道重量的增加,使设计的经济性能降低。 原规范中关于“管道内水流速度可以超过5m/s,但不应大于10m/s”的规定.是参考下述资料提出的: 我国《给排水设计手册》(第三册)建议,管内水的平均流速,钢管允许不大于5m/s;铸铁管为3m/s。 4. 给水水泵房: 1.消防水池补给水管流速:摘自《建筑设计防火规范》GB 50016-2006第8.6.2条第2点: 2 补水量应经计算确定,且补水管的设计流速不宜大于2.5m/s; 2. 给水泵进出水管流速:摘自《室外给水规范GB 50013-2006》: 6.3.1 水泵吸管及出水管的流速,宜采用下列数值; 1 吸水管 直径小于250mm时,为1.0~1.2m/s; 直径在250~1000mm时,为1.2~1.6m/s; 直径大于1000mm时,为1.5~2.0m/s。 2 出水管: 直径小于250mm时,为1.5~2.0m/s。 直径在250~1000mm时,为2.0~2.5m/s; 直径大于1000mm时,为2.0~3.0m/s。 5. 排水水泵房: 排水泵进出水管流速:摘自《室外排水设计规范》GB 50014-2006 5.4.4水泵吸水管设计流速宜为0.7~1.5m/s。出水管流速宜为0.8~2.5m/s。 6. 排水管流速:摘自《室外排水设计规范》GB 50014-2006 (采用重力自流时) 4.2.5排水管道的最大设计流速,宜符合下列规定:
循环水浓缩倍数的计算
1xx温度对冷水机组制冷量的影响 我们都知遭: 从运行费来讲,在蒸发温度和压缩机转数一定的情况下,冷凝温度越低,制冷系数越大,耗电量就越小。据测算,冷凝温度每增加1℃,单位制冷量的耗功率约增加3%-4%.所以,从这一角度来讲,保持冷凝温度稳定对提高冷水机组的制冷量是有益的。但为达到此目的,需采取以下措施: 增加冷凝器的换热面积和冷却水的水量;或提高冷凝器的传热系数,但是,对于一个空调冷却系统来说,增加冷凝器的面积几乎是不可能的。增加冷却水的水量势必增加水在冷凝器内的流速,这将影响制冷机的寿命,同时还增加了冷却水泵的耗电和管材浪费等一系列问题,而且效果也不尽理想。增大冷却塔的型号,考虑一定量的富余系数尚可,但如果盲目加大冷却塔的型号,以追求降低冷却水温也是得不偿失的,而且,冷却水温度还受当地气象参数的限制。提高冷凝器冷却水侧的放热系数,是实际和有效的,而提高放热系的有效途径是减小水侧的污垢热阻,对冷却水补水进行有效的处理. 2xx的补水问题 xx水量损失,包括三部分: 蒸发损失,风吹损失和排污损失,即: Qm=Qe+ Qw+Qb 式中: Qm为冷却塔水量损失;Qe为燕发水量损失;Qw为风吹量损失;Qb为排污水量损失。 (1)蒸发损失 Qe= (0.001+0.002θ)Δt Q (1) 式中:
Qe为蒸发损失量;Δt为冷却塔进出水温度差;Q为循环水量;θ为空气的干球温度。 (2)风吹损失水量 对于有除水器的机械通风冷却塔,风吹损失量为 Qw=(0.2%~0.3%)Q (2) (3)排污和渗漏损失 该损失是比较机动的一项,它与循环冷却水质要求、处理方法、补充水的水质及循环水的浓缩倍数有关.浓缩倍数的计算公式: N =Cr/Cm 式中: N为浓缩倍数;Cr为循环冷却水的含盐量;Cm为补充水的含盐量.根据循环冷却水系统的含盐量平衡,补充水带进系统的含盐最应等于排污,风吹和渗偏水中所带走的含盐量. QmCm= (Qw+Qb)Cr N =Cr/Cm=Qm/(Qw+Qb)=( Qe+ Qw+Qb)/( Qw+Qb) =Qm/Qb(Q w可忽略)( (3)Qm= QeN/(N 一1) N=1+Q e/Q w+Q b(Q
循环水预膜方案
循环水预膜方案 在敞开式循环冷却水系统里,循环冷却水长时间地反复使用,并在冷却塔与空气充分接触,进行物质和热量的传递。使空气中的氧能较好地溶在水中,直到水中的氧接近平恒溶解度。循环水经过换热设备,由于吸收热量,温度升高,降低了氧的溶解度。使水中的溶解氧在局部地区达到饱和,造成溶解氧的去极化作用而使设备腐蚀。经过凉水塔的循环水与含二氧化碳较低的空气接触,水中的CO2被空气抽提而逸入空气中,使水中的重碳酸盐类几乎全部转变为碳酸盐类,使生成碳酸盐垢的趋势增强。随着浓缩倍数的提高,水中溶解固体及杂质将不断浓缩积聚,改变了水的PH、浊度、硬度、碱度等,使循环水的腐蚀性与结垢性并存,且日趋严重。循环水中含盐类和杂质较高,空气中的灰沙土里,还有大量的微生物和它的孢子,而且循环水的温度(32~420C),冷却塔内的光照,充足的氧和养份均有利于菌藻滋生,使微生物及粘泥增加,由于循环水排污比率很小,所以使粘泥和悬浮物大量浓缩,容易在换热器上形成沉积,造成危害。污垢附着在设备上,既增加结垢,又加剧腐蚀,危害很大。 河南龙宇煤化工有限公司50万吨甲醇系统停车检修,由于系统检修时可能存在诸如焊条渣等杂物,设备表面存在大量的粘泥、杂质等,正常运行之前,必须将其除去,这样才能给预膜造就一个良好而光洁的金属表面。 一、循环冷却水系统水量平衡参数: 该循环水系统的进水温度为320C,回水温度为420C,进出口温差为△T=100C。根据热力学及物料平衡原理,系统水量平衡参数如下: 参数数据 循环水量(Q) m3/h 42000 排污水量(B) m3/h 500 蒸发水量(E) m3/h 600 风吹及泄漏损失水量(L)m3/h 100 补充水量(M) m3/h 1200 系统贮水量(V) m3 16000 浓缩倍数(N) 1.5--2.5 循环率(A) % 96.9 二、系统补充水水质全分析见下表: 序号分析项目单位结果序号分析项目单位结果 1 PH值 7.69 10 Mg2+ mg/L 98.45 2 浊度 NTU 4.2 11 Cl- mg/L 235.38 3 电导率 us/cm 5640 12 Si02 mg/L 4.35 4 酚酞碱度 mmol/L 0 13 总溶固 mg/L 2556 5 总碱度 mmol/L 3.61 14 总铁 mg/L 0.83 6 总硬度 mmol/L 10.84 15 总磷 mg/L 0.04 7 Ca2+ mg/L 284.62 16 SO42+ mg/L 1864.3 8 Na+ mg/L 0.96 17 HN4+?N mg/L 12.37 9 K+ mg/L 0.45 18 A13+ mg/L 0.29 三、组织分工 1、给排水车间:
循环水蒸发量计算
我国是一个水资源十分贫乏的国家,一些地区水资源已成为制约经济发展的主要因素之一,节约用水成了一个社会发展所必须面对的问题。火力发电厂是一个耗水大户,其中循环水冷却塔的耗水量约占整个电厂耗水量的60%以上。因此,冷却塔耗水量的变化对整个电厂耗水量有着较明显的影响。那么哪些因素影响冷却塔的耗水量,又是如何影响的呢?下面以一台300MW火电机组为实例具体分析一下其变化的内在规律,以期获得对火电厂节水工作有益的结论。 1.计算所需数据:(机组在300MW工况下) 冷却塔循环水量36000t/h? ?? ?? ?? ?? ?? ?? ?? ? 循环水温升9.51℃ 凝汽器循环水进水温度20℃? ?? ?? ?? ?? ?? ?? ? 空气湿度61% 循环冷却塔的端差5℃(端差为冷却塔循环水出水温度与大气湿球温度之差) 循环水浓缩倍率3.0 2.影响冷却塔耗水量因素分析: 火力发电厂循环水冷却系统运行中,维持系统正常稳定运行的关键是两个平衡,即:水量平衡和盐量平衡。二者相互联系,如果其中一个平衡变化,那么另一个平衡也会随之发生相应变化。 2.1循环水的水量平衡: 水量平衡过程是:机组运行过程中,对于敞开式循环冷却水系统来说,水的损失有蒸发损失、风吹损失、排污损失、漏泄损失(由于量较小,一般可略去不计)等,要维持水量平衡就需要同时对系统进行补水。 循环水系统的水量平衡数学表达式为:PBu =P1+ P2+ P3 [1]公式1 PBu:补充水量占循环水量的百分率,% P1:蒸发损失水量占循环水量的百分率,% P2:风吹损失占循环水量的百分率,% P3:排污损失占循环水量的百分率,% 在以上平衡中通常P1所占的份额较大,而它的大小主要取决于凝汽器的热负荷,以及气候条件(主要是温度因
循环水分析 全套标准
循环水分析 1、碱度的测定 1.1分析原理 用硫酸标准滴定溶液,滴定水中所有能和酸反应的所有物质。以酚酞或甲基橙为指示剂进行滴定,根据酸的浓度及消耗体积进行碱度的计算。 1.2试剂 1.2.1 酚酞指示液1%; 1.2.2 甲基橙指示液0.1%; 1.2.3 硫酸标准滴定溶液 C(1/2H 2SO 4 )= 0.05 mol/L。 1.3 分析步骤 量取100ml透明水样,注入三角瓶中。加入2~3滴酚酞指示液,此时溶液若显红色,则用0.1000mol/L或0.0100mol/L(脱盐水或冷凝水用0.0100mol/L)硫酸标准溶液滴定至恰好为无色,记录消耗酸量V1,在三角瓶中再加入2滴甲基橙指示液,继续用硫酸标准溶液滴定至橙红色为止,记录消耗的总体积数V2。 如果加酚酞后不显色,可直接加甲基橙指示液用硫酸标准溶液滴定,记录消耗酸量V2。 1.4 结果计算 酚酞碱度(mmol/L)JD 酚 =C× V1×10 (1) 总碱度JD(mmol/L) 甲 =C× V2×10 (2) 式中: C -硫酸标准溶液的浓度,mol/L; V 1 -以酚酞为指示剂时消耗酸的体积,mL; V 2 -以甲基橙为指示剂时消耗的总体积数,mL。 1.5 注意事项 1.5.1 总碱度即为甲基橙碱度。 1.5.2 在用此方法区分水中的重碳酸盐、碳酸盐、氢氧化物时,水中不能有其它有机酸或弱无机酸盐。
2 硬度的测定 2.1测定原理 水中的钙镁离子在pH值为10的条件下, 2.2试剂和溶液 0.01mol/L EDTA标准溶液(高硬度用) 0.005mol/L EDTA标准溶液(低硬度用) 氨-氯化铵缓冲溶液 硼砂缓冲溶液 0.5%铬黑T指示液(乙醇溶液) 酸性铬兰K指示剂:5g/l 。 2.2分析步骤 量取100ml透明水样注入250ml三角瓶中,加入5ml氨-氯化铵缓冲溶液和2滴铬黑T指示液(脱盐水加1ml硼砂缓冲溶液,2-3滴酸性格兰K)。在不断的摇动下,用0.01mol/L(或0.005mol/L)EDTA标准溶液滴定至蓝色,即为终点。同时做空白。 2.3结果计算 C(V1-V0)×1000 YD(mmol/L)= v 式中C-EDTA标准溶液的浓度,mol/L -消耗EDTA标准溶液的体积,ml V 1 V-水样的体积,ml 3氯离子含量的测定 3.1试剂和溶液 硝酸银标准滴定溶液0.01mol/L 50g/L铬酸钾溶液 10g/L酚酞指示液 2g/L氢氧化钠溶液
