分离工程作业
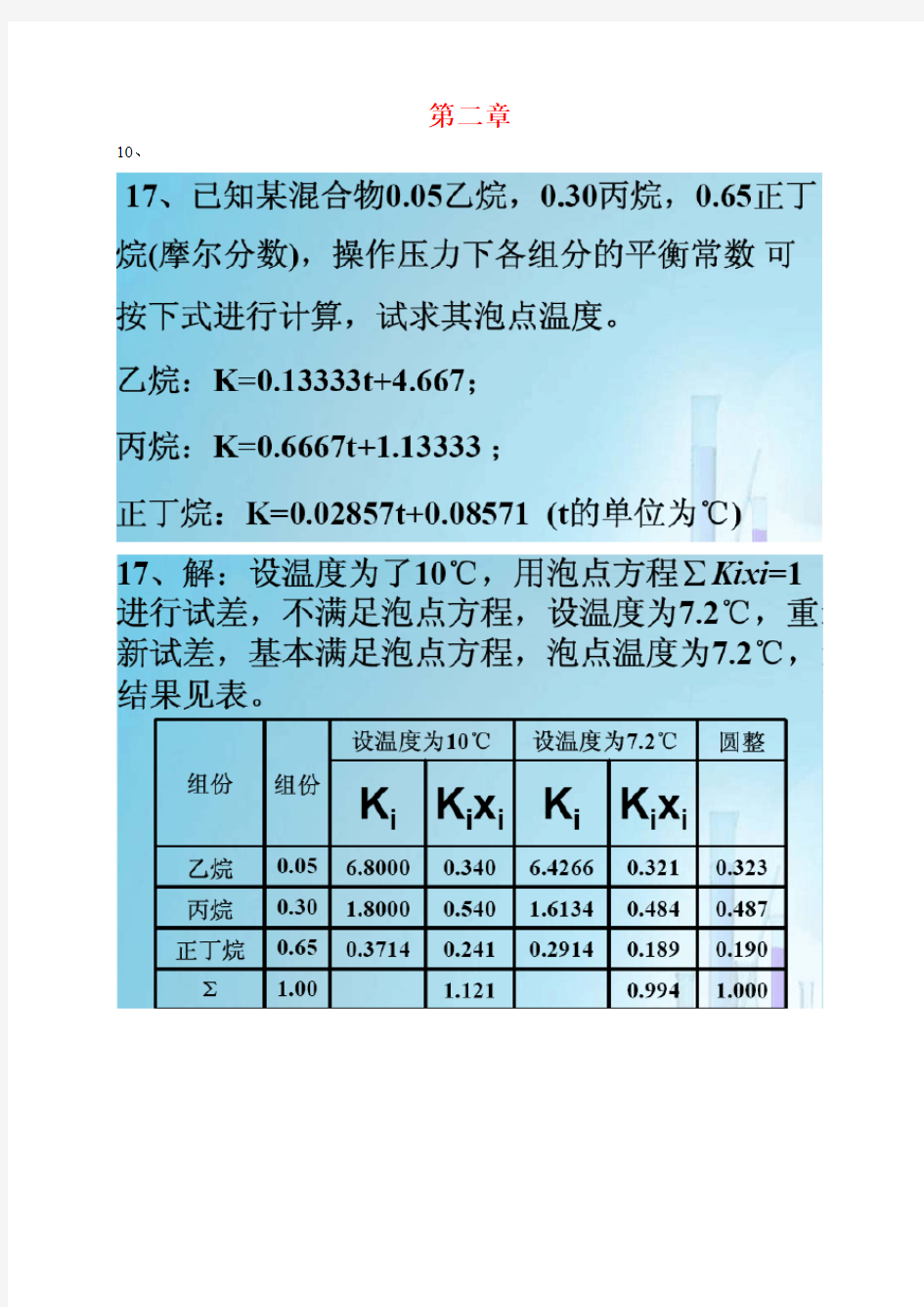
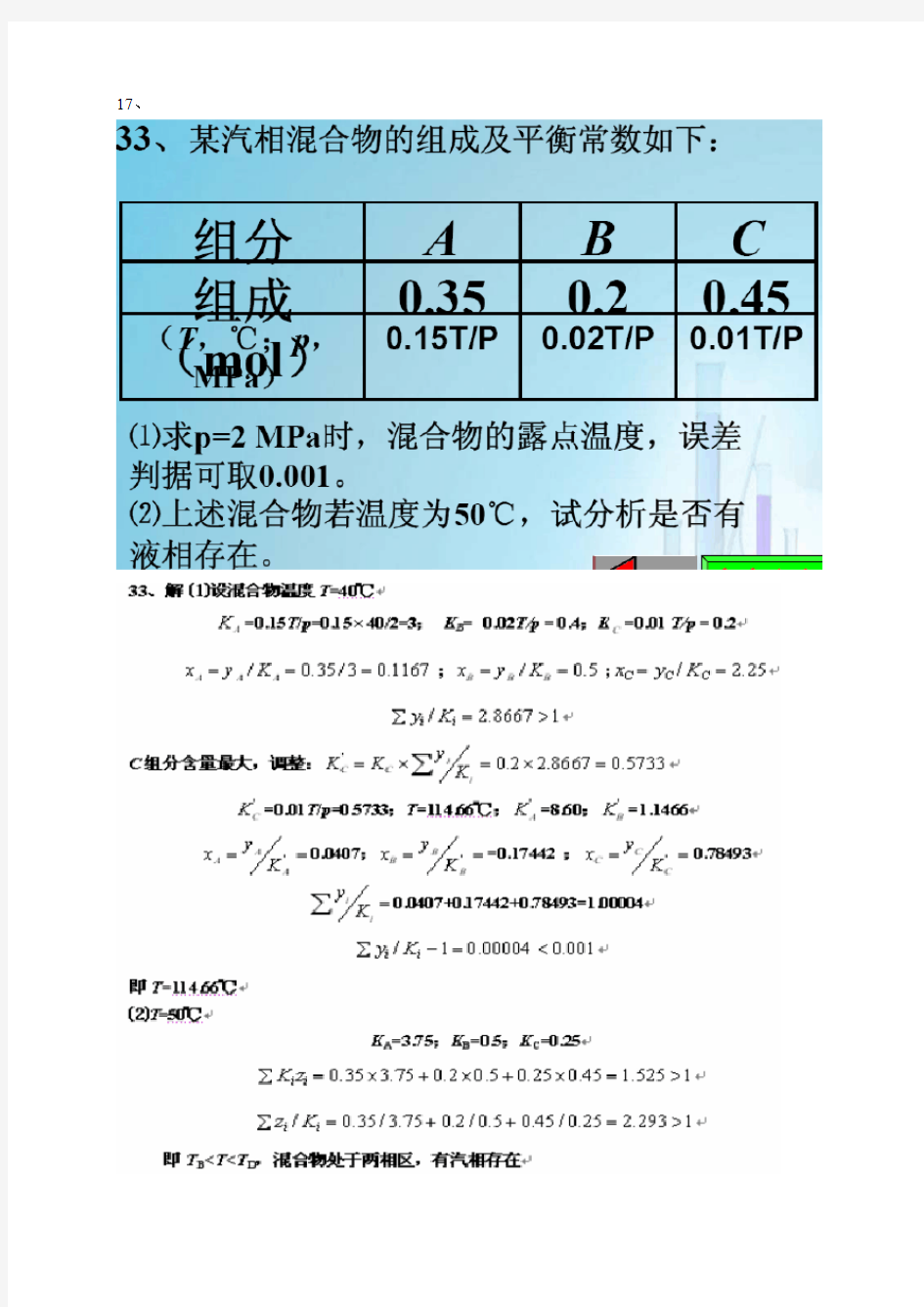
第二章10、
第三章1、
13、
17、某1、2两组分构成二元系,活度系数方程为
,,端值常数与温度的关系:A=1.7884-4.25×10221ln Ax =γ2
12ln Ax =γ-3T (T ,K) 蒸汽压方程为
T P S 4050
0826.16ln 1?
=
T P S 4050
3526.16ln 2?
= (P :kPa :T :K)
假设汽相是理想气体,试问99.75Kpa 时①系统是否形成共沸物?②共沸温度是多少? 解:设T 为350K 则A=1.7884-4.25×10-3×350=1.7884-1.4875=0.3009
3504050
0826.16ln 1?
=S P ;∴S
P 1=91.0284 kPa
3504050
3526.16ln 2?
=S P ;=119.2439 kPa
S
P 2 因为在恒沸点
由1221112==S S
P P γγα得S
S P P 1221=γγ
∴)()(121222121
2121ln ln ln ln x A x x A P P S S ?=?=?==γγγγ
)
(1213009.02439.1190284
.91ln
x ?= 解得:=
0.9487 =0.0513
1
x 2x ∴2
10513.03009.0ln ×=γ;1γ=1.0008 229487.03009.0ln ×=γ;2γ=1.3110
P==1.0008×0.9487∑S
i i i P x γ×91.0284+1.3110×0.0513×119.2439 =95.069275.99≠ kPa
设T 为340K
则A=1.7884-4.25×10-3×340=0.3434
3404050
0826.16ln 1?
=S P ;=64.7695 kPa S
P 13404050
3526.16ln 2?
=S P ;=84.8458 kPa
S
P 2由)(12121ln x A P P
S S ?=;)(1213434.08458.847695.64ln x ?=
解得:=0.8931 =1-0.8931=0.1069
1x 2x ∴2
11069.03434.0ln ×=γ;1γ=1.0039 228931.03434.0ln ×=γ;2γ=1.3151
P==1.00390.8931∑S
i i i P x γ××64.7695+1.3151×0.1069×84.8458 =69.999275.99≠ kPa 设T 为352K
则A=1.7884-4.25×10-3×352=0.2924
3524050
0826.16ln 1?
=S P ;=97.2143 kPa S
P 13524050
3526.16ln 2?
=S P ;=127.3473 kPa
S
P 2由)(12121ln x A P P
S S ?=;)(1212924.03473.1272143.97ln x ?=
∴1x =0.9617 =1-0.9617=0.0383
2x ∴2
10383.02924.0ln ×=γ;1γ=1.0004 229617.02924.0ln ×=γ;2γ=1.3105
P==1.00040.9617∑S
i i i P x γ××97.2143+1.3105×0.0383×127.3473 =99.920275.99≈ kPa
说明系统形成共沸物,其共沸温度为352K 。
判断Q
31
.16738
.7513
.991
2==S S
P
P ,而1γ=1.313,2γ=1.002
2
12
1γγ>>S
S P P ,且,
S
S P P P 21,>∴∴ 故形成最低沸点恒沸物,恒沸物温度为352K 。
18、在101.3Kpa 压力下氯仿(1)-甲醇(2)系统的NRTL 参数为: 12τ=8.9665J/mol ,
12τ=-0.83665J/mol ,12α=0.3。试确定共沸温度和共沸组成。 安托尼方程(:Pa ;T :K)
S P 氯仿:)(16.4679.26968660.20ln 1??=T P S
甲醇:)(29.3455.36264803.23ln 2??=T P S 解:设T 为53.5℃ 则)(16.4665.32679.26968660.20ln 1??=S P )(29.3465.32655.36264803.23ln 2??=S P =76990.1 =64595.6
S P 1S P 2 由)(ij ij ij G τα?=exp ,ij α=ji α
)
(121212exp τα?=G =)(9665.83.0exp ×?=0.06788
)(212121exp τα?=G =)(8365.03.0exp ×=1.2852
??????+++=212
121212221212
21212
21ln )()(G x x G G x x G x ττγ =??
?
???+?×+×?+×??21122122
1]06788.01[06788.09665.8]2852.11[2852.18365.01x x x x x )()()()( =???????+???21
212
193212.016086.02852.02852.13817.11)()()(x x x
??
????+++=2212121
21212122
12122
1
2
ln )()(G x x G G x x G x ττγ =???????+×?++?×21
121122
1
]12852.1[2852.18365.006788.0106788.09665.8)()(x x x x x =??
??????+?21212
1
2852.02852.107507.193212.0104131.0)()(x x x 1ln γ-2ln γ=S S P P 21ln =6
.645951
.76990ln
=0.1755 求得=0.32
1x 1γ=1.2092 2γ=0.8971
222111γγγS S i S
i i P x P x P
x +=∑
=8971.06.6459568.02092.11.7699032.0××+×× =69195.98Pa 101.3kPa
p 设T 为60℃
则)
(16.4615.33379.26968660.20ln 1??=S P )(29.3415.33355.36264803.23ln 2??=S P
=95721.9 =84599.9
S P 1S P 21ln γ-2ln γ=S S P P 21ln =9.845999
.95721ln
=0.1235 设T 为56℃
则)(16.4615.32979.26968660.20ln 1??=S P )(29.3415.32955.36264803.23ln 2??=S P
=83815.2 =71759.3
S P 1S P 21ln γ-2ln γ=S S P P 21ln =3.717592
.83815ln
=0.1553 当1ln γ-2ln γ=0.1553时求得=0.30
1x 1γ=1.1099 2γ=0.9500
222111γγγS S i S i i P x P x P
x +=∑
=9500.03.7175970.01099.12.8381530.0××+×× =75627.8Pa 101.3kPa
p
21、
第四章气体吸收
4.某原料气组成如下:
组分 CH 4 C 2H 6 C 3H 8 i-C 4H 10 n-C 4H 10 i-C 5H 12 n-C 5H 12 n-C 6H 14 y 0(摩尔分率) 0.765 0.045 0.035
0.025 0.045 0.015 0.025 0.045
先拟用不挥发的烃类液体为吸收剂在板式塔吸收塔中进行吸收,平均吸收温度为38℃,压力为1.013Mpa ,如果要求将i-C 4H 10回收90%。试求: (1) 为完成此吸收任务所需的最小液气比。
(2) 操作液气比为组小液气比的1.1倍时,为完成此吸收任务所需理论板数。 (3) 各组分的吸收分率和离塔尾气的组成。 (4)
求塔底的吸收液量
解:(1)最小液气比的计算:
在最小液气比下 N=∞,A 关=?关=0.0.85
关关)(A K V L ?=min =0.56 ×0.85=0.476
(2)理论板数的计算: 操作液气比min
2.1)(V L V L ==1.2×0.476=0.5712
02.156.05712.0===
关
关关V K L A 32.5102
.1log 85.0185.002.1log 1log 1log =???=???=
)()(A A N ?? (3)尾气的数量和组成计算: 非关键组分的
i i
VK L
A =
吸收率
11
1??=++N i N i i
A A A ?
被吸收的量为i N v ??+1,塔顶尾气数量i i N v v =??+)1(1? 塔顶组成
V v y i
i =
1 按上述各式计算,将结果列于下表
组分 1+N v Kmol/h
K i
i
A i φi N v φ1+i v i y
CH 476.5 17.4 0.0330.032 2.524 73.98 0.920 C 2H 6 4.5 3.75 0.1520.1520.684 3.816 0.047 C 3H 8
3.5
1.3 0.4390.436
1.526 1.974 0.025
i-C 4H 10 2.5 0.56 1.02 0.85 2.125 0.375 0.0047 n-C 4H 10 4.5 0.4 1.4280.95 4.275 0.225 0.0028 i-C 5H 12
1.5
0.18 3.17 1.00 1.500 0.0
0.0
n-C 5H 12 2.5 0.144 3.97 1.00 2.500 0.0 0.0 n-C 6H 14 4.5
0.05610.2 1.00 4.500 0.0 0.0
合计 100.0 - - - 19.81080.190
(4)塔底的吸收量 N L 塔内气体平均流率:
185.90237
.80100=+=
v Kmol/h
塔内液体平均流率:514
.51185.905712.020=×=?=+=均均)(V V L
L L L N 而,即100+=80.37+ N N L V L V +=++1010L N L 联立求解得=61.33Kmol/h. =41.70Kmol/h N L 0L 解2:由题意知,i-C 4H 10为关键组分
由P=1.013Mpa ,t 平=38℃ 查得K 关=0.56 (P-T-K 图) (1)在最小液气比下 N=∞,A 关=中关=0.9
关关)(A K V L ?=min =0.56 ×0.9=0.504
(2)min 1.1)(V L V L ==1.1×0.504=0.5544
99.056.05544.0===
关
关关V K L
A
所以 理论板数为
48.9199
.0log 9
.019.099.0log 1log 1log =???=???=
)
()(A A N ??
(3)它组分吸收率公式 i
i
VK L
A =,11
1
??=++N i N i i A A A ? 计算结果如下: 塔顶尾气 组分 进料量 相平衡常数K i i
A i
φ被吸收量数量
组成
CH 476.5 17.4 0.0320.032 2.448 74.05 0.923 C 2H 6
4.5 3.75
0.1480.148
0.668 3.834 0.048
C 3H 8 3.5 1.3 0.4260.426 1.491 2.009 0.025
i-C 4H 10
2.5 0.56
0.99 0.90 2.250 0.250 0.003 n-C 4H 10 4.5 0.4 1.3860.99 4.455 0.045 0.0006i-C 5H 12
1.5 0.18
3.08 1.00 1.500 0.0 0.0 n-C 5H 12 2.5 0.144 3.85 1.00 2.500 0.0 0.0 n-C 6H 14
4.5 0.056 9.9 1.00 4.500 0.0 0.0 合计 100.0 - - - 19.810 80.190
以CH4为例:
i A =032.04.175544
.0==i
VK L
i
φ=32.01032.099
.0032.0148.9148.9=??++ V1(CH4)=(1-i
φ)VN+1=(1-0.032)×76.5=74.05
923
.05.7605
.741
1144==
=
V V y CH CH )()(
(3) 塔内气体平均流率:10.902
190
.80100=+=v Kmol/h
塔内液体平均流率:L=905.92
81.19000+=++L L L )
(
由v l =0.5544
∴0L =40.05Kmol/h
化工分离工程习题答案简介
分离工程习题 第一章 1. 列出5种使用ESA 和5种使用MSA 的分离操作。 答:属于ESA 分离操作的有精馏、萃取精馏、吸收蒸出、再沸蒸出、共沸精馏。 属于MSA 分离操作的有萃取精馏、液-液萃取、液-液萃取(双溶剂)、吸收、吸附。 5.海水的渗透压由下式近似计算:π=RTC/M ,式中C 为溶解盐的浓度,g/cm 3;M 为离子状态的各种溶剂的平均分子量。若从含盐0.035 g/cm 3的海水中制取纯水,M=31.5,操作温度为298K 。问反渗透膜两侧的最小压差应为多少kPa? 答:渗透压π=RTC/M =8.314×298×0.035/31.5=2.753kPa 。 所以反渗透膜两侧的最小压差应为2.753kPa 。 9.假定有一绝热平衡闪蒸过程,所有变量表示在所附简图中。求: (1) 总变更量数Nv; (2) 有关变更量的独立方程数Nc ; (3) 设计变量数Ni; (4) 固定和可调设计变量数Nx , Na ; (5) 对典型的绝热闪蒸过程,你 将推荐规定哪些变量? 思路1: 3股物流均视为单相物流, 总变量数Nv=3(C+2)=3c+6 独立方程数Nc 物料衡算式 C 个 热量衡算式1个 相平衡组成关系式C 个 1个平衡温度等式 1个平衡压力等式 共2C+3个 故设计变量Ni =Nv-Ni=3C+6-(2C+3)=C+3 固定设计变量Nx =C+2,加上节流后的压力,共C+3个 可调设计变量Na =0 解: (1) Nv = 3 ( c+2 ) V-2 F zi T F P F V , yi ,Tv , Pv L , x i , T L , P L 习题5附图
生物分离工程期末考试试卷B
试卷编号: 一、名词解释题(本大题共3小题,每小题3分,总计9分) 1.Bioseparation Engineering:回收生物产品分离过程原理与方法。 2.双水相萃取:某些亲水性高分子聚合物的水溶液超过一定浓度后可形成两相, 并且在两相中水分均占很大比例,即形成双水相系统(two aqueous phase system)。 利用亲水性高分子聚合物的水溶液可形成双水相的性质,Albertsson于50年代 后期开发了双水相萃取法(two aqueous phase extraction),又称双水相分配法(two aqueous phase partitioning)。 3.电渗:在电场作用下,带电颗粒在溶液中的运动。 二、辨别正误题并改正,对的打√,错的打×(本大题共15小题,每小题2分,总计30分) 1.壳聚糖能应用于发酵液的澄清处理是由于架桥作用。错(不确定) 2.目前国内工业上发酵生产的发酵液是复杂的牛顿性流体,滤饼具有可压缩性。错 3.盐析仅与蛋白质溶液PH和温度有关,常用于蛋白质的纯化。错 4.超临界流体是一种介于气体和液体之间的流体,可用于热敏性生物物质的分离。 对 5.膜分离时,当截留率δ=1时,表示溶质能自由透过膜。错 6.生产味精时,过饱和度仅对晶体生长有贡献。对 7.阴离子纤维素类离子交换剂能用于酸性青霉素的提取。对 8.卡那霉素晶体的生产可以采用添加一定浓度的甲醇来沉淀浓缩液中的卡那霉 素。 9.凝胶电泳和凝胶过滤的机理是一样的。错 10.PEG-硫酸钠水溶液能用于淀粉酶的提取。对 11.乙醇能沉淀蛋白质是由于降低了水化程度和盐析效应的结果。对 12.冷冻干燥一般在-20℃—-30℃下进行,干燥过程中可以加入甘油、蔗糖等作为保 护剂。对 13.反相层析的固定相和流动相都含有高极性基团,可用来分离生物物质。错 14.大网格吸附剂由于在制备时加入致孔剂而具有大孔径、高交联度,高比表面积 的特点。错(不确定) 15.PEG沉淀蛋白质是基于体积不相容性。错 三、选择题(本大题共10小题,每小题2分,总计20分) 1.对于反胶束萃取蛋白质,下面说法正确的是:A A 在有机相中,蛋白质被萃取进表面活性剂形成的极性核里 B 加入助溶剂,可用阳离子表面活性剂CTAB萃取带正电荷的蛋白质 C 表面活性剂浓度越高越好 D 增大溶液离子强度,双电层变薄,可提高反胶束萃取蛋白质的能力 2.能进行海水脱盐的是:C A 超滤 B 微滤
系统工程88 大作业
系统工程作业 《关于大学生选购电脑的分析》 09工商3班王浩0914******** 09工商1班周世超0914******** 09工商2班李坤坤0914******** 09工商2班王亚楠0914******** 09工商2班邹鼎恒0914******** 09工商2班申庆山0914******** 2012/5/10
关于大学生选购电脑的分析 摘要: 一:问题的提出: 今年的暑期快到了,大学生购置电脑热潮的时候随之也快了,联想到我们当初第一次买电脑时的迷茫,不知道从哪些方面考虑,不知道自己需要的是什么,往往只是听从他人的个人意见,但是那不一定是自己想要的。所以我们提出这个课题,通过对身边已经熟悉电脑使用的同学的调查,分析得到一般同学的最佳购置电脑方案。 众所周知现在常见的PC机一般有台式机、笔记本和平板电脑三种形式。台式机具有笔记本计算机所无法比拟的优点。对于同价位的笔记本和台式机,台式机的配置一定比笔记本的要高。液晶显示器比较大,看起来较舒服。台式机的机箱具有空间大、通风条件好的因素而一直被人们广泛使用。台式机的机箱方便用户硬件升级,如光驱、硬盘。笔记本电脑除了追求配置更高、速度更快、性能更好、也力求使自身更轻、更小、更方便,更方便,来适应时代发速发展的需要,因为在信息高速并大量传播的今天,人们需要快速地获取最新的信息。平板电脑(英文:Tablet Personal Computer)是一种小型、方便携带的个人电脑,以触摸屏作为基本的输入设备。它拥有的触摸屏(也称为数位板技术)允许用户通过触控笔或数字笔来进行作业而不是传统的键盘或鼠标。用户可以通过内建的手写识别、屏幕上的软键盘、语音识别或者一个真正的键盘(如果该机型配备的话)。 二:研究方法: 利用用层次分析法把问题分解为各个组成因素,将因素按支配关系分组,建立递阶层次结构,通过两两比较的方式确定层次中诸因素的相对重要性既权重,根据有关人员的判断确定备选方案,并用模糊评价法对方案进行评价。 三:研究结果: 我们将购置电脑应该考虑的因素列举为:价格、外观、配置、售后服务、性价比、使用寿命、便于携带,并对其进行层次结构分析,结果表明价格位于最上层,是电脑选购应考虑的最关键因素;性价比和便于携带位于第二层,也是关键因素;配置、寿命、售后服务、外观位于最底层。对三种选购方案评价表明:对于一般需求的大学生而言选择购买笔记本较为合理。 四:结论: 对于购置电脑应考虑的因素,各人的偏重点不一样,本次课题研究针对于普遍要求进行分析,结果分析就有一般性,笔记本使用方便,便于携带,使用时间长,用处广泛,适合与一般大学生,购买笔记本的主要考虑因素是配置与价格! 关键词:电脑;选择;模型;方案;影响因素
生物分离工程期末复习
生物分离工程复习题 第一章绪论 简答题: 1、简述生物分离技术的基本涵义及内容。 答:基本涵义:生物分离技术是指从动植物与微生物的有机体或器官、生物工程产物(发酵液、培养液)及其生物化学产品中提取、分离、纯化有用物质的技术过程。 内容主要包括:离心分离、过滤分离、泡沫分离、萃取分离、沉淀(析)分离、膜分离、层析(色谱)分离、电泳分离技术以及产品的浓缩、结晶、干燥等技术。 2、物质分离的本质是有效识别混合物中不同溶质间物理、化学和生物学性质的差别,利用能够识别这些差别的分离介质和扩大这些差别的分离设备实现溶质间的分离或目标组分的纯化。请从物质的理化性质和生物学性质几个方面简述生物活性物质分离纯化的主要原理。 答:生物大分子分离纯化的主要原理是: 1)根据分子形状和大小不同进行分离,如差速离心与超离心、膜分离、凝胶过滤等; 2)根据分子电离性质(带电性)差异进行分离,如离子交换法、电泳法、等电聚焦法; 3)根据分子极性大小及溶解度不同进行分离,如溶剂提取法、逆流分配法、分配层析法、盐析法、等电点沉淀及有机溶剂分级沉淀等; 4)根据物质吸附性质的不同进行分离,如选择性吸附与吸附层析等; 5)根据配体特异性进行分离,如亲和层析法等。 填空题: 1.为了提高最终产品的回收率:一是提高每一级的回收率,二是减少操作 步骤。 2、评价一个分离过程效率的三个主要标准是:①浓缩程度②分离纯化程
度③回收率。 判断并改错: 原料目标产物的浓度越高,所需的能耗越高,回收成本越大。(×)改:原料目标产物的浓度越低。 选择题: 1. B 可以提高总回收率。 A.增加操作步骤 B.减少操作步骤 C.缩短操作时间 D.降低每一步的收率2.分离纯化早期,由于提取液中成分复杂,目的物浓度稀,因而易采用( A ) A、分离量大分辨率低的方法 B、分离量小分辨率低的方法 C、分离量小分辨率高的方法 D、各种方法都试验一下,根据试验结果确定 第二章细胞分离与破碎 概念题: 过滤:是在某一支撑物上放多孔性过滤介质,注入含固体颗粒的溶液,使液体通过,固体颗粒被截留,是固液分离的常用方法之一。 离心过滤:使悬浮液在离心力作用下产生离心压力,使液体通过过滤介质成为滤液,而固体颗粒被截留在过滤介质表面,从而实现固液分离,是离心与过滤单元操作的集成,分离效率更高。 填空题: 1.在细胞分离中,细胞的密度ρ S 越大,细胞培养液的密度ρ L 越小,则细 胞沉降速率越大。 2.过滤中推动力要克服的阻力有介质阻力和滤饼阻力,其中滤饼占主导作 用。 3.重力沉降过程中,固体颗粒受到重力,浮力,摩擦阻力的作用,当 固体匀速下降时,三个力的关系重力=浮力+摩擦阻力。 4.区带离心包括差速区带离心和平衡区带离心。
分离工程施工第一章作业参考答案
1、说明分离过程与分离工程的区别? 答:分离过程:是生产过程中将混合物转变组成不同的两种或多种相对纯净的物质的操作; 分离工程:是研究化工及其它相关过程中物质的分离和纯化方法的一门技术科学,研究分离过程中分离设备的共性规律,是化学工程学科的重要组成部分。 2、实际分离因子与固有分离因子的主要不同点是什么? 答:前者是根据实际产品组成而计算,后者是根据平衡组成而计算。两者之间的差别用级效率来表示。 错误:固有分离因子与分离操作过程无关 3、怎样用分离因子判断分离过程进行的难易程度? 答:分离因子的大小与1相差越远,越容易分离;反之越难分离。 4、比较使用ESA与MSA分离方法的优缺点。 答:当被分离组分间相对挥发度很小,必须采用具有大量塔板数 的精馏塔才能分离时,就要考虑采用萃取精馏(MSA),但萃取精馏需要加入大量萃取剂,萃取剂的分离比较困难,需要消耗较多能量。通常,分离混合物优先选择能量媒介(ESA)方法。 5、按所依据的物理化学原理不同,传质分离过程可分为哪两类? 答:平衡分离过程:采用平衡级(理论板)作为处理手段,利用两相平衡组成不相等的原理,即达到相平衡时,原料中各组分在两个相中的不同分配,并将其它影响参数均归纳于级效率之中,如蒸发、结晶、精馏和萃取过程等。
大多数扩散分离过程是不互溶的两相趋于平衡的过程。 速率分离过程:通过某种介质,在压力、温度、组成、电势或其它梯度所造成的强制力的推动下,依靠传递速率的差别来操作,而把其它影响参数都归纳于阻力之中。如超滤、反渗透和电渗析等。 通常,速率控制过程所得到的产品,如果令其互相混合,就会完全互溶。 8对乙苯和三种二甲苯混合物的分离方法进行选择。 (1)列出间二甲苯和对二甲苯的有关性质:沸点、熔点、临界温度、临界压力、偏心因子、偶极矩等,利用哪些性质的差别进行该二元物系的分离是最好的? (2)为什么使用精馏方法分离间二甲苯和对二甲苯是不适宜的? (3)为什么工业上选择熔融结晶和吸附分离间二甲苯和对二甲苯? (1)熔点、偶极矩 (2)沸点接近,相对挥发度太小 (3)凝固点、偶极矩相差较大,故可采用熔融结晶、吸附法进行分 离。 6.分离过程常借助分离剂将均相混合物变成两相系统,举例说明分离
系统工程大作业-客舱安全风险综合分析
客舱安全风险综合分析 与控制机制研究 一、研究目标 通过本项目研究,实现清晰辨识客舱安全危险源的诱因及促成要素,建立客舱安全危险源数据库,理清不同危险源之间的相互作用;建立危险源与危险后果之间的关系及演变过程模型。 二、研究内容 1.客舱安全危险源表现形式
2.关系及演变过程 2.1 危险源的分类 危险源应分为三类,即一类危险源、二类危险源和三类危险源。 第一类危险源是系统内存在的,处于某种状态的、能够提供导致事故的最小能量的物质。是事故发生的最基本的因素,是决定事故严重度的因素,是各种能量意外释放的主体。 第二类危险源是满足能够导致第一类危险源的能量意外释放和使意外释放的能量演变为事故所需的必要条件的一切因素。是事故发生的必要条件,是决定事故发生可能性的因素。 第三类危险源是指能够影响或导致第一二类危险源产生的因素。包括人的失误和各种环境因素。第三类危险源虽然不能直接导致事故的发生,但能对第一、二类危险源的产生有直接或间接的影响。 一起安全事故的发生,是在第三类危险源的影响与作用下,第一、二类危险源相互作用的结果。第一类危险源是导致事故的能量主体,第二类危险源是促使第一类危险源导致事故的必要条件,第三类危险
源是第一、第二类危险源出现的前提。第三类危险源的存在,促使第一、二类危险源的出现与作用;第二类危险源的存在,使第一类危险源有可能失去控制而释放危险因素。 第一类危险源决定事故后果的严重程度,第二类危险源决定事故发生的可能性大小,第三类危险源决定第一、二类危险源出现的可能性大小。对第三类危险源的辨识与控制,是实现系统本质安全化的必要条件。 2.2 重大危险源相互作用 里将风险定义为危险源发生事故的可能性和后果的乘积,其中事故的可能性为危险源事故情景发生的概率,事故的后果考虑对人员的影响,以个体死亡率表示。在以上假设的基础上,对于飞机客舱内存在的多个危险源,其对区域内某一空间地理坐标为(x,y)处产生的个人风险由下公式计算: R(x,y) = ∑f s V S (x,y) (1) 式中:R(x,y)为危险源在位置(x,y)处产生的个人风险:f s为第S 个危险源发生事故的概率;V S (x,y) 为由第S个危险源发生事故在位置(x,y)处引起个体死亡的概率。 式(1)所求的个人风险值是一系列危险源发生事故的概率和相应的死亡率乘积的简单叠加,并未考虑到多个危险源之间的相互影响。为了清除的说明危险源之间的影响,如图所示:
生化分离工程 第三章 沉淀
第三章沉淀 主要内容 第一节蛋白质表面特性 第二节蛋白质沉淀方法 第一节蛋白质表面特性 蛋白质表面由不均匀分布的荷电基团形成的荷电区、亲水区和疏水区构成。 蛋白质的水溶液呈胶体性质,在蛋造白质分子周围存在与蛋白质分子紧密或疏松结合的水化层。是蛋白质形成稳定的胶体溶液、防止蛋白质凝聚沉淀的屏障之一。 蛋白质沉淀的另一屏障是蛋白质分子间的静电排斥作用。当双电层的电位足够大时,静电排斥作用抵御分子间的相互吸引作用,使蛋白质溶液处于稳定状态。 第二节蛋白质沉淀的方法 盐析沉淀法 等电点沉淀法 有机溶剂沉淀法 非离子型聚合物 聚电解质 多价金属离子 1.盐析法 盐析沉淀法:蛋白质在高离子强度溶液中溶解度降低,发生沉淀的现象。 中性盐:硫酸铵、硫酸钠、柠檬酸钠等 盐析沉淀原理: 由于加入大量的中性盐破坏了蛋白质的水化膜、中和其所带的电荷从而使蛋白质分子聚集而沉淀析出。 蛋白质的盐析行为常用Cohnx经验式表示: lgS=β-K sμ 式中S为蛋白质的溶解度;μ为离子强度;β为常数,与盐的种类无关,但与温度和pH有关;K s 为盐析常数,与盐的种类有关,但与温度和pH无关。 K s分级盐析法:在一定的pH和温度条件下,改变盐的浓度(即离子强度)达到沉淀的目的。 β分级盐析法:在一定的离子强度条件下,改变溶液的pH和温度达到沉淀的目的。 影响盐析的因素 (1)无机盐种类:离子半径小,带电多,电荷密度高的阴离子,盐析效果好。 (2)pH值:pH影响Cohnx方程中的b值,pH值接近蛋白质pI值时,蛋白
质溶解度最小。 (3)温度:T影响Cohn方程中的b值。温度升高,b降低;温度降低,b升高。 分段盐析 不同的蛋白质分子,由于其分子表面的极性基团的种类、数目以及排布的不同,其水化层厚度不同,故盐析所需要的盐浓度也不一样,因此调节蛋白质的中盐浓度,可以使不同的蛋白质分别沉淀。 ?常用的盐析剂是硫酸铵,因为它的盐析能力强,在水中的溶解度大,价格便宜,浓度高时也不会引起蛋白质活性丧失。 ?盐析沉淀的蛋白质仍保持天然构象,即仍有活性。 ?蛋白质用盐析方法沉淀分离后,还需要脱盐才能进一步精提纯。脱盐常用透析法。 透析是将含有小分子杂质的蛋白质溶液装在半透膜(玻璃纸、火绵纸等)制的透析袋里放在缓冲液中进行,可不断更换缓冲液,直至杂质被除去。 2 等电点沉淀 利用蛋白质在pH等于其等电点的溶液中溶解度下降的原理进行沉淀分级的方法称为等电点沉淀法。 不同的蛋白质有不同的等电点,因此通过调节溶液pH到目的蛋白的等电点,可使之沉淀而与其它蛋白质分开,从而除去大量杂蛋白。 沉淀原理:蛋白质在其等电点时溶解度最低。 3 有机溶剂沉淀法 ?有机溶剂沉淀:向含有目标物质的溶液中加入水溶性的有机溶剂(如丙酮,乙醇等),而使目标物质发生沉淀的方法。 沉淀原理: A 有机溶剂能破坏溶质分子的水化层,降低溶质的溶解度; B 有机溶剂降低水溶液的介电常数,使溶质分子间的静电引力(库仑力)增大,导致溶质的凝集和沉淀。 4 非离子型聚合物 非离子型聚合物:利用一些非离子型的高聚物来沉淀蛋白质的方法。 沉淀原理:可能有降低蛋白质分子表面的水化程度或空间排阻作用
生物分离工程期末复习题
填空题 1. .根据吸附剂与吸附质之间存在的吸附力性质的不同,可将吸附分为物理吸附、化学吸附和交换吸附; 2. 比表面积和孔径是评价吸附剂性能的主要参数。 3. 层析操作必须具有固定相和流动相。 4. 溶质的分配系数大,则在固定相上存在的几率大,随流动相的移动速度 小。 5. 层析柱的理论板数越多,则溶质的分离度越大。 6. 两种溶质的分配系数相差越小,需要的越多的理论板数才能获得较大的 分离度。 7. 影响吸附的主要因素有吸附质的性质,温度,溶液pH值,盐的浓度和吸附物的浓度与吸附剂的用量; 8. 离子交换树脂由网络骨架(载体),联结骨架上的功能基团(活性基)和可交换离子组成。 9. 电泳用凝胶制备时,过硫酸铵的作用是引发剂(提供催化丙烯酰胺和双丙烯酰胺聚合所必需的自由基);甲叉双丙烯酰胺的作用是交联剂(丙烯酰胺单体和交联剂甲叉双丙烯酰胺催化剂的作用下聚合而成的含酰胺基侧链的脂肪族长链);TEMED的作用是增速剂(催化过硫酸胺形成自由基而加速丙烯酰胺和双丙烯酰胺的聚合); 10. 影响盐析的因素有溶质种类,溶质浓度,pH 和温度; 11. 在结晶操作中,工业上常用的起晶方法有自然起晶法,刺激起晶法和晶种起晶法; 12. 简单地说离子交换过程实际上只有外部扩散、部扩散和化学交换反应三步;
13. 在生物制品进行吸附或离子交换分离时,通常遵循Langmuir 吸附方程,其形式为c K c q q 0+= 14. 反相高效液相色谱的固定相是 疏水性强 的,而流动相是 极性强 的; 15. 等电聚焦电泳法分离不同蛋白质的原理是依据其 等电点 的不同; 16. 离子交换分离操作中,常用的洗脱方法有 静态洗脱 和 动态洗脱 ; 17. 晶体质量主要指 晶体大小 , 形状 和 纯度 三个方面; 18. 亲和吸附原理包括 配基固定化 , 吸附样品 和 样品解析 三步; 19. 根据分离机理的不同,色谱法可分为 吸附、离交、亲和、凝胶过滤色谱 20. 蛋白质分离常用的色谱法有 免疫亲和色谱法, 疏水作用色谱法 , 金属螯合色谱法 和 共价作用色谱法 ; 21. SDS-PAGE 电泳制胶时,加入十二烷基磺酸钠(SDS )的目的是消除各种待分离蛋白的 分子形状 和 电荷 差异,而将 分子量 作为分离的依据;加入二硫叔糖醇的目的是 强还原剂,破坏半胱氨酸间的二硫键 ; 22. 影响亲和吸附的因素有 配基浓度 、 空间位阻 、 配基与载体的结合位点 、 微环境 和 载体孔径 ; 23. 阳离子交换树脂按照活性基团分类,可分为 强酸性阳离子交换树脂 、 弱酸性 和 中强酸性 ;其典型的活性基团分别有 3 、 COOH - 、2)(OH PO -; 24. 阴离子交换树脂按照活性基团分类,可分为强碱性、 弱碱性 和 中强碱 性 ;其典型的活性基团分别有-+OH CH RN 33)(、2NH -、兼有以上两种基团; 25. 影响离子交换选择性的因素有 离子水合半径 、 离子价 、 离子强度 、 溶液pH ,温度 、溶液浓度 、 搅拌速率 、和 交联度、膨胀度、颗粒大小 ;
系统工程学论文大作业
系统工程大作业 基于系统动力学的研发投资预算研究 姓名 专业 学号
基于系统动力学的研发投资预算研究 摘要:研发投入是一种高风险的投资,研发投入过多或过少都不利于企业的发展,而如何在企业资源有限的情况下,合理安排研发投入以荻取持续的竞争能力是企业研发管理的重点。应该说,研发投入系统是一种复杂的系统,本文首先对研发投资预算的方法进行了回顾,继而提出了运用系统动力学编制研发投资预算的思路并构建了基于系统动力学的研发投资预算模型,该模型将研发系统分为研发流程、研发团队和现金流等三个子模块并描述了研发投资预算的影响因素及其作用过程。最后,以电子产品为例运用该模型模拟了四种不同研发投资预算方案的效果。 关键词:系统动力学;研发投资;研发强度;研发流程 一、问题的提出 研发支出是企业为了获取长期的竞争能力而进行的一种投资。该项投资具有较高的风险。主要体现在研发本身的特征上。研发行为具有以下特征:其一,研发投资的50%以上为工程技术人员的薪酬支出。而企业的研发形成的知识积累也蕴含于工程技术人员的身上,因此,研发人员的流动就带来了企业研发投资的损耗(Hall,2002)。其二,研发投资本身具有较高的外部性。一个企业研发的产品无法完全排斥其他企业使用该项技术(Arrow,1962)。其三,研发投资存在一种加速陷阱的现象,即随着研发投资的加大,研发投资带给企业的盈利却是不断减少的(Brown,1999)。基于研发投资的以上特征,我们认为,企业的研发投资不是投的越多越好,理论上应该存在一个最优的金额。这样如何将有限的研发资源进行合理的配置,特别是在不同的研发项目以及研发项目的不同阶段进行配置,将是企业研发投资管理的一个重要研究内容。同时,研发系统与其他商业系统一样,具有复杂的结构以及动态的特征,尤其是存在延迟效应、非线性以及多重反馈等,符合系统动力学方法应用的基本条件。系统动力学是分析研究信息反馈系统的学科,它强调系统结构与系统行为动态特性的关系,运用系统t程思想方法,
生物分离工程期末复习资料
第一章 1.生物分离工程的一般过程P4 答:①发酵液的预处理主要采用凝聚和絮凝等技术来加速固相,液相分离,提高过滤速度。过滤、离心是其最基本的单元操作。 ②产物的提取采用沉淀、吸附、萃取、超滤等单元操作。 ③产物的精制常采用色谱分离技术,有层析、离子交换、亲和色谱、吸附色谱、电色谱。 ④成品的加工处理浓缩、结晶、干燥 第二章 一、概念: 1.发酵液的预处理:指采用凝聚和絮凝等技术来加速固相、液相分离,提高过滤速度。 2.凝集(凝聚):指在投加的化学物质(如水解的凝聚剂,铝、铁的盐类或石灰等)作用下,发酵液中的 胶体脱稳并使粒子相互凝集成为1mm大小块状絮凝体的过程。 3.絮凝:指某些高分子絮凝剂能在悬浮粒子之间产生桥梁作用,使胶粒形成粗大絮凝团的过程。 4.离心分离:指在离心场的作用下,将悬浮液中的固相和液相加以分离的方法。主要用于颗粒较细的悬 浮液和乳浊液的分离。(分为差示离心、均匀介质离心、密度梯度离心、等密度梯度离心和平衡等密度离心。) 5.等电点沉淀法:利用蛋白质等两性化合物在等电点时溶解度最低,易产生沉淀的性质,用酸化剂或碱化 剂调节发酵液的pH,使其达到菌体蛋白的等电点而产生沉淀。 二、填空: 1、按过滤时料液流动方向的不同,分为常规过滤和错流过滤。 2、可溶性杂蛋白的去除法包括:等电点沉淀法、热处理法、化学变性沉淀法和吸附法 三、问答 1、发酵液的一般特征? ①组成大部分为水; ②发酵产物的浓度较低; ③发酵液中的悬浮固形物主要是菌体和蛋白的胶状物; ④含有培养基中的残留成分,如无机盐类、非蛋白质大分子及其降解产物; ⑤含有其他少量代谢副产物;
⑥含有色素、毒性物质。热原质等有机杂质。 2、常用的絮凝剂有什么? 无极絮凝剂:Al2(SO4)3·18H2O (明矾)、氯化钙、氯化镁碱式氯化铝、高分子无机聚合物等。 有机絮凝剂:壳多糖及其衍生物、明胶、丙烯酰胺类、聚苯乙烯类、聚丙烯酰类聚乙烯亚胺类。 3、影响絮凝效果的因素? 答:①絮凝剂的种类; ②絮凝剂浓度; ③ pH; 最关键因素,影响絮凝剂活性基团的解离度。 ④搅拌转速和时间。 4、发酵液预处理的方法? 答:①凝聚和絮凝方法 ②加热法 ③调节PH法 ④加水稀释法 ⑤加入助滤剂法 ⑥加吸附剂法或加盐法 ⑦高价态无机离子去除法 Ca2+——草酸、草酸钠→形成草酸钙沉淀 Mg2+——三聚磷酸钠(Na5P3P10)→形成三聚磷酸钠镁可溶性络合物 Fe3+——黄血盐(K4Fe(CN)6) →普鲁士蓝淀 ⑧可溶性杂蛋白的去除法 3、VB12发酵液絮凝预处理的研究 答:由正交试验确定影响絮凝的主要因素,结果表明,最佳絮凝条件:絮凝剂为聚合氯化铝、加入体积分数7%,pH6、搅拌速度14r/min、搅拌时间45s。通过加压过滤实验,得到絮凝后
分离工程课后习题答案-刘家祺
分离工程课后习题答案-刘家祺
分离工程习题 第一章 1. 列出5种使用ESA 和5种使用MSA 的分离操作。 答:属于ESA 分离操作的有精馏、萃取精馏、吸收蒸出、再沸蒸出、共沸精馏。 属于MSA 分离操作的有萃取精馏、液-液萃取、液-液萃取(双溶剂)、吸收、吸附。 5.海水的渗透压由下式近似计算:π=RTC/M ,式中C 为溶解盐的浓度,g/cm 3;M 为离子状态的各种溶剂的平均分子量。若从含盐0.035 g/cm 3的海水中制取纯水,M=31.5,操作温度为298K 。问反渗透膜两侧的最小压差应为多少kPa? 答:渗透压π=RTC/M =8.314×298×0.035/31.5=2.753kPa 。 所以反渗透膜两侧的最小压差应为2.753kPa 。 9.假定有一绝热平衡闪蒸过程,所有变量表示在所附简图中。求: (1) 总变更量数Nv; (2) 有关变更量的独立方程数Nc ; (3) 设计变量数Ni; (4) 固定和可调设计变量数Nx , Na ; (5) 对典型的绝热闪蒸过程,你 将推荐规定哪些变量? 思路1: 3股物流均视为单相物流, 总变量数Nv=3(C+2)=3c+6 独立方程数Nc 物料衡算式 C 个 热量衡算式1个 相平衡组成关系式C 个 1个平衡温度等式 1个平衡压力等式 共2C+3个 故设计变量Ni =Nv-Ni=3C+6-(2C+3)=C+3 固定设计变量Nx =C+2,加上节流后的压力,共C+3个 可调设计变量Na =0 解: V -2 F z i T F P F V , y i ,T v , P v L , x i , T L , P L 习题5附图
系统工程大作业
《系统工程》大作业 姓名:崔敏饶培培廖广旺 陈思路谢超李钦成学院:机械工程学院 班级:12 工业 1 班 指导老师:肖华秀老师
城市道路交通问题分析 ——以武汉市为例 摘要:本文首先介绍了城市道路交通拥挤堵塞的相关概念及相关研究成果,介绍了目前城市道路交通状况,指出城市道路交通面临的主要问题有交通事故频繁发生,道路容量严重不足、汽车增长速度过快、公共交通系统不完善、交通管理技术水平低下、城市道路交通发展缺乏整体的交通发展战略等,然后以武汉市为例,具体分析了武汉市道路交通现状以及道路交通问题产生的原因,运用统计软件minitab,STELLA等对武汉市车辆数据进行了主成分分析,最后根据武汉市的具体情况,给出解决城市道路交通拥挤问题的具体方法和策略。 关键词:城市交通,交通事故,交通拥挤,解决方案 一.背景资料 近年来,随着国民经济的快速增长,人流、物流、信息流以前所未有的密度涌向大中城市并向周边辐射,城市化进程明显加快,城市规模不断扩大,人口不断集中。统计资料显示:超过百万人口的大城市数量从1978年的13个增加到2011年的42个,目前城市化水平已经达到50%。此种状态在带动城市交通需求高速增长,机动车辆增加的同时,也促进城市道路负荷加重,交通事故、交通堵塞日益加剧。交通拥堵使交通延误增大,行车速度降低、时间损失、燃料费用增加、排污量增大、城市环境恶化、诱发交通事故,直接影响人们的工作效率和身体健康。 当前,城市道路交通拥堵及交通事故的发生已经成为阻碍城市快速健康发展的焦点问题之一,其所造成的经济、安全和环境等重大损失已引起社会各方的广泛关注。例如,武汉市城市主干道平均车速比十年前降低50%以上,市区38个交叉口中,严重阻塞的达到40%;为了缓解城市交通拥堵,武汉市政府对交通基础设施投资不断加大,但交通拥堵问题并没用得到明显缓解,城市交通需求与交通供给之间的矛盾日趋尖锐,道路交通拥堵现象越发严重。 二.改进方案的生成 (一)交通事故分析及改进方案
化工分离工程第2章 习 题
第2章 习 题 2.1 1. 计算在0.1013MPa 和378.47K 下苯(1)-甲苯(2)-对二甲苯(3)三元系,当x 1 = 0.3125、x 2 =0.2978、x 3 =0.3897时的K 值。汽相为理想气体,液相为非理想溶液。并与完全理想系的 K 值比较。已知三个二元系的wilson 方程参数(单位: J/mol ): λ12-λ11=-1035.33; λ12-λ22=977.83 λ23-λ22=442.15; λ23-λ33=-460.05 λ13-λ11=1510.14; λ13-λ33=-1642.81 在T =378.4 K 时液相摩尔体积(m 3 /kmol )为: =100.91×10 -3 ; =177.55×10 -3 ; =136.69×10 -3 安托尼公式为(p s :Pa ; T :K ): 苯:1n =20.7936-2788.51/(T -52.36); 甲苯:1n =20.9065-3096.52/(T -53.67); 对 -二甲苯:1n =20.989 1-3346.65/(T -57.84); 2.1 1.答案解: 由Wilson 方程得: Λ12 = l l V V 12exp[-(λ12-λ11)/RT] =3 3 10 91.1001055.177??×exp[-(1035.33)/(8.314×378.47)]=2.4450 Λ21=0.4165 Λ13=0.8382 Λ31=1.2443 Λ23=0.6689 Λ32=1.5034 ln γ1=1-ln(Λ12X 2+Λ13X 3)-[3231 212 21X X X Λ+ΛΛ+ 2 321313 31X X X Λ+ΛΛ ]=0.0497 γ1=1.0509 同理,ln γ2=0.05148, γ2=1.6732 ln γ3=0.4190, γ3=1.5203 lnP 1S =20.7936-2788.51/(378.47-52.36)=12.2428, P 1S =0.2075Mpa lnP 2S =20.9062-3096.52/(378.47-53.67)=11.3729, P 2S =0.0869Mpa lnP 3S =20.9891-3346.65/(378.47-57.84)=10.5514, P 3S =0.0382Mpa
生物分离工程期末复习题
填空题 1. 为了提高最终产品的回收率一是(提高每步分离效率),二是(减少分离步骤)。 2. 评价一个分离过程效率的三个主要标准是:(浓缩率),(分离系数)和(产品回收程度) 3?生物产品的分离过程包括发酵液的预处理和(液固分离),(产品的提取),(产品的精制) 和(产品的加工处理)。 4?生化反应所起的作用是产生目的产物,指标是(产率)和(转化率),而生物分离解决的 是如何从反应液中获取这些物质,涉及的是(收率)和(纯度)。 5?生物分离的主要任务:从发酵液和细胞培养液中以(最高的效率),(理想的纯度)和(最小的能耗)把目的产物分离出来。 6?生物分离过程的特点包括:(生物分离过程的体系特殊),(生物分离过程的工艺流程特殊),(生物分离过程的成本特殊)。 7. 物质分离的本质是识别混合物中不同溶质间(物理),(化学)和(生物)性质的差别利用 能识别这些差别的(分离介质)和扩大这些差别的(分离设备) 8. 性质不同的溶质在分离操作中具有不同的(传质速率)和或(平衡状态) 9. 平衡分离是根据溶质在两相间(分配平衡)的差异实现分离;溶质达到分配。平衡为扩散 传质过程,推动力仅取决于系统的(热力学性质)。 10. 差速分离是利用外力驱动溶质迁移产生的(速度差)进行分离的方法。 1. 在细胞分离中,细胞的密度越(大),细胞培养液的密度越(小),则细胞沉降 2. 区带离心包括(差速)区带离心和(等密度)区带离心。
3. 为使过滤进行的顺利通常要加入(惰性助滤剂)。 4. 发酵液常用的固液分离方法有(离心)和(过滤)等。 5?常用离心设备可分为(离心沉降)和(离心过滤)两大类; 6?常用的工业絮凝剂有(无机絮凝剂)和(有机絮凝剂)两大类。 7. 工业生产中常用的助滤剂有(硅藻土)和(珍珠岩粉)。 8. 重力沉降过程中,固体颗粒受到(重力),(浮力),(摩擦阻力)的作用, 固体匀速下降时,三个力的关系(重力=浮力+摩擦阻力)。 9. 发酵液预处理的方法包括:(凝集),(絮凝),(加热法);(调节pH法),(加水稀释法),加入(助滤剂)和(吸附剂)。 10. 发酵液中胶粒保持稳定的原因:(双电层)和(蛋白质周围水化层)结构。 11. 发酵液预处理过程中的相对纯化主要包括去除(高价态无机离子),(可溶性杂蛋白质),(色素)和(多糖类物质)。 12. 发酵液中杂蛋白的去除方法主要有(等电点沉淀法),(热处理法)和(化学变性沉淀法)。 13. 差速区带离心用于分离(大小)不同的颗粒,与颗粒(密度)无关。等密度区带离心包 括(预形成梯度密度离心)和(自形成梯度密度离心)两种方式。离心达到平衡后,样品颗粒的区带形状和平衡位置(不再发生变化)。 1?单从细胞直径的角度,细胞(直径越小),所需的压力或剪切力越大,细胞越 2. 常用的化学细胞破碎方法有(.酸碱法),(盐法),(表面活性剂处理),(有机溶剂法)和(螯合剂)。 3. 包涵体的溶解需要打断蛋白质分子和分子间的(共价键),(离子键),疏水作用及静电 作用等,使多肽链伸展。因此,包涵体的溶解需要强的变性剂,如(8mol/L尿素)和(6mol/L 盐
分离工程作业
第一章 单级平衡过程 2. 计算在0.1013MPa 和378.47K 下苯(1)-甲苯(2)-对二甲苯(3)三元系,当x 1=0.3125,x 2=0.2978,x 3=0.3897时的K 值。汽相为理想气体,液相为非理想溶液。并与完全理想系的K 值比较。已知三个二元系的Wilson 方程参数。 8 3.977;33.103522121112=--=-λλλλ 15.4422223=-λλ ;05.4603323-=-λλ 14.15101113=-λλ ; 81.16423313-=-λλ (单位:J/mol) 在T=378.47K 时液相摩尔体积为: k m o l m v L 3311091.100-?= ;321055.117-?=L v ;331069.136-?=L v 安托尼公式为: 苯:()36.5251.2788 7936.20ln 1--=T P s ; 甲苯:()67.5352.30969065.20ln 2--=T P s ; 对二甲苯:()84.5765.33469891.20ln 3--=T P s ;(K T Pa P s :;:) 解1:由Wilson 参数方程()[] RT v v ii ij L i L j ij λλ--=Λexp ()[]RT v v L L 11121 212exp λλ--=Λ ()()[]47.378314.833.1035exp 1091.1001055.1173 3 ?--??=-- =1.619 ()[]RT v v L L 22212 121exp λλ--=Λ ()()[]47.378314.883.977exp 1055.1171091.1003 3 ?-??=-- =0.629 同理:838.013=Λ ;244.131=Λ 010.123=Λ ;995.032=Λ 由Wilson 方程∑∑∑ΛΛ-???? ??Λ-=k j j kj k ki j j ij i x x x ln 1ln γ:
分离工程第三章复习题(2020年九月整理).doc
第三章复习题 一填空题 1在塔顶和塔釜同时出现的组分为() 2设计变量与独立量之间的关系可用下式来表示() 3设计变量分为()与()。 4萃取精馏塔在萃取剂加入口以上需设()。 5恒沸剂与组分形成最低温度的恒沸物时,恒沸剂从塔()出来。 6设计变量分为可调设计变量和(),装置的设计变量与各单元设计变量的关系 为()。 7在塔顶和塔釜同时出现的组分为()。 8在塔顶和塔釜同时出现的组分为()。 9萃取精馏塔在萃取剂加入口以上需设()。 10萃取精馏萃取剂从()加入塔中,萃取剂再生塔萃取剂从()取出。 11对于能生成二元最低恒沸物的物系来说,x ,y 大小关系在恒沸点左侧为(),在恒沸点右侧为()。 12在一个塔中精馏某二元最低恒沸物时,塔顶得到的产物是(),塔底得到的 产物是()。 13萃取精馏塔中,当原料以()热状况加入时,精馏段与提馏段中的溶剂浓度 大致相等,萃取剂将从塔()出来。 14活度系数1γ>的溶液为()溶液,活度系数1γ<的溶液为()溶液。 15多组分精馏与多组分吸收过程均不能对所有组分规定分离要求,而只能对分
离操作中起关键作用的组分即关键组分规定分离要求,其中多组分精馏过程最多 只能有()个关键组分。 16端值常数A 为()时体系为理想溶液,A 为()时体系为负偏差溶液。 17用郭氏法分析,串级单元的可调设计变量为(),侧线采出板的可调设计变 量为()。 18根据萃取精馏原理,通常希望所选择的萃取剂与塔顶组分形成具有()偏差 的非理想溶液,与塔底组分形成理想溶液或具有()偏差的非理想溶液。19萃 取精馏塔中,当原料以液相加入时,则提馏段中的溶剂浓度将会因料液的加入而 变得比精馏段(),此时为了保证整个塔内萃取剂的浓度,常将部分溶剂随() 一起加入。 20恒沸精馏过程恒沸剂的加入不仅影响原溶液组分(挥发度或相对挥发度a),同 时与原溶液中的一个或几个组分形成恒沸物,当形成最低温度的恒沸物时恒沸剂 从塔()出来。 21在多组分精馏过程中,由芬斯克公式计算的最少理论板数决定于两组分的分 离要求和(),与进料组成()。 22恒沸精馏溶剂从()加入塔中,溶剂从塔()取出。 23根据萃取精馏原理,通常希望所选择的萃取剂与塔顶组分形成具有()偏差 的非理想溶液,与塔底组分形成理想溶液或具有()偏差的非理想溶液。 24活度系数1γ>的溶液为()溶液,活度系数1γ<的溶液为()溶液。 25对拉乌尔定律产生偏差的溶液称为()或()。 26对于能生成二元恒沸物的物系来说,在恒沸点处气液相两相组成()。在恒 沸点两侧组分的挥发能力()。 二选择题 1设计变量数就是() A. 设计时所涉及的变量数 B.约束数 C.独立变量数与约束数的和 D.独立变量数与约束数的差 2当蒸馏塔的产品不合格时,可以考虑() A.提高进料量 B.降低回流比 C.提高塔压 D.提高回流比
生物分离工程期末总复习
第一章绪论 一、生物分离工程在生物技术中的地位? 二、生物分离工程的特点是什么? 1.产品丰富产品的多样性导致分离方法的多样性 2.绝大多数生物分离方法来源于化学分离 3.生物分离一般比化工分离难度大 3.生物分离工程可分为几大部分,分别包括哪些单元操作? 三、生物分离过程一般分四步: 1.固-液分离(不溶物的去除) 离心、过滤、细胞破碎 目的是提高产物浓度和质量 2.浓缩(杂质粗分) 离子交换吸附、萃取、溶剂萃取、反胶团萃取、超临界流体萃取、双水相萃取 以上分离过程不具备特异性,只是进行初分,可提高产物浓度和质量。 3.纯化 色谱、电泳、沉淀 以上技术具有产物的高选择性和杂质的去除性。 4.精制结晶、干燥 四、在设计下游分离过程前,必须考虑哪些问题方能确保我们所设计的工艺过程最为经济、可靠? (1)产品价值 (2)产品质量 (3)产物在生产过程中出现的位置 (4)杂质在生产过程中出现的位置 (5)主要杂质独特的物化性质是什么? (6)不同分离方法的技术经济比较 上述问题的考虑将有助于优质、高效产物分离过程的优化。 五、.生物分离效率有哪些评价指标? 1.目标产品的浓缩程度——浓缩率m 2.系数α回收率REC 第二章细胞分离与破碎
1.简述细胞破碎的意义 一、细胞破碎的目的 由于有许多生化物质存在于细胞内部,必须在纯化以前将细胞破碎,使细胞壁和细胞膜受到不同程度的破坏(增大通透性)或破碎,释放其中的目标产物,然后方可进行提取。 二、细胞破碎方法的大致分类 破碎方法可归纳为机械破碎法和非机械破碎法两大类,非机械破碎法又可分为化学(和生物化学)破碎法和物理破碎法。 1.机械破碎 处理量大、破碎效率高速度快,是工业规模细胞破碎的主要手段。 细胞的机械破碎主要有高压匀浆、研磨、珠磨、喷雾撞击破碎和超声波破碎等。 2.化学(和生物化学)渗透破碎法 (1)渗透压冲击法(休克法)(2)酶溶(酶消化)法 3.物理破碎法 1)冻结-融化法(亦称冻融法)(2)干燥法 空气干燥法真空干燥法冷冻干燥法喷雾干燥法 三、化学渗透法和机械破碎法相比有哪些优缺点? 化学渗透破碎法与机械破碎法相比优点:化学渗透破碎法比机械破碎法的选择性高,胞内产物的总释放率低,特别是可有效地抑制核酸的释放,料液的粘度小,有利于后处理过程。 化学渗透破碎法与机械破碎法相比缺点:化学渗透破碎法比机械破碎法速度低,效率差,并且化学或生化试剂的添加形成新的污染,给进一步的分离纯化增添麻烦。 第三章初级分离 一、常用的蛋白质沉淀方法有哪些? 盐析沉淀,等电点沉淀,有机溶剂沉淀,热沉淀 二、影响盐析的主要因素有哪些? (1)离子强度:Ks和β值, 强度越大,蛋白质溶解度越小; (2)蛋白质的性质:因相对分子质量和立体结构而异,结构不对称、相对分子质量大的蛋白质易于盐析; (3)蛋白质的浓度:蛋白质浓度大,盐的用量小,共沉作用明显,分辨率低;蛋白质浓度小,盐的用量大,分辨率高;2.5%~3.0% 时最适合; (4)pH值:通常调整到pI附近,盐浓度较大会对等电点产生较大影响,pH对不同蛋白质的共沉影响;
华东《分离工程》2019年春季学期在线作业(二)
------------------------------------------------------------------------------------------------------------------------------ (判断题)1: A: 错误 B: 正确 正确答案: (判断题)2: 当关键组分的相对吸收率大于其吸收因子A时,则吸收塔需有无穷多个理论级才能完成给定分离任务。 A: 错误 B: 正确 正确答案: (判断题)3: 吸收过程只有在贫气吸收的条件下,才能视为恒摩尔流 A: 错误 B: 正确 正确答案: (判断题)4: 吸收因子A的值随着温度的提高而减小,随着压力的升高而增大 A: 错误 B: 正确 正确答案: (判断题)5: 随着构成共沸物的各组分的纯组分的蒸气压差的增大,共沸组成变化规律为最低共沸物向含低沸点组分多的浓度区移动,最高共沸物向含高沸点组分多的浓度区移动 A: 错误 B: 正确 正确答案: (判断题)6: 吸收操作中,吸收量沿塔高分布不均,因而溶解热分布不匀,致使吸收塔温度分布比较复杂 A: 错误 B: 正确 正确答案: (判断题)7: 多组分精馏过程,最少理论级数Nm值与进料组成和进料状态均无关。 A: 错误 B: 正确 正确答案: (判断题)8: 当吸收效果不好时,通过增加塔级数可以提高吸收效率 A: 错误 B: 正确 正确答案: (判断题)9: 一定温度下压缩气体混合物,当开始冷凝产生第一个液滴时的压力叫露点压力。 A: 错误 B: 正确 正确答案: (判断题)10: MESH方程中的M是物料平衡关系,E是热量平衡关系,S是摩尔分率加和式。A: 错误 B: 正确
