(四川专用)高考化学总复习 第5章 第4讲《晶体结构与性质》解析训练
新人教版版高考化学总复习第五章晶体结构与性质教案
教学指导意见核心素养1.了解晶体与非晶体的区别,了解晶格能及晶格能对离子晶体性质的影响。
2.了解晶体类型,了解不同类型晶体中微粒结构、微粒间作用力的区别,能结合晶体结构(实例)描述分子晶体、离子晶体、金属晶体、原子晶体的性质。
3.了解晶胞的概念,能根据晶胞确定晶体组成并进行相关计算。
4.了解过渡晶体、混合型晶体的存在现象。
1.宏观辨识与微观探析:认识晶胞及晶体的类型,能从不同角度分析晶体的组成微粒、结构特点,能从宏观和微观相结合的视角分析与解决实际问题。
2.证据推理与模型认知:能运用典型晶体模型判断晶体的结构特点及组成并进行相关计算。
3.变化观念与平衡思想:认识不同晶体类型的特点,能从多角度、动态的分析不同晶体的组成及相应物质的性质。
考点一晶体常识和常见四种晶体性质[学在课内]1.晶体(1)晶体与非晶体晶体非晶体结构特征结构微粒周期性有序排列结构微粒无序排列性质特征自范性有无熔点固定不固定异同表现各向异性各向同性对固体进行X射线衍射实验(2)得到晶体的途径1熔融态物质凝固。
2气态物质冷却不经液态直接凝固(凝华)。
3溶质从溶液中析出。
(3)晶胞1概念:描述晶体结构的基本单元。
2晶体中晶胞的排列——无隙并置A.无隙:相邻晶胞之间没有任何间隙。
B.并置:所有晶胞平行排列、取向相同。
(4)晶格能1定义:气态离子形成1摩尔离子晶体释放的能量,通常取正值,单位:kJ·mol—1。
2影响因素A.离子所带电荷数:离子所带电荷数越多,晶格能越大。
B.离子的半径:离子的半径越小,晶格能越大。
3与离子晶体性质的关系晶格能越大,形成的离子晶体越稳定,且熔点越高,硬度越大。
[名师点拨](1)具有规则几何外形的固体不一定是晶体,如玻璃。
(2)晶胞是从晶体中“截取”出来具有代表性的“平行六面体”,但不一定是最小的“平行六面体”。
2.四种晶体类型的比较[考在课外]教材延伸判断正误(1)晶体和非晶体的本质区别是晶体中粒子在微观空间里呈周期性的有序排列。
高考化学总复习六 晶体结构与性质试题

目夺市安危阳光实验学校课时跟踪检测三十六晶体结构与性质(时间:45分钟满分:100分)一、选择题 (每小题6分,共36分)1.(联考)氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是( )A.AlON和石英的化学键类型相同B.AlON和石英晶体类型相同C.AlON和Al2O3的化学键类型不同D.AlON和Al2O3晶体类型相同解析:氮氧化铝(AlON)与石英均为原子晶体,所含化学键均为共价键;Al2O3为离子晶体,所含化学键为离子键,D项错误。
答案:D2.金属晶体、离子晶体、分子晶体和原子晶体的根本区别是( )A.基本构成微粒和微粒间的作用力不同B.外部形状不同C.金属晶体和原子晶体属于单质,分子晶体和离子晶体属于化合物D.基本构成微粒做周期性重复排列所遵循的规律不同解析:晶体之所以被分成不同的晶体类型,关键是根据构成晶体的粒子及粒子之间的作用力的不同,金属晶体的构成微粒是金属阳离子和自由电子,作用力是金属键;离子晶体的构成微粒是离子,作用力是离子键;原子晶体的构成微粒是原子,作用力是共价键;分子晶体的构成微粒是分子,作用力是分子间作用力,故选A项。
答案:A3.(南充诊断)下表所列物质晶体的类型全部正确的一组是( )原子晶体离子晶体分子晶体A 氮化硅磷酸单质硫B 单晶硅氯化铝白磷C 石烧碱冰D 铁尿素冰醋酸解析:A项,磷酸属于分子晶体;B项,氯化铝属于分子晶体;D项,铁属于金属晶体,尿素属于分子晶体。
答案:C4.有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )A.①为简单立方堆积,②为六方最密堆积,③为体心立方堆积,④为面心立方最密堆积B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个C.晶胞中原子的配位数分别为:①6,②8,③8,④12D.空间利用率的大小关系为:①<②<③<④解析:A项②为体心立方堆积,③为六方最密堆积,②、③颠倒,错误;B 项根据晶胞计算,每个晶胞含有的原子数分别为:①8×1/8=1个,②8×1/8+1=2个,③8×1/8+1=2个,④8×1/8+6×1/2=4个,正确;C项配位数是指晶胞中与原子紧邻的原子数,所以四种晶胞中原子的配位数分别为:①6,②8,③12,④12,错误;D项空间利用率是指晶胞在所含原子的体积与晶胞体积的比值,根据四种晶胞有空间利用率判断①<②<③=④,错误。
高中化学晶体的结构与性质专项训练专题复习附解析
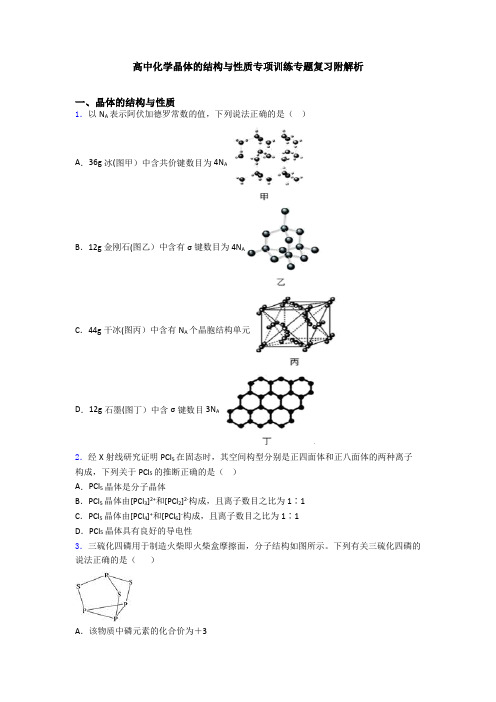
高中化学晶体的结构与性质专项训练专题复习附解析一、晶体的结构与性质1.以N A表示阿伏加德罗常数的值,下列说法正确的是()A.36g冰(图甲)中含共价键数目为4N AB.12g金刚石(图乙)中含有σ键数目为4N AC.44g干冰(图丙)中含有N A个晶胞结构单元D.12g石墨(图丁)中含σ键数目3N A2.经X射线研究证明PCl5在固态时,其空间构型分别是正四面体和正八面体的两种离子构成,下列关于PCl5的推断正确的是()A.PCl5晶体是分子晶体B.PCl5晶体由[PCl3]2+和[PCl2]2-构成,且离子数目之比为1∶1C.PCl5晶体由[PCl4]+和[PCl6]-构成,且离子数目之比为1∶1D.PCl5晶体具有良好的导电性3.三硫化四磷用于制造火柴即火柴盒摩擦面,分子结构如图所示。
下列有关三硫化四磷的说法正确的是()A.该物质中磷元素的化合价为+3B.22 g P4S3含硫原子数目约为1.806×1023C.该物质分子结构中S、P最外层电子数均不为8D.该物质分子中全是极性共价键4.对下列图形解释的说法错误的是()A.晶体金红石的晶胞如图1所示,推知化学式为TiO2(注:氧原子分别位于晶胞的上下底面和内部)B.配合物(如图2)分子中含有分子内氢键C.某手性分子如图3:可通过酯化反应让其失去手性D.可以表示氯化钠晶体,是氯化钠的晶胞5.下列性质中,能充分说明某晶体一定是离子晶体的是A.具有较高的熔点,硬度大B.固态不导电,水溶液能导电C.晶体中存在金属阳离子,熔点较高D.固态不导电,熔融状态能导电6.下列说法不正确的是()A.由于NaCl晶体和CsCl晶体中正负离子半径比不相等,所以两种晶体中离子的配位数不相等B.CaF2晶体中,Ca2+的配位数为8,F-的配位数为4,配位数不相等主要是由于F-、Ca2+所带电荷(绝对值)不相等C.MgO的熔点比MgCl2的高主要是因为MgO的晶格能比MgCl2大D.MCO3中M2+半径越大,MCO3晶体的晶格能越大7.下列叙述正确的是A.离子晶体中,只存在离子健,不可能存在其它化学键B.可燃冰中甲烷分子与水分子之间存在氢键C.Na 2O2、NaHSO4晶体中的阴、阳离子个数比均为12D.晶体熔点:金刚石>食盐>冰>干冰8.元素ⅹ位于第4周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有4个电子。
【四川专用】2014高考化学一轮复习第5章第4讲晶体结构与性质(68张PPT)

• 3.依据晶体的熔点判断 • (1)离子晶体的熔点较高,常在数百至一 千摄氏度以上。 • (2)原子晶体熔点高,常在一千摄氏度至 几千摄氏度。 • (3)分子晶体熔点低,常在数百摄氏度以 下至很低温度。 • (4)金属晶体多数熔点高,但也有相当低 的。
• 4.依据导电性判断
• •
•
(1)离子晶体溶于水形成的溶液及熔融状
金属单质 (金属晶体)
• 二、晶体常识 • 1.晶体与非晶体
晶体 非晶体
结构特征
性质 特征 两者 区别 方法 自范性 熔点
异同表现 间接方法
科学方法
结构微粒 结构微粒 周期性有序 排列 无序 排列 ___________ 有 无 固定 不固定 各向异性 各向同性 熔点 看是否有固定的____ 对固体进行X 射线衍射实验
•
• • •
பைடு நூலகம்
•
• 必考点46 晶体类型的判断方法 1.依据构成晶体的微粒和微粒间的作用判 断 (1)离子晶体的构成微粒是阴、阳离子, 微粒间的作用是离子键。 (2)原子晶体的构成微粒是原子,微粒间 的作用是共价键。 (3)分子晶体的构成微粒是分子,微粒间 的作用为分子间作用力。 (4)金属晶体的构成微粒是金属阳离子和 自由电子,微粒间的作用是金属键。
第三讲 晶体结构与性质
• 1.理解离子键的形成,能根据离子化合物 的结构特征解释其物理性质。 • 2.理解金属键的含义,能用金属键理论解 释金属的一些物理性质。 • 3.了解原子晶体的特征,能描述金刚石、 二氧化硅等原子晶体的结构与性质的关系。 • 4.了解分子晶体与原子晶体、离子晶体、 金属晶体的结构微粒、微粒间作用力的区 别。
•
固体物质都是晶体吗?
玻璃属于晶体吗? • 提示 不是。固体物质可分为晶体与非 晶体。玻璃属于一种特殊的固体叫做玻璃 态物质。
2024-2025学年高考化学一轮复习专题卷: 晶体结构与性质(含解析)

2025届高考化学一轮复习专题卷: 晶体结构与性质一、单选题1.下列推论正确的( )A.的沸点高于,可推测的沸点高于B.为正四面体结构,可推测出也为正四面体结构C.晶体是分子晶体,可推测晶体也是分子晶体,D.是碳链为直线型的非极性分子,可推测也是碳链为直线型的非极性分子2.有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )A.①为简单立方堆积②为六方最密堆积③为体心立方堆积④为面心立方最密堆积B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个C.晶胞中原子的配位数分别为:①6,②8,③8,④12D.空间利用率的大小关系为:①<②<③<④3.下列叙述错误的是( )A.金属键无方向性和饱和性,原子配位数较高B.晶体尽量采取紧密堆积方式,以使其变得比较稳定C.因共价键有饱和性和方向性,所以原子晶体不遵循“紧密堆积”原理D.金属铜和镁均以ABAB…方式堆积4.环六糊精(D-吡喃葡萄糖缩合物)具有空腔结构,腔内极性较小,腔外极性较大,可包合某些分子形成超分子。
图1、图2和图3分别表示环六糊精结构、超分子示意图及相关应用。
下列说法错误的是( )4SiH 4CH 3PH 3NH 4NH +4PH +2CO 2SiO 26C H 38C HA.环六糊精属于寡糖B.非极性分子均可被环六糊精包合形成超分子C.图2中甲氧基对位暴露在反应环境中D.可用萃取法分离环六糊精和氯代苯甲醚5.下列反应的离子方程式正确的是( )A.去除废水中的:B.过氧化钠在潜水艇中作为的来源:C.沉淀溶于氨水:D.在溶液中滴加少量溶液:6.碳硼烷酸是一类超强酸,也是唯一能质子化富勒烯(如)但不会将其分解的酸,2Na S 2Hg +2+2-Hg +S HgS ↓2O 22222O 2H O 4OH O --++↑AgCl ()332AgCl 2NH Ag NH Cl⎡⎤+⎣⎦NaOH ()442NH AlSO ()34Al 4OHAl OH -+-⎡⎤+⎣⎦60C其结构如图所示。
第04讲 晶体结构与性质(课件)-2025年高考化学一轮复习讲练测(新教材新高考)

2024山东卷第4题,3分;2024甘肃卷第12题,3分;2024贵州卷第8题,3分;2023湖南卷第11题,3分;2022湖北卷第9题,3分;2021山东卷第9题,2分
考情分析
分析近三年高考试题,高考命题在本讲有以下规律:1.从考查题型和内容上看,高考命题以非选择题呈现,考查内容主要有以下两个方面:(1)晶体类型的判断,晶体熔沸点大小的判断。(2)晶体的密度、晶胞参数、核间距计算、晶体中原子的空间位置(原子坐标)判断。2.从命题思路上看,侧重以陌生物质的晶胞结构为情境载体考查晶体的密度、晶胞参数计算、晶体中原子的空间位置判断等。3.根据高考命题的特点和规律,复习时要注意以下几个方面:(1)晶胞中配位数、微粒间距离及原子分数坐标判断。(2)晶体化学式的计算及晶体密度的计算。(3)晶体类型的判断、熔点差形,而非晶体没有。
(2)平面上的投影图如图所示________。
测定熔点是否固定:晶体有固定熔点,而非晶体没有。鉴别晶体与非晶体的方法
3.体心立方晶胞结构模型的原子分数坐标与投影图
(1)原子分数坐标:的分数坐标为_______, 9的分数坐标为________。
周期性重复
杂乱无章的分布
排列
(1)构成物质三态的粒子不一定都是______,还可以是______或______等,如水的三态都是由分子构成的,离子液体是熔点不高的仅由离子组成的液体物质。
分子
原子
离子
(2)物质的聚集状态除了____态、____态和____态,还有____态、______态,以及介于晶态和非晶态之间的______态、______态等。
B.已知晶胞结构求空间利用率
③面心立方结构
如图所示,原子的半径为,面对角线为个晶胞中有4个原子,则空间利用率______。
2022届新教材高考化学一轮复习课时练16晶体结构与性质含解析新人教版202106071263

课时规范练16 晶体结构与性质基础巩固1.下列关于晶体的结构和性质的叙述正确的是( )B.共价晶体中共价键越强,熔点越高C.离子晶体中含有离子键,不含有共价键2.(2020四川成都月考)下列有关晶体结构的叙述中错误的是( )A.金刚石的网状结构中,最小的环上有6个碳原子B.分子晶体熔化时,不破坏共价键;共价晶体熔化时,破坏共价键C.在金属铜的晶体中,由于存在自由电子,因此铜能导电D.在氯化铯晶体中,每个氯离子周围最近且距离相等的氯离子有8个3.下列性质适合分子晶体的是( )A.熔点为1 070 ℃,易溶于水,水溶液导电B.熔点为3 500 ℃,不导电,质硬,难溶于水和有机溶剂,熔点为112.8 ℃,沸点为444.6 ℃2D.熔点为97.82 ℃,质软,导电,密度为0.97 g·c m-34.(2020重庆质检)下列排序不正确的是( )A.熔点由高到低:Na>Mg>AlB.硬度由大到小:金刚石>碳化硅>晶体硅C.晶体熔点由低到高:CO<KCl<SiO2D.熔点由高到低:NaF>NaCl>NaBr>NaI5.(2020湖南长沙模拟)下面有关晶体的叙述中,不正确的是( )B.氯化钠晶体中,每个Na+周围距离相等且最近的Na+共有6个C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子6.某离子晶体的晶胞如图所示。
A为阴离子,在晶胞内部,B为阳离子,分别在顶点和面心,则该晶体的化学式为( )A22A44A777.(2020重庆模拟)现有几组物质的熔点(℃)数据:据此回答下列问题:(1)A组属于晶体,其熔化时克服的微粒间的作用力是。
(2)B组晶体共同的物理性质是(填序号)。
①有金属光泽②导电性③导热性④延展性(3)C组中HF熔点反常是由于。
(4)D组晶体可能具有的性质是(填序号)。
①硬度小②水溶液能导电③固体能导电④熔融状态能导电能力提升8.(双选)已知干冰晶胞结构中CO2分子在正方体的顶点和面心位置,晶胞中相邻最近的两个CO2分子间距为a pm,阿伏加德罗常数的值为N A,下列说法正确的是( )分子的配位数是122g·c m-3N(2√2a3×10-30)分子2分子的空间结构是直线形,中心碳原子的杂化轨道类型是sp3杂化29.(2020山东化学,4)下列关于C、Si及其化合物结构与性质的论述错误的是( )A.键能C—C>Si—Si、C—H>Si—H,因此C2H6稳定性大于Si2H6B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度中Si的化合价为+4,CH4中C的化合价为-4,因此SiH4还原性小于CH44D.硅原子间难形成双键而碳原子间可以,是因为Si的原子半径大于C,难形成p-p π键10.(双选)(2020江苏连云港质检)下表是物质对应的熔点(℃):下列判断错误的是( )和干冰是分子晶体311.硅酸盐与二氧化硅一样,都以硅氧四面体作为基本结构单元。
2020高考化学:晶体结构与性质练习含答案

2020高考化学:晶体结构与性质练习含答案主题:晶体结构与性质一、选择题1、下列有关晶胞的叙述中正确的是( )A.晶胞的结构是晶体的结构B.不同的晶体中,晶胞的大小和形状都相同C.晶胞中的任何一个粒子都完全属于该晶胞D.已知晶胞的组成就可推知晶体的组成答案D解析由晶胞的定义可知A项错误;相同晶体中晶胞的大小和形状完全相同,不同晶体中,晶胞的大小和形状不一定相同,B项错误;晶体中的大部分粒子被若干个晶胞所共有,不完全属于某个晶胞,C项错误;知道晶胞的组成,利用“均摊法”即可推知晶体的组成,D项正确。
2、甲烷晶胞结构如图所示,下列说法正确的是( )A.甲烷晶胞中的球只代表1个C原子B.晶体中1个CH4分子周围有12个紧邻的CH4分子C.甲烷晶体熔化时需克服共价键D.1个CH4晶胞中含有8个CH4分子答案B解析 题图所示的甲烷晶胞中的球代表的是1个甲烷分子,并不是1个C 原子,A 项错误;由甲烷的一个晶胞分析可知,与位于晶胞顶点的甲烷分子距离最近且相等的甲烷分子有3个,而这3个甲烷分子在晶胞的面心上,因此被2个晶胞所共用,故与1个甲烷分子紧邻的甲烷分子数目为3×8×12=12,B 项正确;甲烷晶体是分子晶体,熔化时需克服范德华力,C 项错误;甲烷晶胞属于面心立方晶胞,该晶胞中甲烷分子的数目为8×18+6×12=4,D 项错误。
3、金刚石具有硬度大、熔点高等特点,大量用于制造钻头、金属切割刀具等。
其结构如图所示,下列判断正确的是( )A .金刚石中C —C 键的键角均为109°28′,所以金刚石和CH 4的晶体类型相同B .金刚石的熔点高与C —C 键的键能无关C .金刚石中碳原子个数与C —C 键键数之比为1∶2D .金刚石的熔点高,所以在打孔过程中不需要进行浇水冷却答案 C解析 A 项,金刚石是原子晶体,CH 4是分子晶体,二者的晶体类型不同;B 项,金刚石熔化过程中C —C 键断裂,因C —C 键的键能大,断裂时需要的能量多,故金刚石的熔点很高;C 项,金刚石中每个C 都参与了4个C —C 键的形成,而每个C 对每条键的贡献只有一半,故碳原子个数与C —C 键键数之比为⎝ ⎛⎭⎪⎫4×12∶4=1∶2;D 项,金刚石的熔点高,但在打孔过程中会产生很高的温度,如不浇水冷却钻头,会导致钻头熔化。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四讲晶体结构与性质一、选择题(本题共7个小题,每题6分,共42分。
每个小题只有一个选项符合题意) 1.下列有关晶体的叙述中,错误的是()。
A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子B.氯化钠晶体中,每个Na+周围距离相等且最近的Na+共有6个C.金属晶体中,以“……ABCABCABC……”形式的堆积称为面心立方堆积D.干冰晶体中,每个CO2分子周围距离相等且最近的CO2分子共有12个解析NaCl晶体中,Na+周围最近的Na+在小立方体的面对角线上,故有12个Na+最近且等距离。
答案 B2.下列关于晶体的说法,一定正确的是( )。
CaTiO3的晶体结构模型(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角)A.分子晶体中都存在共价键B.如上图,CaTiO3晶体中每个Ti4+和12个O2-相紧邻C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合D.金属晶体的熔点都比分子晶体的熔点高解析稀有气体为单原子分子,晶体中不存在共价键。
据图可知CaTiO3晶体中,Ti4+位于晶胞的顶角,O2-位于晶胞的面心,故Ti4+的O2-配位数为12。
SiO2晶体中每个硅原子与四个氧原子相连。
汞常温下为液态,其熔点比一般分子晶体还低。
答案 B3.(2013·广安质检)下面的排序不正确的是( )。
A.晶体熔点的高低:>B .硬度由大到小:金刚石>碳化硅>晶体硅C .熔点由高到低:Na>Mg>AlD .晶格能由大到小:NaF>NaCl>NaBr>NaI解析 A 项形成分子间氢键的熔、沸点要大于形成分子内氢键的物质,正确;B 项均为原子晶体,原子半径越小,键长越短共价键越牢固,硬度越大,键长有:C —C<C —Si<Si —Si ,故硬度相反,正确;C 项均为金属晶体,熔点大小取决于原子半径大小以及阳离子所带电荷数,其规律是离子半径越小,所带电荷数越多,熔点越高,则熔点Al>Mg>Na ,C 不正确;晶格能越大,则离子键越强,离子所带电荷相同时离子键的强弱与离子半径有关,半径越小,则离子键越强,D 项正确。
答案 C4.现有四种晶体的晶胞,其离子排列方式如下图所示,其中化学式不属MN 型的是( )。
解析 由均摊法可得A 、C 、D 晶胞的M 与N 的个数比为1∶1,而B 晶胞中M 与N 的个数比为1∶3,故B 项不属于MN 型。
答案 B5.钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。
钛酸钡晶体的晶胞结构示意图如图所示,它的化学式是 ( )。
A .BaTi 8O 12B .BaTi 4O 6C .BaTi 2O 4D .BaTiO 3解析 由晶胞结构示意图可知,Ba 在立方体的中心,完全属于该晶胞;Ti 处于立方体的8个顶点,每个Ti 有18属于该晶胞;O 处于立方体的12条棱的中点,每个O 有14属于该晶胞。
即晶体中N (Ba)∶N (Ti)∶N(O)=1∶⎝ ⎛⎭⎪⎫8×18∶⎝⎛⎭⎪⎫12×14=1∶1∶3。
答案 D6.(2013·南充调研)某无机化合物的二聚分子结构如图,该分子中A 、B 两种元素都是第三周期的元素,分子中所有原子最外层都达到8电子稳定结构。
下列关于该化合物的说法不正确的是 ( )。
A .化学式是Al 2Cl 6B .不存在离子键和非极性共价键C .在固态时所形成的晶体是分子晶体D .是离子化合物,在熔融状态下能导电解析 由题意知该化合物为分子晶体,A 为Cl ,B 为Al ,分子的结构式为,存在极性键和配位键。
答案 D7.已知NaCl 的摩尔质量为58.5 g·mol -1,其晶体密度为d g·cm -3,若图中钠离子与最接近的氯离子的核间距离为a cm ,那么阿伏加德罗常数的值可表示为 ( )。
A .117a 3dB .58.5/(2a 3d ) C .234/(a 3d )D .58.5/(4a 3d ) 解析 a 3·dN A =12×58.5,N A =58.52a d。
答案 B二、非选择题(本题共4个小题,共58分)8.(14分)铜及其合金是人类最早使用的金属材料。
(1)铜原子的核外电子排布式是________________。
(2)铜的熔点比钙的高,其原因是________________;如图是金属Ca 和Cu 所形成的某种合金的晶胞结构示意图,则该合金中Ca 和Cu 的原子个数之比为________。
(3)Cu 2+能与NH 3、H 2O 、Cl -等形成配位数为4的配合物。
①[Cu(NH 3)4]2+中存在的化学键类型有________(填序号)。
A .配位键B .金属键C .极性共价键D .非极性共价键E .离子键②[Cu(NH 3)4]2+具有对称的空间构型,[Cu(NH 3)4]2+中的两个NH 3被两个Cl -取代,能得到两种不同结构的产物,则[Cu(NH 3)4]2+的空间构型为________。
解析 (1)铜元素原子的核外电子排布满足“全空、半满、全满稳定”的原理。
(2)金属的物理性质主要取决于金属键的强弱,一般金属键越强,金属的硬度越大、熔点越高;该晶胞中顶点的原子按18计,面上的原子按12计。
(3)[Cu(NH 3)4]2+中Cu 2+和NH 3之间形成配位键,NH 3内形成极性共价键。
[Cu(NH 3)4]2+的立体构型可以参照甲烷的立体构型考虑,若为正四面体形,则[Cu(NH 3)4]2+中的两个NH 3被两个Cl -取代后所得配合物只有一种,若为平面正方形则[Cu(NH 3)4]2+中的两个NH 3被两个Cl -取代后所得配合物有两种。
答案 (1)1s 22s 22p 63s 23p 63d 104s 1或[Ar]3d 104s 1(2)晶体中铜的金属键强度大于钙的 1∶5(3)①AC ②平面正方形9.(14分) (2013·资阳联考)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)请写出元素d 的基态原子电子排布式________________________________________________________________________。
(2)b 元素的氧化物中b 与氧元素之间的共价键类型是________。
其中b 原子的杂化方式是________。
(3)a 单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
若已知a 的原子半径为d ,N A 代表阿伏加德罗常数,a 的相对原子质量为M r ,则一个晶胞中a 原子的数目为________,该晶体的密度为________(用字母表示)。
解析 (1)根据洪特规则的特例,d 轨道半充满时更稳定,其Cr 原子电子排布式是1s 22s 22p 63s 23p 63d 54s 1而不是1s 22s 22p 63s 23p 63d 44s 2。
(2)SiO 2硅氧之间的共价键是“头对头”的方式,所以是σ键,其中Si 的杂化方式是sp 3杂化。
(3)由分摊法计算:8×18+6×12=4;该晶胞的质量m =4×M r N A,该晶胞的体积V =⎝ ⎛⎭⎪⎫4×d ×223=162d 3,晶胞密度ρ=m V =M r 42d 3N A。
答案 (1)1s 22s 22p 63s 23p 63d 54s 1或[Ar]3d 54s 1 (2)σ键或极性共价键 sp 3杂化 (3)4 M r 42d 3N A10.(15分)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
请回答下列问题:(1)Ni 原子的核外电子排布式为_____________________________;(2)NiO 、FeO 的晶体结构类型均与氯化钠的相同,Ni 2+和Fe 2+的离子半径分别为69 pm 和78 pm ,则熔点NiO________FeO(填“<”或“>”);(3)NiO 晶胞中Ni 和O 的配位数分别为________、________;(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图所示。
该合金的化学式为________。
解析 (1)核外电子排布式与价电子排布式要区别开。
(2)NiO 、FeO 都属于离子晶体,熔点高低受离子键强弱影响,离子半径越小,离子键越强,熔点越高。
(3)因为NiO 晶体结构类型与NaCl 相同,而NaCl 晶体中Na +、Cl -的配位数都是6,所以,NiO 晶体Ni 2+、O 2-的配位数也是6。
(4)根据晶胞结构可计算,一个合金晶胞中,La :8×18=1,Ni :1+8×12=5。
所以该合金的化学式为LaNi 5。
答案 (1)[Ar]3d 84s 2或1s 22s 22p 63s 23p 63d 84s 2(2)> (3)6 6 (4)LaNi 511.(15分) (2013·攀枝花模拟)可以由下列反应合成三聚氰胺:CaO +3C=====高温CaC 2+CO↑,CaC 2+N 2=====高温Ca CN 2+C ,CaCN 2+2H 2O===NH 2CN +Ca(OH)2,NH 2CN 与水反应生成尿素[CO(NH 2)2],尿素合成三聚氰胺。
(1)写出与Ca 在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:_____________________________________________。
CaCN 2中阴离子为CN 2-2,与CN 2-2互为等电子体的分子有N 2O 和________(填化学式),由此可以推知CN2-2的空间构型为________。
(2)尿素分子中C原子采取________杂化。
尿素分子的结构简式是________。
(3)三聚氰胺()俗称“蛋白精”。
动物摄入三聚氰胺和三聚氰酸()后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________。
CaO晶体和NaCl晶体的晶格能分别为:CaO 3 401 kJ·mol-1、NaCl 786 kJ·mol-1。
导致两者晶格能差异的主要原因是___________________________________________________________________________ _______________________________________________________________。
