化工原理干燥过程和物料及热量衡算
化工原理物料衡算和热量衡算

化工原理物料衡算和热量衡算引言化工工程涉及许多物料的处理和转化过程,同时也需要考虑热量的平衡。
物料衡算和热量衡算是化工原理的重要内容,对于工程实践和过程优化具有重要的意义。
本文将介绍化工原理中的物料衡算和热量衡算的基本原理和计算方法。
物料衡算物料衡算是指对于化工工程中物料流动和转化过程的计算和分析。
在化工工程中,物料的流动和转化是实现各种反应和分离操作的基础,因此正确的物料衡算是保证工程设计和操作的关键。
在物料衡算中,我们通常需要考虑以下几个方面: 1. 物料的质量衡算:即对物料的质量输入和输出进行计算和分析。
对于物料的质量衡算,我们需要注意物料流动的平衡原则,即质量的输入必须等于输出。
2. 物料的能量衡算:即对物料的能量输入和输出进行计算和分析。
能量的输入和输出会影响物料的温度和相变过程,因此在能量衡算中需要考虑物料的热力学性质。
3. 物料的流动速度衡算:即对物料流动速度进行计算和分析。
物料的流动速度决定了反应和分离操作的效率,因此在物料衡算中需要合理地确定流量和速度的关系。
4. 物料的浓度衡算:即对物料中组分浓度的计算和分析。
物料的浓度会影响其反应和分离的速率和效果,因此在物料衡算中需要考虑不同组分浓度的变化规律。
物料衡算通常使用质量守恒和能量守恒等基本原理进行计算。
同时,还可以利用化学反应平衡的原理和质量流动的平衡原则进行衡算过程中的参数确定。
热量衡算热量衡算是化工工程中热力学过程的计算和分析。
在化工工程中,热量的平衡是保证反应和分离操作能够正常进行的基础。
热量衡算需要考虑以下几个方面: 1. 热量的输入和输出:即对于热量的输入和输出进行计算和分析。
在化工工程中,我们通常需要对热量的输入和输出进行平衡,以保证工程操作的稳定性。
2. 热量的传递和转化:即对于热量的传递和转化过程进行计算和分析。
热量的传递可以通过传导、对流和辐射等方式进行,因此在热量衡算中需要考虑传热方式的影响。
3. 热平衡的计算:即对于反应和分离过程中热量平衡的计算和分析。
化工原理 PPT 第5章 干燥

k H rt w
( H s ,t w H )
:空气向湿棉布的对流传热系数,W/(m2 •℃);
k H :以湿度差为推动力的传质系数,kg/(m2 •s•H);
rtw
H
:湿球温度下水的汽化潜热,kJ/kg水;
H s ,tw:湿球温度tw下空气的饱和湿度,kg水/kg绝干气;
:空气的湿度, kg水/kg绝干气。
30
(2)湿空气状态点的确定
31
(3)简单分析:
a.当H、p一定时, 。 t
因此,提高湿空气温度 t,不仅提高了湿 空气的焓值,使其作为载热体外,也降低了相
对湿度使其作为载湿体。
pv b.因pv py、ps f t 及 100% pS 故t一定时,p ,故加压对干燥不利。
H f ( p,pV )
当p为一定值时,
H f ( pV )
当空气达到饱和时,相应的湿度称为饱和湿度 Hs,此时湿空气中的水汽分压等于该空气温度下纯 水的饱和蒸气压 ps。
0.622pS HS p-pS
即:
H S f (t,p)
10
2.相对湿度百分数(简称相对湿度) 定义:在一定总压下,湿空气中水汽分压pV与同
20
影响湿球温度tw的三方面因素: ①物系性质:与α 、 kH有关的物性; ②空气状态:t、H; ③流动条件: α/kH 。 实验表明,α与 kH都与空气速度的 0.8次幂成正比,故α与kH之比值与流速 无关,只与物性有关。当物系已确定, 则物系性质就不再改变,此时,湿球温 度只与气相状态有关,即:
tas :是由热量衡算与物料衡算导出的,属于静平衡。
• tw与tas 数值上的差异取决于α/kH与cH两者之间的差别。 (1)空气—水蒸气体系, c H ,r0 rt 得 t w t as w kH (2)空气—甲苯体系, k 1.8c H ,tw tas
第八章干燥四、干燥的能量衡算

干燥过程的能量衡算
热量衡算:
预热器提供的热量QP
干燥器输入的热量QD 整个干燥系统的总传热量Q 干燥器的热效率和干燥效率 空气通过干燥器时的状态变化
主讲教师:沈吉林
1
化工原理
热量衡算:
连续干燥过程的热量衡算示意图 主讲教师:沈吉林
2
化工原理
热量衡算:
主讲教师:沈吉林
3
化工原理
热量衡算:
上式称为连续干燥系统热量衡算基本方程式
主讲教师:沈吉林
8
化工原理
热量衡算: 分析
加热干燥系统的总热量Q主要用于
加热空气 加热并汽化水分
L 1.01 1.88H 0 (t2 t0 )
W (2490 1.88t2 4.1871 )
加热湿物料
热损失 主讲教师:沈吉林
GCm (2 1 )
主讲教师:沈吉林
6
化工原理
热量衡算: 湿物料的焓的表示:
以0℃液态湿分及固体的焓为0,则以1kg 绝干物料为基准的焓:
I ' (Cs XCw ) ; C s : 绝干物料的比热 ;
C w : 水分的比热 ; Cm : 湿物料的比热 ;
' LI1 G I1' QD LI 2 G I 2 QL
干燥器
t0=20℃ W2=0.2%,θ2=60℃ Cs=3.5kJ/kg.℃
QD
解:(1)新鲜空气用量,kg/h;
X1 w1 0.03 0.03093 1 w1 1 0.03 X2 w2 0.002 0.002 1 w2 1 0.002
G G1 (1 w1 ) 1200 (1 0.03) 1164 kg / h
(整理)化工原理—干燥.

第九章干燥本章学习要求1.熟练掌握的内容湿空气的性质及其计算;湿空气的湿度图及其应用;连续干燥过程的物料衡算与热量衡算;恒定干燥条件下的干燥速率与干燥时间计算。
2.理解的内容湿物料中水分的存在形态及其;水分在气-固两相间的平衡关系;干燥器的热效率;各种干燥方法的特点;对干燥器的基本要求。
3.了解的内容常用干燥器的主要结构特点与性能;干燥器的选用。
* * * * * * * * * * * *§9.1 概述干燥是利用热能除去固体物料中湿分(水分或其它液体)的单元操作。
在化工、食品、制药、纺织、采矿、农产品加工等行业,常常需要将湿固体物料中的湿分除去,以便于运输、贮藏或达到生产规定的含湿率要求。
例如,聚氯乙烯的含水量须低于0.2%,否则在以后的成形加工中会产生气泡,影响塑料制品的品质;药品的含水量太高会影响保质期等。
因为干燥是利用热能去湿的操作,能量消耗较多,所以工业生产中湿物料一般都采用先沉降、过滤或离心分离等机械方法去湿,然后再用干燥法去湿而制得合格的产品。
一、固体物料的去湿方法除湿的方法很多,化工生产中常用的方法有:1.机械分离法。
即通过压榨、过滤和离心分离等方法去湿。
耗能较少、较为经济,但除湿不完全。
2.吸附脱水法。
即用干燥剂(如无水氯化钙、硅胶)等吸去湿物料中所含的水分,该方法只能除去少量水分,适用于实验室使用。
3.干燥法。
即利用热能使湿物料中的湿分气化而去湿的方法。
该方法能除去湿物料中的大部分湿分,除湿彻底。
干燥法耗能较大,工业上往往将机械分离法与干燥法联合起来除湿,即先用机械方法尽可能除去湿物料中的大部分湿分,然后再利用干燥方法继续除湿而制得湿分符合规定的产品。
干燥法在工业生产中应用最为广泛,如原料的干燥、中间产品的去湿及产品的去湿等。
二、干燥操作方法的分类1、按操作压强分为常压干燥和真空干燥。
真空干燥主要用于处理热敏性、易氧化或要求产品中湿分含量很低的场合。
2、按操作方式分为连续操作和间歇操作。
干燥过程中的物料衡算和热量衡算

干燥过程中的物料衡算和热量衡算
式中qmw——水分的蒸发量,kg水分/s qmc——绝干物料 的质量流量,kg绝干料/s L——绝干空气的消耗量,kg绝干气/s H1,H2——分别为空气进出干燥器时的湿度,kg/kg绝干气; X1,X2——分别为湿物料进出干燥器的干基含水量,kg水分/kg
q′m1,q′m2——分别为湿物料进出干燥器的流量,kg物料/s。
Q=Qp+QD=L(I2-I0)+qmc (I′2-I′1)+QL
(9-24) (9-25)
(9-26)
干燥过程中的物料衡算和热量衡算
式中H0,H1,H2——湿空气进入预热器、离开预热器(即进 入干燥器)及离开干燥器时的湿度,kg/kg
I0,I1,I2——分别为湿空气进入预热器、离开预热器(即进 入干燥器)及离开干燥器时的焓,kg/kg
干燥过程中的物料衡算和热量衡算
图9-8 各流股进出逆流干燥器的示意图
干燥过程中的物料衡算和热量衡算
(1)对预热器进行热量衡算
LI0+Qp=LI1
(9-23)
在预热器中,空气的状态变化是等湿升温过程,即H1=H0,故预热器
Qp=L(I1-I0)=L(1.01+1088H0)(t1-t0) (2
QD=L(I2-I1)+qmc (I′ 2-I′1)+QL (3
干燥过程中的物料衡算和热量衡算
一般干燥过程,湿空气中水汽的量(H0)相对于绝干空气来 说,数值较小,同时湿物料进入干燥器的温度偏低。若忽略空气 中水汽进出干燥系统的焓变1.88H(t2-t0)和湿物料中水分带入干 燥系统的焓4.18Wθ1,则Q=Qp+QD=1.01L(t2-t0)+qmcM (θ2θ1)+qmw (2490+1.88t2)+QL (9-29)
化工原理讲稿2(第五章)(天大版)

干物料] ②干基含水量 X [kg水/kg干物料 水 干物料
湿物料中水分质量 X = 湿物料中绝干物料质量 Gw = G − Gw
湿 物 料 中 绝 干 物 料 质 量 : G C = G − G w;
五、空气通过干燥器时的状态 一、等焓干燥过程 指绝热干燥过程或理想干燥过程; 指绝热干燥过程或理想干燥过程; —— 空气在进、出干燥器的焓值不变; 空气在进、出干燥器的焓值不变;
H ↑ I1 = (1.01 + 1.88 H1 ) t1 + 2490 H1 I1 = I 2 ;其中: t ↓ I 2 = (1.01 + 1.88 H 2 ) t2 + vH vH ( kg 水 k g 干 气 = kg 水 3 m 湿 气 k g干 气 m 3湿 气 )
t1 I2 其中: ⇒ I1 = I 2 ⇒ ⇒ 查 H − I图 ⇒ H H 0 = H1 ϕ 2 ⇒ ∆H = H 2 − H1
2
习题7: 习题 :
w1 X1 = 1 − w1 G = G(1 − w 2) W 2 1. ⇒ ⇒ L= ( a式 ) ; ( H 2 − H1 W = G X 1 − X 2) X = w2 2 1 − w2 ϕ 0 ps 0 a、 H 0 = H 1 = 0.622 ( t 0 → p s 0) p − ϕ 0 ps0 b、 干 燥 器 热 量 衡 算 : L ( I 1 − I 2 ) = G C ( I 2 ' − I 1 ' ) + Q( b 式 ) ; L
'' 3.V(风量) LvH ( m 3湿气 h ) =
天津大学版《化工原理》课件

17/68
§8-1干燥介质的性质及湿焓图
焓
kJ/kg
绝 干 气
=100% tas
水 气 分 压
kPa
H
kg水/kg绝干气
化工原理 干燥
材料与化学工程学院 化学工程教研室
18/68
§8-1干燥介质的性质及湿焓图
焓
kJ/kg
绝 干 气
=100%
水 气 分 压
kPa
H
kg水/kg绝干气
化工原理 干燥
材料与化学工程学院 化学工程教研室
19/68
§8-1干燥介质的性质及湿焓图
焓
kJ/kg
=100%
水 气 分 压
kPa
绝 干 气
H
化工原理 干燥
kg水/kg绝干气
20/68
材料与化学工程学院 化学工程教研室
§8-2 干燥过程的物料衡算和热量衡图
对于空气-水系统:
p H 0.622 P p
Mw=18.02kg/kmol,Mg=28.96 kg/kmol 总压一定时,湿气体的湿度只与湿份蒸汽的分压有关。
化工原理 干燥 材料与化学工程学院 化学工程教研室
6/68
§8-1干燥介质的性质及湿焓图
ps 饱和湿度 H s 0.622 P ps
H 0 H1 H 1 H 0 ( 1 ) H 1 0.05362kg( 苯 ) kg( 绝干氮气) H0
化工原理 干燥 材料与化学工程学院 化学工程教研室
13/68
§8-1干燥介质的性质及湿焓图
ps|T 283 K Mv H 1 H s|T 283 K H 1 M g P ' ps|T 283 K 2788.51 ps|T 283 K exp( 20.7936 ) 6.05kPa 283 52.36 P ' 320.4kPa
化工原理II考点

《化工原理II 》考点:1、p e =Ex2、T 与E 、溶解度的关系,例如T ↑ E ↑ 溶解度↓3、p e =cH ,y e =mx ,ss H M mp E ρ∙=≈ 特别注意:知道E ,p ——>m ,H由操作点与平衡线的位置,判断传质的方向;如果为气(液)膜控制,增大哪相的湍动利于传质?A<1(或A>1),塔无限高时,气液分别会在塔哪端达到平衡判断传质方向: 例如,知道气体的y ,与液体的C A 以及两相的平衡关系如P A *=HC A , 判断传质方向。
分子扩散的种类以及应用范围;吸收剂用量与传质推动力的关系;与操作线的变化;传质系数的计算,气膜控制、液膜控制的判断(知道气体的种类或k y , k x , m 两种情况) xy y k m k K +=11 yx x mk k K 111+= 例题: 在总压为100kPa 、温度为30℃时,用清水吸收混合气体中的氨,气相传质系数k G =3.84×10-6 kmol/(m 2·s·kPa ),液相传质系数k L =1.83×10-4 m/s ,假设此操作条件下的平衡关系服从亨利定律,测得液相溶质摩尔分率为0.05,其气相平衡分压为6.7kPa 。
求当塔内某截面上气、液组成分别为y =0.05,x =0.01时(1) 传质总推动力以及相应的总传质系数、传质速率;(2)分析该过程的控制因素。
吸收操作线方程式及其应用:)(22x G L y x G L y -+= 或:)(11x GL y x G L y -+= 最小液气比2121min )(x x y y G L e --=【2121min )(x m y y y G L --=】 [例题]在一常压逆流操作的吸收塔中,用清水吸收混合气体中的SO 2。
气体处理量为1.20m 3 (标准)•s -1,进塔气体中含SO 28%(体积百分数),要求SO 2的吸收率为85%,在该吸收操作条件下的相平衡关系y e =26.7x ,用水量为最小用量的1.5倍。
化工原理--干燥公式总结

1、湿空气的水汽分压 s p p φ= 相对湿度 * 饱和蒸汽压2、湿度绝干气绝干气总kg kg 03230.0kg kg 936.4100936.4622.0622.0=-⨯=-=p p p H3、密度 湿空气湿空气33HH m kg 06.1m kg 9737.00323.011=+=+=υρH湿空气的比体积()Pt H 5H 10013.1273273244.1772.0⨯⨯+⨯+=υ0.9737= m 3湿空气/kg 绝干气4、湿空气的H –I 图由180t =℃、100.009H H ==kg/kg 绝干气在H -I 图上确定空气状态点,由该点沿等I 线向右下方移动与80%φ=线相交,交点为离开干燥器时空气的状态点,由该点读出空气离开干燥器时的湿度20.027H =kg/kg 绝干气。
故1 m 3原空气获得的水分量为:原湿空气原湿空气33H12m kg 0214.0m kg 84.0009.0027.0=-=-υH H5、空气的焓 湿基物料的焓 ()11s 1187.4θX c I +=' 6、两混合气中绝干气的质量比为1:3,则 02m 134H H H +=02m 134I I I +=7、1 kg 绝干空气在预热器中焓的变化为:()绝干气绝干气kg kJ 61kg kJ 4310401=-=-=∆I I I1 m 3原湿空气焓的变化为:湿空气湿空气33Hm kJ 6.72m kJ 84.061==∆υI()00001.01 1.882490I H t H =+⨯+8、干基含水量绝干料绝干料kg kg 25.0kg kg 20100201111=-=-=w w X w 湿物料的湿基含水量绝干料绝干料kg kg 05263.0kg kg 510051222=-=-=w w X绝干物料()()hkg 800h kg 2.011000111=-=-=绝干料w G G蒸发水量 ()()hkg 9.157h kg 05263.025.080021水水=-=-=X X G W绝干空气用量 20()L H H W -= h kg 8.5444h kg 005.0034.09.15702绝干气绝干气=-=-=H H W L新鲜空气用量 L 0=()h kg 5472h kg 005.18.544410新鲜气新鲜气=⨯=+H L 9、预热器的加热量P 010(1.01 1.88)()Q L H t t =+-()01P I I L Q -=10、干燥器的热效率 ()2W 2490 1.88t Qη+=11、对干燥器做热量衡算得:12、恒速段干燥速率''1122L LI GI LI GI Q +=++''D 2121L ()()0Q L I I G I I Q =-+-+=c w tw()U t t αγ=-13、恒速干燥阶段干燥时间:14、降速段干燥时间:前提:降速干燥阶段干燥速率与物料的自由含水量(X —*X )成正比,因此,临界点处:15、总干燥时间:●9. 在一常压逆流的转筒干燥器中,干燥某种晶状的物料。
北京化工大学_《化工原理》_课件_第八章_干燥

返回
北京化工大学化工原理电子课件
本章主要讨论对流干燥,干燥介质是热 空气,除去的湿分是水分。
对流干燥是传热、传质同时进行的过程,
但传递方向不同,是热、质反向传递过程: 传热 方向 气 固 固 传质 气
推动力
温度差
水汽分压差
5
返回
北京化工大学化工原理电子课件
干燥过程进行的必要条件: * 物料表面水汽压力大于干燥介质中水汽分压;
空气—水体系,
kH 空气—甲苯体系,
cH
, t w t as
kH
c H ,tw tas
当空气为不饱和状态:t tw (tas) td; 当空气为饱和状态: t = tw (tas) = td。
30
返回
北京化工大学化工原理电子课件
8.1.2 空气的湿度图及其应用
11
pw pS
100%
即:
f ( pw,t )
返回
北京化工大学化工原理电子课件
当 φ =1时:
pw = ps,湿空气达饱和,不可作为干燥介质;
当 φ <1时:
pw < ps,湿空气未达饱和,可作为干燥介质。
φ越小,湿空气偏离饱和程度越远,干燥能力越大。
结论:
湿度 H 只能表示出水汽含量的绝对值,而
别被加热到50℃和120℃,求值 。
13
返回
北京化工大学化工原理电子课件
三、湿空气的比热与焓 1、湿比热(湿热)cH [kJ/kg干气•℃]
定义:在常压下,将1kg干空气和其所带有的Hkg水
汽升高温度1℃所需的热量。
cH cg cv H 1.01 1.88 H f ( H )
化工设计物料衡算与能量衡算

• 1.求燃料气组成以C作联系组分,燃烧前后碳原子数不 变,所以CO2mol数等于CH4的mol数,即CH4= 8.12mol,
• 需要氧气量为2×8.12=16.24mol。
• 计算进料的空气量,以N2作联系组分,由烟道气中的N2 可得进料中的总氧气量:72.28×20.92/79=19.14mol,
Φ=
×100%
限制组分的消耗量
(5) 收率
生成目的产物所消耗限制组分的量
η=
×100%
限制组分的输入量
η =xA· Φ
“独立”的含义
对有化学反应的过程,应写独立的反应方
程式或独立反应数。例如碳与氧的燃烧过
程 :C O2 CO2 ①
C
1 2
O2
CO
② ③
CO
1 2
O2
CO2
CO2 C 2CO
湿纸浆 浆: 0.29 水: 0.71
干燥器
干燥纸浆 浆:? 水:?
水分
• 例:每小时将20kmol含乙醇40%的酒精水溶液进 行精馏,要求馏出液中含乙醇89%,残液中含乙醇 不大于3%(以上均为摩尔分数),试求每小时馏出 液量和残液量。
• 解:由全塔物料衡算式可得
•
20 = D + W
(1)
• 20×0.4 = 0.89D + 0.03W
化工设计物料衡算与能 量衡算
2021年7月13日星期二
化工基础数据
化工计算以及化工工艺和设备设计中,要 用到有关化合物的物性数据。例如,进行化 工过程物料与能量衡算时,需要用到密度或 比容、沸点、蒸汽压、焓、热容及生成热等 等的物性数据;设计一个反应器时,则需要 知道化学反应热的数据;计算传热过程时, 需要导热系数的数据等等。
化工原理8章固体物料的干燥

r
t t as ( H H )
as
c
as
H
② 绝热饱和温度是状态函数
t、H
空气 补充水
tas f (t, H )
③ 绝热饱和过程可当作等焓处理
绝热饱和塔示意图
即空气的入口焓近似等于空气的出口焓。
(7) 干、湿球温度 ① 干球温度与湿球温度 干球温度:普通温度计测出的空气温度;
(4) 湿比热容 cH ( kJ/kg干空气C )
c c c H 1.011.88H
H
a
V
ca: 干空气比热容,约1.01 kJ/kg干空气·C; cv: 水蒸汽比热容,约1.88kJ/kg干空气·C。
(5) 湿比焓I ( kJ/kg干空气) 基准: 0C干空气、 0C时液态水的焓为零。
I cat (r0 cV )H (1.01 1.88H )t 2490H
或 qmW qmC ( X1 X 2 ) qm1w1 qm2w2
又 qm C qm1 (1 w1 ) qm 2 (1 w2 )
所以
q mW
qm1
w1 w2 1 w2
qm2
w1 w2 1 w1
(2)空气用量
进入和排出干燥器的湿分相等,故有:
qm C X 1 qmL H1 qm C X 2 qmL H 2
干燥过程: 利用热能除去固体物料中的湿分(水或其他溶剂)的单元操作。
机理 : 质量传递:湿份的转移,由固相到气相,以蒸汽分压为推动力。
热量传递: 由气相到固相,以温度差为推动力。
8.1.2 干燥过程的分类
常压干燥 操作压力 真空干燥
热空气
物料
t
间歇干燥 操作方式
连续干燥
化工原理内容总结(1)

化工原理内容总结绪论篇1.物料衡算、能量衡算步骤。
步骤:画出简单流程示意图,并用带箭头的简单线条表明物料的流入、流出关系,且标注已知流量和单位。
确定好衡算范围、衡算基准。
列出衡算式。
能量衡算的步骤:[1]列出已知条件,即物料衡算的量和选定的工艺参数[2]选定计算基准,一般以KJ/h 计[3]对输入、输出热量分项进行计算[4]列出热平衡方程式,求出传热介质的量[5]热量衡算式如下:Q1+Q2=Q3+Q4+Q5式中:Q1-所处理原料带入热量Q2-由加热剂(或制冷剂)传给设备(或物料)的热量Q3+-所处理的物料从设备中带走的热量Q4-消耗在设备上的热量Q5-设备向四周散发的热量(热损失)2.物料衡算式中,积累量等于0和积累量不等于0的情况判别?因为,输人物料的总和∑G i =输出物料的总和∑G0+累积的物料量∑G a积累量=0则:输人物料的总和=输出物料的总和属于稳态过程,一般连续不断的流水作业(即连续操作)为稳态过程,其特点是在设备的各个不同位置上,物料的流速、浓度、温度、压强等参数可各自不相同,但在同一位置上这些参数都不随时间而变。
积累量<>0,则属于非稳态过程,一般间歇操作(即分批操作)属于非稳态过程,在设备的同一位置上诸参数随时间而变。
3.国际单位制中的基本单位是哪七个?七个基本单位:长度(m)、质量(kg)、时间(s)、温度(k)、物质量(mol)、电流强度(A)、发光强度(烛光或坎德拉,cd)4.哪几个单元操作同时遵循传热和传质基本规律?哪几个遵循流体流动基本规律?各种单元操作依据不同的物理化学原理,采用相应的设备,达到各自的工艺目的。
对于单元操作,可从不同角度加以分类。
根据各单元操作所遵循的基本规律,将其划分为如下几种类型。
①遵循流体动力学基本规律的单元操作,包括流体输送、沉降、过滤、物料混合(搅拌)等。
②遵循热量传递基本规律的单元操作,包括加热、冷却、冷凝、蒸发等。
③遵循质量传递基本规律的单元操作,包括蒸馏、吸收、萃取、吸附、膜分离等。
化工原理 第七章 干燥课后习题及答案

第七章 干 燥湿空气的性质【7-1】湿空气的总压为.1013kP a ,(1)试计算空气为40℃、相对湿度为%60ϕ=时的湿度与焓;(2)已知湿空气中水蒸气分压为9.3kPa ,求该空气在50℃时的相对湿度ϕ与湿度H 。
解 湿空气总压.1013p k P a =(1).06ϕ=,40℃时水蒸气的饱和蒸气压.7375s p k P a = 湿度..../ (0673750622)0622002841013067375ssp H kg kgp p ϕϕ⨯==⨯=--⨯.水干气焓 ()..1011882492I H t H =++ (...)../= 10118800284402492002841133k J k g +⨯⨯+⨯= (2) 湿空气中水汽分压.93V p kPa = 50℃时水的饱和蒸气压.1234s p k P a = 相对湿度 ..9307541234V s p p ϕ===.湿度. (93)0622=062200629101393V Vp H kg kgp p =⨯=--.水/干气【7-2】空气的总压为101.33kPa ,干球温度为303K ,相对湿度%70ϕ=,试用计算式求空气的下列各参数:(1)湿度H ;(2)饱和湿度s H ;(3)露点d t ;(4)焓I ;(5)空气中的水汽分压V p 。
解 总压.,.101333033007p k P a t K ϕ====℃, (1) 30℃时,水的饱和蒸气压.4241s p k P a = 湿度... (0742410622)06220018810133074241ssp H kg kgp p ϕϕ⨯==⨯=--⨯..水/干气 (2) 饱和湿度 (4241)0622062200272101334241s s sp H kg kgp p ==⨯=--.水/干气(3)露点d t 时的饱和湿度.00188s H kg kg =水/干气.0622s s sp H p p =- (10133001882970622062200188)s s spH p kPaH ⨯===++从水的饱和蒸气压为 2.97kPa 查得水的饱和温度为23.3℃,故空气的露点.233℃d t =(4) .3000188t H kg kg ==℃,水/干气时,空气的焓为()..1011882492H H t H=++(...)../= 1011880018830249200188782kJ kg +⨯⨯+⨯=干气 (5) t=30℃时的.4241s p k P a =水汽分压 ...074241297V s p p kPa ϕ==⨯=【7-3】在总压为101.3kPa 下测得湿空气的干球温度为50℃,湿球温度为30℃,试计算湿空气的湿度与水汽分压。
化工原理:干燥

热空气
L , H1
W G1 G2 G(X1 X 2 ) L(H2 H1)
G G1(1 w1) G2 (1 w2 )
汽化W kg湿分所消耗绝干气体量 L
W
H2 H1
绝干气体比消耗
结论:
l L 1 W H2 H1
1.绝干气体比只与空气前后的湿度差有关,与空气经过的途 径无关. 2.从湿物料中需要除去的水分量W决定于物料的初始含水量 X1和干燥程度X2。干燥要求X2一定的情况下,初始含水量 X1愈高,W愈大,需要L愈大,操作费用愈高,因此,通常 湿物料在干燥之前先用能耗低的机械去湿法脱水,尽量降低 X1,以降低干燥操作费用。
湿度 H
解 : 由 t=62℃ 的 等 温 线 和 H=0.092 的 等 湿 度 线 可 以 确 定一个交点P:过P点的等 线上读得 =60%;
cH kJ/(kg绝干气
1.18
体·K)
cH ~ H = 100% = 60%
过P点的绝热冷却线与
=100%的等相对湿度线的交 点在横坐标上对应的值即为绝
cH cg 1 cv H
式中:cg — 绝干气体的比热,J/(kg绝干气体·℃); cv — 湿份蒸汽的比热,J/(kg湿份蒸汽·℃) 。
对于空气-水系统:
cg=1.005 kJ/(kg·℃),cv=1.884 kJ/(kg·℃)
cH 1.01 1.88H
6、湿空气的焓iH ( 或干基湿焓)
第八章 干 燥
第一节、概述
在工业生产中所得到的固态产品或半成品往往含有过多的水分 或有机溶剂 (湿份),要制得合格的产品需要除去固体物料中多 余的湿份。这种除去湿分的操作称为去湿。 例如: 制盐工业中,在过饱和的氯化钠溶液中生成的食盐晶粒; 塑料工业中,氯乙烯单体在水相中聚合制成的塑料颗粒; 食品工业中,由鲜牛奶制奶粉。
化工原理(天大版)干燥过程的物料衡算与热量衡算
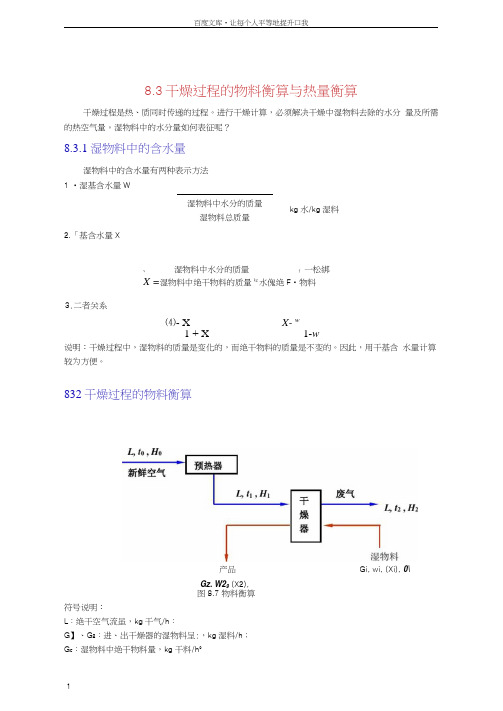
8.3干燥过程的物料衡算与热量衡算干燥过程是热、质同时传递的过程。
进行干燥计算,必须解决干燥中湿物料去除的水分 量及所需的热空气量。
湿物料中的水分量如何表征呢?8.3.1湿物料中的含水量湿物料中的含水量有两种表示方法1 •湿基含水量W2.「基含水量Xv 湿物料中水分的质量f 一松綁 X =湿物料中绝干物料的质量kg 水傀绝F •物料3.二者关系 ⑷- XX- w 1 + X1-w 说明:干燥过程中,湿物料的质量是变化的,而绝干物料的质量是不变的。
因此,用干基含 水量计算较为方便。
832干燥过程的物料衡算图8.7 物料衡算符号说明:L :绝干空气流虽,kg 干气/h :G 】、G 2:进、岀干燥器的湿物料呈:,kg 湿料/h ;G c :湿物料中绝干物料量,kg 干料/h°湿物料中水分的质量湿物料总质量kg 水/kg 湿料产品Gi, wi, (Xi), 0\ Gz. W29 (X2),目的:通过干燥过程的物料衡算,可确定岀将湿物料干燥到指左的含水量所需除去的水分量及所需的空气量。
从而确左在给定干燥任务下所用的干燥器尺寸,并配备合适的风机。
1.湿物料的水分蒸发量W[kg水/h]通过干燥器的湿空气中绝干空气虽:是不变的,又因为湿物料中蒸发岀的水分被空气带走,故湿物料中水分的减少呈等于湿物料中水分汽化虽等于湿空气中水分增加量。
即:[G,-G2 = G, vv,-G2w2=G c(X i-X2)] = [W] = [L(H2 - H.)]14;— IV w— u*所以:W=G|—G2=G| __ =Gj __-1 - w2 1 - W]2•干空气用ML|kg干气/h][kg干气/kg水]/称为比空气用量, 即每汽化lkg的水所需干空气的崑因为空气在预热器中为等湿加热,所以瓯山右 Z与空气的初、终湿度有关,而与路径无关,是状态函数。
湿空气用量: L =厶(1 +乩))kg湿气/h或/ =/(l + H0) kg 湿气/kg 水湿空气体积: V v = L U H m?湿气/h 或V. = Iu H m3湿气/kg水8.3.3干燥过程热量衡算通过干燥器的热量衡算,可以确泄物料干燥所消耗的热疑或干燥器排出空气的状态。
化工原理-干燥

湿球温度计工作原理分析 湿球温度是大量的未饱和空气 (t,H)高速通过湿球温度计湿 纱布表面时,湿纱布表面汽化 湿纱布表面汽化 水分所需的传热率等于空气传 入湿纱布的传热速率时的湿纱 布中水分稳定温度。此温度并 不代表空气的真实温度,但由 于此温度由湿空气的温度、湿 度所决定,故称它为湿空气的 湿球温度,以tw表示。
由上式可见,湿容积随其温度和湿度的增加而增大 由上式可见 湿容积随其温度和湿度的增加而增大。
14
4.比热容c 4.比热容cH [kJ/kg干气•℃] 比热容 在常压下, 干空气和其所带有的H 定义:在常压下,将1kg干空气和其所带有的 干空气和其所带有的 kg水汽升高(或降低)温度1℃所需的热量。 水汽升高(或降低)温度 ℃所需的热量。 水汽升高
当
pv < ps,湿空气未达饱和,可作为干燥介质。 湿空气未达饱和,可作为干燥介质。
当
pv = 0,湿空气中不含水分,为绝干空气。 ,湿空气中不含水分,为绝干空气。 ϕ 越小,干燥能力越大。 结论: 只能表示出水汽含量的绝对值, 结论:湿度 H 只能表示出水汽含量的绝对值, 而相对湿度却能反映出湿空气吸收水汽的能力。 而相对湿度却能反映出湿空气吸收水汽的能力。
2
干燥过程的分类: 干燥过程的分类:
操作压力 常压 真空
操作方式 连续 间歇
传热方式(或组合 传热方式 或组合) 或组合 导热 对流 辐射 介电加热
传导干燥(间接加热干燥) 传导干燥(间接加热干燥):
热能通过壁面以传导方式加热物料。
对流干燥(直接加热干燥) 对流干燥(直接加热干燥):
干燥介质与湿物料直接接触,并以对 流方式加热湿物料。
在与外界绝热情况下, 空气 在与外界绝热情况下 , 与大量水经过无限长时间接触后, 与大量水经过无限长时间接触后 , 空气温度与水温相等, 称这一稳 空气温度与水温相等, 定的温度为湿空气的绝热饱和温 定的温度为湿空气的 绝热饱和温 表示。 度,用tas表示。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
四、空气通过干燥器时的状态变化
1、等焓干燥过程(理想干燥过程 )
规定: •不向干燥器中补充热量QD=0; •忽略干燥器向周围散失的热量QL=0;
•物料进出干燥器的焓相等 GI2 I1 0
Q Qp QD LI2 I1 GI2 I1 QL LI1 I0 Qp LI1 I0
2020/7/10
QD LI1 I0 LI2 I0 GI2 I1 QL
将上述条件代入
I1 I2
I
t1
B I1 I2
C
t2
A
t0
H0
H
2020/7/10
2、非等焓干燥过程
1)操作线在过B点等焓线下方 条件: •不向干燥器补充热量QD=0; •不能忽略干燥器向周围散失的热量 QL≠0;
•物料进出干燥器时的焓不相等 G I2 I1 0
3、换算关系
X
1 X
X 1
2020/7/10
二、干燥系统的物料衡算
1、水分蒸发量
以s为基准,对水分作物料衡算
2020/7/10
LH1 GX1 LH2 GX2
W LH2 H1 GX1 X2
2、空气消耗量L
L GX1 X 2 W
H2 H1 H2 H1
每蒸发1kg水分时,消耗的绝干空气数量l
H2 H1
0.0363 0.005
2020/7/10
预热器的传热速率
Qp LcH (t1 t0 )
L1.011.88H0 t1 t0
0.9641.011.88 0.005140 25
113kJ / s
t2 40 ℃
H2 0.0447kg / kg干空气
L 0.76kg / s
Gcm 2 1 QL
2020/7/10
L W W H2 H1 H 2 H 0
Q
1.01Lt2
t0
W H2
H0
2490
1.88t2
H 2
H0
Gcm2 1 QL
1.01Lt2 t0 W 2490 1.88t2 Gcm2 1 QL
可见:向干燥系统输入的热量用于:加热空气;加热物料;
蒸发水分;热损失
第九章 干燥 Drying
第三节 干燥过程的物料与热
量衡算
一、湿物料中含水量的表示 方法
二、干燥系统的物料衡算 三、干燥系统的热量衡算 四、空气通过干燥器时的状
态变化
2020/7/10
一、湿物料中含水量的表示方法
1、湿基含水量W
水分质量
湿物料的总质量 2、干基含水量X
湿物料中水分的质量 X 湿物料中绝干气的质量
cm cs Xc
2020/7/10
2、干燥系统的热效率
蒸发水分所需的热量
向干燥系统输入的总热量 100%
蒸发水分所需的热量为
QV W 2490 1.88t2 4.1871W
忽略物料中水分带入的焓
QV W 2490 1.88t2
W 2490 1.88t2 100%
Q
2020/7/10
60
0.0363kg / kg干空气
2020/7/10
绝干物料量 :
GC G111 1 1 0.035 0.965kg / s
X1
1 1 1
3.5 0.0363kg水 / kg绝干料 96.5
X
2
0.5 1 0.5
0.00503kg水 /
kg绝干料
绝干空气量
L GC X 2 X 2 0.9650.0363 0.00503 0.964kg / s
2020/7/10
例:某种湿物料在常压气流干燥器中进行干燥,湿物料 的流量为1kg/s,初始湿基含水量为3.5%,干燥产品的湿基含 水量为0.5%。空气状况为:初始温度为25℃,湿度为 0.005kg/kg干空气,经预热后进干燥器的温度为140℃,若离 开干燥器的温度选定为60℃和40℃,
试分别计算需要的空气消耗量及预热器的传热速率。 又若空气在干燥器的后续设备中温度下降了10℃,试分析 以上两种情况下物料是否返潮?假设干燥器为理想干燥器。
2020/7/10
假设: •新鲜干空气中水汽的焓等于离开干燥器废气中水汽的焓
IV 0 IV 2 •湿物料进出干燥器时的比热取平均值 cm
湿空气进出干燥器时的焓分别为:
I0 cgt0 IV 0H0 I2 cgt2 IV 2H2
I2 I0 cg t2 t0 IV 2 H2 H0
2020/7/10
2020/7/10
l L 1 W H2 H1
3、干燥产品流量G2
对干燥器作绝干物料的衡算
G212 G111
G2
G1 1 1
12
2020/7/10
三、干燥系统的热量衡算
1、热量衡算的基本方程
忽略预热器的热损失,以1s为基准,对预热器列焓衡算
LI0 Qp LI1
2020/7/10
单位时间内预热器消耗的热量为:
I2 I0 cg t2 t0 r0 c02t2 H2 H0
1.01t2 t0 2490 1.88t2 H2 H0
湿物料进出干燥器的焓分别为
I1 cm11
I2 cm22
I2 I1 cm2 1
Q Qp QD LI2 I0 GI2 I1 QL
L1.01t2 t0 2490 1.88t2 H2 H0
当t2=40℃时,干燥器出口空气中水汽分压为
p2
101.33 0.0447 0.622 0.0447
6.79kPa
2020/7/10
t=30℃时,饱和蒸汽压ps=4.25kPa, p2 ps
物料可能返潮。
2020/7/10
Qp LI1 I0
对干燥器列焓衡算,以1s为基准
LI1 GI1 QD LI2 GI2 QL
单位时间内向干燥器补充的热量为
QD LI2 I1 GI2 I1 QL
单位时间内干燥系统消耗的总热量为
Q Qp QD LI2 I0 GI2 I1 QL
——连续干燥系统热量衡算的基本方程式
Qp 89kJ / s
2020/7/10
分析物料的返潮情况
当t2=60℃时,干燥器出口空气中水汽分压为
p2
PH2 0.622 H2
101.33 0.0363 5.59kPa 0.622 0.0363
t=50℃时,饱和蒸汽压ps=12.34kPa,ps p2
即此时空气温度尚未达到气体的露点,不会返潮。
2020/7/10
解:因在干燥器内经历等焓过程,IH1 IH 2
1.011.88H1t1 2490H1 1.011.88H2 t2 2490H2
t1 140℃ H1 H0 0.005kg / kg干空气
t2 60 ℃
H2
1.011.88 0.005140
1.88 60 2490
2490 0.005 1.01 1.88 60 2490
LI1 I0 LI2 I0
I1 I2
2020/7/10
I
C3
t1
B
I1
I2 C
C2
t2
C1
H
2020/7/10
2)操作线在过点B的等焓线上方
向干燥器补充的热量大于损失的热量加热物料消耗的
热量之总和
QD GI2 I1 QL
LI1 I0 LI2 I0
I1 I2
3)操作线为过B点的等温线 向干燥器补充的热量足够多,恰使干燥过程在等温下进行
