高中化学经典例题

2013《走向高考》化学总复习专题同步练习(氯气)
1.将氯水分别滴入下列溶液中,由实验现象得出的结论正确的是
选项氯水滴入下列溶液中实验现象结论
A滴有KSCN的FeCl
2溶液变红Cl
2
具有还原性
B滴有酚酞的NaOH溶液褪色氯水具有酸性
C紫色石蕊试液先变红后褪色Cl
2
具有漂白性
D KI-淀粉溶液变蓝色Cl
2
具有氧化性
2.下列说法正确的是
A.向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色
B.欲除去氯气中少量的氯化氢气体,可将此混合气体通过盛饱和食盐水的洗气瓶
C.向滴有酚酞试液的氢氧化钠溶液中通入氯气,溶液红色褪去是由于氯气与NaOH反应导致溶液碱性减弱所致
D.将氯水滴入碳酸钠溶液中,无明显现象出现
3.实验室制Cl2的反应为4HCl(浓)十Mn02
MnCl2+C12↑+2H2O.下列说法错误的是
A.还原剂是HCl,氧化剂是Mn02
B.每生成1 molCl2,转移电子的物质的量为2 mol
C.每消耗1 molMnO2,起还原剂作用的HCl消耗4mol
D.生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质
4.海带中含碘元素,从海带中提取碘有如下步骤:①通入足量Cl2;②将海带焙烧成灰后加水搅拌;③加CCl4振荡;④用分液漏斗分液;⑤过滤。则合理的操作顺序是
A.①②③④⑤ B.②⑤①③④C.①③⑤②④ D.②①③⑤④
5.一定条件下磷与干燥氯气反应,若0.25g磷消耗掉314mL氯气(标准状况),则产物中PCl3与PCl5的物质的量之比接近于
A.1:2 B.2:3 C.3:1 D.5:3
6.向盛有Cl2的三个集气瓶甲、乙、丙中各注入下列液体中的一种,经过振荡,现象如下图所示,则甲、乙、丙注入的液体分别是
①AgNO3溶液②NaOH溶液③水
A.①②③ B.②①③C.③②① D.①③②
7.下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是
①氯气②液氯③新制氯水④氯气的酒精溶液⑤盐酸⑥盐酸酸化的漂白粉溶液A.①②③ B.①②③⑥C.③⑥ D.③④⑥
8.某溶液中可能含有I-、NH4+、Cu2+、SO32-,向溶液中加入适量的溴水,反应后溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I-②肯定不含Cu2+③肯定含有SO32-④可能含有I-
A.①② B.①③C.②③④ D.①②③
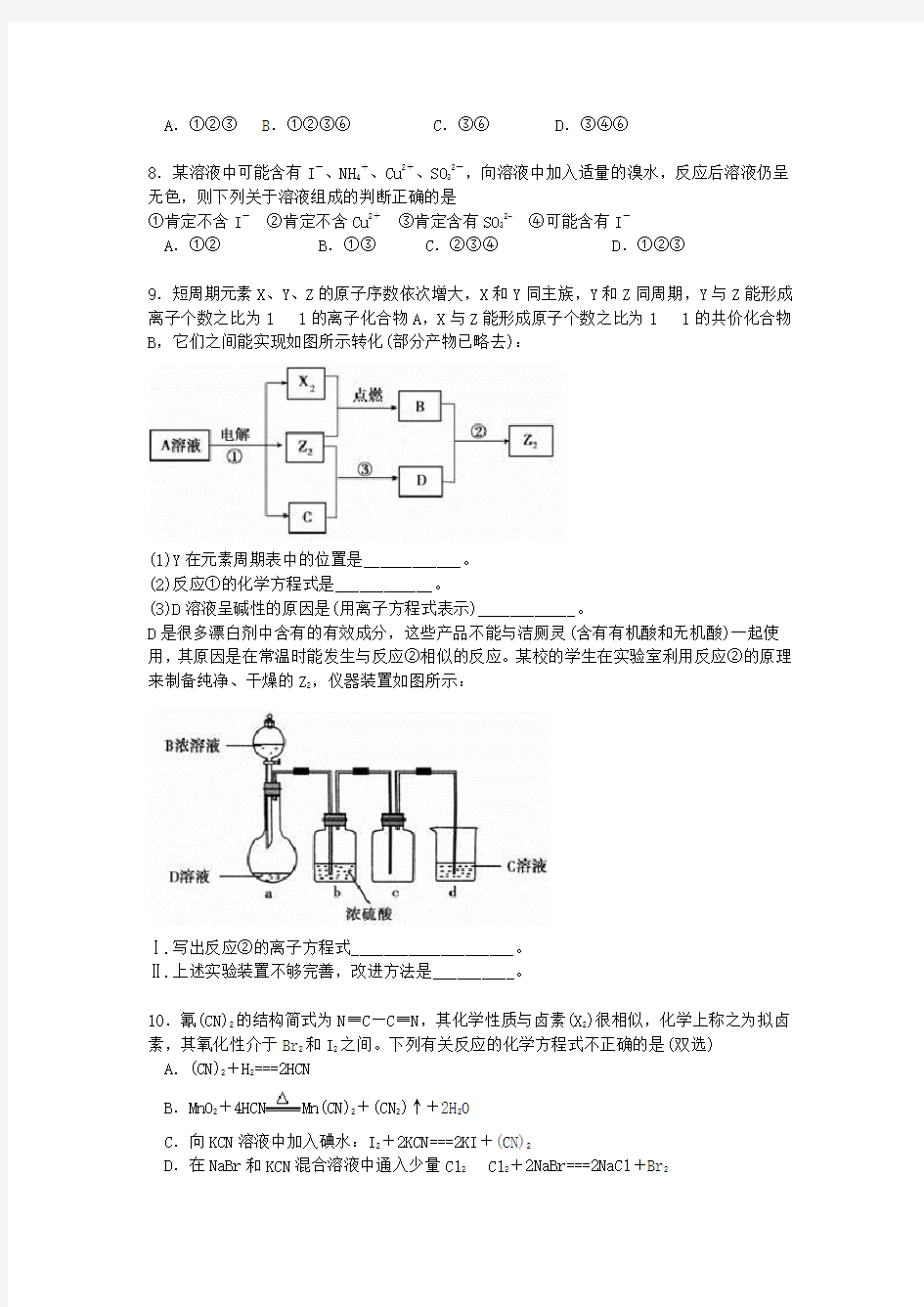
9.短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数之比为11的离子化合物A,X与Z能形成原子个数之比为11的共价化合物B,它们之间能实现如图所示转化(部分产物已略去):
(1)Y在元素周期表中的位置是____________。
(2)反应①的化学方程式是____________。
(3)D溶液呈碱性的原因是(用离子方程式表示)____________。
D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如图所示:
Ⅰ.写出反应②的离子方程式____________________。
Ⅱ.上述实验装置不够完善,改进方法是__________。
10.氰(CN)2的结构简式为N≡C—C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间。下列有关反应的化学方程式不正确的是(双选) A.(CN)2+H2===2HCN
B.MnO2+4HCN Mn(CN)2+(CN2)↑+2H2O
C.向KCN溶液中加入碘水:I2+2KCN===2KI+(CN)2
D.在NaBr和KCN混合溶液中通入少量Cl2Cl2+2NaBr===2NaCl+Br2
11.下列能够检验出KI中是否含有Br一的实验是
A.加入足量的新制氯水,溶液变色则有Br—
B.加入酸性KMn04溶液,观察溶液颜色是否褪去
C.加入少量的碘水,再加入CCl4振荡,有机层有色,则有Br—
D.加入足量FeCl3溶液,用CCl4萃取后,在无色的水层中加入氯水,溶液呈橙黄色,则含有Br一
12.有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。
请回答下列问题:
(1)反应①的化学方程式为
(2)反应②的离子方程式为
(3)写出另外一种实验室制取H的化学方程式
(4)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10—9。将等体积的D溶液与Pb(NO3)2溶液混合,若D的浓度为1×10—2mo1/L,则生成沉淀所需Pb(NO3)2溶液的最小浓度为。
《2013《走向高考》化学总复习专题同步练习(氯气)》参考答案
1.D
2.B
3.C
4.B
5.C
6.B
7.C
8.D
9.(1)第3周期ⅠA族(2)2NaCl+2H2O2NaOH+Cl2↑+H2↑(3)ClO-+H2O HClO +OH-
Ⅰ.ClO-+Cl-+2H+===Cl2↑+H2O
Ⅱ.在a、b装置之间加一盛有饱和食盐水(或水)的洗气瓶,除去HCl
10.CD
11.D
12.(1)MnO2+4HCl(浓)MnCl2+Cl2+2H2O (2)6I-+ClO3-+6H+=3I2+Cl-+3H2O
(3)2H2O22H2O+O2↑
(4)5.6×10-4 mol/L
2013《走向高考》化学总复习专题同步练习(基本概念、胶体)
1.2010年8月8日《联合早报》报道:墨西哥湾漏油危机告一段落。下列对石油的说法正确的是
A.石油属于有机物
B.石油分馏能得到汽油、煤油等,此过程属于发生物理变化
C.石油燃烧只生成二氧化碳和水
D.石油在海水中过一段时间会沉于海底,影响海底生物生存
2.下列物质按照混合物、非电解质、碱、酸式盐的顺序排列正确的是
A.漂白粉、Cl2、氨水、NaHCO3
B.福尔马林、苯、Cu2(OH)2、CO3、明矾
C.盐酸、SO2、纯碱、NH4Cl
D.食醋、C2H5OH、苛性钾、NaHSO4
3.生物学家借助新的显微技术,成功观察到小于200纳米的微粒。下列分散系中,分散质微粒半径最小的是
A.雾 B.蛋白质溶液 C.石灰乳 D.KNO3溶液
4.奥运会会标是五环旗,假定奥运五环旗中的每一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应。且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是
5.纳米材料是指颗粒的三维线度中的任一维在1 nm~100 nm范围的材料。纳米技术所带动的技术革命及其对人类的影响,远远超过电子技术。下列关于纳米技术的叙述不正确的是A.将纳米材料分散到液体分散剂中可制得液溶胶
B.用纳米级金属颗粒粉剂作为催化剂可加快化学反应速率
C.将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,说明“纳米铜”比铜片更易失电子
D.银器能抑菌、杀菌,将纳米银粒子植入内衣织物中,有奇异的抑菌、杀菌效果
6.下列叙述正确的是
A.有单质参加或单质生成的化学反应一定是氧化还原反应
B.生成物只有一种的化学反应不一定是化合反应
C.生成阳离子的反应一定是氧化反应
D.有电解质参加的化学反应一定可以用离子方程式表示
7.下列有关物质分类或归纳的说法中,正确的一组是
①蔗糖和麦芽糖的化学式都可用C12H22O11表示,它们互为同分异构体
②聚乙烯、聚氯乙烯、纤维素都属于合成高分子
③明矾、石膏、冰醋酸、水都是电解质
④盐酸、漂白粉、水玻璃都是混合物
⑤分馏、干馏、裂化都是化学变化
⑥植物油、直馏汽油都可与溴水反应
A.①③⑤ B.②④⑥C.①③④ D.②④⑤
8.下列现象或应用不能用胶体的知识解释的是
A.可吸入颗粒(如硅酸盐粉尘),吸入人体,对人体健康危害极大
B.土壤表面积巨大且一般带负电,能吸收NH4+等营养离子,使土壤具有保肥能力
C.水泥、冶金工厂常用高压电除去工厂烟尘,减少对空气的污染
D.氯化铝溶液中加入碳酸钠溶液会出现白色沉淀
9.下列说法中正确的是
A.不能发生丁达尔效应的分散系有氯化钠溶液、水等
B.在 1L2mol·L-1的Fe(OH)3胶体中含有氢氧化铁胶粒数为2N A
C.在Fe(OH)3胶体中滴入少量的硫酸将有沉淀产生
D.胶体粒子能作布朗运动
10.下面是对日常生活中常见的一些做法的解释或现象的描述,其中正确的是
①生产面粉的工厂车间应“严禁烟火”:面粉颗粒很小,悬浮在空气中的单位质量的面粉与O2的接触面积大,遇到明火易发生爆炸
②使用冰箱贮存食物可延长食物保鲜期:冰箱内气温较低,微生物的生长、繁殖速率慢
③镀锡铁桶在镀层破损后破损处很快会出现破洞
④铝比铁性质活泼得多,但铝制品比铁制品耐腐蚀得多:铝表面能形成致密的氧化物保护膜
⑤用酒精擦拭皮肤后,相应部位有清凉感:酒精具有消毒杀菌能力
A.①②③④⑤ B.①②③④C.①②④ D.③④⑤
11.下列说法正确的是
A.大量使用化石燃料,有利于“节能减排”
B.糖类、油脂、蛋白质都属于高分子化合物
C.维生素C具有还原性,在人体内起抗氧化作用
D.向海水中加入铝盐、铁盐等净水剂可使海水淡化
12.下列说法在一定条件下可以实现的是
①酸性氧化物与碱发生反应②弱酸与盐溶液反应可生成强酸③没有水生成,也没有沉淀和气体生成的复分解反应④两种酸溶液充分反应后的溶液体系为中性⑤有单质参加的非氧化还原反应⑥两种含氧化合物反应的产物有气体
A.①②③④⑤⑥ B.②④⑤⑥
C.①②③⑤ D.③④⑤⑥
13.据中科院网报道,纳米Fe3O4晶体材料中可以作为核磁共振造影增强剂,用于疾病的诊断和作为药物载体用于疾病的治疗。其制备过程如下:
下列叙述不合理的是( )
A.Fe3O4可以表示为FeO·Fe2O3,属于混合物
B.反应③的化学方程式为6FeOOH+CO===2Fe3O4+3H2O+CO2
C.纳米四氧化三铁分散在适当分散剂中,形成的分散系可能有丁达尔效应
D.在反应②中环丙胺()的作用可能是促进氯化铁水解
14.下表各组物质之间通过一步反应不可能实现如图所示转化关系的是
15.取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为
______________________,反应后得到的溶液呈________色。用此溶液进行以下实验:(1)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为__________________,此反应属于____________。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴几滴FeCl3溶液,继续煮沸
直至溶液呈________色,即可制得Fe(OH3)胶体。
(3)取另一小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一直放置于暗处,分别用激光笔照射烧杯中的液体,可以看到________烧杯中的液体产生丁达尔效应。这个实验可以用来区别
____________。
(4)乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可以看到溶液红褐色逐渐变浅,最终得到黄色的FeCl3溶液,发生此变化的化学方程式为
____________________________,此反应也属于____________反应。
(5)已知Al(OH)3胶体能够净水,则Fe(OH)3胶体________(填“能”或“不能”)净水。16.A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:
(1)若上图中B、C均为氧化物,D、E均为盐,则A可能是________。
①Na ②N2③C ④S
(2)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液均显碱性,且等浓度时碱性C>D>E,B可用在呼吸面具中作为氧气的来源,则B中含有的化学键类型为(填“离子键”、“极性键”或“非极性键”)________________________;
A转化成C的离子方程式为______________;
D转化成E的离子方程式为______________。
(3)若常温下B、C、D均为气体,且D为红棕色气体。
①B→C的化学方程式为____________。
②将B和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式为
______________。
