注射液工艺验证方案

此工艺验证是建立在厂房,空气洁净度,工艺用水及设备和设备清洁已验证并合格的基础上展开的,拟通过连续三批生产来验证该产品的工艺规程,对维生素C 注射液生产中可能影响产品质量的各种生产系统条件和生产工艺变化因素控制在工艺规程规定的标准范围内,确保产品的可靠性和稳定性,生产出符合企业内控标准的--注射液。 2、适用范围:
适用于维生素C 注射液的工艺验证。 3、责任者:
参加维生素C 注射液工艺验证的人员。 4、方案
4.1、验证方法:
本产品工艺验证方案计划在水针新车间生产前三批的生产过程中进行验证。 4.2、相关文件 《验证SMP 》
《----注射液工艺规程》 YBSTP -SC027-03
4.3、方案概要
4.3.1主要工艺内容及生产条件如下:
4.3.2验证过程具体分为六个生产工艺过程:
⑴ 洗瓶、杀菌干燥 ⑵ 配液 ⑶ 灌封 ⑷ 灭菌 ⑸ 灯检 ⑹ 印包
4.3.3每个生产工艺过程验证的每一项内容中均包括描述与生产过程相关的规程,文件和相关的设备,并阐述生产系统各种元素的评价方法及生产过程中各种可能影响产品质量的因素提供变量的评价方法。
生产系统各种元素的评价方法中阐述了在生产前、生产过程中及生产过程结束后对生产系统各种元素特征的检查内容及评价标准。每项检查评价结束后,评价及检查结果应记录于本方案中设计的记录表中,并附于验证报告中。
生产过程中各种可能影响产品质量的工艺变量的评价方法,阐述了生产过程中应进行的一系列有关工艺变量的评价方法及评价标准。评价结果应记录于本方案设计的记录表中并附于验证报告中。
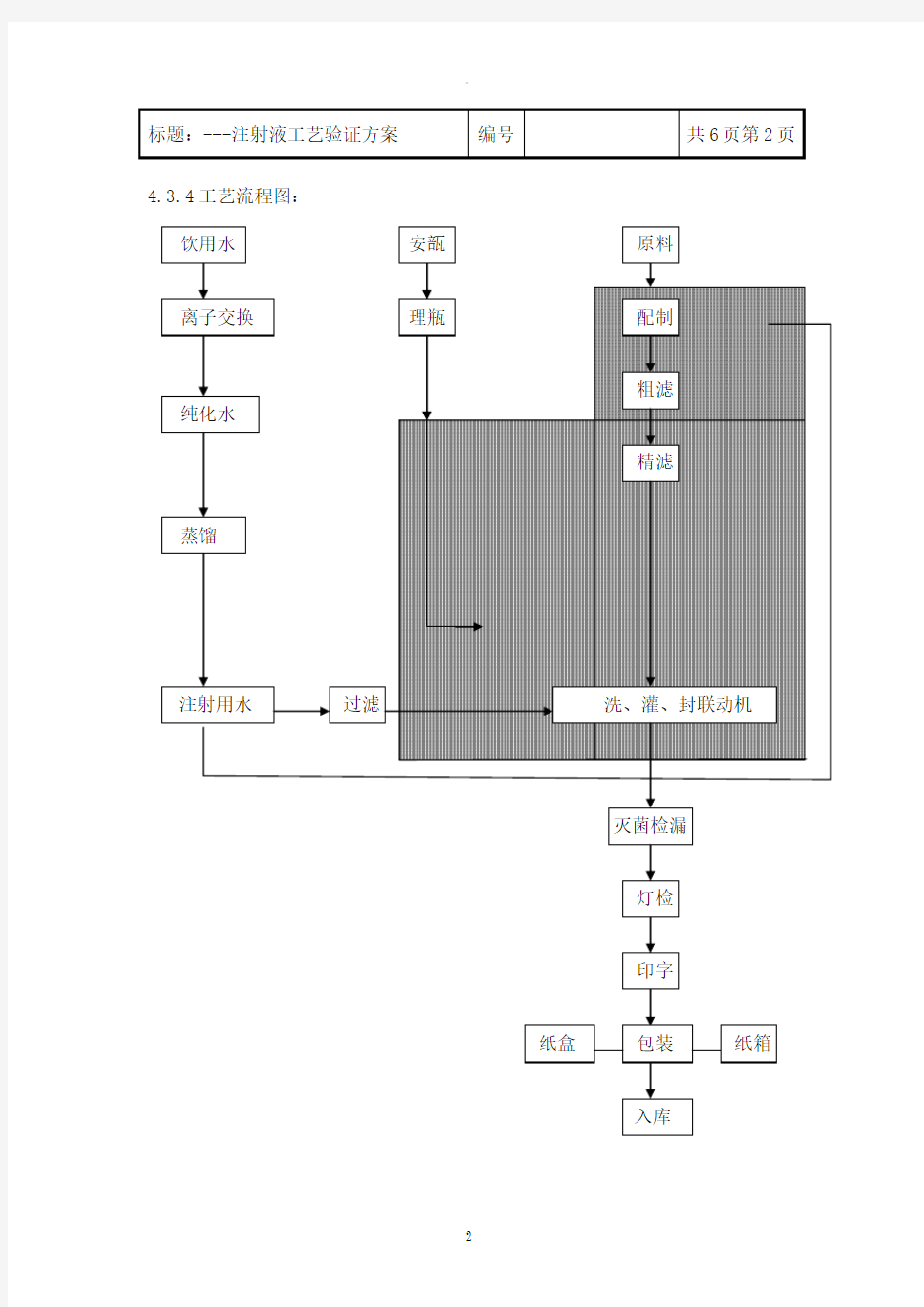
4.3.4工艺流程图:
4.3.5质量标准及文件
《质量标准》《中国药典》2000版二部
《--注射液中间体质量标准》《YBSTP-QA209-00》
《--注射液成品质量标准》《YBSTP-QA300-00 》
目的:提供文字依据证明生产系统要素符合维生素注射液生产准备和工艺条件.从而保证用此系统生产的各种物料符合质量标准,最终生产出符合质量林求的合格的产品.
⑴项目:相关文件
洗瓶、杀菌干燥SOP YBSOP-WS214-00
YBSOP-WS201-00 YBSOP-WS202-00
YBSOP-SC260-00 YBSOP-SC261-00
配液 YBSOP-WS213-00
YBSOP-SC262-00 YBSOP-WS203-00
灌封 YBSOP-WS215-00
YBSOP-SC264-00 YBSOP-WS204-00
灭菌 YBSOP-WS216-00
YBSOP-SC269-00 YBSOP-WS209-00
灯检 YBSOP-WS217-00
印字 YBSOP-WS218-00
YBSOP-SC270-00 YBSOP-WS207-00
评价方法检查所有文件的完备情况。
判断标准所有相关文件内容齐全,文件齐备。
⑵项目:操作间清洁、清场
评价方法在每批产品的生产准备开始前检查操作间清场和清洁情况。
判断标准所有的房间已得到清洁,并没有任何前一批生产的遗留物,有房间清洁状态标识。
⑶项目:设备清洁
评价方法在每批产品的生产准备开始前检查设备的清洁情况。
判断标准所有的设备都是清洁的,没有前一批生产的污染物,且有清洁待用
的状态标识。
⑷项目:文件完备
评价方法具有前一次清场合格证,进行生产前的准备。
判断标准前一次的清场合格证及本次的清洁均已签字认可。
⑸项目:环境质量(温度和相对湿度,空气压力,空气质量)
评价方法在每批产品的生产准备开始前,生产中检查并记录各操作间的温湿度,洁净区操作间相对于走廊的空气压力及空气尘埃粒子。
判断标准
温度:18℃~26℃相对温度:45~65%
操作间相对于走廊保持相对正压。标准≥5Pa
十万级区尘埃粒子:≥0.5μm 的粒子≤3500000个/m3
≥5μm 的粒子≤20000个/m3
沉降菌: ≤10个/皿
万级区尘埃粒子: ≥0.5μm 的粒子≤350000个/m3
≥5μm 的粒子≤2000个/m3
沉降菌: ≤3个/皿
⑹项目:人员培训
评价方法查阅操作者技能培训表,确认上岗操作人员已进行下述基本技术
培训
①设备操作规程及清洁规程培训
②所在岗位的操作技能培训.
判断标准上岗操作人员已接受了生产技术培训,并具有上岗证.
4.3.7验证步骤
(一)洗瓶、杀菌干燥过程
1、验证目标
本工序验证的目标是保证维生素C注射液洗瓶、杀菌干燥的准备条件及生产环境符合生产工艺要求。
2、生产工艺变量的评价
目的:提供文字依据证明生产准备过程所采用工艺条件和各种标准操作规程将生产出符合生产需要的中间产品。
(1)监测变量水质
评价方法定时检测水质澄明度,瓶子清洁度
判断标准符合洗瓶水质标准,瓶子清洁度标准
(2)监测变量杀菌、干燥效果
评价方法定时检测杀菌、干燥后的安瓿
判断标准细菌内毒素≤0.25EU/ml。微生物指标≤10CFU/100ml
(二)配液过程
1、工艺验证目标
配液过程验证的目的是证明并保证由此工艺过程生产的维生素C注射液中间体质量符合企业质量标准。
2、设备
配液罐,电子称,天平
上述设备已经清洁完毕,并且标示清楚,设备完好。
3、生产工艺变量的评价
目的:
提供文字依据证明配料工序所采用的工艺过程和各操作规程将保证生产所生产的注射液中间体符合企业内控标准。
(1)监测变量 PH值
评价方法配制后测量药液PH值
判断标准 5.4~6.6
(2)监测变量含量
评价方法配制后测药液含量
判断标准98~103%
(3)监测变量滤器的完整性
评价方法在药液过滤前进行滤器的完整性测试
判断标准孔径0.45μm:≥0.24Mpa
孔径0.22μm:≥0.34Mpa
(4)监测变量药液精滤功效
评价方法取精滤后的药液对澄明度、细菌内毒素、微生物指标进行测试。
判断标准澄明度:部颁《澄明度检查细则及判断标准》
细菌内毒素:≤0.25EU/ml
微生物指标≤100CFU/100ml
(三)灌封过程
1、工艺验证的目标
灌封的工艺验证的目标是保证生产最终产品符合产品质量标准
2、设备
DGA8/1-20 安瓿灌封机
设备已清洁,并且表示清楚,设备完好
3、生产工艺的评价
目的:
提供文字依据证明灌封过程能保证注射液的质量标准。
(1)监测变量药液灌装量
评价方法岗位操作人员每隔30分钟检查一次装量
判断标准 2.10~2.15ml
(2)监测变量灌封速度
评价方法壁上是否有药液
判断标准无
(3)监测变量封口质量
评价方法抽查
判断标准无漏气、封口圆整、无歪头、瘪头、焦头。
(四)灭菌检漏过程
1、验证目标
此项工艺验证的目标是保证灭菌检漏过的产品符合质量要求。
2、设备
AM-2.5型灭菌检漏柜
3、生产工艺变量的评价
目的
提供文字依据证明灭菌检漏过程能保证产品达到灭菌检漏的效果。
工艺过程灭菌检漏
评价方法按柜次,根据不同位置各取样一次,进行热原和无菌检查。
判断标准100℃15分钟,热原、无菌检查符合要求。
(五)灯检过程
1、验证目标
此工序的验证目标是保证灯检出的产品符合质量标准。
2、灯检台
3、生产工艺变量的评价
目的:
提供文字依据证明注射液灯检过程能保证产品的外观和澄明度。
监测变量外观,澄明度
评价方法每60分钟抽取200支,进行外观和澄明度检查
判断标准外观合格,澄明度合格
(六)印包过程
1、工艺验证的目标
此项工序的验证目标是保证印包过程生产的最终产品符合产品质量标准。特别是符合产品的外观质量指标。
2、生产工艺变量的评价
目的:
提供文字依据证明印包生产中所采用的工艺过程和操作规程将保证包装出的产品符合企业质量标准。
(1)监测变量印字质量、包装规格及包装质量
评价方法对印字质量、包装规格及包装质量每30分钟检查一次
判断标准印字清晰,符合包装规格,无漏装、多装现象。
(2)监测变量印刷包材的物料平衡
评价方法审核印刷包材的物料平衡表
判断标准包材的物料平衡在允许范围内。
(3)检测变量产成品的物料平衡
评价方法审核产成品的物料平衡表
判断标准产成品的物料平衡允许范围内。
(七)最终产品质量
由化验室按产品抽样规程对整批产品进行抽样检验,并出具产品检验报告。
工艺验证方案
工艺验证方案
工艺验证方案 XXXXXXXXXXXXX
目录 1验证方案的起草与审批 1.1 验证方案的起草 1.2 验证方案的审批 2 概述 3 验证人员 4 时间进度表 5 验证目的 6 作业流程 7 有关的文件 7.1 工艺验证记录表 7.2 质量标准 7.3 “工艺验证总结审批”会议记录表 8 验证内容 8.1 清洗工作尖的数量。 8.1.1 本次验证工作尖的数量确定为一个标准的数量1000pcs。 8.2 清洗工作尖所用清水的量。 8.2.1 本次实验三种情况:清水用量:6L、7L、8L。 8.3 洗洁精的用量。 8.3.1本次验证五种情况:30ml、40ml、50ml、60ml、
8.4 清洗工作尖所用的时间。 8.4.1 本次验证5种情况:20分钟、25分钟、30分钟、35分钟、40分钟。 9 验证结论、最终评价和建议 1 验证方案的起草与审批 1.1 验证方案的起草 1.2 验证方案的审批
工作尖的超声波清洗为本厂已生产多年的产品工艺,当前搬到新厂房,采用新的设备、公用设施进行生产,为了保证产品质量,须对本品的超声波清洗生产工艺进行验证。 本方案采用同步验证的方式,因已具备以下条件: —生产及工艺条件的监控比较充分,工艺参数的适当波动不会造成工艺过程的失误或产品的不合格; —所采用的检验标准以质管部定制的检验标准为允收依据; 本次验证是以清洗1000个工作尖为标准进行验证,实际生产中工作尖的数量按1000的百分比进行配比洗洁精的用量。 3 验证人员 工艺验证小组人员组成: 4 时间进度表
08月05日至 08月06日完成各工艺因素验证 08月11日小组会议经过相关参数设定 5 验证目的 我们对新厂房、采用新的设备、公用设施进行生产,为了保证产品质量,须对本品的超声波清洗生产工艺进行验证。 6 作业流程 工作尖放入超声波清洗机 倒入清水、洗洁精 开启超声波清洗机 取出工作尖 清水冲洗 7 有关文件
非无菌原料药工艺验证方案模版
工艺验证方案 本公司氯化钾产品是非无菌原料药产品,为保证生产工艺在实际生产中的有效性和可靠性,故对其进行工艺验证,本工艺验证采用同步验证的方式。本生产工艺的验证是由质量管理部负责组织,生产技术部、设备工程部、生产车间及QC检验室有关人员参与实施。 本工艺验证方案参考了GMP2010年版的生产工艺验证的指导原则。 验证小组成员 方案制订 方案审核 方案批准
目录 1. 基本情况 (4) 1.1. 概述 (4) 1.2. 生产工艺 (4) 1.2.1. 生产工艺流程图 (4) 1.2.2. 生产工艺的详细描述 (4) 1.2.3. 关键工艺步骤和参数 (4) 2. 验证目的 (5) 3. 验证前提 (5) 3.1. 工艺环境包括公用系统情况 (5) 3.2. 工艺设备情况 (5) 3.3. 所用原辅料和包装材料情况 (5) 3.4. 所用文件的准备情况 (6) 3.5. 人员情况 (6) 4. 验证方案 (6) 4.1. 验证计划 (6) 4.2. 第一步反应(生产XXXXX粗品)的验证(应包括所有重点 考察的生产关键参数、结晶、离心、干燥) (6) 4.2.1第一步反应(生产XXXXX粗品)关键工艺参数验证 (6) 4.2.2第一步反应收率情况验证 (7) 4.2.3第一步反应中间体的质量情况验证 (7) 4.3. 粗品精制工序的验证 (8) 4.3.1溶解脱色验证 (8) 4.3.2 结晶工序验证 (8) 4.3.3 分离工序验证 (9) 4.3.4 干燥工序验证 (10) 4.3.5小批成品收率情况验证 (10) 4.3.6小批成品的质量情况验证 (11) 4.4批混合工艺的验证 (11) 4.4.1批混合工序关键工艺参数验证 (11) 4.4.2批混合效果的验证 (11) 4.5最终成品的质量情况验证 (12)
注射剂工艺验证模板
注册分类:化学药品4类 补充申请(12):新药技术转让 注射用XXXXXX(0.1g、0.2g) 工艺研究资料——资料项目编号:5-1 (附件2:转让方注射用XXXXXX0.1g工艺验证资料) 注册申请机构:XXXXXX 注册申请机构地址:XXXXXX2 注册申请机构电话:XXXXX 注册申请机构负责人:XXXXX 原始资料的保存地点:XXXXXX 联系人姓名:XXXXX 联系电话:XXXXXXX (0)XXXXXXX 药品注册申请人名称:XXXXXX
验证证书 兹有,经按号验证方案实施检查及验证试验,各项结果均合格,通过我公司验证,批准投入使用,特颁此证。 本次验证有效期至:年月日,即在无异常状况下再验证周期为年。 XXXXXX 验证委员会 主任委员: 年月日
验证委员会组织机构 主任委员: 副主任委员: 委员: 职责:委员会负责本公司GMP验证的日常管理工作及验证方案的起草、实施、审核及批准,委员会实行主任委员会负责制。
验 证 管 理 V ALIDATE ADMINISTER 题目:注射用XXXXXX (0.1g )工艺 颁发部门:质量保证部 验证方案 制定: 日期: 审核: 日期: 批准: 日期: 分发:质量保证部、生产组织部、设备动力部 1目的 为评价注射用XXXXXX (0.1g )冻干粉针剂生产系统要素和生产过程中可能影响产品质量的各种工艺变化因素,特根据GMP 要求制定本验证方案,对其整个生产过程进行验证,以保证在正常的生产条件下,生产出合格、均一、稳定的注射用XXXXXX 冻干粉针剂。 2范围 本验证方案使用于在本方案指定的厂房、设施、设备、工艺条件下注射用XXXXXX 冻干粉针剂的生产,当上述条件改变时,应重新验证。 3职责 3.1验证委员会 3.1.1负责验证方案的审批。 3.1.2负责验证的协调工作,以保证本验证方案规定项目顺利实施。 3.1.3负责验证数据及结果的审核。 3.1.4负责验证报告的审批。 3.1.5负责发放验证报告证书。 3.1.6负责再验证周期的确认。 3.2设备动力部 3.2.1负责组织试验所需仪器、设备的验证。 XXXXXX 页码:1/10 编号:VA-803401 生效日: 年 月 日
注射用水验证方案
注射用水系统验证方案 (滴眼液车间) 一.系统概述 注射用水即无热原蒸馏水,它是用纯化水通过多效蒸馏水机再蒸馏获得的。注射用水为配制注射液与无菌冲洗剂的溶剂,或用于无菌水针、粉针生产洗瓶洗胶塞等直接接触无菌药品的包装材料的最后一次精洗用水,无菌原料药精制工艺用水、直接接触无菌原料药的包装材料的最后洗涤用水、无菌制剂的配料用水等。注射用水系统由注射用水制备,储存,输送和循环使用等几个部分组成。 1.制备过程简述 经过反渗透处理的合格纯化水经过其用水点进入蒸馏水进料水箱,再经多级泵进入多效蒸馏水机(六效),经工业蒸汽加热,列管降膜多效蒸发,六次蒸馏, 螺旋板分离热原和各种杂质,产生合格蒸馏水,水质符合中国药典(2010版)注射用水要求,水温达97~ 99℃,合格蒸馏水进入注射用水储罐,不合格注射用水直接排放。 注射用水贮罐的注射用水经不锈钢水泵增压后经0.22μm精密过滤器后送入车间各使用点。
2. 工艺流程详见图1 3. 设备一览表 详见表1 表 (1): 主 要 设 备 一 览 表 4. 冻干剂、水针剂车间注射用水系统图 详见图2 图2 : 冻干水针车间注射用水流程方框示意图:
二. 注射用水系统验证主要程序与内容 1.验证目的 考验和验证该注射用水系统在生产能力0.5T/H, 工艺流程采用先进的多级离心泵进料,列管降膜,五次蒸馏,螺旋板分离热原结构,控制上选用高温电导仪,PLC+双变频全自动控制下的多效蒸馏水机(五效)系统能有效保证产出去除热源和其它杂质的注射用水,同时注射用水在注射用水贮罐中80℃以上保温,管道中70℃以上保温循环,即注射用水制备,储存,输送和循环使用整个系统的长期稳定运行,水质符合中国药典(2000版)注射用水要求,
工艺验证方案
文件编号:******* 版本号:00 *****工艺再验证方案
*****有限公司
验证方案
目录 1.概述 (3) 1.1产品基本信息 (3) 1.2验证背景 (3) 1.3验证目的 (3) 1.4适用范围 (3) 2.职能部门及职责 (4) 3.风险评估 (4) 3.1目的 (4) 3.2范围 (4) 3.3评估方法 (4) 3.4评估标准 (5) 3.5风险评估结果及风险控制 (5) 4.验证项目、接受标准、实测结果及验证结论 (9) 4.1验证文件确认 (9) 4.2设备、设施及公用系统确认 (10) 4.3关键人员确认 (11) 4.4工艺参数控制确认 (12) 4.5成品质量确认 (14) 4.6稳定性考察试验 (15) 4.7偏差和变更控制 (15)
5.验证结果评定与结论 (15) 6.时间进度安排 (15) 7.附件 附件1:称量情况确认表 附件2:制粒生产过程记录表 附件3:压片生产过程记录表 附件4:包装质量检查记录表 其他附件:合格物料供应商名单、中间产品报告单、成品报告单、生产记录、培训记录、药品生产工艺验证合格证 1.概述 1.1产品基本信息 1.1.1产品名称:*** 1.1.2产品剂型:片剂 1.1.3产品规格:***
1.1.4药品批准文号:国药准字*** 1.1.5制剂批量:*** 1.1.6内包装:**** 1.1.7产品有效期:*** 1.1.8制剂生产工艺流程图: 1.2验证背景 ****为我公司中药制剂品种,制剂生产工艺于***年进行了再验证,验证结果判定为合格。***年月因生产需要,*******。 1.3验证目的 按照GMP及“附录2 确认与验证”的要求,应对*****制剂生产工艺进行再验证,以证明*******按照现行批准的生产工艺仍能生产出符合GMP要求、质量标准及注册标准要
滴眼液生产工艺规程
中试工艺规程 xxxx制药有限公司
1、目的 xxxx滴眼液生产工艺规程是按照xxxx滴眼液注册质量标准和企业生产条件而制定的,工艺规程规定了xxxx滴眼液生产的工艺参数,技术要求,原辅材料、包装材料、中间产品和成品的质量标准,关键控制点及监控,物料平衡计算及监控等。 2. 适用范围 本工艺规程适用于xxxx滴眼液的生产及质量检查,是生产操作、工艺管理、技术检查、质量控制的依据。 3、产品概述 xxxx为天然高分子化合物,是构成组织基质的重要成分,具有较好的黏弹性,对角膜具有保护作用;与纤黏连接蛋白结合,促进角膜上皮细胞的连接和伸延,加快角膜创伤愈合。此外,xxxx分子具有强亲水能力和润滑作用,可稳定泪膜、防止角结膜干燥和减轻眼组织摩擦,缓解干眼症的不适症状。 xxxx滴眼液(Sodium Hyaluronate Eye Drops)用于干燥综合症、史蒂文斯-约翰逊综合症,干眼症等内因性疾患及各种外因性疾患(如手术,药物性,外伤,佩戴隐形眼镜等)所致的角结膜上皮损伤。尤其适用于干燥综合症和史蒂文斯-约翰逊综合症需长期用药的患者。 1.1 产品名称:xxxx滴眼液 汉语拼音: 英文名称:Eye Drops 1.2 剂型:滴眼剂 1.4 规格:5ml:5mg 1.5 本品主要成分:xxxx 1.6 化学结构: 1.7 性状:本品为无色澄明的黏稠液体。 1.8 适应症:用于干燥综合症、史蒂文斯-约翰逊综合症,干眼症等内因性疾患及各种外因性疾患(如手术,药物性,外伤,佩戴隐形眼镜等)所致的角结膜上皮损伤。 1.9 用法用量:一般1次1滴,一日滴眼5~6次,可根据症状适当增减。 禁忌:对本品任何成分过敏者禁用。 注意事项:仅限滴眼使用。滴眼时,应注意药瓶前段不要直接接触眼睛,滴眼后应盖
大容量注射剂生产工艺流程图
目录 1.大容量注射剂生产区概况 2.需要验证的关键工序及工艺验证3.工艺流程的实施 4.操作过程及工艺条件 5.技术安全、工艺卫生及劳动保护6.物料平衡及技经指标 7.设备一览表 8.岗位定员 9.附件(含设备操作、清洁规程)10.变更记录
1.大容量注射剂生产区概况 本生产区面积904㎡,其中1万级净化区域167㎡,10万级净化区域174㎡。 大容量注射剂车间采用10万级和1万级(局部百级)空气净化洁净级别,10万级区域设置缓冲、更衣、洗涤、洁具、称量、配碳、浓配、洗瓶等,1万级区域设置缓冲、更衣更鞋、稀配、化验、灌装、加塞、轧盖、洗涤、存放、洁具等功能间,所有隔断采用无粉尘产生的静电喷涂彩钢板,结合处采用圆角处理,不易产生积灰;人员经过三次更衣和二次更鞋后进入洁净区操作,物料进入洁净区均采用传递窗或气闸进行传递,人流、物流的进入相对分开,保证了洁净区空气洁净度要求;生产设备均采用优质不锈钢材料制造,采用洗瓶、灌装、压塞、轧盖联动线生产,其中洗瓶出口、灌装、加塞采用百级层流保护,灭菌器采用水浴式灭菌器。 1.1 大容量注射剂生产工艺流程图(见后页) 1.2 大容量注射剂生产区工艺布局布置图(见后页) 1.3 大容量注射剂生产区工艺设备布置图(见后页) 1.4 大容量注射剂生产区送回风口平面布置图(见后页) 2.需要验证的关键工序及工艺验证 以上项目按验证文件规定,均已在规定周期进行相关的验证,验证方案及报告见相应文件。
大容量注射剂生产工艺流程图
3.工艺流程的实施 3.1 批生产指令的签发 3.1.1 批生产指令由车间技术负责人根据生产计划表起草,并依据产品工艺规程于生产前一个工作日制定。 3.1.2 批生产指令应经QA质监员审核并签字,由车间主任签字批准后生效。 3.2 生产批记录的发放 3.2.1 除配制工序和包装工序外,工序相应的生产批记录于生产当日由车间工艺质监员发放给各工序负责人,并于工序结束当日填写完整返回车间工艺质监员处汇总。 3.2.2 配制工序和包装工序的生产批记录于生产前一天由车间工艺质监员随同批生产指令或批包装指令一同发放,并于工序结束当日填写完整返回车间工艺质监员处汇总。 3.2.3 所有生产工序必须按批生产(包装)指令执行。 3.3 工艺用水的管理使用 3.3.1 纯化水、注射用水系统由工程设备科管理,制水工序制备而得。 3.3.2 按照SMP-ZL-qa024,纯化水每周生产第一个工作日由QA质监员取样送QC检验,注射用水在生产期间每天下午三点由QA质监员取样送QC检验, QC检验合格后出具报告单由QA质监员交至车间工艺质监员。 3.3.3 车间配料岗位投料前,确认所用注射用水经检验符合规定,记录使用注射用水的批号检验报告单附批生产记录中。 3.3.4 车间在没有收到工艺用水检验报告单的情况下,不得进行生产操作。 3.4 各工序取(留)样一览 3.5 批包装指令的签发 3.5.1 车间技术负责人在灭菌工序完成后对半成品数量、质量等方面进行审核并对照生产工艺检查已完成的工作是否按工艺执行。 3.5.2 车间技术负责人计算理论成品率和预计成品率后根据SMP-JS-016判定生产是否异常,如有异常按SMP-JS-012调查分析原因。 3.5.3 批审查通过后车间技术负责人依据产品工艺规程于包装前一个工作日签发批包装指令。批包装指令应经QA质监员审核并签字,由车间主任签字批准后生效。
片剂工艺验证方案及报告
XXXXX工艺验证方案 YZS-G-1XX037 类别:验证管理工艺验证方案 制定人:制定日期:年月日 审核人:审核日期:年月日 批准人:批准日期:年月日 颁发部门:生效日期:年月日 复印数:份
目录 1.概述 2.目的 3.产品简介 4.验证内容、方法及标准 4.1粉碎过筛 4.2配料混合 4.3压片 4.4包装 4.5成品质量 4.6各工序收率及物量平衡 5验证结果评定与结论 6.稳定性考察 7.相关文件 8.图一 9.相关记录
1.主题内容 本方案规定了XXXXX生产工艺验证的目的,步骤、标准及评价内容 2.适用范围 本方案适用于XXXXX生产工艺的验证 3.责任人 3.1工艺验证小组 组长: 组员: 3.2其他相关人员 4.验证的内容 4.1概述 XXXXX是我公司的主要产品,在以往的生产过程中,此产品生产工艺是稳定可靠的,但是为符合GMP要求,我公司新建了厂房,引进了先进的设备,因此在该产品正式投入生产前进行工艺验证,进行工艺验证的前提条件是: 1.厂房、设施、设备已经过验证并验证合格可投入使用。 2.相应的文件已批准执行。 3.物料通过供应商审计并审计合格。 4.人员已进行全面健康检查和系统培训且已有健康证和培训上岗证。 本验证方案拟在XXXXX试生产时实施 4.2目的: 本产品工艺验证方案的目的在于通过对XXXXX生产工艺的验证,证明该生产工艺可靠性和稳定性 4.3产品简介: 4.3.1处方:原辅料名称万片的用量 4.3.2工艺流程图(见图一) 4.3.3生产、质、量管理文件 批生产指令及记录 XXXXX批生产指令及记录 生产工艺规程 XXXXX批生产工艺规程 质量标准 XXXXX质量标准及主要物料质量标准
工艺验证方案模板
Verification department (department):验证科室(部门): Verify completion date: 验证完成日期: Validity: 有效期:
Index 目录 1.Purpose目的 (5) 2.Scope范围 (5) 3.Responsibility职责 (5) 3.1 AAA responsibilities AAA的职责 (5) 3.2 XXX responsibilities XXX的职责 (6) 4.Regulation and Guidance 法规和指南 (8) 5.Abbreviations缩略语 (9) 6.Protocol Description方案说明 (11) 7.Product And Process Description产品和工艺描述 (14) 7.1 Product specification (14) 7.2 Drug approval No. (14) 7.3 Standard Followed: (14) 7.4 Raw Materials and Adjuvants原辅料情况 (14) 7.5 Process description: (16) 7.6 Process Recipe工艺处方: (21) 7.7 List of Production Plants生产车间一览 (26) 7.8 List of Production Equipment 生产设备一览 (29) 7.9 Process Flow Diagram 工艺流程图 (33) 7.10 CPP Identification CPP确认 (34) 7.11 Validation Plan验证计划 (49) 8.Validation prerequisite验证先决条件 (51) 8.1 Personal Identification人员确认 (51) 8.2 Process Documentation Verification 生产文件确认 (51) 8.3 Training Verification 培训确认 (52) 8.4 System and Equipment Instruments Calibration Verification 系统和设备仪表校验确认.. 52 8.5 System and Equipment Instruments Calibration Verification 生产相关验证状态确认 (53) 8.6 Test Instruments Calibration Verification 测试仪器和仪表校验确认 (53)
注射剂无菌保证工艺及常见验证问题
1、按照欧盟决策树的要求,不能达到121℃,15分钟灭菌,可选择F0≥8的残存概率法。请问,若产品能达到121℃,12分钟灭菌,是否就不能选择121℃,10分钟,同样,能达到10分钟,就不能选择8分钟,都是F0≥8的情况。 答:从微生物杀灭的数学模型可知,在初始污染相同的情况下,灭菌F0值越大,无菌保证水平越高。因此,显然为降低产品残留微生物的风险,尽量选择高的F0值是顺理成章的。 2、在产品质量稳定的条件下,均能满足121℃,8分钟和115℃,30分钟,哪个条件应该优先选择呢? 答:不考虑产品理化质量稳定性,理论上这两种条件达到的F0值几乎相等,无所谓优选哪个。但实际生产中,还要考虑灭菌器内产品中热穿透的情况,灭菌器内不同部位的产品实际获得的F0值的差异,不同灭菌批次间产品的F0的差异等。应该选择热分布差异小,产品F0值差异较小的灭菌工艺。 2℃,灭菌30分钟”,这种表示法是否规范?±3、申报资料中的灭菌条件为“101℃ 40min。?15min或116℃?2℃,灭菌30分钟”几乎不能计算F0值。灭菌条件的表示可以参照中国药典2005年版二部附录168灭菌法,121℃±2℃,灭菌30分钟”本身不能称为终端灭菌,因“101℃±2℃,灭菌30分钟”是否规范,“101℃±答:暂不说灭菌条件为“101℃ 4、同品种10ml、20ml注射剂,采取相同的灭菌方式是否合适? 答:同品种10ml、20ml注射剂,可以采取相同的灭菌方式,但应进行热穿透试验,考察不同体积样品的热穿透是否有一致,同时考虑采用的灭菌方式应能保证大体积产品的无菌保证水平。 5、选择最高无菌保证水平的灭菌工艺,可能会与产品的质量,如有关物质、稳定性等方面有冲突,如何平衡这一矛盾?另外,国外上市的是粉针剂,国内申报时是否还需要进行灭菌工艺的选择研究?
滴眼液生产工艺规程
滴眼液生产工艺规程 中试工艺规程 xxxx 制药有限公司 1、目的 xxxx 滴眼液生产工艺规程是按照xxxx 滴眼液注册质量标准和企业生产条件而制定的,工艺规程规定了xxxx 滴眼液生产的工艺参数,技术要求,原辅材料、包装材料、中间产品和成品的质量标准,关键控制点及监控,物料平衡计算及监控等。 2. 适用范围 本工艺规程适用于xxxx 滴眼液的生产及质量检查,是生产操作、工艺管理、技术检查、质量控制的依据。 3、产品概述 xxxx 为天然高分子化合物,是构成组织基质的重要成分,具有较好的黏弹性,对角膜具有保护作用;与纤黏连接蛋白结合,促进角膜上皮细胞的连接和伸延,加快角膜创伤愈合。此外,xxxx 分子具有强亲水能力和润滑作用,可稳定泪膜、防止角结膜干燥和减轻眼组织摩擦,缓解干眼症的不适症状。 xxxx 滴眼液(Sodium Hyaluronate Eye Drops)用于干燥综合症、史蒂文斯-约翰逊综合症,干眼症等内因性疾患及各种外因性疾患(如手术,药物性,外伤,佩戴隐形眼镜等)所致的角结膜上皮损伤。尤其适用于干燥综合症和史蒂文斯-约翰逊综合症需长期用药的患者。 1.1 产品名称:xxxx 滴眼液 汉语拼音: 英文名称: Eye Drops 1.2 剂型:滴眼剂 1.4 规格:5ml :5mg 1.5 本品主要成分:xxxx 1.6 化学结构: 1.7 性状:本品为无色澄明的黏稠液体。 1.8 适应症:用于干燥综合症、史蒂文斯-约翰逊综合症,干眼症等内因性疾患及各种外因性疾患(如手术,药物性,外伤,佩戴隐形眼镜等)所致的角结膜上皮损伤。 1.9 用法用量:一般1次1滴,一日滴眼5~6次,可根据症状适当增减。 禁忌:对本品任何成分过敏者禁用。 注意事项:仅限滴眼使用。滴眼时,应注意药瓶前段不要直接接触眼睛,滴眼后应盖 紧瓶盖,佩戴软性隐形眼镜时不应使用本品。 1.10 有效期:暂定24个月
工艺验证方案
工艺验证方案 1
下载文档 收藏 1工艺验证方案 体外诊断试剂质量管理体系文件 北京生物医学科技有限公司生产工艺验证方案类别:验证方案编号: 部门:XXXXXX 诊断试剂盒(AAAA)工艺验证小组页码:共 23 页,第 1 页 XXXX(XXXX) XXXX(XXXX)诊断试剂盒 (AAAA)工艺验证方案 AAAA)版次: □ 新订□ 替代: 年月日制定人: 审批会签: (验证小组) 批准人: 生效日期: 年年月月日日共 23 页,第 1 页 北京易斯威特生物医学科技有限公司生产工艺验证方案目录一. 目的 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈3 二、范围 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈3 三、职责 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈3 1、验证委员会 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈3 2、工艺验证小组 2
备科 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈4 4、生产部 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈4 5、质量检验部 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈4 四、验证内容 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈4 1、文件 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈4 2、方案概要 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈5 3、验证步骤 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈5 五、时间进度表 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈10 六、验证周期 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈11 七、验证结果评价和建议 ┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈11 八、附件 3
工艺验证方案模版
验证方案 ***********生产过程
方案签核单 目录
1.概述........................................................................ 2.目的........................................................................ 3.验证范围.................................................................... 4.依据........................................................................ 5.验证组织及职责.............................................................. 6.产品的工艺描述.............................................................. 6.1产品处方................................................................... 6.2验证产品工艺流程及洁净区域划分示意图....................................... 7.验证前检查确认.............................................................. 7.1人员培训确认............................................................... 7.2系统设施及公用介质SOP的确认............................................... 7.3仪表校验确认............................................................... 7.4关键设备验证确认........................................................... 7.5关键设备、工艺文件确认..................................................... 8.验证实施.................................................................... 8.1验证实施步骤及进度计划..................................................... 8.2环境监测(无菌制剂工艺验证需做此项)....................................... 8.3*****工序操作.............................................................. 8.4验证数据分析及验证结论:................................................... 9.验证过程的偏差处理......................................................... 10. 附件清单.................................................................. 11.验证的总结、评价及审核..................................................... 12.验证执行的审核和批准.......................................................
注射剂生产工艺核查要求
附件6: 中药注射剂生产工艺处方核查一般要求 一、概述 依据《药品注册管理办法》及相关规定、《注射剂类药品生产工艺和处方核查工作方案》制定本要求。 本要求针对已获准上市中药注射剂生产工艺环节上的变化,包括变更药品生产设备,变更药品生产工艺,变更制剂处方等。企业应当参照相关技术指导原则,评估其变更对药品安全性、有效性和质量可控性的影响,进行相应的研究,以确保药品的安全性、有效性及质量可控性,并按照规定申报。 由于中药注射剂的潜在风险性较高,应充分重视其生产工艺、制剂处方等的变更对安全性、有效性和质量控制性的影响。中药注射剂生产工艺、制剂处方等的变更,应建立在充分研究、全面评估的基础之上。 为便于把握变更可能对产品质量、安全性、有效性产生的影响,对中药注射剂生产工艺变更划分为两类。类别划分是根据目前药品注册管理对补充申请的有关要求而确立的,目的是为了帮助审查人员有效地开展生产工艺变更申请的审查。 I类变更,是指对药品的物质基础及其质量基本不产生影响的变更。一般可通过对变更前后药品物质基础及质量的比较分析,来判断变更前后的一致性。以上研究包括:对工艺变更情况的分析研究、对药质量量的比较研究、制剂安全性的比较研究、对药品稳定性的比较研究,等等。 II类变更,一般分两种情况:第一种情况为简单改变,其变化程度可能较小,对药品的安全性、有效性和质量可控性可能没有重大影响。第二种情况为重大改变,对药品的安全性、有效性和质量可控性可能有较大影响。由于中药成分的特殊性,此类变更仅通过对药品物质
基础及质量等研究难以充分证明对变更对药品的影响,需要通过药学、药理毒理、临床试验等全面研究考察变更对药品的影响。II类变更的临床试验可参照《中药、天然药物注射剂基本技术要求》进行,简单改变的参照仿制注射剂的要求进行研究,重大改变的参照新药注射剂要求进行研究。 本要求仅从技术角度对中药注射剂的生产工艺、制剂处方等变更应进行的相关研究工作进行了阐述。由于中药注射剂变更的复杂性,需要具体问题具体分析,应根据品种的特点开展研究工作。对于其他情况,可按照本要求的基本原则,进行相应的研究。 本要求中提及的各项研究工作的具体要求可参见相应的技术指导原则。如果企业通过其他科学、合理的研究工作所得到的结果亦能支持工艺变更对药品的安全性、有效性及质量可控性不产生负面影响,也可以接受。 二、基本原则 (一)“必要、科学、合理”原则 中药注射剂生产工艺变更应体现其必要性、科学性、合理性。已上市中药注射剂的工艺具有一定的研究基础,并实现了规模化生产,对其进行变更应以科学、合理的研究为基础,并充分考虑其必要性。变更的提出与研究应基于对拟变更药品的充分了解,并以既往药品注册阶段以及实际生产过程中的研究为基础。注册阶段的研究工作越系统、深入,生产过程中积累的数据越充分,对上市后的变更研究越有帮助。 工艺变更研究的主体是企业,企业对其药品的研发和生产等应有较全面的认识,对变更的必要性以及变更带来的影响应当清楚,应对变更前后药品的安全性、有效性及质量可控性进行全面的研究,对研究结果进行全面的分析,对变更对药品的影响进行全面评估。 (二)“安全、有效及质量可控”原则 中药注射剂生产工艺的变更应保证其安全、有效及质量可控性。药品发生变更后,企业
A注射液灭菌工艺验证方案
A注射液灭菌工艺验证方案 公司名称
目录 1.概述 2.验证目的 3.验证依据 4.支持文件 5.验证小组成员及职责 6. 生物指示剂验证试验方法 7.验证合格标准 7.1A注射液生产全过程部分微生物污染监控措施 7.2灭菌釜技术要求 7.3湿热灭菌工艺的生物学验证技术要求 7.3.1沸腾试验阴性 7.3.2沸腾试验阳性 8.湿热灭菌验证操作步骤 8.1 X.PSM.B型旋转水浴式灭菌釜确认 8.1.1概述 8.1.2运行确认 8.1.3空载热分布 8.1.4满载热分布 8.1.5热穿透试验 8.1.6升温速率试验 8.2生物指示剂验证(挑战性试验) 9.取样计划及样品编号 10.验证结果、分析及评价 10.1 A注射液工艺优化、偏差处理及整改措施汇总 10.2 A注射液灭菌前药液微生物限度警戒线及行动线的确认 11.验证培训 12.验证合格证书 13.附件 附件1A注射液无菌保证与国际GMP差距
附件2 生物指示剂制备方法 附件3 A注射液灭菌工艺验证预试验取样计划(系列) 附件4 A注射液灭菌前不同工艺环节的药液生物负荷及沸腾试验调查总结附件5 A注射液湿热灭菌工艺验证待确认修改的相关SOP目录 附件6 A注射液湿热灭菌工艺验证待建立相关SOP目录 14.附录: 附录1 A注射液射液灭菌前药液生物负荷及无菌保证值汇总表 附录2 灭菌釜运行测试记录 附录3 空载热分布汇总记录 附录4 满载热分布汇总记录 附录5升温速率试验记录 附录6 A注射液灭菌工艺微生物学验证记录 附录7 A注射液灭菌工艺验证取样计划及项目编号 附录8 A注射液灭菌工艺验证取样记录 附录9 偏差处理记录 附录10验证培训记录 附录11验证合格证书
工艺验证报告模板
工艺验证报告 内部资料禁止外传) 文件编码:100200 目录 1. 介绍. ....................... 错误!未定义书签。 2. 验证目的. ..................... 错误! 未定义书签。 3. 验证范围. ..................... 错误!未定义书签。 4. 验证类型. ..................... 错误!未定义书签。 5.验证日期与相关批号. .................. 错误! 未定义书签。 6.验证小组成员及职责. .................. 错误!未定义书签。 7.简单工艺描述(略). .................. 错误!未定义书签。 8. 胺化工艺验证. .................... 错误!未定义书签。 . 工艺参数.......................... 错误! 未定义书签。 . 验证人员及日期. ................ 错误! 未定义书签。 . 验证标准、分析方法. ........... 错误! 未定义书签。 . 验证数据. .................. 错误! 未定义书签。 . 验证结果分析、评价及建议. ............ 错误! 未定义书签。 9. 纯化工艺验证. .................... 错误!未定义书签。 . 工艺参数.......................... 错误! 未定义书签。 . 验证人员及日期. ................ 错误! 未定义书签。 . 验证标准、分析方法. ........... 错误! 未定义书签。 . 验证数据. .................. 错误! 未定义书签。 . 验证结果分析、评价及建议. ............ 错误! 未定义书签。 10. .......................... 成盐工艺验证 错误!未定义书签。 . 工艺参数. .................. 错误! 未定义书签。 . 验证人员及日期. ............. 错误! 未定义书签。 . 验证标准. .................. 错误! 未定义书签。 . 分析方法. .................. 错误! 未定义书签。 . 验证数据. .................. 错误! 未定义书签。 . 验证结果分析、评价及建议. ............ 错误! 未定义书签。 11. .................... 验证结果批准、会签及日期 错误!未定义书签
工艺验证方案及计划
XXXXX 有限公司 XXXX机型生产 工艺验证方案 起草人: 审核: 批准: 生效日: 制造部工艺组
1、目的 按S1.5L机型的生产工艺规程,有关的管理文件,标准操作规程及验证文件要求,连续二批生产,证实设计的工艺过程的实用性,设计的生产工艺和设计产品质量能够符合质量标准,确认本生产工艺稳定、操作规程合理,设备与生产能力相匹配,质量监控点合理,具有可靠性和重复性,确保生产处于受控状态,确保能生产出合格的产品。 2、范围 本验证方案适用于S1.5L机型工艺验证,以及可能影响生产工艺的各种因素 3、术语和定义 生产工艺: 指通过一项作业或一系列作业并与设备系统、人员、文件及环境有关的将原材料转变为成品的过程。工艺规程: 为生产S1.5L机型的成品,规定所需原辅料的数量、加工说明(包括中间控制)、注意事项的一个或一套文件,包括生产原材料、生产操作要求和质量控制要求等 工艺性能:一个工艺实现能满足产品要求的产品的能力。
控制策略: 源自于现行产品和工艺理解的一组规划过的控制,用于保证工艺性能和产品质量。这些控制可包括与原材料和技术要求、设施和设备运行条件、过程控制、成品质量标准和监控与控制的关联方法与频次相关的参数与属性。 关键性能指标: 用于衡量质量目标以反映一个组织,工艺或体系的性能表现的度量。 受控状态: 生产控制能始终如一地保证持续的工艺性能和产品质量的状态 4 工艺验证条件: 4.1工艺文件(过程流程图、控制计划、PFMEA、工艺指导书、检验指导书、设备点检保养书、整机BOM、装机技术条件、AUDIT检验文件、设备技术协议、现场5S管理制度等)准备齐全并培训到位。 4.2设备联动调式完毕同时生产线设备参数符合合同技术要求和产品装配技术要求 4.3工艺验证参与人员全部经过培训,熟知工艺验证输出物的要求,参与工艺验证的操作人员需经培训取得上岗资格的员工。
【精品】注射剂无菌保证工艺研究与验证常见技术问题解答
注射剂无菌保证工艺研究与验证常见技 术问题解答 在检品中存在微量的微生物时,往往难以用现行的无菌检查法检出。因此,有必要对灭菌方法的可靠性进行验证。F与F0值可作为验证灭菌可靠性的参数。 F0值为一定灭菌温度(T)下,Z为10℃时所产生的灭菌效果与121℃,Z值为10℃所产生的灭菌效果相同时所相当的时间(min)。也就是说,不管温度如何变化,t分钟内的灭菌效果相当于在121℃下灭菌F0分钟的效果。 在湿热灭菌时,参比温度定为121℃,以嗜热脂肪芽孢杆菌作为微生物 指示菌,该菌在121℃时,Z值为10℃.则: 显然,即把各温度下灭菌效果都转化成121℃下灭菌的等效值.因此称F0为标准灭菌时间(min)。F0目前仅应用于热压灭菌。 以下是关于在生产中遇到的注射剂无菌保证工艺研究与验证常见技术问题的汇总及解决方法.以供参考. 1、按照欧盟决策树的要求,不能达到121℃,15分钟灭菌,可选择F0≥8的残存概率法。请问,若产品能达到121℃,12分钟灭菌,是否就不能选择121℃,10分钟,同样,能达到10分钟,就不能选择8分钟,都是F0≥8的情况。 答:从微生物杀灭的数学模型可知,在初始污染相同的情况下,灭菌F0值越大,无菌保证水平越高。因此,显然为降低产品残留微生物的风险,尽量选择高的F0值是顺理成章的。
2、在产品质量稳定的条件下,均能满足121℃,8分钟和115℃,30分钟,哪个条件应该优先选择呢? 答:不考虑产品理化质量稳定性,理论上这两种条件达到的F0值几乎相等,无所谓优选哪个.但实际生产中,还要考虑灭菌器内产品中热穿透的情况,灭菌器内不同部位的产品实际获得的F0值的差异,不同灭菌批次间产品的F0 的差异等。应该选择热分布差异小,产品F0值差异较小的灭菌工艺。 3、申报资料中的灭菌条件为“101℃2℃,灭菌30分钟”,这种表示法是否规范? 答:暂不说灭菌条件为“101℃2℃,灭菌30分钟"是否规范, “101℃2℃,灭菌30分钟”本身不能称为终端灭菌,因“101℃2℃,灭菌30分钟”几乎不能计算F0值。灭菌条件的表示可以参照中国药典2005年版二部附录168灭菌法,121℃15min或116℃40min。
滴眼液生产工艺规程
中试工艺规程 制药有限公司xxxx 1、目的 xxxx滴眼液生产工艺规程是按照xxxx滴眼液注册质量标准和企业生产条件而制定的,工艺规程规定了xxxx滴眼液生产的工艺参数,技术要求,原辅材料、包装材料、中间产品和成品的质量标准,关键控制点及监控,物料平衡计算及监控等。 2. 适用范围 本工艺规程适用于xxxx滴眼液的生产及质量检查,是生产操作、工艺管理、技术检查、质量控制的依据。 3、产品概述 xxxx为天然高分子化合物,是构成组织基质的重要成分,具有较好的黏弹性,对角膜具有保护作用;与纤黏连接蛋白结合,促进角膜上皮细胞的连接和伸延,加快角膜创伤愈合。此外,xxxx分子具有强亲水能力和润滑作用,可稳定泪膜、防止角结膜干燥和减轻眼组织摩擦,缓解干眼症的不适症状。
xxxx滴眼液(Sodium Hyaluronate Eye Drops)用于干燥综合症、史蒂文斯-约翰逊综合症,干眼症等内因性疾患及各种外因性疾患(如手术,药物性,外伤,佩戴隐形眼镜等)所致的角结膜上皮损伤。尤其适用于干燥综合症和史蒂文斯-约翰逊综合症需长期用药的患者。 1.1 产品名称:xxxx滴眼液 汉语拼音: 英文名称:Eye Drops 1.2 剂型:滴眼剂 1.4 规格:5ml:5mg 1.5 本品主要成分:xxxx 1.6 化学结构: 1.7 性状:本品为无色澄明的黏稠液体。 1.8 适应症:用于干燥综合症、史蒂文斯-约翰逊综合症,干眼症等内因性疾患及各种外因性疾患(如手术,药物性,外伤,佩戴隐形眼镜等)所致的角结膜上皮损伤。 1.9 用法用量:一般1次1滴,一日滴眼5~6次,可根据症状适当增减。 禁忌:对本品任何成分过敏者禁用。 注意事项:仅限滴眼使用。滴眼时,应注意药瓶前段不要直接接触眼睛,滴眼后应盖紧瓶盖,佩戴软性隐形眼镜时不应使用本品。 个月24有效期:暂定1.10 1.11 贮藏:密闭,室温(1-30℃)保存 2、处方和处方依据 2.1 处方 处方理论用量处方理论用量处方理论用量 2.2处方解析 处方中作用原辅料名称 xxxx 活性成分 渗透压调节剂氯化钠 渗透压调节剂氯化钾 金属离子络合剂依地酸二钠缓冲剂氨基己酸pH值调节剂硼酸pH值调节剂砂硼 防腐剂葡萄糖酸氯己定溶剂注射用水 本处方依据申报资料研究制定。2.3处方依据:万支622.4生产批量:万支、生产工艺操作要求和技术参数3. 称量备料工艺流程图:3.1 降温到配注射用水1、依次加入溶2、依地酸二钠、葡萄糖酸氯己定液溶胀完全xxxx 3、罐依次加入溶4、氨基己酸、氯化钠、氯化钾、硼酸、硼砂pH调硼酸或硼砂溶液、5. 0.450.22μm
