洁净区环境监控管理规程

1目的
规范洁净区环境监控管理,确保洁净区的环境符合GMP要求。
2范围
适用于各生产车间的洁净区的监控。
3职责
QA负责各车间洁净区的环境监控。
4内容
4.1定义
4.1.1静态
4.1.1.1静态a:洁净室(区)在净化空气调节系统已安装完毕且功能完备的情况下,生产工艺设备已安装,洁净室(区)内没有生产人员的状态。
4.1.1.2静态b:洁净室(区)在生产操作全部结束,生产操作人员撤离现场并经过20min自净后。
4.1.2动态:洁净室(区)已处于正常生产状态,设备在指定的方式下进行,并且有指定的人员按照规范操作。
4.2测试项目、标准及频次
4.2.1风速、风量及换气次数
4.2.1.1风速测试:A级区进行风速测试,检测频次:每个月一次。
4.2.1.2风量及换气次数测试:A级区外的其它区域测量风量及换气次数。检测频次:至少每年一次。
4.2.1.3标准
a.A级区风速:层流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s。
b.换气次数:B级洁净室换气次数n≥50次/h,C级洁净室换气次数n≥25次/h,D级洁净室换气次数n≥15次/h。
4.2.2流型
4.2.2.1检测区域:A级区,检测频次:至少每年一次。
4.2.2.2标准:应为层流
4.2.3压差
4.2.3.1检测频次:正常投产时每天一次。
4.2.3.2标准
a.洁净区与非洁净区之间、不同等级洁净区之间的压差应不低于10帕斯卡。
b.相同洁净度等级不同功能的操作间之间应保持适当的压差梯度,以防止污染和交叉污染。
4.2.4温度、相对湿度
4.2.4.1检测频次:正常投产时每天一次。
4.2.4.2标准:温度18-26℃,相对湿度45-65%。
4.2.5高效过滤器检漏
4.2.
5.1检测频次:A级区每半年用尘埃粒子计数扫描巡检法进行一次过滤器完整性测试,每年用气溶胶法进行一次过滤器完整性测试;B级、C级区每年用气溶胶法进行一次过滤器完整性测试,D级区每年用尘埃粒子计数扫描巡检法进行一次过滤器完整性测试。新更换高效过滤器要进行完整性测试。悬浮粒子检测结果异常,调查怀疑高效泄漏的可进行完整性测试。
4.2.
5.2标准:气溶胶法泄漏率应≤0.03%。(气溶胶法需外协检测)
4.2.6空气悬浮粒子
4.2.6.1灌装间A级区每批一次在线监测;B级区每个月进行一次动态监测,所有房间每3个月进行一次静态监测;C级区每2个月进行一次监测,动、静态不限;D级区每3个月进行一次静态监测,特殊情况下可进行动态监测。
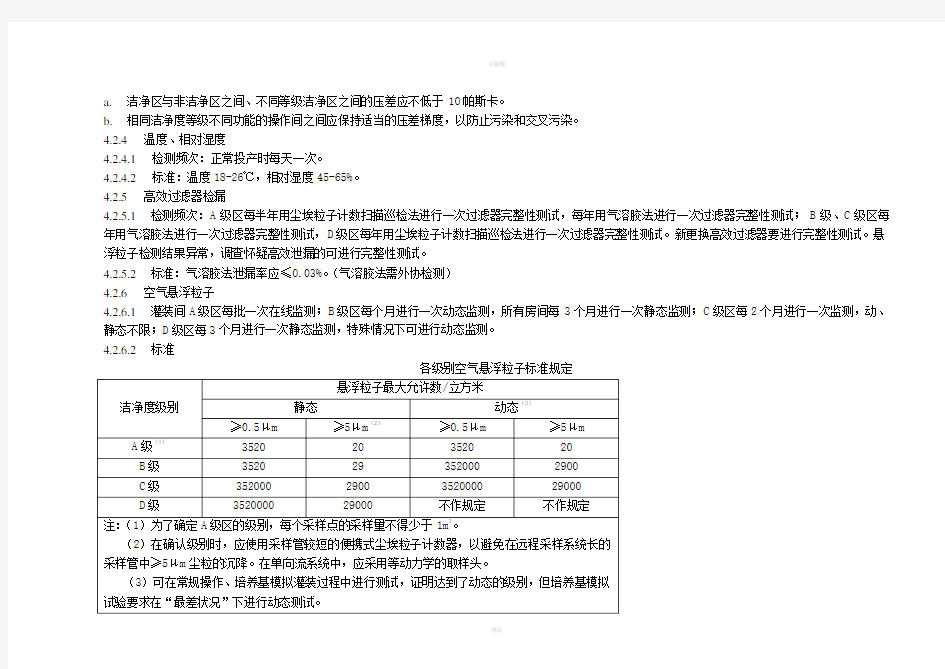
4.2.6.2标准
各级别空气悬浮粒子标准规定
4.2.7空气沉降菌、空气浮游菌、表面微生物及操作者手套和操作服表面微生物:
4.2.7.1检测频次
不同洁净环境微生物的常规取样频率和监控项目
4.2.7.2标准:
洁净区微生物监测动态标准(1)
沉降菌(90mm)cfu /4小时(2)接触碟(55mm)
cfu /碟
1111
4.3测试完后应及时记录。
4.4如果出现异常情况应及时报告质量管理部和生产制造部负责人。
4.5悬浮粒子和微生物监控警戒和纠偏限度、结果超标时应采取的措施。
4.5.1洁净区(室)动态环境监测内控警戒与纠偏限度规定如下:
洁净区(室)动态环境微生物监测警戒限度及纠偏限度
洁净区(室)静态环境悬浮粒子监测纠偏及警戒限度
4.5.2洁净区(室)静态环境微生物监测限度不得超过动态环境微生物监测限度的警戒限。
4.5.3悬浮粒子测试当浓度达到纠偏限度时必须对操作区进行清洁。
4.5.4微生物测试当数量达到纠偏限度时必须对洁净区及空调系统进行消毒。
4.5.5当悬浮粒子浓度和微生物数量达到纠偏限度时,必须按《偏差处理管理规程》进行调查分析和处理。
4.5.6在停产期长达一个月以上再开工生产前,车间做好清洁消毒后,必须先经QA静态测试车间洁净度,测试合格才能生产。
4.5.7由质量管理部对每季度和全年洁净度监测结果进行趋势分析,形成季度或年度回顾报告,交质量受权人审批。回顾分析内容:
(1)是否按规定进行监测?
(2)将日常监测数据的回顾监控数据进行汇总,并对数据和趋势进行分析;
(3)出现不合格情况及所采取的措施;
(4)对出现不合格时所生产的产品和批次是否进行了调查和处理。
4.5.8注意事项
4.5.8.1人员卫生监测及表面微生物取样时每点取样面积宜控制在25cm2左右。
4.5.8.2为避免干扰,表面微生物及人员卫生监测应在生产活动结束时取样。
4.5.8.3表面微生物取样时不宜每次均固定在同一点取样,应在取样点附近的不同位置取样。5相关文件
6附件
.
洁净区管理规程
字号:大中小 洁净区管理规程 1 目的 建立洁净区人、物流管理规定,防止人员、物品对环境的污染。 2 范围 本规程适用于制盖车间十万级洁净区的清洁,人流及物流的管理。 3 责任 3.1制盖车间负责本规程的贯彻执行。 3.2质量管理部负责本规程的监督考核。 4 操作规程及要求 4.1环境要求: 4.1.2洁净室内墙壁、房顶、门窗、地面要无灰尘,无死角。 4.1.3设备表面要无油污、无灰尘,见本色。 4.1.5洁净室内禁止吸烟、禁止随地吐痰等不良行为。 4.1.7洁具要见本色,地漏口要清洁。 4.1.9洁净工作服饰的衣柜不应采用木质材料,应与GMP对设备选型的要求一致。 4.1.10操作人员不许穿工作服出洁净区。 4.1.12洁净厂房应定期清洗消毒。使用的消毒剂不得对设备、原材料、产品等产生污染。(新洁尔灭1%) 4.1.13洁净室内的工装设备、工位器具也应定期清洗消毒或清洁处理。
4.1.14洁净室于非洁净室内的工位器具应严格区分,标示明显,不得交叉使用。 4.1.15对于与产品或零件直接接触的设备及工作台面每天工作前应用消毒液浸过的洁净卫生不脱落纤维的抹布进行擦拭。 4.1.16每天上班前和下班后应打开净化车间内的紫外线灯照射各30分钟灭菌或用溴氧发生器进行消毒。 4.1.17洁净区所有门窗户平时不许开,工作时门必须关紧,通道门的开关必须 遵循前门不关后门不开的原则。 4.1. 19洁净区内进行各种操作活动要稳、准、轻,不做与工作无关的动作,各种活动(操作)应限制在最低限度。 4.1. 20不允许将食品或与生产无关的物品带入洁净区。生产过程中产生的废弃物应及时装入洁净的不产尘的容器或袋中,密闭放在洁净区内指定地点,并按规定在工作结束后将其及时清除出洁净区。 4.2清洁规程 4.2.1清洁范围:洁净区地面、门把手、配电箱、水池、地漏、墙面、门、窗、天花板、灯罩、高效过滤器的层流罩、紫外灯管、回风口、鞋橱等。 4.2.2清洁频次: 4.2.2.1每天生产结束后清洁; 4.2.2.2每周最后一个工作日; 4.2.2.3停产三天后再生产前清洁; 4.2.3清洁用品: 4.2.3.1清洁工具:丝光毛巾、不锈钢桶、水托、毛刷等。 4.2.3.2清洁剂:洗洁精、纯化水;消毒剂:5%甲酚皂溶液,0.1%新洁而灭溶液,75%的乙醇溶液。
洁净区环境监测管理规程
1.目的:规定了公司洁净区洁净度的测试规则和控制标准。目的是规范洁净区的洁净度的监测,确保洁净区符合生产及质量检测要求。 2.范围:适用于我公司所有洁净区的洁净度测试和管理。 3.职责: 3.1.生产管理部:负责洁净区高效过滤器的检漏和补漏的监督管理工作; 3.2.生产管理部:负责空调净化系统的调试和使用,确保空调净化系统的正常运行; 3.3.质量管理部QA:负责悬浮粒子、浮游菌、沉降菌测试; 3.4.质量管理部QC:配合负责浮游菌、沉降菌的测试。 4.内容: 4.1.1.洁净区:对尘粒及微生物污染规定需进行环境控制的功能间或区域。其建筑结构、装备及其使用均具有减少对该区域污染源的介入、产生和滞留的功能。 4.1.2.洁净工作台:一种工作台或者与之类似的一个封闭围挡工作区。其特点是自身能够供给经过过滤的空气或气体,如垂直层流罩、水平层流罩、垂直层流洁净工作台、水平层流洁净工作台、自净器等。 4.1.3.局部空气净化:仅使室内工作区域特定的局部空间的空气含悬浮粒子浓度达到规定的空气洁净度级别,这种方式称局部空气净化。 4.1.4.洁净度:洁净环境内单位体积空气中含大于或等于某一粒径悬浮粒子的允许统计数。 4.1. 5.菌落:细菌培养后,由一个或几个细菌繁殖而形成的细菌集落,简称CFU。通常用个数表示。 4.1.6.单向流:沿着平行流线,以一定流速、单一通路、单一方向流动的气流。 4.1.7.垂直单向流:与水平面垂直的单向流。 4.1.8.水平单向流:与水平面平行的单向流。 4.1.9.非单向流(曾称为乱流):具有多个通路循环特性或气流方向不平行的,不满足单向流定义的气流。 4.1.10.静态测试:功能间净化空气调节系统已处于正常运行状态,工艺设备已安装,功能间内没有生产人员的情况下进行的测试。 4.1.11.动态测试:功能间已处于正常生产状态下进行的测试。 4.1.12.置信上限(UCL)
洁净室环境监测项目及要求
审批及颁发/APPROV AL & ISSUANCE 会审/COLLECTIVE REVIEW 分发/DISTRIBUTION 一、目的/PURPOSE 明确洁净级别的范围,规范洁净室环境监测,确保生产环境达到要求。
二、范围/SCOPE 适用于车间及微生物室洁净室照度、温度、相对湿度、换气次数、风速、压差、悬浮粒子数、沉降菌、浮游菌、表面微生物、高效过滤器完整性测试等项目的监测管理。 三、职责/RESPONSIBILITY 1 质量保证部 1.1 负责本规程制订。 1.2 及时处理超警戒限/行动限监测结果。 1.3 审核趋势分析数据,及时发现不良趋势。 1.4 审查该SOP的执行情况。 2 质量控制部 2.1 负责培训环境监测取样人员。 2.2 负责取样、测试样品及记录监测结果。 2.3 负责日常环境监测记录的归档管理。 2.4 负责风速、换气次数、高效过滤器的完整性测试、悬浮粒子、沉降菌、浮游菌、表面微生物监测及记录。 2.5 参与处理超警戒限度/行动限度监测结果。 3 各车间 3.1 配合质量控制部的取样工作。 3.2 负责温度、相对湿度、压差监测及记录。 3.3 及时处理超警戒限度/纠偏限度监测结果。 3.4根据监测数据进行趋势分析。 四、术语/GLOSSARY 1 洁净区(室): 需要对环境中尘粒及微生物数量进行控制的房间(区域),其建筑结构、装备及其使用应当能够减少该区域内污染物的引入、产生和滞留。 2 洁净度: 洁净环境单位体积空气中含大于或等于某一粒径的悬浮粒子的允许统计数。
3 洁净区分四个级别: A级:高风险操作区。如灌装区、放置胶塞桶和与无菌制剂直接接触的敞口包装容器的区域及无菌装配或连接操作的区域,应当用单向流操作台(罩)维持该区的环境状态。单向流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s(指导值)。应当有数据证明单向流的状态并经过验证。在密闭的隔离操作器或手套箱内,可使用较低的风速。 B级:指无菌配制和灌装等高风险操作A级洁净区所处的背景区域。 C级:指无菌药品生产过程中重要程度较低操作步骤的洁净区。 D级:指无菌药品生产过程中重要程度较低操作步骤的洁净区和非无菌原料药精制、干燥、粉碎、包装等生产操作的暴露环境。 4 单向流: 指空气朝着同一个方向,以稳定均匀的方式和足够的速率流动。单向流能持续清除关键操作区域的颗粒。 5 动态: 指生产设备按预定的工艺模式运行并有规定数量的操作人员在现场操作的状态。 6 静态: 指所有生产设备均已安装就绪,但没有生产活动且无操作人员在场的状态。 7 警戒限度: 系统的关键参数超出正常范围,但未达到纠偏限度,需要引起警觉,可能需要采取纠正措施的限度标准。 8 纠偏限度: 系统的关键参数超出该限度,需要进行调查并采取纠正措施的限度标准。 五、内容/CONTENT 1 洁净室监测的项目: 照度、温度、相对湿度、风速、换气次数、压差、悬浮粒子、沉降菌、浮游菌、表面微生物、高效过滤器的完整性测试。 2 日常环境监测的标准、频次
洁净区管理规程完整
字号:大中小洁净区管理规程 1目的 建立洁净区人、物流管理规定,防止人员、物品对环境的污染。 2围 本规程适用于制盖车间十万级洁净区的清洁,人流及物流的管理。 3责任 3.1制盖车间负责本规程的贯彻执行。 3.2质量管理部负责本规程的监督考核。 4操作规程及要求 4.1环境要求: 4.1.2洁净室墙壁、房顶、门窗、地面要无灰尘,无死角。 4.1.3设备表面要无油污、无灰尘,见本色。 4.1.5洁净室禁止吸烟、禁止随地吐痰等不良行为。 4.1.7洁具要见本色,地漏口要清洁。 4.1.9洁净工作服饰的衣柜不应采用木质材料,应与GMP对设备选型的要求一致。 4.1.10操作人员不许穿工作服出洁净区。 4.1.12洁净厂房应定期清洗消毒。使用的消毒剂不得对设备、原材料、产品等产生污染。 (新洁尔灭1%) 4.1.13洁净室的工装设备、工位器具也应定期清洗消毒或清洁处理。
4.1.14洁净室于非洁净室的工位器具应严格区分,标示明显,不得交叉使用。4.1.15对于与产品或零件直接接触的设备及工作台面每天工作前应用消毒液浸过的洁净卫生不脱落纤维的抹布进行擦拭。 4.1.16每天上班前和下班后应打开净化车间的紫外线灯照射各30分钟灭菌或用溴氧发生器进行消毒。 4.1.17洁净区所有门窗户平时不许开,工作时门必须关紧,通道门的开关必须遵循前门不关后门不开的原则。 4.1.19洁净区进行各种操作活动要稳、准、轻,不做与工作无关的动作,各种活动(操作)应限制在最低限度。 4.1. 20不允许将食品或与生产无关的物品带入洁净区。生产过程中产生的废弃物应及时装入洁净的不产尘的容器或袋中,密闭放在洁净区指定地点,并按规定在工作结束后将其及时清除出洁净区。 4.2清洁规程 4.2.1清洁围:洁净区地面、门把手、配电箱、水池、地漏、墙面、门、窗、天花板、灯罩、高效过滤器的层流罩、紫外灯管、回风口、鞋橱等。 4.2.2清洁频次: 4.2.2.1每天生产结束后清洁; 4.2.2.2每周最后一个工作日; 4.2.2.3停产三天后再生产前清洁; 4.2.3清洁用品: 4.2.3.1清洁工具:丝光毛巾、不锈钢桶、水托、毛刷等。 4.2.3.2清洁剂:洗洁精、纯化水;消毒剂:5%甲酚皂溶液,0.1%新洁而灭溶液,75%的乙醇溶液。 4.2.4清洁方法:
制药厂洁净室洁净区环境监测各类问题汇总解答
制药厂洁净室洁净区环境监测各类问题汇总解答 1.问:纯化水系统和注射用水系统,用紫外线定期消毒等是否就可以了?若不行,应该用什么方法? 答:《药品生产质量管理规(2010年修订)》要求企业应对纯化水、注射用水管道进行清洗消毒,而没有强制要求消毒的方式方法。紫外线消毒效果的影响因素较多,如紫外线波长、强度、照射时间、水层厚度等,不易控制,可作为消毒的辅助手段。 纯化水系统和注射用水的消毒有多重方式,例如:纯化水系统可采用巴氏消毒或纯蒸汽灭菌,注射用水可采用纯蒸汽灭菌或过热水灭菌等。而紫外线仅仅是辅助的方式,可以延长消毒周期,但其效果十分有限。 企业可以根据自身的设备情况以及消毒周期来确定具体的消毒和灭菌方式,并对其进行充分的验证。但一般情况下,不建议纯化水系统和注射用水系统仅仅采用紫外线定期消毒这一种方式。 2.问,洁净区监控,半球型摄像头每次清洗清洁不干净,而且死角清洗不等,非常不卫生环保,请问有什好的清洁方法? 答:针对洁净区洁净室专业研发生产的洁净区专用摄像头,洁净区专用摄像头是维远泰克针对洁净区、无尘车间的特殊使用环境,专门为药厂、电子厂、医院手术室、食品厂等的洁净区/无菌室/无尘车间开发的专用网络摄像头。该摄像头可以无缝嵌入彩钢板安装,纯平圆形外表面与彩钢板平齐,无卫生死角,易清洁易消毒。 该摄像头可对关键工序、关键岗位进行24小时的定点监控。摄像头与维远泰克OPCMES软件结合使用可实现洁净区监测报警事件与视频片段关联。洁净
区作为制药企业的生产场所,对环境、着装、人员流动等有严格的规定和要求。通过单个半球型摄像头无法全面的监控洁净室人员的操作,更无法对重要设备的运行状态、操作过程进行实时定点监控。如何实现洁净区远程非现场的重点岗位、关键设备的定点实时监控? 要实现洁净区操作间的多点监控,现有技术条件下,需要增加洁净室的监控摄像头的数量。半球型摄像头安装于天花板,安装位置过高,清理不方便,同时存在卫生死角,加大了洁净室清洁和验收的工作量。 洁净区嵌入式专用摄像头解决了该项难题。洁净区嵌入式专用摄像头安装于洁净区彩钢板墙体上,通过嵌入彩钢板的方式安装,安装高度距离天花板约40-60cm。该摄像头平面为纯平面板,嵌入彩钢板后,摄像头平面与彩钢板平面平齐,在利用墙擦清洁墙面的同时实现了摄像头的清洁。同时,摄像头的纯平面板零卫生死角,不存在清理不到位的情况。 3.问:药品生产企业洁净厂房空气洁净度环境参数的监测标准与依据是什么?《药品生产质量管理规(2010年修订)》未明确规定洁净室的技术标准,例如:换气次数、温度、湿度等,那么第三方在对洁净室进行洁净度级别检测确认时应采用何种标准? 答:《药品生产质量管理规(2010年修订)》第四十二条规定:"厂房应当有适当的照明、温度、湿度和通风,确保生产和储存的产品质量以及相关设备性能不会直接或间接地受到影响"。企业应结合产品和工艺特点确定洁净区的温度和湿度围。 关于洁净室技术标准,我国有多个国标均有所涉及,如:《医药工业洁净厂房设计规》(GB50457-2008)、《洁净室施工及验收规》(GB 50591-2010)
洁净区环境监控管理规程
1目的 规范洁净区环境监控管理,确保洁净区的环境符合GMP要求。 2范围 适用于各生产车间的洁净区的监控。 3职责 QA负责各车间洁净区的环境监控。 4内容 4.1定义 4.1.1静态 4.1.1.1静态a:洁净室(区)在净化空气调节系统已安装完毕且功能完备的情况下,生产工艺设备已安装,洁净室(区)内没有生产人员的状态。 4.1.1.2静态b:洁净室(区)在生产操作全部结束,生产操作人员撤离现场并经过20min自净后。 4.1.2动态:洁净室(区)已处于正常生产状态,设备在指定的方式下进行,并且有指定的人员按照规范操作。 4.2测试项目、标准及频次 4.2.1风速、风量及换气次数 4.2.1.1风速测试:A级区进行风速测试,检测频次:每个月一次。 4.2.1.2风量及换气次数测试:A级区外的其它区域测量风量及换气次数。检测频次:至少每年一次。 4.2.1.3标准 a.A级区风速:层流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s。 b.换气次数:B级洁净室换气次数n≥50次/h,C级洁净室换气次数n≥25次/h,D级洁净室换气次数n≥15次/h。 4.2.2流型 4.2.2.1检测区域:A级区,检测频次:至少每年一次。 4.2.2.2标准:应为层流 4.2.3压差 4.2.3.1检测频次:正常投产时每天一次。 4.2.3.2标准
a.洁净区与非洁净区之间、不同等级洁净区之间的压差应不低于10帕斯卡。 b.相同洁净度等级不同功能的操作间之间应保持适当的压差梯度,以防止污染和交叉污染。 4.2.4温度、相对湿度 4.2.4.1检测频次:正常投产时每天一次。 4.2.4.2标准:温度18-26℃,相对湿度45-65%。 4.2.5高效过滤器检漏 4.2. 5.1检测频次:A级区每半年用尘埃粒子计数扫描巡检法进行一次过滤器完整性测试,每年用气溶胶法进行一次过滤器完整性测试;B级、C级区每年用气溶胶法进行一次过滤器完整性测试,D级区每年用尘埃粒子计数扫描巡检法进行一次过滤器完整性测试。新更换高效过滤器要进行完整性测试。悬浮粒子检测结果异常,调查怀疑高效泄漏的可进行完整性测试。 4.2. 5.2标准:气溶胶法泄漏率应≤0.03%。(气溶胶法需外协检测) 4.2.6空气悬浮粒子 4.2.6.1灌装间A级区每批一次在线监测;B级区每个月进行一次动态监测,所有房间每3个月进行一次静态监测;C级区每2个月进行一次监测,动、静态不限;D级区每3个月进行一次静态监测,特殊情况下可进行动态监测。 4.2.6.2标准 各级别空气悬浮粒子标准规定
洁净区清洁消毒管理规程
文件名称洁净区清洁消毒管理规程文件编号/SMP-WS-10 版本/修改 A/0 生效日期页次第1/4页次 制定日期 审核日期 批准日期 分发 1目的 建立洁净区清洁消毒管理规程,确保洁净区的洁净卫生及产品质量。 2 范围 适用于所有洁净区的控制。 3 责任人 洁净区操作人员实施、生产主管、质检员负责监督。 4 内容 4.1 清洁消毒工具 4.1.1洁净区必须配备专用清洁消毒工具,清洁消毒工具必须储藏在专用 的房间内,房间应位于相应的级区内并有明显标志。 4.1.2洁净工具为:不脱落纤维的清洁抹布、洁净扫帚、洁净拖把等。 4.1.3 清洗方法:用洁净的饮用水洗净晾干即可。 4.1.4存放:放于洁具间架子上,摆列整齐,分色管理。 4.2 消毒剂 4.2.1本公司采用甲醛、臭氧熏蒸消毒法及表面消毒法,常用的表面消毒 剂有乙醇、新洁尔灭。 4.2.2 消毒剂的浓度应按规定准确配制,稀释的消毒剂应存放在洁净容器 内,未经灭菌的不应超过贮存期。 4.2.3 使用时,每5升消毒剂所擦洗面积不得大于25m2,以确保清洁效果。 4.2.4消毒剂由车间化验员按规定配制和存放。
4.2.4消毒液应交叉使用,定期更换,避免细菌产生耐药性。 4.3 三十万级洁净区 4.3.1每日 4.3.1.1 生产前,室内用紫外线消毒半小时,同时开启送风机。 4.3.1.2 生产结束后,用洁净区扫帚清扫地面,将生产遗留的废弃物清理 出本区域。 4.3.1.3按清洁工具及存放的管理规程中要求,用不同颜色的干的抹布分 别将设备外壳、工作台面、凳子、门窗及室内其他用具的擦拭一遍,然后将抹布洗净,再用抹布浸泡新洁尔灭溶液或70%—75%的乙醇后 将以上部位重新擦拭一遍。 4.3.1.4 将洁净区拖把洗湿,拧水至拖把不滴水。然后将地面全部拖洗, 将污迹、灰尘拖净,然后将拖把洗净,再用拖把浸泡新洁尔灭溶液或70%—75%的乙醇后将地面重新擦拭一遍。 4.3.2 每周 4.3.2.1 按每日清洁要求进行清洁。 4.3.2.2每周一早晨,用臭氧发生器进行空气消毒。每次消毒30分钟。消 毒完毕后,用净化系统进行换风30分钟。 4.3 3 每月 4.3.3.1 除按每日和每周的要求进行清洁外,应全面清洁。 4.3.3.2全面擦拭工作场所、墙面、顶棚、照明、送风口、回风口、地面、 用具及其他附属设施后,再用新洁尔灭溶液或70%—75%的乙醇将以 上部位重新擦拭一遍。 4.3.3.3室内空气消毒根据室内菌落情况决定消毒周期,一般每三个月用臭 氧消毒一次,消毒时间为2小时,同时开启送风机。 4.3.4 不连续生产 4.3.4.1更换批号或品种时按工作周的清洁内容进行清洁。
SMP-SC013-01一般生产区卫生管理规程
目的:建立一般生产区的工艺卫生、个人卫生、环境卫生管理规程。 适用范围:一般生产区工艺卫生、环境卫生、个人卫生管理。 责任人:一般生产区全体工作人员负责实施本规程。车间主任、QA部主管、检查员监督整个规程的执行。 内容: 1. 工艺卫生 1.1 原辅料的卫生。 1.1.1原辅料,包装材料的包装要求完好,无受潮、混杂、变质、发霉、虫蛀、鼠咬等,各种标牌齐全,有检验合格证,方可进入车间。 1.1.2原辅料的存放,按照品种、规格码放整齐,有状态标记,必须放在原辅料存放的规定区域。 1.1.3原辅料进入操作间,应在拆包室脱去外包装(如不能脱去外包装需擦洗干净),保证清洁,无尘,码放在操作人员使用的位置。 1.1.4工作结束后,应将剩余原辅料整理,包装好(封口)要及时结料、退料。工作区域不允许存放多余的物料,避免交叉污染。 1.2生产过程的卫生 1.2.1各操作岗位都有相应的清洁规程。 1.2.2不得存放与药品生产无关的物料或杂物。 1.2.3清洁用具放于清洁间,清洁剂、消毒剂放于洗衣间的贮柜中,以避免在药品生产过程中造成污染。 1.2.4生产中使用的各工器具、容器应清洁,表面不得有遗留物。容器在用后应立即按清
洁规程清洗干净,不得有清洁剂,消毒剂的残留物,以防造成对药品的污染。 1.2.5在生产工作间应有卫生状态标记。 1.2.6更换品种时要严格执行清场制度。 1.3 设备卫生 1.3.1设备管道应按设备操作、维护保养规程定期检查、维修、清洗保养。 1.3.2产尘而又暴露的加工设备应加以封闭或遮盖,并且有捕吸尘装置。 13.3做到轴见光,沟见底,设备见本色,设备周围无油垢、无污水、无油污及杂物。1.3.4设备表面不得有附着加工物。 1.3.5设备使用的润滑剂或冷却剂不得与保健食品原料、容器、塞子、中间体或药品本身接触。 1.3.6所有的管道要表明输送的介质内容和流向。 1.3.7不用的工具不得存放在操作间内,应存放在指定的工具柜内,整齐堆放、专管。1.3.8工作间内气道必须定期清洁,不得有污物及浮尘。 1.3.9管道安装不得有盲端、死角,要留有消毒,清洁口,有一定的坡度以保证排空。 2. 个人卫生 2.1全体员工持身体健康合格证。 2.2在工作期间,每年必须体检一次,持有周期合格证方继续留在本岗位工作。 2.3一旦发现患有传染病、隐性传染病、皮肤病及精神病及时上报主管领导,调离工作,不得继续从事保健食品生产。 2.4因病离岗的员工,在身体疾病痊愈康复后,需持医生开具的健康合格证明方可重新上岗。 2.5每日上岗前应在更衣室穿戴好清洁完好且符合区域着装要求的工衣、工鞋、帽。 2.6随时保持个人清洁卫生,勤剪指甲,勤理发剃须,勤换衣,勤洗澡。 2.7工作前要将手洗干净,不得涂抹化妆品。 2.8上岗时不得化妆,佩戴饰物。 2.9离开工作场地(吃饭、上厕所)必须脱掉工衣、工鞋、工帽。 3. 环境卫生 3.1窗明壁净见本色,无浮尘,无霉斑、无渗漏、无不清洁的死角。 3.2地面光滑、平整、清洁、无积水、无杂物。 3.3厂房严密,无啮齿类动物及其它害虫,设置电子捕虫装置,防止蚊蝇进入。
洁净区环境监测管理规定
1.目的: 洁净区是药品生产及药品微生物检测的重要场所,为确保药品生产及检测环境符合要求,因此需要对洁净区(室)、层流工作台环境进行定期监测。 2.适用范围: 适用于洁净区(室)、层流工作台环境的监测。 3.职责: 质量管理部QA、QC以及生产人员对本规定的实施负责。 4.内容: 4.1 区域划分: D级,口服液体和口服固体制剂的暴露工序区域;C级,主要用于物料微生物检测背景区域;A级,微生物检测暴露操作区域; 4.2 监测项目:尘埃粒子数、微生物、温度、相对湿度、换气次数、压差、照度; 4.3 测试方法依据:悬浮粒子测试方法按国家标准GB/T 16292-2010及ISO14644-1执行,沉降菌测试按国家标准GB/T 16294-2010执行,浮游菌测试按国家标准GB/T 16293-2010执行;灯检区照度应在3000LX,其他工作区域不低于300LX。 2000 ~ 4.4 监测状态:压差、温、湿度的监测应动态测试,换气次数、尘埃粒子和微生物在静态条件下测试;照度每班需检查灯管是否完整,如发现灯管损坏或更坏需仪器检测。 4.5 洁净区空调系统,在非生产班次时,空调系统作值班运行,使室内保持正压并防止结露; 4.6 各项指标监测工具、标准、监测点及监测周期见表1; 4.7 空气洁净度超过标准时的纠正措施 4.7.1 当空气洁净度中的悬浮粒子数量超过规定的标准时,由质量部联合设备部查明原因,如果换气次数和风速均正常,则可通过进行洁净环境重新清洁,按要求净化至少半小时,依法测定,应符合规定;如属过滤器问题,由设备部对初效、中效过滤器进行处理或更换高效过滤器; 4.7.2 当微生物数量超标时,则必须对此区域进行重新进行清洁,然后重新监测,测试结果应符合规定。 4.7.3 若仍旧不符合规定,则彻底调查分析原因,并采取措施经过重新监测合格后方可继续使用或生产。 4.7.4 若相对湿度及压差不符合要求,由设备部对空气净化系统进行调整,确保符合规定要求。 4.8 当生产间断10天以上,必须在生产前对洁净室进行清洁消毒,并监测悬浮粒子及微生物,应符合规定。
洁净室使用管理规范
洁净室使用管理规范 TYYGROUP system office room 【TYYUA16H-TYY-TYYYUA8Q8-
洁净室管理制度 洁净室洁净区人员卫生行为要求: 1、生产人员卫生与健康要求 2、人员进出更衣室卫生要求 3、人员进出洁净区卫生要求 洁净室洁净区卫生清洁操作规范: 1、区域洁净卫生要求 2、洁净车间卫生清洁操作程序 3、消毒剂配制使用SOP 4、灯具清洁SOP 5、墙壁清洁SOP 6、地面清洁SOP 7、地漏清洁SOP 8、初中效空气过滤清洗规范 洁净室设备使用规范: 1、紫外灯使用SOP 2、传递窗使用规范 3、高效过滤器更换程序 洁净室洁净区卫生检查制度: 1、卫生现场卫生检查 2、洁净区空气检查制度 3、卫生执行及处罚制度 生产人员卫生与健康要求 1.范围:本制度使用于各车间生产人员与健康管理。 2. 目的:防止污染,确保产品质量。 3. 程序: 3、1 . 个人卫生 3、1、1生产人员必须保持良好的个人卫生,不得留长指甲和涂指甲油,佩戴首饰,勤(理)洗发、勤洗澡、勤换衣。 3、1、2进洁净室前,穿戴整洁的工作服、工作帽、工作鞋,工作服应盖住外衣,头发不得露于帽外,洗手消毒。 3、1、3洗手要求:生产人员上岗后遇下述情况之一者,必须洗手消毒:上厕所之后;处理被污染的物品之后;从事与生产无关的其他活动之后。
3、1、4不得将手表和各种饰物及与生产无关的个人用品带入车间。 3、1、5不得穿工作服、鞋进入厕所。 3、1、6洁净室人员工作时应戴口罩,其他工作服、工作帽和口罩应每天清洗消毒(一次性口罩除外)。 3、1、7严禁在车间内吸烟、吃食及做其他有碍卫生的活动。 人员进出更衣室卫生要求 1、范围:第一更衣室、第二更衣室。 2、责任:所用进出更衣室人员。 3、目的:确保洁净区的卫生,防止产品污染。 4、程序: 4、1更衣室分为一更(第一更衣室)和第二更(第二更衣室),一更用于一级洁净区工作人员的外衣脱放和二、三级洁净区工作人员洁净服的更换,二更用于一级洁净区工作人员洁净服的更换。放于一更和二更的衣服不得混淆。 4、2人员进入洁净区必需遵循下列要求: 4、2、1更衣室是操作者进入生产岗位更衣的场所,非生产操作人员未经部门负责人允许不得擅自进入。 4、2、2进出更衣室必须先换上工作鞋,更换下的鞋应存放在指定的鞋架上,不得随意放置。 4、2、3进出更衣室必须关好一道门,违者将给予处罚。 4、3更衣室内换下的衣服,必须存放在各自的更衣柜内,不得悬挂在更衣柜外。 洁净室人员进出洁净区要求 1、范围:本制度适用于各车间生产人员卫生与健康管理。 2、责任:质控部门及生产人员。 3、目的:防止污染,确保产品质量。 4、程序: 4、1下列人员不淮进入洁净室; 4、1、1发烧、感冒、皮肤有晒焦、剥离、外伤、炎症、搔痒症者; 4、1、2皮肤过敏及打喷嚏、咳嗽多者; 4、1、3头皮多者; 4、1、4有搔头、挖鼻孔、摸脸、搓皮肤不良习惯的; 4、1、5未按规定洗去化妆品、指甲油和未穿洁净服者; 4、1、6吸烟过量者(烟粒子在说话、呼吸过程中能再次喷出)。 4、2进入洁净室的人员应注意一下事项: 4、2、1争取每天冲澡、换衣、经常洗头,保持身体清洁。 4、2、2男子尽量每日刮胡子; 4、2、3进入洁净室前应洗手、剪指甲; 4、2、4进入洁净室动作要轻,室内行走不要跑,不要做剧烈的大动作;
洁净区环境检验规程
洁净区环境检验规程 一、范围: 本规程规定了洁净室(区)检测的测试要求,测试方法和判定规则。 本规程适用于洁净室(区)测试的六项指标(尘埃悬浮粒子、沉降菌、风速、换气次数、温度、湿度等性能测试。 二、检测依据 GB 50073—2001 洁净厂房设计规范 GB 50591—2010 洁净室施工及验收规范 GB/T 16292—2010 医药工业洁净室(区)悬浮粒子的测试方法 GB/T 16293—2010 医药工业洁净室(区)浮游菌的测试方法 GB/T 16294—2010 医药工业洁净室(区)沉降菌的测试方法 YY 0033 —2000 无菌医疗器具生产管理规范 三、测试规则 3.1悬浮粒子的测试: 3.1.1测试条件: a.温度和湿度 洁净室(区)的温度和相对湿度应与生产及工艺要求相适应(温度18℃~28℃,相对湿度45%~65%。 b.压差 空气洁净度不同的洁净室(区)之间的压差应≥5Pa,空气洁净度级 别要求高的洁净室(区) 对相邻的空气洁净度级别低的洁净室(区)一般要求呈相对正压。 3.1.2测试状态:
静态测试时,室内测试人员不得多于2人。测试报告中应表明测试时所采用的状态。 3.1.3测试时间: a.对单向流,测试应在净化空气调节系统正常运行时间不少于10min后开始。 b.对非单向流,测试应在净化空气调节系统止常运行时间不少30min后开始。 3.1.4采样点数目及采样位置布置: 悬浮粒子洁净度监侧的采样点数目及其布置应根据产品的生产及工艺关键操作区设置。采样点布置规则见GB/T 16292- 2010医药工业洁净室(区)悬浮粒子的测试方法附录A。 3.1. 4.1最少采样点数目及限定: a.最少采样点数目:
GMP管理文件卫生部分
GMP管理文件 (第五部分) 卫生
目录 文件名称文件编号 一、管理标准文件 1、卫生管理规程 SMP?05?0001 2、厂区环境卫生管理规程 SMP?05?0002 3、非洁净区环境卫生管理规程 SMP?05?0003 4、非洁净区个人卫生管理规程 SMP?05?0004 5、非洁净区工艺卫生管理规程 SMP?05?0005 6、洁净区环境卫生管理规程 SMP?05?0006 7、洁净区个人卫生管理规程 SMP?05?0007 8、洁净区工艺卫生管理规程 SMP?05?0008 9、工作服管理规程 SMP?05?0009 10、洁具管理规程 SMP?05?0010 11、洁具室管理规程 SMP?05?0011 12、废物处理规程 SMP?05?0012 13、卫生状态标志管理规程 SMP?05?0013 14、特殊清洁管理规程 SMP?05?0014 15、消毒剂和清洁剂使用规程 SMP?05?0015 记录名称记录编号 10、提取车间洁净区岗位清洁记录 R?05?009 11、口服液车间洁净区岗位清洁记录 R?05?011
依据:《卫生措施有效地实施,防止药品生产中交叉污染及微生物污染。 范围:环境卫生GMP》、企业药品生产实际 目的:保证、工艺卫生、个人卫生 1.企业要依据《药品生产质量管理规范》建立相应的卫生管理标准,即各项卫生管理规程,经生产管理部及有关部门会审,并经生产副总经理批准后予以实施。 2.卫生管理规程包括:环境卫生、工艺卫生(生产全过程清洁消毒、清场等)、个人卫生三部分。 2.1 环境卫生包括办公环境卫生、生产环境卫生以及生活辅助设施的卫生等。 2.2 工艺卫生包括非洁净区、洁净区(不同级别)、更衣室、清洁室的卫生,生产用物料、设备、容器的卫生以及生产辅助设施、库房的卫生等。 2.3 个人卫生包括人员健康状况、非洁净区人员卫生、不同级别洁净区人员卫生等。 3.各项卫生管理规程一经颁布,即为卫生管理的基准性文件,是质量部实施卫生监控、生产管理部门实施卫生管理、建立清洁规程和依据的准则。任何管理不得背离这一标准,任何人不得任意修改,以确保能够建立有效的预防交叉污染和微生物污染的措施。 4.卫生标准的实施 4.1 为确保卫生标准的实施,生产管理部门必须建立各种卫生标准实施的标准操作程序,即“清洁规程”。 4.2 生产过程中涉及的人、机、料、法、环每一个细节都必须有相应的清洁规程,不得遗漏,以保证生产全过程达到卫生管理规程的标准要求。 4.3 清洁工作的要求不仅是简单的大扫除,而是要求在生产前、生产中和生产结束后都必须保持同样的符合标准的清洁状态,这是保证药品质量必不可少的手段。 5.卫生标准的监控
洁净生产区卫生管理规程
洁净生产区卫生管理规程 一、目的: 规范洁净区卫生管理工作,使洁净区卫生管理工作标准化、规范化。 二、适用范围: 公司所有洁净生产区和洁净检验区。 三、责任人: 操作人员、工序负责人、车间主任、部门负责人、QA人员及进入该区的其他所有人员对本规程的实施负责。 四、内容: 1. 环境卫生 1.1洁净区的内表面(墙壁、顶棚、门窗、地面等)应当平整光滑、无裂缝、接口严密、无颗粒物脱落,无积尘,便于有效清洁和消毒。 1.2 洁净区的温湿度、尘埃粒子、沉降菌数、静压差等应符合相应级别洁净区的控制要求。 1.3 洁净区内各气闸及所有闭锁装置应完好无损。洁净区的空调净化系统应于每天上班前2小时开启,其中运行1小时后,臭氧消毒半小时,置静半小时。洁净区空调净化系统应连续运行,工作间歇时空调应做值班运行,保持室内正压,并防止结露。 1.4洁净生产区不得安排三班生产,每天必须有足够的时间用于清洁与消毒,更换品种要保证有足够的时间间歇用于清场、清洁与消毒。 1.5洁净区内进行各种操作活动时要稳、准、轻,不得做与工作无关的动作,各种活动(操作)应限制在最低而有效的幅度范围内。
1.6 生产过程中应关闭操作间门窗,尽量减少出入次数;产生的废弃物应及时入桶并密闭存放在洁净区内指定地点,工作结束后将其及时清除出洁净区。 1.7 洁净生产区内应尽量减少使用不易清洗的凹陷或凸出的壁架、橱柜和设备,生产所用纸笔不得发尘,不能用铅笔、橡皮、钢笔,一般用中性笔进行书写工作。洁净区不设告示板、记事板。 1.8 洁净区清洁间和清洁工具除应符合一般生产区的清洁要求外,还应保持清洁间通风干燥;清洁工具如拖把、抹布等应采用不产脱落物材质,并在使用后及时清洁晾干,防止产生霉菌。清洁剂、消毒剂应轮换使用,以免产生耐药性微生物。 1.9 不得将非生产用物品、个人杂物等不必要的物品带入洁净区。所用各种器具、容器、设备、工具应使用耐清洗、耐腐蚀的材料制作。 1.10所有器具、容器、设备、工具等应按规定程序进行清洁、消毒后方可按《物料、物品进出生产区标准操作规程》带入洁净区。 1.11洁净区内过道、内走廊不得随意放置、堆置生产用具、半成品或其它物品,保持通道的清洁、畅通。 1.12 洁净区厂房应严密、无缝,无啮齿类动物及其它虫害,同时应设置专门的昆虫、动物隔挡装置,防止蚊蝇、老鼠等动物进入。 1.13各生产车间空间消毒采用饱和臭氧(O 3),质管部采用饱和臭氧(O 3 )加紫外 灯。具体空间消毒管理按照《洁净厂房空气消毒管理规程》进行。 2. 工艺卫生 2.1 进入洁净区的原辅料、内包装材料、容器及工具等均应按《物料、工具、容器、用具进出洁净区标准操作规程》在脱外包间对其外表面采取有效清洁、消毒措施后方可进入洁净区。 2.2原辅料,半成品应分类存放在远离回风口和排风口处,定点码放整齐,不得影响气流循环。并有遮盖防尘措施,有明显的质量状态标记,防止交叉污染和差错。 2.3称量应该在专门设置的称量间进行,操作时应打开层流排尘装置防止粉尘飞扬,并保持操作间的相对负压。 2.4物料在配制过程中应尽可能遮盖,尽量减少抛洒,不可避免时应及时清理。 2.5配制结束后剩余物料应及时清退,生产操作间不得存放与本批生产无关的物
洁净室环境监测操作规程
青岛有限公司文件 目的建立洁净区环境监测规程,规范洁净区沉降菌、浮游菌、悬浮粒子的测试,保证药品在规定的洁净级别内进行生产。 范围本标准适用于洁净区沉降菌、浮游菌、悬浮粒子的监测。 责任环境监测员 内容 1、检验依据: 1.1 GB/T16294-2010《医药洁净室(区)沉降菌的测试方法》 1.2 GB/T16293-2010《医药洁净室(区)浮游菌的测试方法》 1.3 GB/T16292-2010《医药洁净室(区)悬浮粒子的测试方法》 2、悬浮粒子的监测 2.1概述:本测试方法采用计数浓度法,即通过测定洁净区环境内单位体积空气中含大于或等于某粒径悬浮粒子数,来评定洁净室(区)的悬浮粒子洁净度等级。 2.2仪器和设备:尘埃粒子计数器,严格按照《尘埃粒子计数器操作、维护保养规程》(SOP-ZL95-1)操作。 2.3测试步骤 2.3.1测试条件:在测试之前,要对洁净室(区)相关参数进行预先测试,包括温度控制在18-26℃、相对湿度控制在45-65%、压差等,同时应满足仪器的使用范围。 2.3.2测试状态:静态测试,人员不得多于2人。测试报告中应明确测试时所采用的状态及测试人员数。 2.3.3测试时间:在空态或静态a测试时,对单向流洁净室(区)而言,测试宜在净化空气调节系统正常运行时间不少于10min后开始。对非单向流洁净室(区),测试宜在净化空气调节系统正常运行时间不少于30min开始。在静态b测试时,对单向流洁净室(区),测试宜在生产操作人员撤离现场并经过10min后开始;对非单向流洁净室(区),测试宜在生产操作人员撤离现场并经过20min自净后开始。
2.4采样点数目及其布置 2.4.1在空态或静态测试时,悬浮粒子采样点数目及其布置应力求均匀,并不得少于最少采样点数目。在动态测试时,悬浮粒子采样点数目及其布置应根据产品的生产及工艺关键操作区设置。最少采样点数目如下 采样点的布置: 2.4.2采样点位置:一般在离地0.8m 高度的水平面上均匀布置,并避开回风口。测试人员应在采样口的下风侧。 2.4.3采样次数的限定:对于任何小洁净室或局部空气净化区域,采样点的数目不得少于2个,总采样次数不得少于5次。 2.5 2.6监测频率: 2.6.1每季度对微生物洁净实验室进行监测,并及时填写监测记录(附件2)。 2.6.2 D 级取样间每季度监测所有房间,并及时填写监测记录(附件1) 2.6.3每季度对D 级洁净区所有房间进行监测,并及时填写监测记录(附件1)。
洁净区环境卫生管理规程
依据:《GMP》、企业药品生产实际 目的:建立洁净区的环境卫生管理标准并遵照执行,以保证洁净区的环境卫生 范围:洁净区环境卫生 1.洁净区环境卫生除必须达到非洁净区环境卫生规程的要求外,还必须达到以下要求: 1.1保持洁净区所有的建筑物内表面光滑平整、无裂缝、接口严密、无颗粒脱落,并能耐受清洗和消毒,墙壁与地面的交界处应采取措施,以减少灰尘积聚和便于清洁。 1.2 洁净区与非洁净区之间缓冲间应完好,缓冲间两侧门不能同时打开。 1.3 工作中必须关开门时,尽量减少开启次数及控制洁净区的人数为最少。 1.4 洁净区内各种操作活动要稳、准、轻,不做与工作无关的动作,各种活动(操作)应限制在最低限度,不得做剧烈运动。 2.不必要的物品不允许带入洁净区,各种进入洁净区的器具、容器、工具及其它必须按规定程序进行清洁、消毒后方可进入。 3.应尽量减少使用不易清洗的凹陷和凸出的壁架、橱柜和设备。 4.洁净区洁具室除符合非洁净区清洁要求外,还应保持通风、干燥;洁具架、拖把、抹布等要及时干燥,防止产生霉菌。
5.记录用纸、笔需经洁净、消毒程序后方可带入洁净区。所用纸笔不发尘,不能用铅笔、橡皮、钢笔,而应用圆珠笔。洁净区内不设记事板。 6.生产过程中的废弃物应及时装入洁净的容器中密闭,放入指定地点,并按规定在工作结束后及时清除出洁净区。 7.及时按规定对洁净区的设备表面、容器、管道、环境及其它进行清洁、消毒。 8.洁净区使用的清洁剂、消毒剂不得对设备、物料或成品产生污染;消毒剂方式以臭氧、紫外灯照射或一定浓度的消毒剂为宜;消毒剂应交替使用,防止产生耐药菌株。 9.洁净区空调在生产中不得中断运行,保持室内正压,并防止室内结露。 10.洁净室不得安排三班生产,每天必须有足够的时间用于清洁与消毒。更换批次或品种时,要保证有足够的时间间歇清场、清洁与消毒。 11.洁净区环境控制标准 11.1洁净级别:100级、10000级、30万级 温度:18℃-26℃,相对湿度:45%-65% 压差:洁净区空气洁净级别不同的相邻房间之间的静压差应大于5Pa;洁净室与室外大气的静压差应大于10Pa。 11.2若监测达不到标准应采取相应措施。 11.3湿度偏离应在送风箱内置入硅胶吸潮或采取其他除湿措施。 11.4压差≤5Pa时,应检查滤器是否堵塞,并更换或调整送风口开关,若调整时应对所有房间重新检测,以避免影响其它房间的环境参数。 11.5沉降菌超出规定应重新消毒,直至合格。 11.6尘粒数超标应检查滤器是否泄漏或洁净室气密性是否良好。 11.7换气次数不足时,应调大进风量。
制药企业洁净区 室 环境监测质量标准
页号:1/4 [目的]建立洁净区(室)环境监测质量标准,以确保洁净区(室)环境能满足生产要求。 [范围]适用于洁净区(室)环境监测的控制。 [职责]检验人员:按本标准对洁净区(室)环境进行质量监测,并依照本标准做出正确 的判定。 复核人员:按本标准对洁净区(室)环境质量监测过程及记录进行复核。 [程序] 1.标准依据:《药品生产质量管理规范(2010年修订)》、ISO-14644-1、 ISO-14698-1、《医药工业洁净室(区)悬浮粒子的测试方法》GB/T 16292-2010、《医药工业洁净室(区)浮游菌的测试方法》GB/T 16293-2010、《医药工业洁净 室(区)沉降菌的测试方法》GB/T 16294-2010。 2.检测项目: 页号:2/4
页号:3/4 (1)判断悬浮粒子的洁净度级别的条件:①每个采样点的平均悬浮粒子浓度必须不大于规定的级别界限。②全部采样点的悬浮粒子浓度平均值均值的95%置信上限必须不大于规定的级别界限。 (2)判断沉降菌的结果评定:①每个测点的沉降菌平均菌落数必须低于所选定评定标准
中的界限。②在静态测试时,若某测点的沉降菌平均菌落数超过评定标准,则应重新采样两次,两次测试结果均合格才能判为符合。 (3)判断浮游菌的结果评定:①每个测点的浮游菌平均浓度必须低于所选定的评定标准中的界限。②在静态测试时,若某测点的浮游菌平均浓度超过评定标准,则应重新采样两 次,两次测试结果均合格才能判为符合。 3.静态沉降菌质量标准: 4.静态浮游菌质量标准: 页号:4/4 [涉及的文件和记录] 无 [附件] 无 [变更记载及原因]
洁净区清洁标准操作规程
目的 建立洁净区清洁消毒管理规程,确保洁净区的洁净卫生及产品质量 * 2. 适用范围 适用于所有洁净区的控制 3. 职责 洁净区操作人员实施、生产主管、质检员负责监督 4. 工具 5. 清洁频率及范围: 每天清洁 每天生产操作前、工作结束后进行1次清洁,直接接触产品设备表面清洁后再用消毒剂进行消毒。 , 清洁范围:用纯化水擦拭墙面、门窗、地面、室内用具及设备外壁污迹。 每周清洁 每周工作结束后,进行清洁、消毒1次。 清洁范围:用纯化水擦洗室内所有部位,包括地面、废物贮器、地漏、灯具、排风口、顶棚等。 每月清洁 每月的生产结束后,进行大清洁消毒1次,包括拆洗设备附件及其它附属装
置。 消毒 根据室内菌检情况,决定消毒频率。 ^ 6.清洁程序 临近正常清洁周期,提前在清洁室配制好所用清洁液。 由洁具存放间取出丝光毛巾、塑料笤帚、簸箕、一次性废弃物袋、塑料容器等清洁用具。 操作室内先完成工序清场操作,将待清洁区域内废弃物清理到塑料簸箕中,倒入废弃物袋中。 将丝光毛巾在清洁液中荡洗三遍,提起,折叠拧至半干,然后将半干丝光毛巾平整开,沿中线折叠两次,使其成为四层,将折叠好的丝光毛巾平展在手掌中(下同)。 然后在相应清洁区域内,对照相应的清洁内容和方法要求进行环境清洁操作。各清洁区域的总体清洁顺序为由上到下,有里到外,避免重复污染。 】 日常清洁的有效期为24小时,每周的大清洁有效期为7天;间断性生产开始前或更换品种生产前,必须按每周大清洁的要求进行彻底清场清洁,按《清场标准操作规程》检查合格后方可开始生产。 7.清洁内容
¥ 清洁注意事项 若有玻璃破碎,一定要将玻璃屑清除后,再用丝光毛巾或塑料笤帚清洁,以免划伤操作者或损坏地面。 擦拭设备设施的丝光毛巾、擦拭地面的丝光毛巾和擦拭环境的丝光毛巾分类标识和悬挂,不能混用。 清洁时不能干扫或干擦,以免起尘造成污染。 严格按清洁规定的擦拭面积进行清洁,以保障清洁效果。 不能用水直接冲洗地面。 灯具清洁后要停数分钟后开启电源开关。
