分子模型晶体模型的制作

分子模型、晶体模型的制作
赤壁一中化学组 刘光利
二○○四年五月
制作目的:
1.充分利用分子模型等直观的教学用具,有利于培养学生的联想能力,通过各种模型可以提高教学速度和教学质量,解决书上难以表明的立体结构,从而达到突破难点的目的。
2.理解分子结构和晶体结构 培养用物质结构特点来认识物质的特性
制作材料:厚硬纸板、胶水或透明胶、铁丝、直尺、三角板、剪刀
制作方法:
1、正四面体的制作
在厚硬纸板上划好四个等边三角形如图1a 所示,然后沿实线剪下,再沿虚线划痕迹以便折叠,折叠后用粘合剂粘牢即成图1b 所示。
2、三角双锥分子模型的制作 在厚硬纸板上划好六个等腰三角形如图2a 所示,然后沿实线剪下,再沿虚线划痕迹以便折叠,折叠后用粘合剂粘牢即成图2b 所示。
图2a 图
2b
图1a
图
1b
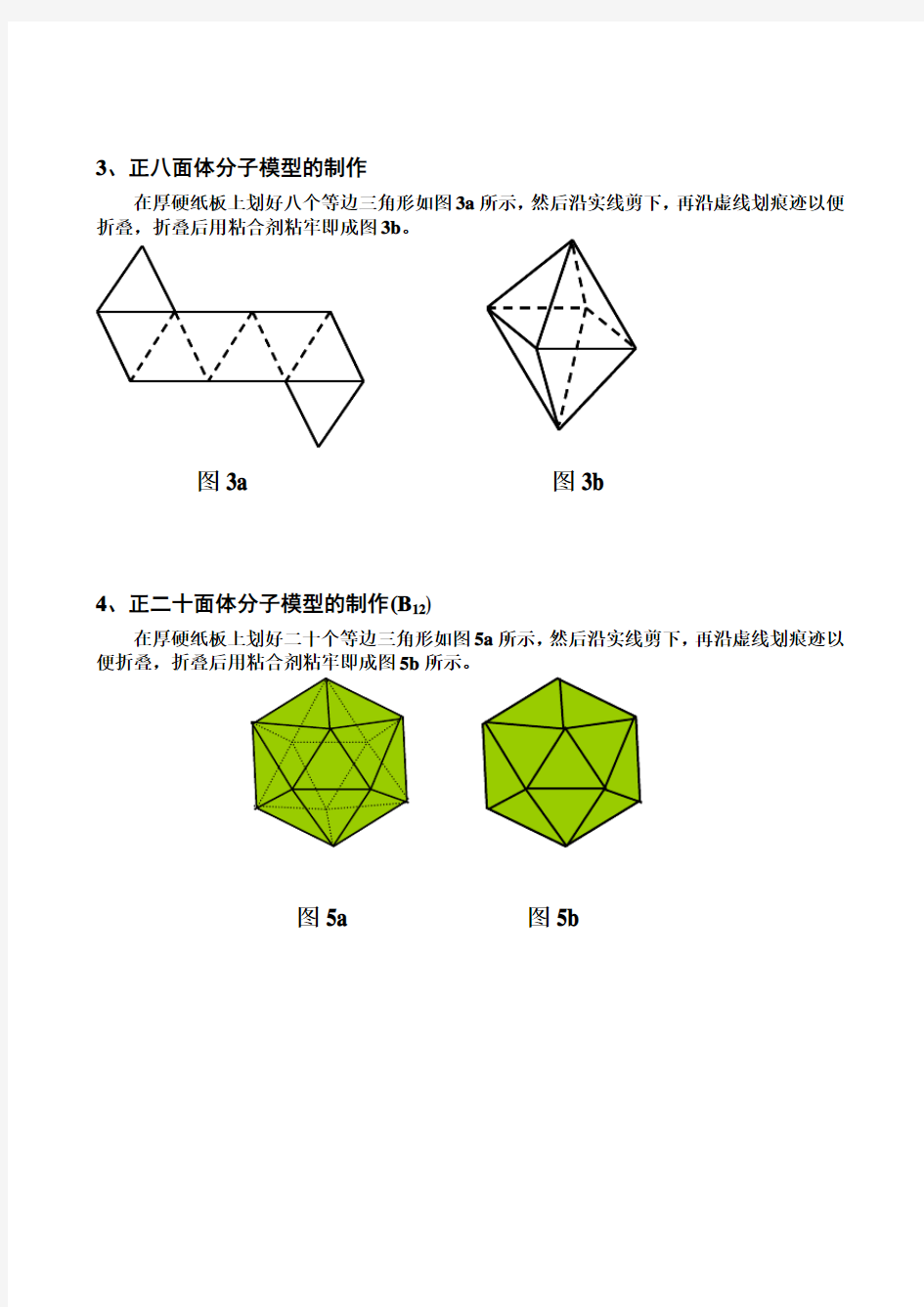
3、正八面体分子模型的制作
在厚硬纸板上划好八个等边三角形如图3a所示,然后沿实线剪下,再沿虚线划痕迹以便折叠,折叠后用粘合剂粘牢即成图3b。
图3a 图3b
4、正二十面体分子模型的制作(B12)
在厚硬纸板上划好二十个等边三角形如图5a所示,然后沿实线剪下,再沿虚线划痕迹以便折叠,折叠后用粘合剂粘牢即成图5b所示。
图5a 图5b
使用说明
1.正四面体模型直接应用于白磷分子、甲烷分子、四氯化碳分子等正四面体分子结构的教学,也可应用于数学中立体几何的有关异面直线等方面的教学。利用正四面体还可以组合成其他形状的立体图形。例如,由一个正四面体可以切割成较小的正八面体,其方法是将正四面体的四个顶点从它的三条棱的中点切下,便可得到一个较小的正八面体。如果以一个正四面体为中心,另用四个与之全等的正四面体分别与它的四个面相連接,就可以得到一个十二个面全等的凹十二面体。
2.三角双锥模型直接应用于五氯化磷(PCl5)等具有三角双锥结构的分子结构的教学。也可用于数学教学。
3.正八面体应用于分子或离子组成为RX6、RX6n-型结构的教学。两个或两个以上的正八机体之间还可以进行不同方式的重叠就可以得到多种空间图形,对讲解超八面体等空间结构教学有很大的帮助。
4.正二十面体是专门用于B12分子结构的教学。在正二十面体中,每个顶点上有一个硼原子,每一条棱表示一根B—B键。有了这个模型,我们就可以清楚地算出在B12分子中所含有的B—B键数以及每一个硼原子跟周围的五个硼原子以五个B—B单键相结合。
在教学过程中,常常遇到有关C60的结构的教学难点,如果我们从硼12的结构开始讲起,就可以达到教学目的。因为B12是由12个硼原子构成的正二十面体,将正二十面体的每条棱三等分,然后将十二个硼原子等同地割下,因每个硼原子原有五条棱,所以割下后留下了一个正五边形的面,一个顶点就变成了五个顶点,原来的正三角形的面成变成了一个以原三角形边长的三分之一为边长的正六边形,这样新的图形就有5×12=60个顶点,有12个正五边形和20个正六边形。这种结构就是我们通常所说的C60的结构。
以上的使用说明只是一些典型的应用,其实它们应该还有很多的应用,这就得看看每个教学工作者在实际教学中如何发挥它们的用途。
赤壁一中化学组刘光利
二00四年五月二十八日
(完整版)常见晶胞模型
氯化钠晶体 离子晶体 (1)NaCI晶胞中每个Na+等距离且最近的Cl-(即Na+配位数)为6个 (2) (3)NaCI晶胞中每个CI-等距离且最近的Na+(即CI-配位数)一个晶胞内由均摊法计算出一个晶胞内占有的Na+4个; 占有的CI-4个。 在该晶体中每个Na+周围与之最接近且距离相等的Na+ 与每个Na+等距离且最近的CI-所围成的空间几何构型为 CsCI晶体(注意:右侧小立方体为CsCI晶胞;左侧为8个晶胞) (1)CsCI晶胞中每个Cs+等距离且最近的C「(即Cs+配位 数)为8个 CsCI晶胞中每个CI-等距离且最近的Cs+(即CI-配位数)为 8个,这几个Cs+在空间构成的几何构型为正方体。 (2)在每个Cs+周围与它最近的且距离相等的Cs+有6个这 几个Cs+在空间构成的几何构型为正八面体。 ? Cs* OCI- (3)一个晶胞内由均摊法计算出一个晶胞内占有的Cs+ 1个;占有的CI- 1个CaF2晶体 (1))Ca2+立方最密堆积,F-填充在全部四面体空隙中。 (2)CaF2晶胞中每个Ca2+等距离且最近的F-(即Ca2+配位数)为8个CaF2晶胞中每个F-等距离且最近的Ca2+(即F-配位数)为4个 (3)一个晶胞内由均摊法计算出一个晶胞内占有的Ca2+4个; 占有的F-8个。 ZnS晶体: (1)1个ZnS晶胞中,有4 个S2「,有4个 Zn2+ (2)Zn2+的配位数为4个, S2_的配位数为4个 O£n?,?
原子晶体 (1) 金刚石晶体 a 每个金刚石晶胞中含有 8个碳原子,最小的碳环为 6元环,并且不在同一平面(实际为椅 式结 构),碳原子为sp 3杂化,每个C 以共价键跟相邻的_4_个 C 结合,形成正四面体。键角109° 28' b 、 每个碳原子被12个六元环共用,每个共价键被6个六元环共用 c 、 12g 金刚石中有2mol 共价键,碳原子与共价键之比为 (2) Si 晶体 由于Si 与碳同主族,晶体Si 的结构同金刚石的结构。将金刚石晶胞中的 C 原子全部换成Si 原 子,健长稍长些便可得到晶体硅的晶胞。 (3) 某些非金属化合物【SiO 2、SiC (金刚砂)、BN (氮化硼)、Si 3N 4等】 例如SiC 将金刚石晶胞中的一个C 原子周围与之连接的4个C 原子全部换成Si 原子, 键长稍长些便可得到SiC 的晶胞。(其中晶胞的8个顶点和6个面心为Si 原子,4个互不相邻的立方 体体心的为C 原子,反之亦可) a 每个SiC 晶胞中含有 4个硅原子,含有 A 个碳原子 b 、1mol SiC 晶体中有4mol Si —C 共价键 (4)SiO 2晶体:在晶体硅的晶胞中,在每2个Si 之间插入1个O 原子, 便可 得到SiO 2晶胞。 a 每个硅原子都采取sp 3杂化,与它周围的4个氧原子所形成的空间 结构为正四面体型,SiO 2 晶体中最小的环为 _J2_ 元环 b 、每个Si 原子被 亚个十二元环共用,每个 O 原子被_6_个 十二元环共用 c 、每个SiO 2晶胞中含有_8_个Si 原子,含有J6_个O 原子 d 、1mol Si O 2晶体中有_4 mol 共价键 (5)晶体硼 已知晶体硼的基本结构单元是由 B 原子构成的正二十面体,其中有 20个等边三角形的面和一定 数目的顶点,每个顶点各有一个 B 原子。通过观察图形及推算,可知此结构单元是由 12个B 原子构成,其中B —B 键间的夹角是 60 ° 。假设将晶体硼结构单元中每个顶角均削去,余下 部分 的结构与G 。相同,贝U Go 由_12_个正五边形和 20个正六边形构成。 金刚石 金刚石晶胞 金刚石晶胞分位置注释 Si O
几种常见晶体结构分析
几种常见晶体结构分析文档编制序号:[KK8UY-LL9IO69-TTO6M3-MTOL89-FTT688]
几种常见晶体结构分析 河北省宣化县第一中学 栾春武 邮编 075131 栾春武:中学高级教师,张家口市中级职称评委会委员。河北省化学学会会员。市骨干教师、市优秀班主任、模范教师、优秀共产党员、劳动模范、县十佳班主任。 联系电话: E-mail : 一、氯化钠、氯化铯晶体——离子晶体 由于离子键无饱和性与方向性,所以离子晶体中无单个分子存在。阴阳离子在晶体中按一定的规则排列,使整个晶体不显电性且能量最低。离子的配位数分析如下: 离子数目的计算:在每一个结构单元(晶胞)中,处于不同位置的微粒在该单元中所占的份额也有所不同,一般的规律是:顶点上的微粒属于该 单元中所占的份额为18,棱上的微粒属于该单元中所占的份额为1 4,面上 的微粒属于该单元中所占的份额为1 2,中心位置上(嚷里边)的微粒才完 全属于该单元,即所占的份额为1。 1.氯化钠晶体中每个Na +周围有6个Cl -,每个Cl -周围有6个Na +,与一个Na +距离最近且相等的Cl -围成的空间构型为正八面体。每个Na +周围与其最近且距离相等的Na +有12个。见图1。 图1 图2 NaCl
晶胞中平均Cl-个数:8×1 8 + 6× 1 2 = 4;晶胞中平均Na+个数:1 + 12×1 4 = 4 因此NaCl的一个晶胞中含有4个NaCl(4个Na+和4个Cl-)。 2.氯化铯晶体中每个Cs+周围有8个Cl-,每个Cl-周围有8个Cs+,与一个Cs+距离最近且相等的Cs+有6个。 晶胞中平均Cs+个数:1;晶胞中平均Cl-个数:8×1 8 = 1。 因此CsCl的一个晶胞中含有1个CsCl(1个Cs+和1个Cl-)。 二、金刚石、二氧化硅——原子晶体 1.金刚石是一种正四面体的空间网状结构。每个C 原子以共价键与4个C原子紧邻,因而整个晶体中无单 个分子存在。由共价键构成的最小环结构中有6个碳原 子,不在同一个平面上,每个C原子被12个六元环共用,每C—C键共6 个环,因此六元环中的平均C原子数为6× 1 12 = 1 2 ,平均C—C键数为 6×1 6 = 1。 C原子数: C—C键键数= 1:2; C原子数: 六元环数= 1:2。 2.二氧化硅晶体结构与金刚石相似,C被Si代替,C与C之间插 氧,即为SiO 2晶体,则SiO 2 晶体中最小环为12环(6个Si,6个O), 图3 CsCl 晶 图4 金刚石晶
常见的金属晶体结构
第二章作业 2-1 常见的金属晶体结构有哪几种它们的原子排列和晶格常数有什么特点 V、Mg、Zn 各属何种结构答:常见晶体结构有 3 种:⑴体心立方:-Fe、Cr、V ⑵面心立方:-Fe、Al、Cu、Ni ⑶密排六方:Mg、Zn -Fe、-Fe、Al、Cu、Ni、Cr、 2---7 为何单晶体具有各向异性,而多晶体在一般情况下不显示出各向异性答:因为单晶体内各个方向上原子排列密度不同,造成原子间结合力不同,因而表现出各向异性;而多晶体是由很多个单晶体所组成,它在各个方向上的力相互抵消平衡,因而表现各向同性。第三章作业3-2 如果其它条件相同,试比较在下列铸造条件下,所得铸件晶粒的大小;⑴金属模浇注与砂模浇注;⑵高温浇注与低温浇注;⑶铸成薄壁件与铸成厚壁件;⑷浇注时采用振动与不采用振动;⑸厚大铸件的表面部分与中心部分。答:晶粒大小:⑴金属模浇注的晶粒小⑵低温浇注的晶粒小⑶铸成薄壁件的晶粒小⑷采用振动的晶粒小⑸厚大铸件表面部分的晶粒小第四章作业 4-4 在常温下为什么细晶粒金属强度高,且塑性、韧性也好试用多晶体塑性变形的特点予以解释。答:晶粒细小而均匀,不仅常温下强度较高,而且塑性和韧性也较好,即强韧性好。原因是:(1)强度高:Hall-Petch 公式。晶界越多,越难滑移。(2)塑性好:晶粒越多,变形均匀而分散,减少应力集中。(3)韧性好:晶粒越细,晶界越曲折,裂纹越不易传播。 4-6 生产中加工长的精密细杠(或轴)时,常在半精加工后,将将丝杠吊挂起来并用木锤沿全长轻击几遍在吊挂 7~15 天,然后再精加工。试解释这样做的目的及其原因答:这叫时效处理一般是在工件热处理之后进行原因用木锤轻击是为了尽快消除工件内部应力减少成品形变应力吊起来,是细长工件的一种存放形式吊个7 天,让工件释放应力的时间,轴越粗放的时间越长。 4-8 钨在1000℃变形加工,锡在室温下变形加工,请说明它们是热加工还是冷加工(钨熔点是3410℃,锡熔点是232℃)答:W、Sn 的最低再结晶温度分别为: TR(W) =(~×(3410+273)-273 =(1200~1568)(℃)>1000℃ TR(Sn) =(~×(232+273)-273 =(-71~-20)(℃) <25℃ 所以 W 在1000℃时为冷加工,Sn 在室温下为热加工 4-9 用下列三种方法制造齿轮,哪一种比较理想为什么(1)用厚钢板切出圆饼,再加工成齿轮;(2)由粗钢棒切下圆饼,再加工成齿轮;(3)由圆棒锻成圆饼,再加工成齿轮。答:齿轮的材料、加工与加工工艺有一定的原则,同时也要根据实际情况具体而定,总的原则是满足使用要求;加工便当;性价比最佳。对齿轮而言,要看是干什么用的齿轮,对于精度要求不高的,使用频率不高,强度也没什么要求的,方法 1、2 都可以,用方法 3 反倒是画蛇添足了。对于精密传动齿轮和高速运转齿轮及对强度和可靠性要求高的齿轮,方法 3 就是合理的。经过锻造的齿坯,金属内部晶粒更加细化,内应力均匀,材料的杂质更少,相对材料的强度也有所提高,经过锻造的毛坯加工的齿轮精度稳定,强度更好。 4-10 用一冷拔钢丝绳吊装一大型工件入炉,并随工件一起加热到1000℃,保温后再次吊装工件时钢丝绳发生断裂,试分析原因答:由于冷拔钢丝在生产过程中受到挤压作用产生了加工硬化使钢丝本身具有一定的强度和硬度,那么再吊重物时才有足够的强度,当将钢丝绳和工件放置在1000℃炉内进行加热和保温后,等于对钢丝绳进行了回复和再结晶处理,所以使钢丝绳的性能大大下降,所以再吊重物时发生断裂。 4-11 在室温下对铅板进行弯折,越弯越硬,而稍隔一段时间再行弯折,铅板又像最初一样柔软这是什么原因答:铅板在室温下的加工属于热加工,加工硬化的同时伴随回复和再结晶过程。越弯越硬是由于位错大量增加而引起的加工硬化造成,而过一段时间又会变软是因为室温对于铅已经是再结晶温度以上,所以伴随着回复和再结晶过程,等轴的没有变形晶粒取代了变形晶粒,硬度和塑性又恢复到了未变形之前。第五章作业 5-3 一次渗碳体、二次渗碳体、三次渗碳体、共晶渗碳体、共析渗碳体异同答:一次渗碳体:由液相中直接析出来的渗碳体称为一次渗碳体。二次渗碳体:从 A 中析出的渗碳体称为二次渗碳体。三次渗碳体:从 F 中析出的渗碳体称为三次渗碳体共晶渗碳体:经共晶反应生成的渗碳体即莱氏体中的渗碳体称为共晶渗碳体共析渗碳体:经共析反应生成的渗碳体即珠光体中的渗
“制作DNA分子双螺旋结构模型”教学设计
“制作DNA分子双螺旋结构模型”教学设计 【活动目的与意义】 1制作模型的过程是一个知识内化的过程,通过亲手制作,可以促进学生对DNA分子“双螺旋结构”和“反向平行”特点的理解和认识。 2通过讨论、交流与撰写活动报告,培养学生观察问题、分析和归纳问题的能力以及语言表达和书面表达能力。 3通过制作DNA分子双螺旋结构模型,培养学生互助合作的精神和严谨的科学态度,并使他们在具体的制作过程中体验到成功的喜悦。 4通过分析DNA分子结构模型,将抽象知识形象化,有利于学生准确把握DNA分子结构的知识,为后续学习遗传部分的知识奠定良好的基础。 【活动程序】 1制定活动方案 1.1课前进行相应的知识储备 课前学生学习了DNA分子结构的基础知识,以及通过图书馆、网络等途径收集和掌握了一些有关DNA结构发现的科学史的材料,为课上进行相互讨论、交流与模型的顺利制作提供了必要的知识准备。
1.2活动材料用具的准备 硬塑料方框、不同颜色的硬纸板、金属细丝、订书机、订书钉、剪刀、粗铁丝。 1.3提供模型制作的参考数据 1.4设计活动方案流程 2实施活动方案 2.1分组并发放活动材料 每班分若干个小组,每小组4人。各组都配发硬塑料方框2个(5cm×10?M)、六种不同颜色的硬纸板各1张(20?M ×20?M)、细铁丝2根(长0.5m)、粗铁丝2根(长约10?M)订书机1个、订书钉若干、剪刀1把、活动报告(每人一份)。 2.2分组讨论制作模型的步骤和注意事项 在学生讨论之前,教师先展示预设的问题和制作模型的参考数据,为学生讨论模型的制作提供帮助。设计的问题如下: (1)分别用何材料表示磷酸基团、脱氧核糖、各种含氮碱基?这几种物质在什么部位相连接? (2)如何表示磷酸二酯键、氢键以及氢键的数目? (3)如何体现DNA分子两条链之间的反向平行关系? (4)怎样才能使DNA分子的平面模型改变成立体模型? 以实验小组为单位,观察并分析教材上的DNA分子结构的立体图和平面图,然后根据实验桌上所提供的材料,以
建筑模型制作报告
建筑模型制作报告 Company number【1089WT-1898YT-1W8CB-9UUT-92108】
建筑模型制作报告学院:合肥学院 专业:建筑学 年级: 12级(1)班 学号: 姓名:骆家伟 指导教师:张程王恺 一、模型制作的时间:13—14学年8、9两周 二、模型制作的目的 本次实践是建筑学专业的综合性实践教学环节,旨在培我们的实际动手能力。其主要任务是使我们理解模型制作在作品设计中的重要性,掌握模型制作的基本工具、方法和过程,锻炼我们的动手实践能力,完善我们的设计知识和设计实践能力。《建筑模型制作》是我们从图纸到实体之间的桥梁,它具有综合性强、涉及面广和实践性强等显着特点。通过这一环节的学习,能培养我们读懂图纸、了解设计,综合运用所学理论知识分析、解决实际问题。随着我国城乡城市化建设的快速发展,人们对房地产业的要求越来越高,模型市场需求越来越大,为其今后走上工作岗位从事有关实际工作打下一个良好的基础。 三、模型制作的内容 1.查找资料老师布置下任务后,我们就对制作建筑模型有了初步的印象。我们查阅书籍并在网上心细查找,最后决定制作现代简约的装饰风
格。该风格是大家比较熟悉的,室内的装饰品也不是很多,且制作比较简单,我们初次做模型比较容易接受。 2.完成模型的制作根据所绘制的建筑草图,利用建筑模型所使用的工具(三合板、KT板、双面胶、AB胶、丁字尺、三角板、剪刀等等)正确地表现所选建筑的三维空间,并能做到与平、立、剖面图一致。此外,模型制作尽可能准确细致、简洁美观! 3.成果报告写成果报告,总结这次模型制作的心得体会与成果。其中包括做得好的地方继续发展与做的不足需要日后改进的方面。通过这种方式,有助于更好地提升自我。 四:收获与体会 在未开工之前,组员间讨论,分工合作(绘图、收集材料、动手制作);准备用建筑方案。首先,从班里我们已备齐了所有的工具,包括模型刀,丁字尺,三角板,剪刀,模型胶,铅笔,橡皮,双面胶,砂纸,界尺,颜料。选择材料时要考虑的因素①模型的制作速度。②预期达到的修改和实验的程度。③在模型尺寸范围内,材料保持形状和跨度的能力。④模型所反映的组件的厚度。通过比较分析,我们决定使用木板来做为模型的基本材料,不选用其他的补充材料。接下来就是看似不重要却很重要的一步了,那就是选择适合自己的装饰风格,对此老师并没有太多的要求。我们仔细研究了所有的方案,发现家具是不好做的,因为它小、多,而且还要做的精致,这个部分不仅考验人的耐心也考研人得细心程度。这种装饰风格刚好适合我们的特点,我们自己比较容易专注于细部,在细部打造方面可能会比较有优势,我们认为只有掌握好比例与材料纹理,是比较容易打造出好作品的,若装饰太烦
DNA模型制作
DNA分子结构特点 DNA衍射图谱沃森和克里克在生命的旋梯上制作D N A分子模型 主要学科:生物 操作难度:★★☆☆☆ 知识难度:★★★☆☆ 预计完成时间:2 小时 适合实践场所:家庭、学校 ●了解DNA分子结构的发展史 ●使用废旧材料亲手制作DNA分子模型 ●改进、创新实验材料和制作方法 DNA分子结构的发展史 20世纪30年代,科学家发现:组成DNA分子的单位是脱 氧核苷酸。 20世纪30年代,科学家们还发现:DNA分子是由含4种碱基的脱氧核苷酸长链构成的。 1951年春天,英国科学家威尔金斯和富兰克林在意大利生物大分子结构会议上展示了DNA的X射线衍射图谱。 沃森和克里克根据DNA衍射图谱的有关数据为基础,推算出DNA分子呈螺旋结构。沃森和克里克经过反复尝试最终构建了一个将磷酸-脱氧核糖骨架安排在螺旋外部,碱基安排在螺旋内部的双链螺旋。在这个模型中是相同的碱基进行配对,即A与A、T与T配对。但是有化学家指出这种配对方式违反了 化学规律。 1952年,奥地利著名生物化学家查哥夫应用层析法对多种生物DNA的碱基进行了分析发现:腺嘌呤(A)的量总是等于胸腺嘧啶(T)的量,鸟嘌呤(G)的量总是等于胞嘧啶(C)的量。 于是沃森和克里克利用查哥夫的成果改变了碱基配对方式,让A与T配对,G与C配对(氢键连接),构建出新的DNA模 型。 于是沃森和克里克利用查哥夫的成果改变了碱基配对方式,让A与T配对,G与C配对(氢键连接),构建出新的DNA模型。 发现·探索
扫一扫二维码,看看教师做的“DNA 分子模型”,看看有没有可以改进和创新的地方。 材料用具: 硬纸方块2个(长约10cm ),卡纸片,剪刀,订书机,订书针,钳子,长0.5米细铁丝两根。 方法与步骤: 1、用不同颜色的卡纸剪成长方形碱基,用其他颜色的 卡纸剪成圆形代表磷酸,另一种颜色的卡纸剪成五 边形,代表脱氧核糖。 2、使用订书机将磷酸、脱氧核糖。碱基连接,制作成 一个个含有不同碱基脱氧核糖核苷酸模型。 3、用订书机把一个个脱氧核糖核苷酸模型连接起来, 形成一条多核苷酸的长链; 根据接碱基互补配对原 则,制作一条与这条链完全互补的脱氧核糖核苷酸 长链。 4、将脱氧核糖核苷酸中的磷酸固定在细铁丝上,然后 把两条链平放在桌子上,用订书机把配对的碱基两 两连接在一起。 5、将两条的链的末端分别与硬纸方块连接在一起, 两手分别提起硬纸方块、轻轻旋转、即可得到一个 DNA 分子双螺旋结构模型。 亲手制作 DNA 分子模型 动手·制作 学 习任务 动手·制作 在现实生活中,有很多可以利用的废旧材料,对照老师的制作方法,你看看有什么可以创新和改进的地方?最好利用身边的废旧材料,亲手制作一个DNA 分子模型吧!
常见典型晶体晶胞结构.doc
典型晶体晶胞结构1.原子晶体 (金刚石 ) 2.分子晶体
3.离子晶体 + Na - Cl
4.金属晶体 堆积模型简单立方钾型镁型铜型典型代表Po Na K Fe Mg Zn Ti Cu Ag Au 配位数 6 8 12 12 晶胞 5.混合型晶体——石墨 1.元素是Cu 的一种氯化物晶体的晶胞结构如图 13 所示,该氯化物的化学 式,它可与浓盐酸发生非氧化还原反应,生成配合物H n WCl 3,反应的化 学方程式为。 2.( 2011 山东高考)CaO 与NaCl 的晶胞同为面心立方结构,已知CaO 晶体密度为ag·cm-3,N A表示阿伏加德罗常数,则CaO 晶胞体积为cm3。 2.( 2011 新课标全国)六方氮化硼BN 在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚 石相当,晶苞边长为361.5pm ,立方氮化硼晶胞中含有______各氮原子、 ________各硼原子,立方氮化硼的密度是_______g ·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为N A)。
解析:描述晶体结构的基本单元叫做晶胞,金刚石晶胞是立方体,其中8 个顶点有8 个碳原子, 6 个面各有 6 个碳 原子,立方体内部还有 4 个碳原子,如图所示。所以金刚石的一个晶胞中含有的碳原子数= 8×1/8+6 ×1/2+4=8 ,因此立方氮化硼晶胞中应该含有 4 个 N 和 4 个 B 原子。由于立方氮化硼的一个晶胞中含有 4 个 4 25g 是,立方体的体积是(361.5cm)3,因此立方氮化硼的密度是 N 和 4 个 B 原子,其质量是 1023 6.02 g·cm-3。 3.( 4)元素金( Au )处于周期表中的第六周期,与Cu 同族, Au 原子最外层电子排布式为______;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu 原子处于面心, Au 原子处于顶点位置,则该合金中Cu 原子与 Au 原子数量之比为 _______;该晶体中,原子之间的作用力是________; ( 5)上述晶体具有储氢功能,氢原子可进入到由Cu 原子与 Au 原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为_____。 4.( 2010 山东卷)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心, O2-处于晶胞棱边中心,该化合物化学式为,每个 Ba2+与个 O2-配位。 5.(4) CaC2晶体的晶胞结构与NaCl晶体的相似(如右图所示),但 CaC2晶体中含有的中哑 铃形 C 22 的存在,使晶胞沿一个方向拉长。CaC 2晶体中1个 Ca 2 周围距离最近的 C 22 数目 为。 6.( 09 江苏卷 21 A )③在 1 个 Cu2O 晶胞中(结构如图所示),所包含的Cu 原子数目 为。
分子模型晶体模型的制作
分子模型、晶体模型的制作 赤壁一中化学组 刘光利 二○○四年五月 制作目的: 1.充分利用分子模型等直观的教学用具,有利于培养学生的联想能力,通过各种模型可以提高教学速度和教学质量,解决书上难以表明的立体结构,从而达到突破难点的目的。 2.理解分子结构和晶体结构 培养用物质结构特点来认识物质的特性 制作材料:厚硬纸板、胶水或透明胶、铁丝、直尺、三角板、剪刀 制作方法: 1、正四面体的制作 在厚硬纸板上划好四个等边三角形如图1a 所示,然后沿实线剪下,再沿虚线划痕迹以便折叠,折叠后用粘合剂粘牢即成图1b 所示。 2、三角双锥分子模型的制作 在厚硬纸板上划好六个等腰三角形如图2a 所示,然后沿实线剪下,再沿虚线划痕迹以便折叠,折叠后用粘合剂粘牢即成图2b 所示。 图2a 图 2b 图1a 图 1b
3、正八面体分子模型的制作 在厚硬纸板上划好八个等边三角形如图3a所示,然后沿实线剪下,再沿虚线划痕迹以便折叠,折叠后用粘合剂粘牢即成图3b。 图3a 图3b 4、正二十面体分子模型的制作(B12) 在厚硬纸板上划好二十个等边三角形如图5a所示,然后沿实线剪下,再沿虚线划痕迹以便折叠,折叠后用粘合剂粘牢即成图5b所示。 图5a 图5b
使用说明 1.正四面体模型直接应用于白磷分子、甲烷分子、四氯化碳分子等正四面体分子结构的教学,也可应用于数学中立体几何的有关异面直线等方面的教学。利用正四面体还可以组合成其他形状的立体图形。例如,由一个正四面体可以切割成较小的正八面体,其方法是将正四面体的四个顶点从它的三条棱的中点切下,便可得到一个较小的正八面体。如果以一个正四面体为中心,另用四个与之全等的正四面体分别与它的四个面相連接,就可以得到一个十二个面全等的凹十二面体。 2.三角双锥模型直接应用于五氯化磷(PCl5)等具有三角双锥结构的分子结构的教学。也可用于数学教学。 3.正八面体应用于分子或离子组成为RX6、RX6n-型结构的教学。两个或两个以上的正八机体之间还可以进行不同方式的重叠就可以得到多种空间图形,对讲解超八面体等空间结构教学有很大的帮助。 4.正二十面体是专门用于B12分子结构的教学。在正二十面体中,每个顶点上有一个硼原子,每一条棱表示一根B—B键。有了这个模型,我们就可以清楚地算出在B12分子中所含有的B—B键数以及每一个硼原子跟周围的五个硼原子以五个B—B单键相结合。 在教学过程中,常常遇到有关C60的结构的教学难点,如果我们从硼12的结构开始讲起,就可以达到教学目的。因为B12是由12个硼原子构成的正二十面体,将正二十面体的每条棱三等分,然后将十二个硼原子等同地割下,因每个硼原子原有五条棱,所以割下后留下了一个正五边形的面,一个顶点就变成了五个顶点,原来的正三角形的面成变成了一个以原三角形边长的三分之一为边长的正六边形,这样新的图形就有5×12=60个顶点,有12个正五边形和20个正六边形。这种结构就是我们通常所说的C60的结构。 以上的使用说明只是一些典型的应用,其实它们应该还有很多的应用,这就得看看每个教学工作者在实际教学中如何发挥它们的用途。 赤壁一中化学组刘光利 二00四年五月二十八日
高中化学选修三几种典型晶体晶胞结构模型总结
学生版:典型晶体模型 晶体晶体结构晶体详解 原子晶体 金 刚石 (1)每个碳与相邻个碳以共价键 结合, 形成体结构 (2)键角均为 (3)最小碳环由个C组成且六个原子不 在同一个平面内 (4)每个C参与条C—C键的形成,C 原子数与C—C键数之比为 S iO 2 (1)每个Si与个O以共价键结合,形成正 四面体结构 (2)每个正四面体占有1个Si,4个“ 1 2 O”,n(Si)∶n(O)= (3)最小环上有个原子,即个O,个 Si 分子晶体 干 冰 (1)8个CO 2 分子构成立方体且在6个面心 又各占据1个CO 2 分子 (2)每个CO 2 分子周围等距紧邻的 CO 2 分子 有个 冰 每个水分子与相邻的个水分子,以 相连接,含1 mol H 2 O的冰中,最多可形成 mol“氢键”。 N aCl(型) 离 子晶 体 (1)每个Na+(Cl-)周围等距且紧邻的 Cl-(Na+)有个。每个Na+周围等距且紧邻 的 Na+有个 (2)每个晶胞中含个Na+和个Cl-
C sCl (型) (1)每个Cs+周围等距且紧邻的Cl-有个,每个Cs+(Cl-)周围等距且紧邻的Cs+(Cl-) 有个 (2)如图为个晶胞,每个晶胞中含 个Cs+、个Cl- 金属晶体 简 单六 方堆 积 典型代表Po,配位数为,空间利用率 52% 面 心立 方 最 密堆 积 又称为A 1 型或铜型,典型代表, 配位数为,空间利用率74% 体 心立 方 堆 积 又称为A 2 型或钾型,典型代表, 配位数为,空间利用率68% 六 方最 密 堆 积 又称为A 3 型或镁型,典型代表, 配位数为,空间利用率74% 混合晶体石墨 (1)石墨层状晶体中, 层与层之间的作用是 (2)平均每个正六边形 拥有的碳原子个数是,C
制作甲烷分子模型试题
实验1、《制作甲烷分子模型》试题 考生姓名:、组别考号 说明: 1、实验操作前,请仔细阅读本试卷。请独立完成试题布置的要求。 2、本实验时间20分钟,试题满分为20分。 一、实验目的: 1、学会使用多种工具和材料,完成简单分子模型的制作; 2、通过甲烷分子(由一个C原子和四个H原子构成)模型的制作,加深对分子构成的认识;学习通过分子模型认识分子的科学方法。 二、器材: 小刀、各色橡皮泥、泡沫塑料、牙签、酒精灯(火柴) 三、实验准备: 甲烷分子的比例模型甲烷分子的球棍模型经过科学实验证明甲烷分子的结构是正四面体结构,碳原子位于正四面体的中心,4个氢原子分别位于正四面体的4个顶点上(键角是109°28)。 五、回顾与反思: 1、甲烷这种物质在微观上是由构成的。 2、甲烷分子是由构成的。 3、上述学习是通过模型认识分子的科学方法。模型可以是物理实体,也可以是某种图形或者是一种数学表达式。请你再举出初中科学学习中利用模型的2个实例:。 4、请你画出水分子的结构模型:。
表现性评价:实验1、《制作甲烷分子模型》组别: 评分教师签名:________、________
实验2、《电学实验专题探究》试题 考生姓名:、组别考号 说明: 1、实验操作前,请仔细阅读本试卷。请独立完成试题布置的任务。 2、本实验时间30分钟,试题满分为30分。 情景1:在同一个的照明电路中,不同阻值的灯泡亮度不同。 一、实验目的: 1、探究导体中的电流与导体阻值的定量关系; 2、控制变量法使用;实验数据的分析处理。 二、器材: 不同阻值的定值电阻3个、电流表、电压表、滑动变阻器、学生电源、导线若干、开关1个 三、实验步骤和记录: 实验:探究电流与导体阻值的关系。 1、提出问题:。 2、你的猜想:。 3、实验思路:按照探究目的设计并连接电路;先测某电压下的其中一个电阻 的电流;更换电阻,保持电压不变测出对应的电流;分析数据得出结论。 请在右边方框内画出本实验的电路图: 5、改变电压的预定值,多次实验,记录数据。(注:本次实验此步骤省略)。 6、分析数据,得出结论:。 情景2见后
SVAR模型制作过程
设置月度数据MONTHLY>start date:2008M01>end date 2018M08 一,数据的季节调整(利用x-12进行季节性调整) 由于在建模时所选取的是宏观经济的月度数据,而月度数据容易受到季节因素的影 响,从而掩盖经济运行的客观规律,因此我们采用Census X13(功能时最强大的)调整方法对各个变量数据进行季节性调整。分别记做CPI’、FOOD’、HOUSE’、M2’、 VMI’。 时间序列按照时间次序排列的随机变量序列,任何时间序列经过合理的函数变换后都可以被认为由几个部分叠加而成。三个部分:趋势部分(T),季节部分(S) 和随机噪声部分(I)。常见的时间序列都是等间隔排列的。 时间序列调整各部分构成的基本模型 X t=T t++T t+I t对任何时刻有,E(I t)=0,Var(I t)=σ2加法模型 X t=T t*T t*I t对任何时刻有,E(I t)=1,Var(I t)=σ2加法模型 (1)判定一个数据序列究竟适合乘法模型还是加法模型,可考察其趋 势变化持性及季节变化的波动幅度。 (2)所谓季节调整就是按照上述两种模型将经济时间序列进行分解, 去掉季节项的序列成为调过序列。 对于时间序列而言是否存在整体趋势?如果是,趋势是显示持续存在还是显示将随时间而消逝? 对于时间序列而言是否显示季节性变化?如果是,那么这种季节的波动是随时间而加剧还是持续稳定存在? 对于时间序列的分解模型主要有加法模型和乘法模型。 加法模型适用于T、S、C相互独立的情形。 乘法模型适用于T、S、C相关的情形。由于时间序列分解的四大要素一般都存在相 互影响,因此大多数的经济数据都采用乘法模型进行季节性分解。 第一步:双击进行季节性调整的变量组CPI,proc >Seasonal Adjustment>x-12
角色模型制作流程
幻想之旅角色模型制作流程 1.拿到原画后仔细分析角色设定细节,对不清楚的结构、材质细节及角色身高等问题与 原画作者沟通,确定对原画理解准确无误。 2.根据设定,收集材质纹理参考资料。 3.开始进行低模制作。 4.制作过程中注意根据要求严格控制面数(以MAX为例,使用Polygon Counter工具查 看模型面数)。 5.注意关节处的合理布线,充分考虑将来动画时的问题。如有疑问与动作组同事讨论咨 询。 6.由于使用法线贴图技术不能使用对称复制模型,可以直接复制模型,然后根据具体情 况进行移动、放缩、旋转来达到所需效果。 7.完成后,开始分UV。 分UV时应尽量充分利用空间,注意角色不同部位的主次,优先考虑主要部位的贴图(例如脸,前胸以及引人注意的特殊设计),为其安排充分的贴图面积。使用Relax Tool 工具确保UV的合理性避免出现贴图的严重拉伸及反向。 8.低模完成后进入法线贴图制作阶段。 现在我们制作法线贴图的方法基本上有三种分别是: a.在三维软件中直接制作高模,完成后将低模与高模对齐,然后使用软件工具生成法 线贴图。 b.将分好UV的低模Export成OBJ格式文件,导入ZBrush软件。在ZB中添加细节 制作成高模,然后使用Zmapper插件生成法线贴图。 c.在Photoshop中绘制纹理或图案灰度图,然后使用PS的法线贴图插件将灰度图生成 法线贴图。 (具体制作方法参见后面的制作实例) 建议在制作过程中根据实际情况的不同,三种方法结合使用提高工作效率。 9.法线贴图完成后,将其赋予模型,查看法线贴图的效果及一些细小的错误。 10.进入Photoshop,打开之前生成的法线贴图,根据其贴在模型上的效果对法线贴图进行 修整。(例如边缘的一些破损可以使用手指工具进行修补,或者在绿色通道中进行适当的绘制。如需加强某部分法线贴图的凹凸效果可复制该部分进行叠加可以起到加强
建筑模型制作流程
建筑制作项目流程 1、制作前期策划 根据甲方提供的平面图、立面图、效果图及模型要求,制定模型制作风格。 2、模型报价预算 预算员根据[1]、模型比例大小、材料工艺及图纸深度确定模型收费、签订制作服务订单。 3、制作组织会审 技术人员将核对分析图纸,确定模型材质、处理工艺、制作工期及效果要求。 (1)建筑制作进程: 建筑制作师根据甲方提供的图纸施工制作,效果以真实、美观为原则。所有建筑均采用AutoCAD绘图,电脑雕刻机切割细部、建筑技师手工粘接的流水线作业法,既保证了各部件的质量又保证了工期。 (2)环境景观设计制作进程: 总体环境将由专业景观设计师进行把控。专业制作人员结合图纸进行设计制作。原则是根据甲方的设计图纸再现设计师的设计意图。切不可胡乱操作,自由发挥。同时使用仿真树木、小品、雕塑等进行点缀,使得整个景观部分美观精致。 (3)建筑环境灯光组装: 灯光系统根据甲方要求进行设计制作,体现沙盘的夜景效果。 4、制作完工检验 质检部经理及项目负责人对照图纸,进行细部检查和调整。 5、模型安装调试 模型服务人员在模型展示地现场调试安装清洁,达到甲方满意后离开。 编辑本段 建筑模型分类 黏土模型 黏土材料来源广泛取材方便价格低廉经过“洗泥”工序和“炼熟过程其质地更加细腻。黏土具有一定的粘合性可塑性极强在塑造过程中可以反复修改任意调整修刮填,补比较方便。还可以重复使用是一种比较理想的造型材料,但是如果黏土中的水分失去过多则容易使黏土模型出现收缩龟裂甚至产生断裂现象不利于长期保存。另外,在黏土模型表面上进行效果处理的方法也不是很多,黏土制作模型时一定要选用含沙量少,在使用前要反复加工,把泥和熟,使用起来才方便。一般作为雕塑、翻模用泥使用。 油泥模型 油泥是一种人造材料。凝固后极软,较软,坚硬。油泥可塑性强,黏性、韧性比黄泥(黏土模型)强。它在塑造时使用方便,成型过程中可随意雕塑、修整,成型后不易干裂,可反复使用。油泥价格较高,易于携带,制作一些小巧、异型和曲面较多的造型更为合适。一般像车类、船类造型用油泥极为方便。所以选用褐油泥作为油泥的最外层是很明智的选择。油泥的材料主要成分有滑石粉62%、凡士林30%、工业用蜡8%。 石膏模型 石膏价格经济,方便使用加工,用于陶瓷、塑料、模型制作等方面。石膏质地细腻,成型后易于表面装饰加工的修补,易于长期保存,适用于制作各种要求的模型,便于陈列展示。 塑料模型 塑料是一种常用制作模型的新材料。塑料品种很多,主要品种有五十多种,制作模型应
……网络游戏角色模型制作流程
网络游戏角色模型制作流程: 工具:3D max or Maya (模型制作) Bodypaint and photoshop(贴图绘制) Ufold(Uv插件) 面数:534 贴图一张大小:512X512 (最终效果) 模型制作:跳过…… 制作完成后把模型导出导出格式为OBJ 分UV: 网游角色分UV插件Unfold 打开Unfold 打开刚刚导出的OBJ格式的模型文件
调整操作方式:点击右上角edit mouse binding 在Load presets下选择Alias Wavefront Maya 点击OK 把控制方式调整成Maya的操作方式 Alt+鼠标左键:平移 Alt+鼠标中键:缩放 Alt+鼠标右键:旋转 Ctrl+鼠标左键:减选+鼠标右键:框选减选
右侧工具栏从上只下分别是: 1.光影显示 2.线框显示 3.光影线框显示 4.UV棋盘格显示 5.关闭开启灯光 6.视角回归物体 7.断开 8.线选择 9.面选择 鼠标左键点击线选择按住shift可选择整条线 选择后按断开线 断开后线成橙黄色表明已断开 然后点击上方的工具栏中的Unfold 在右边的显示框内得到UV
图中有黄色的地方说明UV有拉伸颜色越靠近橙黄色说明拉伸越严重 如上图的的颜色可忽视 可根据具体情况切分UV 完成后Ctrl+S保存Unfold将自动保存为新的OBJ文件文件名为 文件名_Unfold3d 然后将分好UV的OBJ模型导入MAYA或者3DMAX里面调整大小布局 Unfold使用方法介绍完毕 第二部分 网络游戏的贴图绘制 主要软件Bodypainter 3D 这里在使用软件不同的情况下有3种启动BP的方式 直接用MAX的启动方式: 将BP安装包中的b3d.bmi和bodyex.dlu两个文件放到MAX安装地址中的插件管理包“plugins”这个文件夹中 然后进入MAX
(完整版)常见晶胞模型
氯化钠晶体 (1)NaCl晶胞中每个Na+等距离且最近的Cl-(即Na+配位数)为6个 NaCl晶胞中每个Cl-等距离且最近的Na+(即Cl-配位数)为6个 (2)一个晶胞内由均摊法计算出一个晶胞内占有的Na+4_个; 占有的Cl-4个。 (3)在该晶体中每个Na+周围与之最接近且距离相等的Na+共有12个; 与每个Na+等距离且最近的Cl-所围成的空间几何构型为正八面体 CsCl晶体(注意:右侧小立方体为CsCl晶胞;左侧为8个晶胞) (1)CsCl晶胞中每个Cs+等距离且最近的Cl-(即Cs+配位数) 为8个 CsCl晶胞中每个Cl-等距离且最近的Cs+(即Cl-配位数) 为8个,这几个Cs+在空间构成的几何构型为正方体。 (2)在每个Cs+周围与它最近的且距离相等的Cs+有6个 这几个Cs+在空间构成的几何构型为正八面体。 (3)一个晶胞内由均摊法计算出一个晶胞内占有的Cs+ 1个;占有的Cl- 1个。 CaF2晶体 (1))Ca2+立方最密堆积,F-填充在全部四面体空隙中。 (2)CaF2晶胞中每个Ca2+等距离且最近的F-(即Ca2+配位数)为8个CaF2晶胞中每个F-等距离且最近的Ca2+(即F-配位数)为4个 (3)一个晶胞内由均摊法计算出一个晶胞内占有的Ca2+4个; 占有的F-8个。 ZnS晶体: (1)1个ZnS晶胞中,有4个S2-,有4个Zn2+。 (2)Zn2+的配位数为4个,S2-的配位数为 4个。
Si O 金刚石 金刚石晶胞 金刚石晶胞分位置注释 (1)金刚石晶体 a 、每个金刚石晶胞中含有8个碳原子,最小的碳环为6元环,并且不在同一平面(实际为椅 式结构),碳原子为sp 3杂化,每个C 以共价键跟相邻的_4_个C 结合,形成正四面体。键角109°28’ b 、每个碳原子被12个六元环共用,每个共价键被6个六元环共用 c 、12g 金刚石中有2mol 共价键,碳原子与共价键之比为 1:2 (2)Si 晶体 由于Si 与碳同主族,晶体Si 的结构同金刚石的结构。将金刚石晶胞中的C 原子全部换成Si 原子,健长稍长些便可得到晶体硅的晶胞。 (3)某些非金属化合物【SiO 2、SiC (金刚砂)、BN (氮化硼)、Si 3N 4等】 例如SiC 将金刚石晶胞中的一个C 原子周围与之连接的4个C 原子全部换成Si 原子, 键长稍长些便可得到SiC 的晶胞。(其中晶胞的8个顶点和6个面心为Si 原子,4个互不相邻的立方体体心的为C 原子,反之亦可) a 、每个SiC 晶胞中含有 4 个硅原子,含有 4 个碳原子 b 、1mol SiC 晶体中有4 mol Si —C 共价键 (4)SiO 2 晶体:在晶体硅的晶胞中,在每2个Si 之间插入1个O 原子, 便可得到SiO 2晶胞。 a 、每个硅原子都采取sp 3杂化,与它周围的4个氧原子所形成的空间 结构为__正四面体_型,S iO 2晶体中最小的环为 12 元环 b 、每个Si 原子被 12 个十二元环共用,每个O 原子被 6 个 十二元环共用 c 、每个SiO 2晶胞中含有 8 个Si 原子,含有 16 个O 原子 d 、1mol Si O 2晶体中有 4 mol 共价键 (5)晶体硼 已知晶体硼的基本结构单元是由B 原子构成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个顶点各有一个B 原子。通过观察图形及推算,可知此结构单元是由__12_个B 原子构成,其中B —B 键间的夹角是__60°__。假设将晶体硼结构单元中每个顶角均削去,余下部分的结构与C 60相同,则C 60由_12_个正五边形和_20个正六边形构成。
《模型制作》教案-胡校峰课件
江西现代职业技术学院 教案 课程名称模型制作班级 14环艺1、2班,14室内6、7、8班授课学期: 2015 ~ 2016 学年第一学期任课教师:胡校峰 教研室:室内设计 教学分院(系):设计分院
完成课时登记表
课题模型制作的基本概念课次:1 重点内容:模型制作的基本概念 模型的种类 模型制作的工具与材料介绍 1:简易裁切工具材料训练 难点内容:模型的属性与价值 模型的特点 讲授方法与实验方法:讲述,实例分析与讲解,提问,师生互动。作业:要学生们准备好模型制作的工具与材料。
课题:第一章第二节模型制作方法与实践课次:2 重点内容:模型制作的工具与材料 难点内容:模型制作的工具与材料的应用 讲授方法与实验方法:讲述,实例分析与讲解,教师先做示范演示,学生再按要求做练习,教师巡视指导学生做练习。 作业:练习1:简易模型训练制作训练基础:用A3卡纸,制作:1、50个高、宽为1CM的窗户,2、50个高为3CM、宽1.5CM,顶部为半圆形的窗户。要求:裁切工整,并保持纸张整洁、干净。不得有折痕、破损、污迹等。
课题:第一章第三节易加工材料的单体模型制作训练一课次:3 重点内容:纸质模型制作练习:1、特点介绍:适宜构思的训练,常作为短期实体建筑的模型。2、读懂立体图(三视图)3、立面展开图4、模型的尺寸与比例 难点内容:制作工艺:1、画制作图2、工具材料的正确使用3、模型的裁切方法4、模型的组装(卡纸模型具有制作简便,材料加工方便、粘接容易、在表现质感方面容易进行模拟处理等特点。纸质模型容易受潮而产生变形,不宜长期保存。) 讲授方法与实验方法:讲述,实例分析与讲解,教师先做示范演示,学生再按要求做练习,教师巡视指导学生做练习。 作业:练习2:用纸材料完成一个简易建筑模型制作练习。
常见晶胞模型
常见晶胞模型
氯化钠晶体 (1)NaCl晶胞中每个Na+等距离且最近的Cl-(即Na+配位数)为6个 NaCl晶胞中每个Cl-等距离且最近的Na+(即Cl-配位数)为6个 (2)一个晶胞内由均摊法计算出一个晶胞内占有的Na+4_个; 占有的Cl-4个。 (3)在该晶体中每个Na+周围与之最接近且距离相等的Na+共有12个; 与每个Na+等距离且最近的Cl-所围成的空间几何构型为正八面体 CsCl晶体(注意:右侧小立方体为CsCl晶胞;左侧为8个晶胞) (1)CsCl晶胞中每个Cs+等距离且最近的Cl-(即Cs+配位数) 为8个 CsCl晶胞中每个Cl-等距离且最近的Cs+(即Cl-配位数) 为8个,这几个Cs+在空间构成的几何构型为正方体。 (2)在每个Cs+周围与它最近的且距离相等的Cs+有6个 这几个Cs+在空间构成的几何构型为正八面体。 (3)一个晶胞内由均摊法计算出一个晶胞内占有的Cs+ 1个;占有的Cl- 1个。CaF2晶体 (1))Ca2+立方最密堆积,F-填充在全部四面体空隙中。 (2)CaF2晶胞中每个Ca2+等距离且最近的F-(即Ca2+配位数)为8个CaF2晶胞中每个F-等距离且最近的Ca2+(即F-配位数)为4个 (3)一个晶胞内由均摊法计算出一个晶胞内占有的Ca2+4个; 占有的F-8个。 ZnS晶体: (1)1个ZnS晶胞中,有4个S2-,有4个Zn2+。 (2)Zn2+的配位数为4个,S2-的配位数为 4个。
金刚石 金刚石晶胞 金刚石晶胞分位置注释 (1)金刚石晶体 a 、每个金刚石晶胞中含有8个碳原子,最小的碳环为6元环,并且不在同一平面(实 际为椅式结构),碳原子为sp 3杂化,每个C 以共价键跟相邻的_4_个C 结合,形成 正四面体。键角 109°28’ b 、每个碳原子被12个六元环共用,每个共价键被6个六元环共用 c 、12g 金刚石中有2mol 共价键,碳原子与共价键之比为 1:2 (2)Si 晶体 由于Si 与碳同主族,晶体Si 的结构同金刚石的结构。将金刚石晶胞中的C 原子全部换成Si 原子,健长稍长些便可得到晶体硅的晶胞。 (3)某些非金属化合物【SiO 2、SiC (金刚砂)、BN (氮化硼)、Si 3N 4等】 例如SiC 将金刚石晶胞中的一个C 原子周围与之连接的4个C 原子全部换成Si 原 子, 键长稍长些便可得到SiC 的晶胞。(其中晶胞的8个顶点和6个面心为Si 原子,4个互 不相邻的立方体体心的为C 原子,反之亦可) a 、每个SiC 晶胞中含有 4 个硅原子,含有 4 个碳原子 b 、1mol SiC 晶体中有4 mol Si —C 共价键 (4)SiO 2 晶体:在晶体硅的晶胞中,在每2个Si 之间插入1个O 原子, 便可得到SiO 2晶胞。 a 、每个硅原子都采取sp 3杂化,与它周围的4个氧原子所形成的空间 结构为__正四面体_型,SiO 2晶体中最小的环为 12 b 、每个Si 原子被 12 个十二元环共用,每个O 原子被 6 个 十二元环共用 c 、每个SiO 2晶胞中含有 8 个Si 原子,含有 16 个O 原子 d 、1mol Si O 2晶体中有 4 mol 共价键 ( 5)晶体硼
