专题一:化学实验操作

专题一:化学实验基本方法
提升点一化学实验安全与防护
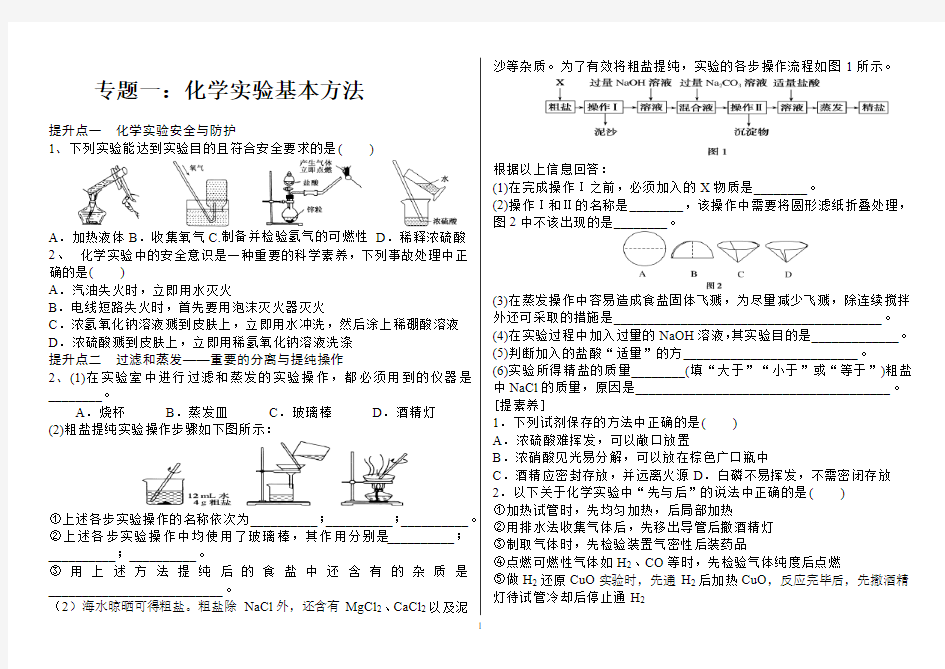
1、下列实验能达到实验目的且符合安全要求的是()
A.加热液体B.收集氧气C.制备并检验氢气的可燃性D.稀释浓硫酸2、化学实验中的安全意识是一种重要的科学素养,下列事故处理中正确的是()
A.汽油失火时,立即用水灭火
B.电线短路失火时,首先要用泡沫灭火器灭火
C.浓氢氧化钠溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液D.浓硫酸溅到皮肤上,立即用稀氢氧化钠溶液洗涤
提升点二过滤和蒸发——重要的分离与提纯操作
2、(1)在实验室中进行过滤和蒸发的实验操作,都必须用到的仪器是________。
A.烧杯B.蒸发皿C.玻璃棒D.酒精灯
(2)粗盐提纯实验操作步骤如下图所示:
①上述各步实验操作的名称依次为__________;__________;__________。
②上述各步实验操作中均使用了玻璃棒,其作用分别是__________;__________;__________。
③用上述方法提纯后的食盐中还含有的杂质是__________________________。
(2)海水晾晒可得粗盐。粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操作流程如图1所示。
根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是________。
(2)操作Ⅰ和Ⅱ的名称是________,该操作中需要将圆形滤纸折叠处理,图2中不该出现的是________。
(3)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取的措施是________________________________________。
(4)在实验过程中加入过量的NaOH溶液,其实验目的是_____________。
(5)判断加入的盐酸“适量”的方__________________________。
(6)实验所得精盐的质量________(填“大于”“小于”或“等于”)粗盐中NaCl的质量,原因是______________________________________。[提素养]
1.下列试剂保存的方法中正确的是()
A.浓硫酸难挥发,可以敞口放置
B.浓硝酸见光易分解,可以放在棕色广口瓶中
C.酒精应密封存放,并远离火源D.白磷不易挥发,不需密闭存放2.以下关于化学实验中“先与后”的说法中正确的是()
①加热试管时,先均匀加热,后局部加热
②用排水法收集气体后,先移出导管后撤酒精灯
③制取气体时,先检验装置气密性后装药品
④点燃可燃性气体如H2、CO等时,先检验气体纯度后点燃
⑤做H2还原CuO实验时,先通H2后加热CuO,反应完毕后,先撤酒精灯待试管冷却后停止通H2
⑥碱液流到桌子上,先加稀醋酸溶液中和,后用水洗
A.①②③⑤⑥B.①②④⑤C.①②③④⑤D.全部
3.分离FeCl3、KCl、BaSO4的固体混合物,应采用的一组试剂是() A.水、硝酸银、稀硝酸B.水、氢氧化钠、盐酸
C.水、氢氧化钾、盐酸D.水、氢氧化钾、硫酸
4.为确定某溶液的离子组成,进行如下实验:
①取少量溶液滴加Ba(NO3)2溶液,产生白色沉淀;
②然后继续加入稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的气体;白色沉淀部分溶解;
③取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。
根据实验,以下推测不.正确的是()
A.一定有SO2-4B.一定有CO2-3
C.不能确定Cl-是否存在D.不能确定SO2-4是否存在
5.除去下列物质中混有的少量杂质,把适当的试剂、操作方法的序号写在相应的横线上。
A.加适量盐酸、过滤B.加适量水、过滤、蒸发
C.加适量水、过滤D.加热(高温或灼烧)
E.加适量盐酸、蒸发F.冷却热的饱和溶液、结晶
(1)碳酸钙中混有少量的碳酸钠_________________________;
(2)氯化钾粉末中混有碳酸钾___________________________;
(3)氧化钙中混有少量的碳酸钙___________________________;
(4)氯化钠中混有少量的炭粉__________________________________;
(5)硝酸钾中混有少量的食盐_________________________。
6.实验小组的同学欲对一粗盐样品进行初步提纯。所用实验仪器或用品如下:
(1)D的名称是________。
(2)提纯的步骤是:溶解、过滤、________、计算产率。
(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中“二低”的含义是______________________________________。
(4)实验小组通过正确的计算发现,所得实验结果与该粗盐的实际含量对比,实验测得的结果比实际偏低,请分析可能的原因:______________________。
7.为了除去氯化钠样品中的杂质碳酸钠,某兴趣小组最初设计了如下所示方案进行实验。
(1)沉淀A的化学式是____________________________________。
(2)加入过量氯化钙溶液后,分离除去沉淀A的实验操作过程是_________。
(3)他们在实验过程中,又发现了新的问题:此方案很容易引入新的杂质。固体物质B的成分为______________________________(用化学式表示)。
(4)他们继续探究后又提出了新的方案:将混合物溶解,滴加盐酸至不再产生气泡为止,然后加热煮沸。有关反应的化学方程式为
提升点一蒸馏
1、右图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。(1)图中的两处明显的错误是_____________________、___________________。
(2)A仪器的名称是____________,B仪器的名称是____________。
(3)实验时A中除加入自来水外,还需加入少量________,其作用是_________。
(4)收集完蒸馏水后,是先撤酒精灯还是先停冷凝水?________________。
提升点二 萃取与分液 2、下列说法不正确的是( )
A .从碘水中提取单质碘时,不能用无水乙醇代替CCl 4
B .进行如图1操作后,实验现象为:液体分层,下层呈紫红色
C .利用如图2装置可以分离CCl 4 和水
D .萃取操作时,应选择有机萃取剂,且萃取剂密度必须比水大 3、 实验课上几名同学对萃取与分液结合进行的操作(CCl 4为萃取剂,从碘水中萃取碘)中错误的是( )
A .碘水和CCl 4加入分液漏斗中后,塞上上口处的塞子,用一手压住分液漏斗上口处,一手握住活塞部分,把分液漏斗倒转过来振荡
B .静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体)
C .打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出
D .最后继续打开活塞,另用容器承接并保存上层液体 4.选取萃取剂将碘水中的碘萃取出来,其中萃取剂应具备的性质是( ) A .不溶于水,且必须易与碘发生化学反应B .不溶于水,且比水更容易使碘溶解
C .不溶于水,且必须比水密度大
D .不溶于水,且必须比水密度小 5.下列实验装置不适用于物质分离的是( )
化铵晶体
7.选择下列实验方法分离物质,将分离方法的序号填在横线上。 A .萃取分液法 B .结晶法 C .分液法 D .蒸馏法 E .过滤法 (1)________分离饱和食盐水与沙子的混合物。 (2)________分离水和汽油的混合物。
(3)________分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物。
(4)________从碘的水溶液里提取碘。
8.如图所示,a 、b 、c 、d 分别是几种常见漏斗的上部,A 、B 、C 、D 是实际操作中各漏斗的下部插入容器中的示意图,请指出A 、B 、C 、D 分别与a 、b 、c 、d 相匹配的组合及其组合后装置在实验中的应用,例如:C 和a 组合,用于制取气体。
(1)A与________组合,用于_____________________________。
(2)B与________组合,用于____________________________。
(3)B与________组合,用于________________________________
(4)D与________组合,用于_____________________________。
9.工业上通常用工业酒精和生石灰混合蒸馏法制取无水乙醇。是实验室中模拟工业原理制取无水乙醇的装置。
回答下列问题:
(1)指出图中的三处错误:________、________、________。
(2)在除去工业酒精中的水时,下列做法不可取的是________。(号)
A.加入过量的生石灰后过滤B.加入过量的生石灰后蒸馏C.加入过量的生石灰后分液
(3)由(2)可知除去工业酒精中的水的原理是(用化学方程式示
_____。
(4)装置中仪器A、B、C的名称分别是A________;B________ C________。
(5)在蒸馏操作中,仪器B中加入沸石(或碎瓷片)的作用是
(6)有同学认为该装置没必要使用温度计,你认为可以吗?
