崩解时限检查法操作规程
崩解时限检查操作规程 第 1 页/共 1 页
1. 主题内容与适用范围
1.1 本规程规定了片剂崩解时限检查操作的内容与方法与要求。 1.2 本规定适用于片剂崩解时限的检查。
2. 引用标准
2.1 《中华人民共和国药典》(2010年版)二部附录
3. 简述
4.仪器与用具
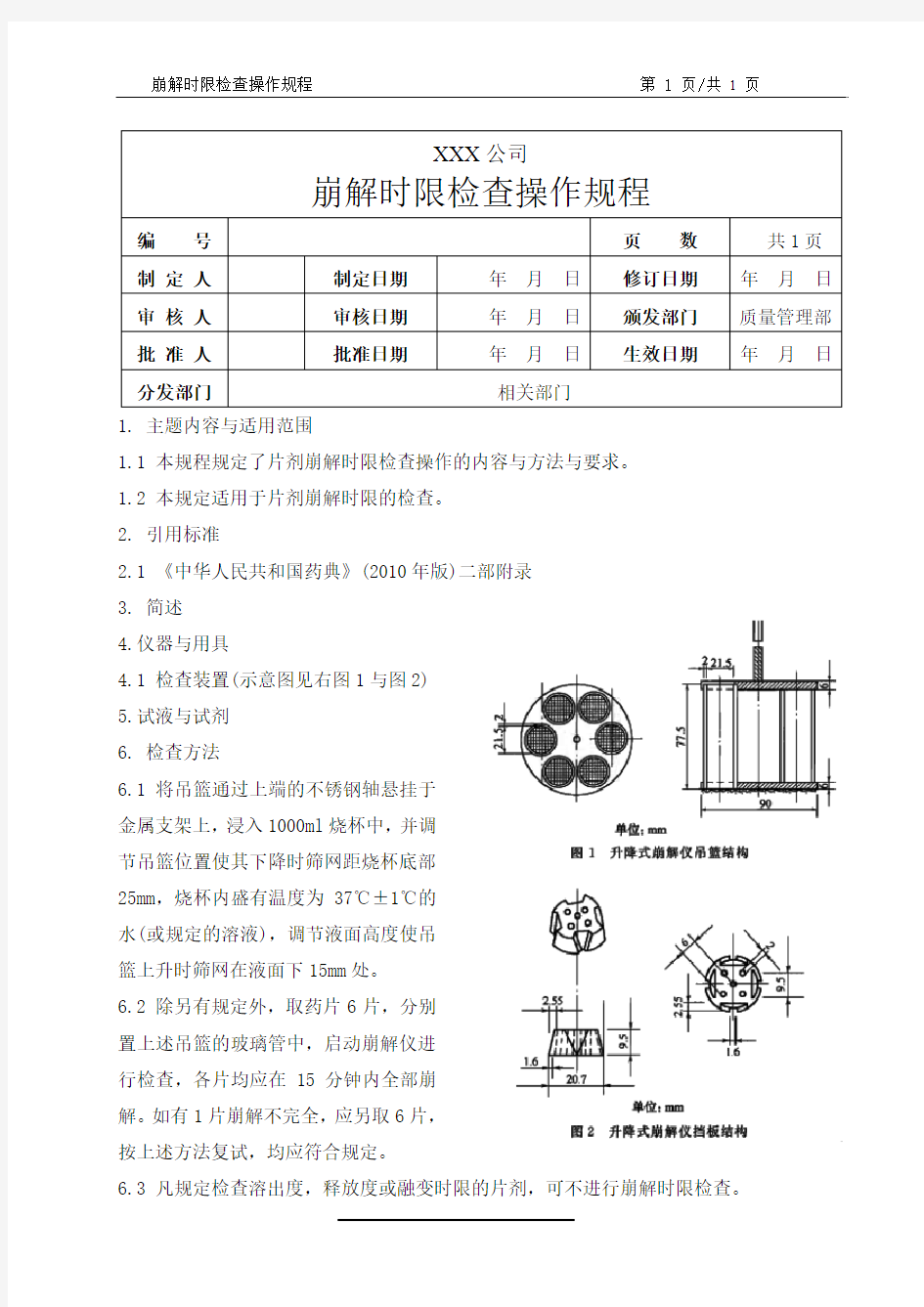
4.1 检查装置(示意图见右图1与图2)
5.试液与试剂
6. 检查方法
6.1 将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000ml 烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm ,烧杯内盛有温度为37℃±1℃的水(或规定的溶液),调节液面高度使吊篮上升时筛网在液面下15mm 处。 6.2 除另有规定外,取药片6片,分别置上述吊篮的玻璃管中,启动崩解仪进行检查,各片均应在15分钟内全部崩解。如有1片崩解不完全,应另取6
片,按上述方法复试,均应符合规定。
6.3 凡规定检查溶出度,释放度或融变时限的片剂,可不进行崩解时限检查。
片剂崩解时限检查法
片剂崩解时限检查法 1 简述 1.1 本法(《中国药典》2010年版二部附录X A)适用于片剂(包括口服普通片、薄膜衣片、糖衣片、肠溶衣片、结肠定位肠溶片、含片、舌下片、可溶片及泡腾片)、胶囊剂(包括硬胶囊剂、软胶囊剂及肠溶胶囊剂),以及滴丸剂的溶散时限检查。凡规定检查溶出度、释放度或融变时限的制剂,不再进行崩解时限检查。 1.2 片剂口服后,需经崩散、溶解,才能为机体吸收而达到治疗目的;胶囊剂的崩解是药物溶出及被人体吸收的前提,而囊壳常因所用囊材的质量,久贮或与药物接触等原因,影响溶胀或崩解;滴丸剂中不含有崩解剂,故在水中不是崩解而是逐渐溶散,且基质的种类与滴丸剂的溶解性能有密切关系,为控制产品质量,保证疗效,《中国药典》规定本检查项目。 1.3 本检查法中所称“崩解”,系指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶囊壳外,应全部通过筛网。如有少量不能通过筛网,但已软化或轻质上浮且无硬芯者,可作符合规定论。 2 仪器与用具 2.1 崩解仪(见《中国药典》2010年版二部附录X A的仪器装置)。 2.2 滴丸剂专用吊篮按 2.1项下所述仪器装置,但不锈钢丝筛网的筛孔内径改为0.425mm。 2.3 烧杯1000ml。 2.4 温度计分度值1℃。 3 试药与试液 3.1 人工胃液(供软胶囊剂和以明胶为基质的滴丸剂检查用)取稀盐酸16.4ml,加水约800ml与胃蛋白酶10g,摇匀后,加水稀释成1000ml,即得。临用前制备。 3.2 人工肠液(供肠溶胶囊剂检查用)即磷酸盐缓冲液(含胰酶)(pH6.8)(见《中国药典》2010年版二部附录XV D缓冲液)。临用前制备。 4 操作方法 4.1 将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底25mm,烧杯内盛有温度为37℃±1℃的水(或规定的溶液),调节液面高度使吊篮上升时筛网在液面下15mm处。除另有规定外,取供试品6片,分别置上述吊篮的玻璃管中,每管各加1片,立即启动崩解仪进行检查。 4.2 片剂 4.2.1 口服普通片按4.1项下方法检查,各片均应在15min内全部崩解。 如有1片不能完全崩解,应另取6片复试,均应符合规定。 4.2.2 薄膜衣片按4.1项下方法检查,并可改在盐酸溶液(9→1000)中进行检查,各片均应在30min内全部崩解。 如有1片不能完全崩解,应另取6片复试,均应符合规定。 4.2.3 糖衣片按4.1项下方法检查,各片均应在1h内全部崩解。 如有1片不能完全崩解,应另取6片复试,均应符合规定。 4.2.4 肠溶衣片按4.1项下方法,先在盐酸溶液(9→1000)中检查2h,每片均不得有裂缝、崩解或软化等现象;继将吊篮取出,用少量水洗涤后,每管各加档板1块,再按上述方法在磷酸盐缓冲液(pH6.8)中进行检查,各片均应在1h内全部崩解。 如有1片不能完全崩解,应另取6片复试,均应符合规定。 4.2.5 含片除另有规定外,按4.1项下方法检查6片,各片均不应在10min内全部崩
热原测温仪操作规程
标准操作规程 1 目的规范热原测温仪的使用操作。 2 适用范围热原测温仪的使用操作。 3 责任者质管部QC检验人员。 4 内容 4.1 系统进入 4.1.1 接通电源,依次打开主机、打印机电源,进入WINDOW系统。 4.1.2 在WINDOW程序管理器中,用鼠标双击“2000版热原实验”快捷图标,进入热原程序主功能窗口。 4.2 探头标定 4.2.1 把待标定的探头与一根最小分度值为0.1℃的精密温度计置于恒温水浴箱中。 4.2.2 在主功能窗口中,用鼠标点击“标定探头”窗口或“其它”菜单下的“探头自动标定”项,进入自动标定窗口。 4.2.3 在“自动标定”窗口,分别输入起始探头号和终止探头号,按“确认”键。 4.2.4 待水浴温度达到第一个设定点(37.0±0.2℃),水浴温度恒温时(“窗口”右半部分同时显示的每个探头的数字电压基本保持不变),在“第一点温度”项目中输入此刻温度计的数值,按回车键,再按左侧相对应的“OK”按钮,进入第二个温度点。 4.2.5 待水浴温度达到第二个设定点(38.0±0.2℃)且恒定后,按上法输入温度计读数,进入第三个温度点。 4.2.6 按上述操作方法,依次输人第三个温度点(39.3±0.2℃)、第四个温度点(39.9±0.2℃)、第五个温度点(41.0±0.2℃)的温度计读数,上述数据输完后,再按“存盘”,微机存盘后“返回”主功能窗口,至此标定完毕。
标准操作规程 4.2.7 注意事项:在标定过程中,窗口右半部分显示探头的数字电压差异,可以判断探头好坏。如果某个探头的数字电压比其它探头的数字电压高很多,说明该探头短路;相反,如果某个探头的数字电压比其它探头的数字电压低很多或为零,说明该探头按触不良或断路。对于短路或断路的探头,标定时必须换掉。 4.3 新兔挑选 4.3.1 在主功能窗口点击“准备工作”项下的“体重输入”项或点击“体重输入”按钮,输入对应探头下的实验兔体重后,返回主功能窗口。 4.3.2 在主功能窗口点击“准备工作”菜单,再点击“选兔”项,从“新兔挑选”子项进入“新兔挑选”窗口。 4.3.3 在“新兔挑选”窗口中先按“预览”按钮,待兔温稳定后,再按“开始”按钮开始测温,测温过程完成后,微机自动整理保存数据,返回主功能窗口。 4.4 热原检查 4.4.1 在主功能窗口按上法输入实验兔的体重,返回主功能窗口。 4.4.2 点击“试验样品”输入按钮或“准备工作”菜单下的试验样品输入项,进入试样输入窗口,输入试验样品名称、批号等数据,返回主功能窗口。 4.4.3 点击“正常测温”窗口进入测温窗口,先点击“预览”按钮,稳定10~15分钟再点击“开始”按钮,进入正常体温测定程序,30分钟后自动进入家兔分组窗口。 4.4.4 如果家兔数不够实验所需数量,可选择按“重选”按钮,继续选兔15分钟,或者按“删除部分供试品”按钮删掉部分供试品。 4.4.5 点击“家兔分组”按钮,自动分组,输入室温数据,按“打印”按钮打印出家兔分组一览表以供注射用。 4.4.6 注射完毕后,点击“继续”按钮,进入自动测温程序,直至测温结束。 4.4.7 在测温过程中如暂时停电或探头脱落,可点击“异常测温”按钮,正确输入已测试时间,再按“继续”按钮,使实验继续进行。
氯化物检查法操作规程
1.目的 建立氯化物检查法操作规程。 2.适用范围 本规程适用于氯化物检查法。 3.编制依据 《药品生产质量管理规范(1998年修订)》国家药品监督管理局(1999)4.责任 4.1 QC质检员对本规程的实施负责。 4.2 QC主管对本规程的有效执行承担监督检查责任。 5.正文 5.1简述 5.1.1微量氯化物在硝酸酸性溶液中与硝酸银作用生存氯化银浑浊,与一定量的标准氯化钠溶液在同一条件下生成的氯化银浑浊液比较,以检查供试品中氯化物的限量。 5.1.2本法(中国药典2010年版二部附录Ⅷ A)适用于药品中微量氯化物的限度检查。 5.2仪器与用具 5.2.1纳氏比色管50ml,应选玻璃质量较好、配对、无色(尤其管底)、管的直径大小相等、管上的刻度高低一致的纳氏比色管进行实验。 5.3试药与试液 5.3.1标准氯化钠溶液的配制称取氯化钠0.165g,置1000ml量瓶中,加水适量使其溶解并稀释至刻度,摇匀,作为贮备液。临用前,精密量取贮备液10ml,置100ml量瓶中,加水稀释至刻度,摇匀,即得(每1ml相当于10μg的Cl)。 5.4 操作方法 5.4.1 供试溶液的配制除另有规定外,取规定量的供试品,置50ml(纳氏比色管中,加水溶解使成约25ml(溶液如显碱性,可滴加硝酸使遇pH试纸显中性),再加稀硝酸10ml;溶液如不澄清,应滤过;再加水使成约40ml,摇匀,即得供试溶液。 5.4.2 对照溶液的配制取规定量的标准氯化钠溶液,置另一50ml纳氏比色管中,加稀硝酸10ml,加水使成约40ml,摇匀,即为对照溶液。 5.4.3 于供试溶液与对照溶液中,分别加入硝酸银试液1.0ml,用水稀释使成50ml,摇匀,在暗处放置5分钟,同置黑色背景上,从比色管上方向下观察,比较所产生的浑浊。 5.4.4 供试溶液如带颜色,除另有规定外,可取供试溶液两份,分置50ml纳氏比色管
药典四部通则崩解时限检查法
药典四部通则崩解时限 检查法 文件管理序列号:[K8UY-K9IO69-O6M243-OL889-F88688]
0921崩解时限检查法本法系用于检查口服固体制剂在规定条件下的崩解情况。 崩解系指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶襄壳外,应全部通过筛网。如有少量不能通过筛网,但已软化或轻质上漂且无硬心者,可作符合规定论。 除另有规定外,凡规定检查溶出度、释放度、融变时限或分散均匀性的制剂,不再进行崩解时限检查。 一、片剂 仪器装置采用升降式崩解仪,主要结构为一能升降的金属支架与下端镶有筛网的吊篮,并附有挡板。 升降的金属支架上下移动距离为55mm±2mm,往返频率为每分钟30?32次。 (1)吊篮玻璃管6根,管长77.5mm±2.5mm,内径21.5mm,壁厚2mm;透明塑料板2块,直径90mm,厚6mm,板面有6个孔,孔径26mm;不锈钢板1块(放在上面一块塑料板上),直径90mm,厚lmm,板面有6个孔,孔径22mm;不锈钢丝筛网1张(放在下面一块塑料板下),直径90mm,筛孔内径2.0mm;以及不锈钢轴1根(固定在上面一块塑料板与不锈钢板上),长80mm。将上述玻璃管6根垂直置于2块塑料板的孔中,并用3只螺丝将不锈钢板、塑料板和不锈钢丝筛网固定,即得(图1)。 (2)挡板为一平整光滑的透明塑料块,相对密度1.18?1.20,直径 20.7mm±0.15mm,厚9.5mm±0.15mm;挡板共有5个孔,孔径2mm,中央1个孔,其余4个孔距中心6rmn,
各孔间距相等;挡板侧边有4个等距离的V形槽,V形槽上端宽9.5mm,深 2.55mm, 底部开口处的宽与深度均为1.6mm(图2)。 检査法将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸人1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37°C±1".的水,调节水位高度使吊篮上升时筛网在水面下15mm处,调节吊篮顶部不可浸没于溶液中。 除另有规定外,取供试品6片,分别置上述吊篮的玻璃管中,启动崩解仪进行检查,各片均应在15分钟内全部崩解。如有1片不能完全崩解,应另取6片复试,均应符合规定。 中药浸膏片、半浸膏片和全粉片,按上述装置吊篮的玻璃管中,启动崩解仪进行检查,全粉片各片均应在30分钟内全部崩解;浸膏(半浸膏)片各片均应在1个小时内全部崩解。如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。如有1片不能完全崩解,应另取6片复试,均应符合规定。 薄膜衣片,按上述装置与方法检査,并可改在盐酸溶液(9—1000)中进行检查,化药薄膜衣片应在30分钟内全部崩解。中药薄膜衣片,则每管加挡板1块,各片均应在1个小时内全部崩解,如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。如有1片不能完全崩解,应另取6片复试,均应符合规定。 糖衣片,按上述装置与方法检查,化药糖衣片应在1个小时内全部崩解。中药糖衣片则每管加挡板1块,各片均应在1个小时内全部崩解,如有供试品
GMP认证全套文件资料027-胶囊崩解时限检查标准操作规程
目的: 制订胶囊充填过程中(或成品)胶囊剂崩解时限检查标准操作规程,以进行胶囊充填的质量控制。 适用范围: 胶囊充填中的胶囊剂或成品胶囊剂崩解时限的测定。 责任: 胶囊充填操作工和车间质管员、检验室检验员执行本规程,质管部负责监督本规程的执行。程序: 1.仪器:ZB-IB崩解仪。 2.方法:按中国药典规定的方法依法测定(中国药典2000年版二部附录X A)。 2.1 取样:从灌装机出口至少取6粒。 2.2 测定:使用规定的崩解介质,从样品中取6片,分别放入崩解仪的6个管子中, 按下列时间表检查崩解情况。 允许的最大崩解时间在下述规定时间检查胶囊≤2分钟连续观察 3分钟 1,2,3分钟 5分钟 1,3,5分钟 8分钟 4,6,8分钟 10分钟 5,8,10分钟 15分钟 5,10,15分钟 20分钟 10,15,20分钟 25分钟 15,20,25分钟 30分钟 15,25,30分钟 60分钟 30,45,60分钟记录每一组药片的崩解时间。出现不合格结果时,要停机检查原因。 3.结果: 3.1 在控制限度内:如果测得的结果在控制限度内,通知操作工灌装可继续进行,如
测定结果恰好在限度内或有接近限度的趋势,则须立即告知操作工调整机器。调整后,另取样品再进行试验。 3.2 超出控制限度:一旦测得的结果超出控制限度,再次取样重复测定以证实结果。 如果第二次测定的结果与上次一致时,应立即通知操作工对过程进行适当的调整。 调整后,取一新样品重新测定,如再次测定结果在控制范围内,立即通知操作工必须更换另一容器收集胶囊。调整前最后一次测定结果合格与调整后重新得到合格品之间压出的胶囊,必须与该批合格的胶囊分开放置,并在容器上贴上“待处理”标签,直到作出处理决定为止。如工艺过程调整后,测定结果仍超出规定范围,应立即报告质管员及质管部。
氯化钠检验标准操作规程
范围:氯化钠 职责:检验员室对本规程的实施负责 正文: 1.性状 ——本品为无色,透明的立方形结晶或白色结晶性粉末;无臭,味咸。本品在水中易溶,在乙醇中几乎不溶。 2.鉴别 ——本品的水溶液显钠盐与氯化物的鉴别反应。 2.1执行SOP-QM-417-00《一般鉴别标准操作规程》中的钠盐、氯化物的鉴别操作。 3.检查 3.1酸碱度 ——取本品5.0g,加水50ml溶解后,加溴麝香草酚蓝指示液2滴,如显黄色,加氢氧化钠滴定液(0.02mol/L)0. 10ml,应变为蓝色;如显蓝色或绿色,加盐酸滴定液(0.02mol/L)0.20ml,应变为黄色。 3.2溶液的澄清度 ——取本品5.0g,加水25ml溶解后,溶液应澄清。 3.2.1执行SOP-QM-411《澄清度检查标准操作规程》。 3.3碘化物 ——取本品的细粉5.0g,置瓷蒸发皿内,滴加新配制的淀粉混合液(取可溶性淀粉0.25g,加水2ml,搅匀,再加沸水至25ml,随加随搅拌,放冷,加0.025mol/L 硫酸溶液2ml、亚硝酸钠试液3滴与水25ml混匀)适量使晶粉湿润,置日光下(或日光灯下)观察,5分钟内晶粒不得显蓝色痕迹。 3.4溴化物 ——取本品2.0g,加水10ml使溶解,加盐酸3滴与氯仿1ml,边振摇边滴加2%氯胺T溶液(临用新制)3滴,氯仿层如显色,与标准溴化钾溶液(精密称取在105℃干燥至恒重的溴化钾0.1485g,加水使溶解成100ml,摇匀)1.0ml用同一方法制成的对照液比较,不得更深。 3.5硫酸盐 取本品5.0g,依法检查,与标准硫酸钾溶液1.0ml制成的对照液比较,不得更浓(0.002%)。 3.5.1执行SOP-QM-406-00《硫酸盐检查标准操作规程》。 3.6钡盐 ——取本品4.0g,加水20ml溶解后,滤过,滤液分为两等份,一份中加稀硫酸2ml,另一份中加水2ml,静置15分,两液应同样澄清。 3.7钙盐 第1页共2页
崩解时限检查法
目的:建立崩解时限检查法的标准操作程序,规范崩解时限检查法的操作 范围:适用于崩解时限检查法 职责:检验科主管、检验员 规程: 1 简述 1.1 本法(中国药典2000年版二部附录X A)适用于片剂(包括普通片,薄膜衣片,糖衣片,肠溶衣片及泡腾片),胶囊剂(包括硬胶囊剂,软胶囊及肠溶胶囊剂),以及丸剂的溶散时限检查.凡规定检查溶出度,释放度或融变时限的制剂,不再进行崩解时限检查。 1.2 片剂口服后,需经崩散,溶解,才能为机体吸收而达到治疗目的;胶囊剂的崩解是药物溶出及被人体吸收的前提,而囊壳常因所用囊材的质量,久贮或与药物接触等原因,影响溶胀或崩解;尺剂中不含有崩解剂,故在水中不是崩解而是逐渐溶散,且基质的种类与尺剂的溶解性能有密切关系,为控制产品质量,保证质量,保证疗效,药内规定本检查项目。 1.3 本检查法中所称“崩解”,系指固体制剂于规定条件下在检查时限内全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶囊壳外,应通过筛网。 2 仪器与用具 2.1 崩解仪(见中国药典2000年版二部附录X A的仪器装置)。 2.2 滴丸剂专用吊篮,按2.1项下所述仪器装置,但不锈钢丝筛网的筛孔内径改为0.425mm。 2.3 烧杯1000ml 2.4 温度计,分度值1℃ 3试药与试液 3.1人工胃液(供办胶囊剂和以明胶为基质的滴丸剂检查用),取稀盐酸16.4ml,加水约800ml与胃蛋白酶10g,摇匀后,加水稀释成1000ml,即得.临用前制备。 3.2人工肠液(从肠溶胶囊剂检查用)取磷权二氢钾6.8g,加水500ml使溶解,用0.4%氢氧化钠
溶液调节pH值至6.8;另取胰酶10g,加水适量使溶解,将两液混合后,加水稀释成1000ml,即得,临用前制备。 4 操作方法 4.1 将吊篮通过上端的不锈钢轴悬持于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使共下降时筛网距烧杯底部25mm,烧杯内盛有温度为37±1℃的水(或规定的溶液),调节液面高度使吊篮上升时筛网在液面下15mm处.除另有规定外,取药片6片,分别置上述吊篮的玻璃管中,每管各加1片,立即启动崩解仪进行检查。 4.2 片剂 4.2.1 普通片,按4.1项下方法检查,各片均应15分钟内全部崩解。 4.2.2 薄膜衣片,按4.1项下方法,并可改在盐酸溶液(9→1000)中进行检查,各片均应在30分钟内全部崩解。 如有1片崩解不完全,应另取6片,按上述方法复试,均应符合规定。 4.2.3 糖衣片,按4.1项下方法检查,各片均应在1小时内全部崩解。 4.2.4 肠溶衣片按4.1项下方法,先在盐酸溶液(9→1000)中检查2小时,每片均不得有裂缝,崩解或软化等现象,继将吊篮取出,用少量水洗涤后,每管各加档板1块,再按上述方法在磷酸盐缓冲溶液(pH6.8)中进行检查,各片均应在1小时内全部崩解。 如有1片不能完全崩解,应另取6片,按上述方法复试,均应符合规定。 4.2.5 泡腾片,取药片6片,分别置6个250ml伐杯(烧杯内各盛有200ml水,水温为15~25℃中,有许多气泡放出,当药片或碎片周围的氧化停止逸出时,药片应崩解,溶解或分散在水中,无聚集的颗粒剩留.除另有规定外,各片均在5分钟内崩解。 4.3 胶囊剂 4.3.1 硬胶囊剂,除另有规定外,取供度品6粒,分别置吊篮的玻璃管中,每管各加1粒,按4.1项下方法检查(若供试品漂浮在液面,应加档板),各粒均应在30分钟内全部崩解。 如有1粒不能完全崩解,应另取6粒复试,均应符合规定. 4.1项下方法检查 4.3.2 软胶囊剂除另有规定外取供试品6粒,分别置吊篮的玻璃管中,每管各加1粒, 4.1项下方法检查(若供试品漂浮在液面,应加档板) ,或改在人工胃液中进行检查,各粒均应在1小时内全部崩解。
热原检查法标准操作规程
热原检查法标准操作规程 目的: 建立热原检查的基本操作,为热原检查人员提供正确的操作规程。 2.依据: 《中华人民共和国药典》2000年版二部。 3.范围: 本标准适用于采用家兔法进行的热原检查的操作。 4.职责: QC热原检查操作人员对本标准的实施负责。 5. 程序: 5.1.实验材料及用具: 5.1.1. 天平(精度50g,家兔称重用)。 5.1.2.电热干燥箱(50~300±1)℃ 5.1.3.保温箱(室温+3~60)℃ 5.1.4.智能热原检测仪。 5.1.5.家兔固定盒 5.1. 6.实验用具:注射器、针头、刻度吸管、锥形瓶、硫酸纸、砂轮、洗耳球、金 属直镊、注射器盒、时钟、75%酒精棉球、手术镊。 5.1.7. 稀释剂:灭菌注射用水、氯化钠注射液。 5.2. 供试品溶液的配制: 5.2.1.打开洁净台的风机及照明开关,并用75%酒精棉球擦拭台面消毒。 5.2.2. 用75%酒精棉球擦手消毒。 5.2.3. 取供试品适量,置锥形瓶中,并标明批号。 5.2.4. 加入规定的稀释剂,制成符合规定浓度的供试品溶液,锥形瓶瓶口用经过灭菌的硫酸纸封好,放入保温箱中,温热至约38℃。 5.2.5. 供试品配制完毕后,应在30分钟内注射于家兔体内。 5.3. 实验动物:应符合规定。见家兔预选操作规程(SOP ZL5001)。 5.4. 实验前的准备:
5.4.1. 智能热原检测仪探头应每月校验一次,见智能热原检测仪使用规程(SOP ZL0058)。 5.4.2. 用具的除热原:所有与药液接触的器具,都必须清洗干净后,置电热干燥箱 中经250℃、30分钟加热除热原。注射器、针头、手术镊清洗干净后,放入注射器盒内,密闭,放入电热干燥箱中经250℃,30分钟加热除热原。 5.4.3. 实验室的温度: 实验室的温度应在(17-28)℃范围内 实验室与饲养室的温度相差不得大于5℃ 试验全过程中,室温变化不得大于3℃ 5.5. 检查法: 5.5.1.选符合规定的家兔,停止给饲料和水,称重后置于家兔固定盒中至少1小时。 5.5.2.每隔30分钟测量家兔体温一次,一般测量两次。两次体温之差不得超过0.2 ℃,以此两次体温的平均值作为该兔的正常体温。 5.5.3.测量体温时,测温探头插入肛门的深度和时间各兔应相同。深度为6cm,时 间约为1分半钟。 5.5.4. 当日使用的家兔,正常体温应在(38.0-39.6)℃范围内,且各兔间相差不得 超过1℃。 5.5.5. 每个供试品用家兔3只,在测定正常体温后15分钟内给药。供试品的剂量, 应按各该药项下的规定注射。 注射前,先用75%酒精棉球轻擦家兔耳静脉的注射部位,从耳尖端静脉进针,如进针不利,则顺序向前进行。 5.5.7. 注射完毕,拔出针头时,用75%酒精棉球按压针孔数秒钟,止血,注射时间一般每只家兔不超过3分钟。 5.5.8.每隔30分钟,按前法测家兔体温一次,共测6次。 5.6. 温差计算: 5.6.1.注射药液后,以6次测得体温中最高的一次减去正常体温,为该兔体温的升 高度数,如6次体温均低于正常体温,则升温度数以“0”计。 5.6.2.6次体温中最低的一次,减去正常体温,即为降温值。 5.7. 结果判断:
成品取样标准操作规程
成品取样标准操作规程 1 目的:规范取样程序,以保证检验结果的准确性。 2 范围:适用于我司成品取样标准操作。 3 职责:中控室现场QA 人员、灌装、轧盖、灯检岗位对本程序实施负责。 4 内容: 4.1取样量 最终取样数量一般不得少于全部检验所需用量的3倍。即1份供实验室分析用,2份作为留样品。 4.2取样方法 4.2.1 冻干粉针剂生测检验样品取样(包括无菌、热原或细菌内毒素) 4.2.1.1 冻干粉针剂在生产过程中,灌装岗位人员应对以下灌装过程的样品进行标识存放:①开始灌装时的100-300支样品,在冻干盘上标识“KS ”字样;②生产过程因异常情况(如设备维修、停电后重新启动灌装机或净化系统等可能造成微生物污染的因素)停止生产后,重新开始的100-300支样品,在冻干盘上标识为“YC ”字样;③灌装即将要结束的100-300支样品,在冻干盘上标识为“JS ”字样,以上标识各取样不少于20瓶,总取样量见附表1。在生产过程中,QA 人员认为存在偏差的样品,有权要求灌装岗位人员进行标识取样; 4.2.1.2 灌装岗位人员对有以上标识的出箱样品,应进行单独存放; 4.2.1.3 轧盖岗位人员,应先取有以上标识的样品进行依次轧盖; 4.2.1.4 灯检岗位人员,按轧盖的顺序先对以上标识样品进行依次灯检; 4.2.1.5 QA 人员对以上标识的产品按轧盖前中后的顺序进行取样,分别从前、中、后样品中各平均抽取适量,抽取总数应够完成两次生测检验量。 4.2.2 粉针剂生测检验样品取样(包括无菌、热原或细菌内毒素) 4.2.2.1 按包装序号,分别从开始序号及结束序号样品中抽取; 4.2.2.2 生产过程异常情况(同上)的样品,QA 人员也应及时进行取样,每次取样数不得少于10瓶; 4.2.2.3 生产前、后及过程异常情况样品的抽取总数应够完成两次生测检验量。 4.2.3冻干粉针剂、粉针剂理化检验样品与口服固体制剂全部检验样品取样 车间在产品内包装结束之后即可填写成品请验单通知QA 人员取样。QA 人员根据请验单上的内容,准备好相应的取样工具,在外包装生产线或待包装产品中间站进行随机取样,取样面应分散,广泛,不能集中在某一区域,取样单位以最小内包装单位为准,取样量参照下表,一般由产品的包装特性而定。 QA 根据本批产品数量(件数),计算好抽样件数,并拟定取样数量: n ≤3时,每样均抽;3<n ≤300时,取n +1件;n >300时,取2 n +1件; 取样量应能满足理化检验所需样品的数量,总取样量见附表1和附表2。
氯化物检查标准操作规程
范围:原辅料、成品 职责:检验室对本规程的实施负责 正文 1.原理 1.1微量氯化物在硝酸酸性溶液中与硝酸银作用生成氯化银浑浊液,与一定量的标准氯化钠溶液在同一条件下生成的氯化银浑浊液比较,以检查供试品中氯化物限量。 1.2本法适用于药品中微量氯化物的限度检查。 2.仪器与用具 ——纳氏比色管 50ml,应选玻璃质量较好、配对、无色(尤其管底)、管的直径大小相等、管上的刻度高低一致的纳氏比色管进行实验。 3.试药与试液 ——标准氯化钠溶液的配制称取氯化钠0.165g,置1000ml量瓶中,加水适量使其溶解稀释至刻度,摇匀,作为贮备液。临用前,精密量取贮备液10ml,置100ml 量瓶中,加水稀释至刻度,摇匀,即得(每1ml相当于10μg的C1)。 4.操作方法 4.1供试溶液的配制除另有规定外,取规定量的供试品,置50ml纳氏比色管中,加水溶解使成约25ml(溶液如显碱性,可滴加硝酸使遇pH试纸显中性),再加稀硝酸10ml;溶液如不澄清,应滤过;再加水使成约40ml,摇匀,即得供试溶液。 4.2对照溶液的配制取规定量的标准氯化钠溶液,置另一50ml纳氏比色管中,加稀硝酸10ml,加水使成约40ml,摇匀,即为对照溶液。 4.3于供试溶液与对照溶液中,分别加入硝酸银试液1.0ml,用水稀释使成50ml,摇匀,在暗处放置5分钟,同置于黑色背景上,从比色管上方向下观察,比较所产生浑浊。 4.4供试溶液如带颜色,除另有规定外,可取供试溶液两份,分置50ml纳氏比色管中,一份加硝酸银试液1.0ml,摇匀,放置10分钟,如显浑浊,可反复滤过,至滤液完全澄清,再加规定量的标准氯化钠溶液与水适量使成50ml,摇匀,在暗处放置5分钟,作为对照溶液;另一份中加硝酸银试液1.0ml与水适量使成50ml,摇匀,在暗处放置5分钟,两份同置黑色背景上,从比色管上方向下观察,比较所产生的浑浊。 5.结果与判断 ——供试品管的浑浊浅于对照管的浑浊,判为符合规定;如供试品管的浑浊浓于对照管,则判为不符合规定。 6.注意事项 6.1供试溶液与对照溶液应同时操作,加入试剂的顺序应一致。 6.2应注意按操作顺序进行,先制成40ml的水溶液,再加入硝酸银试液1.0ml 第1页共2页
崩解时限
崩解时限检查法标准操作规程 1主要内容 本标准规定了崩解时限检查法标准操作程序。 2适用范围 崩解时限检查法。 3职责 QC主任:按本规定进行监督管理。 QC检查员:按本规定对需要崩解时限检查法检测的物料进行检测。 4内容 4.1 原理 本法适用于片剂(包括口服普通片、薄膜衣片、糖衣片、肠溶衣片、结肠定位肠溶片、含片、舌下片、可溶片及泡腾片)、胶囊剂(硬胶囊剂、软胶囊剂及肠溶胶囊剂)以及滴丸剂的溶散时限检查。凡规定检查溶出度、释放度或融变时限的制剂,不再进行崩解时限检查。片剂口服后,需经崩散、溶解,才能为机体吸收而达到治疗的目的;胶囊剂的崩解是药物溶出及被人体吸收的前提,而囊壳常因所用囊材的质量、久贮或药物接触等原因,影响溶胀或崩解:滴丸剂中不含崩解剂,故在水中不是崩解而是逐渐溶散,且基质的种类与滴丸剂的溶解性能有密切关系,为控制产品质量,保证疗效,《中华人民共和国药典》规定本检查项目。本检查法中所称“崩解”,系指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶囊壳外,应全部通过筛网。如有少量不能通过筛网,但已软化或轻质上浮且无硬芯者,可作为符合规定论。 4.2 仪器与用具 4.2.1 崩解仪 4.2.1.1 仪器装置:采用升降式崩解仪,主要结构为一能升降的金属支架与下端有筛网的吊篮,并附有挡板。升降的金属支架上下移动距离为55mm±2mm,往返频率30~32次/min。 4.2.1.2 吊篮:玻璃管6根,管长77.5mm±2.5mm;内经21.5mm,壁厚2mm;透明塑料板2块,直径90mm,厚6mm,板面有6个孔,孔径26mm;不锈钢板1块(放在上面一块塑料板上),直径90mm,厚1mm,板面有6个孔,孔径22mm;不锈钢丝筛网1张(放在下面一块塑料板上),直径90mm,筛孔内径2.0mm;以及不锈钢轴1根(固定在上面一块塑料板与不锈钢板上),长80mm。将上述玻璃管6根垂直于2块塑料板的孔中,并用3只螺丝
热原测温仪操作规程
药业有限公司 标准操作规程 题目 制订人 制订日期 颁发部门热原测温仪操作规程 质管部审核人 审核日期编号 SOP-EM-329 批准人 批准日期版本号 A 共3 页第1 页生效日期分发部门质管部 1 目的规范热原测温仪的使用操作。 2 适用范围热原测温仪的使用操作。 3 责任者质管部QC 检验人员。 4 内容 4.1 系统进入 4.1.1接通电源,依次打开主机、打印机电源,进入WINDOW系统。 4.1.2在WINDOW程序管理器中,用鼠标双击“ 200版热原实验”快捷图标,进入热原程序主功能窗口。 4.2 探头标定 4.2.1把待标定的探头与一根最小分度值为
0.1 C的精密温度计置于恒温水浴箱中。 4.2.2在主功能窗口中,用鼠标点击“标定探头”窗口或“其它”菜单下的“探头自动标定”项,进入自动标定窗口。 4.2.3在“自动标定”窗口,分别输入起始探头号和终止探头号,按“确认” 键。 4.2.4待水浴温度达到第一个设定点( 37.0 ± 0.2C),水浴温度恒温时(窗口”右半部分同时显示的每个探头的数字电压基本保持不变),在“第一点温度”项目中输入此刻温度计的数值,按回车键,再按左侧相对应的“0!”钮,进入第二个温度点。 4 . 2 . 5待水浴温度达到第二个设定点( 38.0 士 0.2C )且恒定后,按上法输入温度计读数,进入第三个温度点。 4.2.6按上述操作方法,依次输人第三个温度点( 39.3 士 0.2C)、第四个温度点( 39.9 士 0.2C)、第五个温度点( 41.0 士 0.2C )的温度计读数,上述数据输完后,再按存盘”,微机存盘后返回” 主功能窗口,至此标定完毕。药业有限公司 标准操作规程 题目热原测温仪操作规程编号
3-崩解时限检查法检验标准操作规程
目的:建立崩解时限检查法检验操作规程,保证操作正确,确保检品质量。 范围:本标准规定了崩解时限的检查方法和操作要求;适用于本公司检品的崩解时限检查。职责:QC执行,QC主任、质量部经理监督执行。 内容: 一、仪器与用具 1、升降式崩解仪:主要结构为一能升降的金属支架与下端镶有筛网的吊篮,并附有档板。升降的金属支架上下移动距离为55mm±2mm,往返频率为30-32次/分钟。 2、吊篮:玻璃管6根,管长77.5mm±2.5mm,内径21.5mm,壁厚2mm;透明塑料板2块,直径90mm,厚6mm,板面有6个孔,孔径26mm,不锈钢板1块(放在上面一块塑料板上),直径90mm,厚1mm,板面有6个孔,孔径22mm;以及不锈钢丝筛网一张(放在下面的一块塑料板下),直径90mm,筛孔内径2.0mm;以及不锈钢轴1根(固定在上面一块塑料板与不锈钢板上),长80mm。将上述玻璃管6根垂直于2块塑料板的孔中,并用3只螺丝将不锈钢板,塑料板和不锈钢丝筛网固定,即得。 3、档板:为一平整光滑的透明塑料块,相对密度1.18-1.20,直径20.7mm±0.15mm,厚9.5mm±0.15mm;挡板共有5个孔,孔径为2mm,中央1个孔,其余4个孔距中心6mm,各孔间距相等;档板侧边有4个等距离的V形槽,V形槽上端宽9.5mm,深2.55mm,底部开口处的宽与深度均为1.6mm。 4、平底烧杯:(1000ml) 5、温度计:分度值1℃。 二、定义: 崩解系指固体制剂在检查时限内全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶囊壳外,应通过筛网,全部崩解所需的最长时间为崩解时限。 三、操作方法 1、将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37±1℃的水。调节水位高度使吊篮上升时筛网在水面下25mm处。 2、除另有规定外,取供试品6片,分别置上述吊篮的玻璃管中,加档板,启动崩解仪时进行检查,药材原粉片各片均应在30分钟内全部崩解;浸膏(半浸膏)片、糖衣片 第 1 页共 2 页
026-片剂崩解时限检查标准操作规程
****制药厂操作标准----生产管理 文件名称片剂崩解时限检查标准 操作规程编码SOP-SJ-026-00 页数2-1实施日期 制订人审核人批准人 制订日期审核日期批准日期 制订部门质管部分发部门生产部、生产车间、车间质管员、检验室 目的:制订片剂在压片过程中(或成品)片剂崩解时限检查标准操作规程。 适用范围:压片过程中或片剂成品崩解时限的测定。 责任:压片操作工、车间质管员、检验室检验员执行本规程,质管部负责监督本规程的执行。 程序: 1.仪器:ZB-IB崩解仪。 2.方法:按中国药典规定的方法依法测定(中国药典2000年版二部附录X A)。 2.1取样:从压片机出口或每锅包衣片中至少取6片。 2.2测定:使用药典所指定的崩解介质,从样品中取6片,分别防入崩解仪的6个管 子中,按下列时间表检查崩解情况。 允许的最大崩解时间在下述规定时间检查药片≤2分钟连续观察 3分钟1,2,3分钟 5分钟1,3,5分钟 8分钟4,6,8分钟 10分钟5,8,10分钟 15分钟5,10,15分钟 20分钟10,15,20分钟 25分钟15,20,25分钟 30分钟15,25,30分钟 60分钟30,45,60分钟记录每一组药片的崩解时间。出现不合格结果时,要停机检查原因。 3.结果: 3.1在控制限度内:如果测得的结果在控制限度内,压片可继续进行,但若测定结果 恰好在限度内或有接近限度的趋势,则须立即告知操作工对机器设备进行适当的
****制药厂操作标准----生产管理 文件名称 片剂崩解时限检查标准 操作规程编码SOP-SJ-026-00页数2-2 调整。调整后,另取样品再进行试验。 3.2超出控制限度:一旦测得的结果超出控制限度,则须重新取样测定,以证实结果。 如果第二次测定的结果与上次一致时,应立即通知操作工对过程进行适当的调整。对压片机调整后,取一新样品,再次测定,一旦再次测定结果在控制范围内,则通知操作工必须更换另一收集容器收集药片。在调整前,最后一次测定结果合格与调整后重新得到合格品之间压出的药片必须与该批合格的药片分开放置,并在容器上贴上“待处理”标签,直到作出有关的决定为止。如工艺过程调整后崩解时限仍超过控制限度,则必须立即报告质管员及质管部。
(2020年7月整理)《中华人民共和国药典》四部 通则0921崩解时限检查法.doc
0921 崩解时限检查法 本法系用于检查口服固体制剂在规定条件下的崩解情况。 崩解系指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶襄壳外,应全部通过筛网。如有少量不能通过筛网,但已软化或轻质上漂且无硬心者,可作符合规定论。 除另有规定外,凡规定检查溶出度、释放度、融变时限或分散均匀性的制剂,不再进行崩解时限检查。 一、片剂 仪器装置采用升降式崩解仪,主要结构为一能升降的金属支架与下端镶有筛网的吊篮,并附有挡板。 升降的金属支架上下移动距离为55mm±2mm,往返频率为每分钟30?32次。 (1) 吊篮玻璃管6根,管长77.5mm± 2.5mm,内径21.5mm,壁厚2mm;透明塑料板2块,直径90mm,厚6mm,板面有6个孔,孔径26mm;不锈钢板1块(放在上面一块塑料板上),直径90mm ,厚lmm,板面有6个孔,孔径22mm;不锈钢丝筛网1张(放在下面一块塑料板下),直径90mm,筛孔内径2.0mm;以及不锈钢轴1根(固定在上面一块塑料板与不锈钢板上),长80mm。将上述玻璃管6根垂直置于2块塑料板的孔中,并用3只螺丝将不锈钢板、塑料板和不锈钢丝筛网固定,即得(图1)。 (2) 挡板为一平整光滑的透明塑料块,相对密度1.18?1.20,直径20.7mm±0.15mm,厚9.5mm±0.15mm;挡板共有5个孔,孔径2mm,中央1个孔,其余4个孔距中心6rmn,各孔间距相等;挡板侧边有4个等距离的V形槽,V形槽上端宽9.5mm,深2.55mm,底部开口处的宽与深度均为1.6mm(图2)。
检査法将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸人1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37°C ±1".的水,调节水位高度使吊篮上升时筛网在水面下15mm处,调节吊篮顶部不可浸没于溶液中。 除另有规定外,取供试品6片,分别置上述吊篮的玻璃管中,启动崩解仪进行检查,各片均应在15分钟内全部崩解。如有1片不能完全崩解,应另取6片复试,均应符合规定。 中药浸膏片、半浸膏片和全粉片,按上述装置吊篮的玻璃管中,启动崩解仪进行检查,全粉片各片均应在30分钟内全部崩解;浸膏(半浸膏)片各片均应在1个小时内全部崩解。如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。如有1片不能完全崩解,应另取6片复试,均应符合规定。 薄膜衣片,按上述装置与方法检査,并可改在盐酸溶液(9—1000)中进行检查,化药薄膜衣片应在30分钟内全部崩解。中药薄膜衣片,则每管加挡板1块,各片均应在1个小时内全部崩解,如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。如有1片不能完全崩解,应另取6片复试,均应符合规定。 糖衣片,按上述装置与方法检查,化药糖衣片应在1个小时内全部崩解。中药糖衣片则每管加挡板1块,各片均应在1个小时内全部崩解,如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。如有1片不能完全崩解,应另取6片复试,均应符合规定。 肠溶片,按上述装置与方法,先在盐酸溶液(9— 1000)中检査2小时,每片均不得有裂缝、崩解或软化现象;然后将吊篮取出,用少量水洗涤后,每管加人挡板1块,再按上述方法在磷酸盐缓冲液(PH6.8)中进行检查,1小时内应全部崩解。如有1片不能
解读2020药典热原检查法
说到热原检查,我们先了解几个概念,热原、热原反应、内毒素、实验动物。 热原(p yr o g e n):指能引起恒温动物体温异常升高的致热物质。 它包括细菌性热原、内源性高分子热原、内源性低分子热原及化学热原等。注射液中的热原主要是指细菌性热原,是某些细菌的代谢产物、细菌尸体及内毒素。致热能力最强的是革兰氏阴性杆菌的产物,其次是革兰阳性杆菌类,革兰阳性球菌则较弱,霉菌、酵母菌、甚至病毒也能产生热原。 热原反应:临床上在进行静脉滴注大量输液时,由于药液中含有热原,病人在0.5~1h内出现冷颤、高热、出汗、昏晕、呕吐等症状,高热时体温可达40℃,严重者甚至可休克,这种现象称为热原反应。 细菌内毒素:是革兰氏阴性菌的细胞壁成分,当细菌死亡或自溶后便会释放出内毒素。因此,细菌内毒素广泛存在于自然界中。如自来水中含内毒素的量为1至100E U/m l。 当内毒素通过消化道进入人体时并不产生危害,但内毒素通过注射等方式进入血液时则会引起不同的疾病。注射液中如果含有内毒素,就会产生代谢产物,内毒素大量进入血液就会引起发热反应即热原反应。 因此,生物制品类、注射用药剂、化学药品类、放射性药物、抗生素类、疫苗类、透析液等制剂以及医疗器材类(如一次性注射器,植入性生物材料)必须经过细菌内毒素检测试验合格后才能使用。
由于家兔对热原的反应与人基本相似,对热原比较敏感,所以半个世纪以来一直用家兔来检测热原,家兔为保障药品质量和用药安全发挥了重要作用。 鲎试验在某些情况下,比如西药注射液、生理盐水等成分明确的药品,现在大多采用鲎试验来检测,但在一些中药注射剂、血液制品,抗毒素等由于自身特殊性无法通过稀释法消除干扰,还在使用兔法来检测热原,因此鲎试验目前还无法完全取代家兔热原试验。 检查法药典要求一 雌兔应无孕,家兔怀孕了会出现腹围会变大,体重也会增大,情绪变得多变,在试验固定台上不容易固定,怀孕后温度波动也会变得不敏感,药物反应小,影响检验结果的准确性。 新兔使用前要预测体温,有的兔子本身体温就低,不符合试验要求,要挑出来,也有运动健将型的,在试验台上固定着老是动来动去的,由于运动频繁体温也自然升高,一旦注射药物,有时候会出现假阳性可能。 有疾病的动物也不能使用,这些有病的动物可能本身就在发烧,如果注射药物后体温会降下来,就是药物发挥了治疗作用或急据升高,加重病情,总之不确定性太多,所以我们要选择体重合格、体温合格、精神状态好的。 大概的选择依据是这样的,兔身体匀称,肌肉结实丰满,背毛光滑。对外界反应表现出很机灵的样子。食欲旺盛是家兔健康的表现,粪便呈球形或椭圆形,大小均匀,外表光滑圆润,松散均匀,呈黑褐
GMP认证全套文件资料63-崩解时限检查法标准操作规程
崩解时限检查法标准操作规程 目的:制订崩解时限检查法标准操作规程。 适用范围:崩解时限检查。 责任:检验室检验人员按本规程操作,检验室主任监督本规程的实施。 程序: 1. 简述 1.1 本法(中国药典2000年版二部附录X A)适用于片剂(包括普通片、薄膜衣片、糖衣片、 肠溶衣片及泡腾片)、胶囊剂(包括硬胶囊剂、软胶囊剂及肠溶胶囊剂),以及丸剂的溶散时限检查。凡规定检查溶出度、释放度或融变时限的制剂,不再进行崩解时限检查。 1.2 片剂口服后,需经崩散、溶解,才能为机体吸收而达到治疗目的;胶囊剂的崩解是药物 溶出及被人体吸收的前提,而囊壳常因所用囊材的质量,久贮或与药物接触等原因,影响溶胀或崩解;丸剂中不含有崩解剂,故在水中不是崩解而是逐渐溶散,且基质的种类与丸剂的溶解性能有密切关系,为控制产品质量,保证疗效,药典规定本检查项目。 1.3 本检查法中所称“崩解”,系指固体制剂于规定条件下在检查时限内全部崩解溶散或成碎 粒,除不溶性包衣材料或破碎的胶囊壳外,应通过筛网。 2.仪器与用具 2.1 崩解仪(见中国药典2000年版二部附录X A的仪器装置) 2.2 滴丸剂专用吊篮按2.1项下所述仪器装置,但不锈钢丝筛网的筛孔内径改为0.425mm. 2.3 烧杯1000ml 2.4 温度计分度值1℃ 3. 试药与试液
3.1 人工胃液(供软胶囊剂和以明胶为基质的滴丸剂检查用)取稀盐酸16.4ml,加水约800ml 与胃蛋白酶10g,摇匀后,加水稀释成1000ml,即得。临用前制备。 3.2 人工肠液(供肠溶胶囊剂检查用)取磷酸二氢钾6.8g,加水500ml使溶液解,用0.4% 氢氧化钠溶液调节PH值至6.8;另取胰酶10g,加水适量使溶解,将两液混合后,加水稀释成1000ml,即得。临用前制备。 4. 操作方法 4.1 将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使 其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37±1℃的水(或规定的溶液),调节液面高度使吊篮上升时筛网在液面下15mm处。除另有规定外,取药片6片,分别置上述吊篮的玻璃管中,每管各加1片,立即启动崩解仪进行检查。 4.2 片剂 4.2.1 普通片按4.1项下方法检查,各片均应在15分钟内全部崩解。如有1片崩解不完全, 应另取6片,按上述方法复试,均应符合规定。 4.2.2 薄膜衣片按4.1项下方法,并可改在在盐酸溶液(9→1000)中进行检查,各片均应 在30分钟内全部崩解。如有1片不能完全崩解,应另取6片,按上述方法复试,均应符合规定。 4.2.3 糖衣片按4.1项下方法检查,各片均应在1小时内全部崩解。如有1片不能完全崩解, 应另取6片,按上述方法复试,均应符合规定。 4.2.4 肠溶衣片按4.1项下方法,先在盐酸溶液(9→1000)中检查2小时,每片均不得有 裂缝、崩解或软化等现象;继将吊篮取出,用少量水洗涤后,每管各加档板1块,再按上述方法在磷酸盐缓冲溶液(PH6.8)中进行检查,各片均应在1小时内全部崩解。如有1片不能完全崩解,应另取6片,按上述方法复试,均应符合规定。 4.2.5 泡腾片取药片6片,分别置6个250ml烧杯(烧杯内各盛有200ml水,水温为15-25℃) 中,有许多气泡放出,当药片或碎片周围的气体停止逸出时,药片应崩解、溶解或分散在水中,无聚集的颗粒剩留。除另有规定外,各片均应在5分钟崩解。 4.3 胶囊剂
