化学相对分子质量表
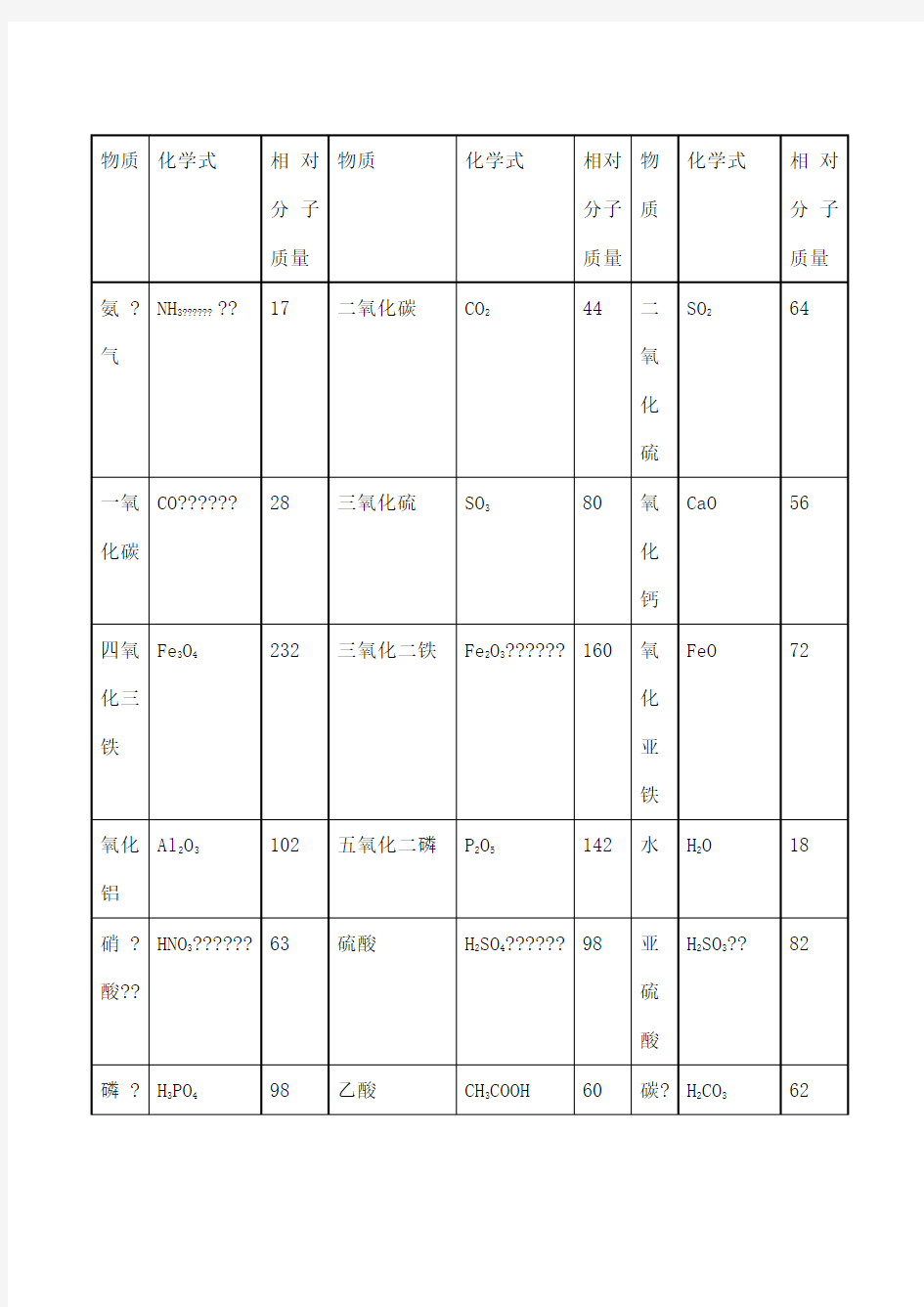

初中化学常见化合物相对分子质量
高中化学中常见物质的相对分子质量
高中化学中常见物质的相对分子质量 注:下划线的建议记下来(计算题经常要用到)。 Na 2O 62 Na 2 O 2 78 NaOH 40 NaCl 58.5 Na 2 CO 3 106 NaHCO 3 84 Na 2 S 78 Na 2SO 4 142 NaNO 3 85 NaClO 74.5 KOH 56 KCl 74.5 K 2CO 3 138 KHCO 3 100 K 2 SO 4 174 KNO 3 101 MgO 40 Mg(OH) 2 58 MgCl 2 95 MgCO 3 84 MgSO 4 120 CaO 56 Ca(OH) 2 74 CaCl 2 111 CaCO 3 100 Ca(HCO 3 ) 2 162 CaSO 4 136 Ca(ClO) 2 143 Ba(OH) 2 171 BaCl 2 208 BaCO 3 197 BaSO 4 233 Ba(NO 3 ) 2 164 Al 2O 3 102 Al(OH) 3 78 AlCl 3 133.5 Al 2 (SO 4 ) 3 342 KAl(SO 4 ) 2 ·12H 2 O 474 NaAlO 2 82 SiO 2 60 H 2 SiO 3 78 Na 2 SiO 3 122 SiCl 4 170 NH 3 17 N 2 H 4 32 NO 30 NO 2 46 HNO 3 63 NH 4 Cl 53.5 (NH 4 ) 2 CO 3 94 NH 4 HCO 3 79 (NH 4) 2 SO 4 132 NH 4 NO 3 80 CO(NH 2 ) 2 (尿素)60 P 2O 5 142 H 3 PO 4 98 Na 3 PO 4 164 Ca 3 (PO 4 ) 2 310 H 2O 18 H 2 O 2 34 H 2S 34 SO 2 64 SO 3 80 H 2 SO 4 98 HF 20 CaF 2 78 HCl 36.5 HClO 52.5 HBr 81 HI 128 MnO 2 87 KMnO 4 158 K 2 Cr 2 O 7 294 FeO 72 Fe 2O 3 160 Fe 3 O 4 232 Fe(OH) 3 107 FeCl 2 127 FeCl 3 162.5 FeS 88 FeS 2 120 FeSO 4 152 Fe 2 (SO 4 ) 3 400 CuO 80 Cu 2O 144 Cu(OH) 2 98 CuCl 2 135 CuS 96 Cu 2 S 160 CuSO 4 160 CuSO 4·5H 2 O 250 Cu(NO 3 ) 2 188 AgCl 143.5 AgBr 188 AgI 235 Ag 2SO 4 312 Ag 2 CO 3 276
中考化学专题复习探究分子性质与宏观现象的联系答案版
、中考回放 1.(2013?岳阳)交警在查“酒驾”时,先请司机打幵车窗,若闻到酒精气味;则 要求司机必须接受酒精含量的测试?交警能闻到酒精气味是因为酒精() A.分子间有间隙 B .分子很小 C .分子在不断运动 D .分子 可分 【答案】C; 【解析】分子总是在不断运动,酒精分子不断运动向四周扩散,使交警旬到恃殊的酒精气味,与分子的旦它特性无关I故选⑺ 【考点】分子的特性、分子在不断运动。 【点评】本题考查运用分子性质解释生活中的某些现象,闻到某些物质的味道与分 子在不断运动有关。 2.(2014?杭州)液氧转化为氧气的过程中,发生的变化是() A.混合物变为纯净物 B .分子间的空隙增大C .化学性质发生变化D.分子 总数增加 【答案】B; 【考点】分子的特性、分子之间有间隙。 【点评】物质的三态变化,是分子间的间隙发生了变化。气态分子的间隙〉液态分
子的间隙〉固态分子的间隙。 3.(2014?黑龙江)用分子的相关知识解释生活中的现象,下列说法正确的是() A.“酒香不怕巷子深”说明分子在不断运动 B.压瘪的乒乓球放入热水中重新鼓起是因为分子体积增大 C.分离液态空气制氧气说明分子可以再分 D.冰融化成水,说明分子种类发生改变 【答案】A; 【解析】A. “酒香不怕巷子深”说明分子在不断运动。闻到物质的味道,是因为物 质的分子不断运动向四周造成的;故A答案正确; B.压瘪的乒乓球放入热水中重新鼓起是因为分子体积增大。分子的体积是 固定不变的,压瘪的乒乓球放入热水中重新鼓起,是因为乒乓球内的气体受热之后运动速度 加快,分子间的间隙增大,乒乓球内的气压随之增大,使压瘪的乒乓球重新鼓起;故B答案 错误; c.分离菠态空汽舊懐气说明分子可以再分.空气是由氮汽、牽气、二氧化碳、稱有气体和其他 成分组成的,分离液态空气是利用氮气和髦气的沸点不同,把氧气分离出来,也就是诜把氧气 分子肺选出来.这牛过程没步圧到分子分裂成原子的过程,故匚答嘉错误? D.冰融化成水,说明分子种类发生改变.冰和水是同一种物质的不同形态,和是由水并子构亦 冰融化咸水,从需{观的吊匿分析,是水分子之间的间隙变尢而不是分子种类发主此变-故D 答案错误.
初中化学分子 教学设计
分子教学设计 课题名称分子及其性质课题来源人教版九年级上册化学第三单元课题二 授课教师化学化工学院 王鹤 教学对象九年级上学期学生 教材分析 本节课内容选自人教版初中九年级上册化学第三单元课题二。本课题之前,学生已经学习过关于“物质的变化”、“空气的组成”以及“水的组成”等知识点,对化学学科建立了初步的认识,并产生一定兴趣,明确了“化学是一门以实验为基础的学科”;本课题后将进一步探究学习“原子的性质和构成”、“元素的基本知识”等内容。因此本节课将引导学生们从宏观的实验现象和化学变化过渡到微观世界,进一步研究变化的本质。在整学期的教学过程中起到重要的承前启后的过渡作用。 本节课首先从学生熟悉的宏观物质和日常现象入手,引入物质的可分性,展示科学家对分子的猜想及研究成果,确立物质是由分子等微小粒子组成的观点。进而通过实验探究,教师讲述,小组讨论,类比迁移的手段进一步探究分子的性质。 学情分析 本课题针对的是九年级上学期的学生。该阶段学生接触化学学科时间尚短,不具备深厚的化学基础,却有浓厚的学习兴趣。从本节课开始,学生们对化学的学习和对身边事物的认知将从宏观向理解微观世界过渡。在此过程中,学生对微观世界的接触较少,认识比较抽象,因此需要用生活总常见的事物和现象做类比,也可与其它学科中的知识点做类比迁移,引导学生将知识点具体化,进而直观地掌握本节课的重点,攻克难点。 教学策略 本节课所学内容在九年级化学学习中具有重要的地位和作用。本节课将引领学生从宏观的认知过渡到微观的探索。而微观世界对学生来说接触不多,有一定认知难度。因此我将用两条线索贯穿整堂课的教学: 明线----水 由生活中随处可见的水作为主线,通过对水的分析以及与水相关的实验来确立分子的真实存在性,并引导学生总结归纳出分子的相关性质。同时使学生认识到知识源于生活,抽象的知识点可以用来解释生活中的自然现象。暗线----分子的性质 整堂课将以分子的性质为中心,引导学生们通过学科迁移,联系生活实际,观察并思考实验现象,小组讨论等手段,正确归纳并掌握分子的性质。 教学目标知识与技能: 1、认识物质的可分性,确立物质由分子等微粒构成的观点。 2、了解分子的基本特点。 3、能用分子的观点解释一些简单的生活现象。 过程与方法: 1、学习从自然现象和身边事例中获取知识的能力和方法。 2、学会运用实验探究、迁移、类比、归纳、小组研讨等方法从已知现象及结论学习新知识。 3、培养学生观察实验现象,归纳总结,并得出相应结论的能力。
常用相对分子质量
相对分子质量: 氢H 1 氩 Ar 40 碳C 12 钙 Ca 40 氮N 14 锰 Mn 55 氧O 16 铁 Fe 56 氟F 19 铜 Cu 64 氖Ne 20 锌 Zn 65 钠Na 23 银 Ag 108 镁Mg 24 碘 I 127 铝Al 27 钡 Ba 137 硅Si 28 钨 W 184 磷P 31 铂 Pt 195 硫S 32 金 Au 197 氯Cl 35.5 汞 Hg 201 钾 K 39 铅 Pb 207 氢气H2 2 氨气NH3 17 氮气N228 氧气O232 一氧化碳 CO 28 二氧化碳 CO244 一氧化硫 SO 48 二氧化硫 SO264 三氧化硫 SO380 二氧化锰 MnO2 87 二氧化硅 SiO2 60 一氧化氮 NO 30 二氧化氮 NO 246 三氧化钨 WO3232 二硫化碳 CS2 76 二硫化亚铁FeS2 120 五氧化二磷P2O5142 氧化铁Fe2O3 160 氧化亚铁FeO 82 四氧化三铁Fe3O4 232 氧化铜CuO 80 氧化亚铜Cu2O 144 氧化钠Na2O 62 氧化镁MgO 40 氧化钙CaO 56 氧化铝Al2O3102 氧化汞HgO 217 氧化银Ag2O 232 氧化铅PbO 223 氧化锌ZnO 81 过氧化氢H2O234 氯气Cl271 氯化钾KCl 74.5 氯化钠NaCl 58.5 氯化镁MgCl295 氯化钙CaCl2111 氯化铜CuCl2135 氯化锌ZnCl2136 氯化钡BaCl2208 氯化铝AlCl3133.5 氯化铁FeCl3162.5 氯化亚铁FeCl2127 氯化银AgCl 143.5 氯化氢HCl 36.5 氯酸钾KClO3122.5 氯化铵NH4Cl 53.5 硫酸H2SO498 硫酸锌ZnSO4161 硫酸铵(NH4)2SO4132 硫酸铜CuSO4160 硫酸钡BaSO4233 硫酸钙CaSO4136 硫酸钾KSO4135 硫酸钠Na2SO4142 硫酸镁MgSO4120 硫酸铁Fe2(SO4)3 400
九年级化学 相对分子质量及化学式的计算 人教四年制版
九年级化学相对分子质量及化学式的计算人教四年制版【本讲教育信息】 一. 教学内容: 相对分子质量及化学式的计算 二. 重点、难点 1. 掌握化学式所表示的相关意义 2. 掌握各种计算方法和基本公式 三. 具体内容 化学学习有三大用语:元素符号、化学式和化学方程式。从学习化学式开始,就接触了有关化学计算的相关内容。首先,我们应该从化学式中读出信息。 例如:HO能表示哪些含义呢, 2 能表示物质,能表示分子,能表示物质的组成,能表示分子的构成,还能表示物质中各元素的质量比值和某元素所占的质量关系。下面,我们来回顾几种基本的计算类型。 1. 求相对分子质量 HO 的相对分子质量, 2 相对分子质量应是2个氢原子和1个氧原子的相对原子质量之和。即:1×2+16 = 18 那氢氧化钙、碱式碳酸铜呢,CuSO?5HO呢, 42 2. 求物质中各元素质量比 HO中氢、氧元素的质量比为多少, 2 在这一章中,一定要建立宏观和微观紧密联系的学习思维方式。宏观的元素对应微观的原子。求氢、氧元素的质量比就相当于求氢、氧原子的质量比。在一个水分子中,有2个氢原子和1个氧原子,因此质量比应为:(1×2):16 = 1:8
那NHNO、呢, Cu(OH)CO43223 3. 求物质中某元素的质量分数 求水中氢元素的质量分数, 宏观的元素对应微观的原子,宏观的物质对应微观的分子。因此,求水中氢元素的质量分数就相当于求一个水分子中,两个氢原子所占的比例,即:H% = 2H / HO=(1×2)?18 2= 11.1 % 那NHNO中N%、(NH)SO中N%怎么计算, 43424 4. 元素质量和物质质量的换算(学会应用关系式法) 根据某元素% = 元素质量 / 物质质量,所以得出公式: 元素质量=物质质量×该元素% 该公式在化学式计算中比较重要,所以在做题时要时常注意,只要求元素质量,首先考虑此公式。 例:18g水中含氢元素多少克, 解:18g×(1/9)= 2g 那么,多少克三氧化硫中含氧元素24g, 1 用心爱心专心 【典型例题】 [例1] 多少克NHNO与79g NHHCO中所含氮元素质量相等, 4343 答案:40g 解析:根据求元素的公式 [例2] 若使二氧化硫和三氧化硫里氧元素质量相等,则两物质质量比, 答案:6:5 解析:把题中的已知量氧元素的质量设为具体数值 关于质量相同的CO和CO的叙述正确的是( ) [例3] 下列2
初中化学原子、分子、离子讲义
原子、分子、离子 知识点1:原子核外电子的排布 1、核外高速运动的电子是按能量由低到高,离核由近至远的顺序分层排布的 核外电子的运动状况: 电子层数:一二三四五六七…… 电子能量:逐渐升高 离核距离:逐渐增大 2、原子结构示意图:
核电荷数=质子数=电子数 相对原子质量≈质子数+中子数 3、元素周期表 元素:具有相同核电荷数(即质子数)的一类原子的总称 元素周期表与原子结构的关系: ①同一周期的元素原子的电子层数相同,电子层数=周期数 ②同一族的元素原子的最外层电子数相同,最外层电子数=主族数 4、原子的最外层电子数与元素的分类及化学性质的关系 最外层电子数得失电子元素性质 金属元素一般<4易失活泼
①元素的化学性质决定于原子的最外层电子数。 ②原子最外层电子数为8(氦为2)的结构称为稳定结构。 说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2) 最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构) 知识点2:离子的形成 1、定义:带电的原子或原子团叫离子. (原子团:常作为一个整体参加反应的原子集团) 2、分类: (1)阳离子:带正电荷的离子(原子失电子) (2)阴离子:带负电荷的离子(原子得电子) 3、离子的表示方法: (1)离子符号:(离子符号歪戴帽,先写数字后写号)Na+、Cl-、O2-、2Mg2+ Mg2+——表示镁离子(一个镁离子) 2Mg2+:小2表示每个镁离子带两个单位的正电荷,大2表示两个镁离子 离子符号表示的意义:表示离子(或一个离子) 离子符号前面的化学计量数(系数)表示离子的个数; (2)离子结构示意图:(特点:最外层稳定结构) 阳离子:质子数>电子数 阴离子:质子数<电子数
初三化学分子和原子练习题
原子结构 1.物质在不同条件下的三态变化,主要是由于()。 A.分子的大小发生了变化 B.分子的质量发生变化 C.分子之间的间隔发生了变化 D.分子的形状发生变化 2.分子和原子的主要区别是()。 A.分子大、原子小 B.分子的质量大,原子的质量小 C.分子可直接构成物质,原子则要先构成分子后再构成物质 D.在化学变化中分子可再分,原子则不能再分 3.下列变化能证明分子在化学反应中可分的是()。 A.铁矿石磨成粉末 B.碘受热升华 C.加热水有水蒸气生成 D.加热氧气汞生成汞和氧气 4.构成二氧化碳气体的分子与构成液态二氧化碳的分子具有()。 A.相同的质量 B.不同的质量 C.相同的化学性质 D.不同的化学性质 5.下列有关分子的说法中错误的是()。 A.酒精的挥发是由于酒精分子不断的运动而扩散到空气里去的缘故 B.相同体积的冰和水含有相同数目的水分子 C.从空气中分离得到的氧气分子和高锰酸钾分解得到的氧气分子性质相同 D.1体积的水与1体积的无水酒精混合后总体积小于2体积,是因为分子间有间隔
6.下列能说明在化学变化中分子可分而原子不可分的是() A. 水受热变成水蒸气 B. 水在通电条件下生成氢气和氧气 C. 品红扩散 D. 酒精温度计能指示出温度高低 7. 关于氧气、液态氧、固态氧,下列说法:①它们的物理性质不同②它们的化学性质相同③它们的化学性质不同④它们由同种分子构成⑤它们为不同的物质。其中正确的是() A. ①②④ B. ①③④ C. ①②④ D. ②④⑤ 8.下列叙述中正确的是( ) A. 氧分子是保持氧气性质的最小粒子 B. 氯酸钾中含有氧分子,故加热时能放出氧气 C. 氮气和氧气混合后,它们的化学性质都会改变 D. 氮分子是保持氮气化学性质的最小粒子 9.由分子参加的化学反应,反应前后一定发生变化的是()。 A分子种类 B.分子数目 C.原子种类 D.原子数目 10. 以下说法都是是错误的() A. 分子的体积比原子大 B. 分子的质量比原子大 C. 分子能构成物质,原子不能构成物质 D. 分子是保持物质化学性质的一种粒子,原子不能保持物质化学性质 11.下列现象中不能用分子运动解释的是()。 A.把两块表面平滑的铅压紧,就不容易将它们拉开 B.在室内,同样表面积的热水比冷水蒸发得快
初中常用相对分子质量及计算公式
氢 气 H 2 2 五氧化二磷 P 2O 5 142 氧 气 O 2 32 氢氧化钙(熟石灰) Ca(OH)2 74 氯 气 Cl 2 71 氢氧化铜 Cu(OH)2 98 氨 气 NH 3 17 氢氧化钠 NaOH 40 氮 气 N 2 28 过氧化氢(双氧水) H 2O 2 34 一氧化碳 CO 28 碱式碳酸铜(绿) Cu 2(OH)2CO 3 222 二氧化碳 CO 2 44 盐酸(氯化氢) HCl 36.5 一氧化硫 SO 48 氯化钙 CaCl 2 111 二氧化硫 SO 2 64 氯化钾 KCl 74.5 三氧化硫 SO 3 80 氯化铁(淡黄溶) FeCl 3 162.5 二氧化锰 MnO 2 87 氯酸钾 KClO 3 122.5 碳 酸 H 2CO 3 62 高锰酸钾(灰锰氧) KMnO 4 158 碳酸钙 CaCO 3 100 硫酸铜(白固 蓝溶) CuSO 4 160 碳酸氢铵 NH 4HCO 3 79 硫酸钠 Na 2SO 4 142 硝 酸 HNO 3 63 硝酸铵 NH 4NO 3 80 硫 酸 H 2SO 4 98 甲 烷 CH 4 16 亚硫酸 H 2SO 3 82 尿 素 CO(NH 2)2 60 磷 酸 H 3PO 4 98 甲 醇 CH 3OH 32 水 H 2O 18 乙醇(酒精) C 2H 5OH 46
氧化铜(黑)CuO 80 乙炔C H226 2 氧化镁(白)MgO 40 乙酸(醋酸)CH COOH 60 3 氧化钙(白)CaO 56 四氧化三铁(黑)Fe O4232 3 氧化铁(红)Fe O3160 2 氧化亚铁(黑)FeO 72 硫酸亚铁(淡绿)FeSO 152 4 硫酸锌(白/无)ZnSO 161 4 初中化学常用计算公式 一. 常用计算公式: (1)相对原子质量= 某元素一个原子的质量/ 一个 碳原子质量的1/12 (2)设某化合物化学式为AmBn ①它的相对分子质量=A的相对原子质量×m+B的相 对原子质量×n ②A元素与B元素的质量比=A的相对原子质量×m: B的相对原子质量×n
初三化学分子教案
初三化学分子教案 一.教学目标 知识与技能使学生能认识分子的真实存在,理解分子的概念,了解分子的基本性质。 过程与方法1.学习运用日常生活现象与课本理论相结合的方式,用课本理论来解释日常生活中的现象; 2.充分发挥空间想象能力; 3.学习运用比较、分析、归纳等方法对实验所得信息进行加工。 情感态度价值观形成良好的科学态度和辩证地看问题的思想方法 二.教学内容 1.分子的概念:分子是保持物质化学性质的最小粒子。 2.分子的基本性质:①分子的体积和质量都很小。 ②分子处于不断的运动中。 ③分子之间有间隔。 重点:分子概念的建立及对分子性质微观想象的形成 难点:建立微观粒子想象表象,初步体会它与宏观物体运动的不同。 三.教学方法 启发式,讲授式,实验探究等与多媒体教学相结合 四.教学材料:醋、香水、纯净水、红墨水、酒精、黄豆、大米,烧杯(3个)、 黑板、粉笔、多媒体课件等 五.教学过程: 引入请大家边欣赏这些漂亮的图片边看我做两个小实验 PPT展示几幅美图 实验1.红墨水滴入纯净水中; 2.把醋和香水滴在纸上。 现象:实验1中纯净水逐渐变红;
实验2中闻到有香味的是香水,有酸味的是醋。 师以上两个实验从表面上看好像没有什么联系,但是当人们认识到一切物质都是有相应的“粒子”(副板)所构成的以后,这些现象就比较容易理解了。谁来解释一下实验1中为什么滴入红墨水之后变红了? 学生1红墨水粒子扩散到了水的粒子中 提问为什么我们通过闻到他们的气味就能判断出他们是醋或者是香水呢? 学生2因为在醋或者香水中他们的粒子扩散到了空气中,接触到人的嗅觉细胞,因而使人嗅到了他们的气味。 师上述我们所说的这些粒子,在化学上我们称之为“分子” 板书2.1分子 讲解分子是构成物质的一种粒子。上一章学到过的N2就是由氮气分子所构成。我们呼进去的氧气由氧气分子所构成,那吐出来的CO2就是由什么所构成的? 学生二氧化碳分子 师由分子构成的物质在发生物理变化的时候,物质的分子本身没有变化。比如:水变成水蒸气,水分子本身没有变,那水的化学性质有没有变? 回答没有 副板1.物理变化――分子不变 师而由分子所构成的物质在发生化学变化的时候,它的分子去发生了变化,变成了别的物质。举个例子:C在O2中燃烧时,C和O2分子都发生了变化,生成了什么?对,二氧化碳是一种新的分子,那么C和O2的化学性质能不能保持啊?当然也就不能了。 副板2.化学变化――分子改变 过渡那什么是分子呢? 板书一.定义:分子是保持物质化学性质的最小粒子。 注意是保持:“化学性质”而不是物理性质。同种物质的分子性质相同,不同种的物质的分子性质不同。 解释这个数据有多大呢?这么说吧,如果我们全中国人都来数这一滴水里的水分子,每个人每分钟数100个,日夜不停,需要数多久了?学要2万多年! PPT如果把水分子大小跟乒乓球相比就好像师拿乒乓球跟地球相比一样。
初中化学分子式
初中常用化学分子式(实用) 酸 硫酸H2SO4 亚硫酸H2SO3 盐酸HCl 硝酸HNO3 硫化氢H2S 碳酸H2CO3 初中常见物质的化学式 氢气碳氮气氧气磷硫氯气(非金属单质) H2 C N2 O2 P S Cl2 钠镁铝钾钙铁锌铜钡钨汞(金属单质) Na Mg Al K Ga Fe Zn Cu Ba W Hg 水一氧化碳二氧化碳五氧化二磷氧化钠二氧化氮二氧化硅 H2O CO CO2 P2O5 Na2O NO2 SiO2 二氧化硫三氧化硫一氧化氮氧化镁氧化铜氧化钡氧化亚铜 SO2 SO3 NO MgO CuO BaO Cu2O 氧化亚铁三氧化二铁(铁红)四氧化三铁三氧化二铝三氧化钨FeO Fe2O3 Fe3O4 Al2O3 WO3 氧化银氧化铅二氧化锰(常见氧化物)
Ag2O PbO MnO2 氯化钾氯化钠(食盐) 氯化镁氯化钙氯化铜氯化锌氯化钡氯化铝 KCl NaCl MgCl2 CaCl2 CuCl2 ZnCl2 BaCl2 AlCl3 氯化亚铁氯化铁氯化银(氯化物/盐酸盐) FeCl2 FeCl3 AgCl 硫酸盐酸硝酸磷酸硫化氢溴化氢碳酸(常见的酸) H2SO4 HCl HNO3 H3PO4 H2S HBr H2CO3 硫酸铜硫酸钡硫酸钙硫酸钾硫酸镁硫酸亚铁硫酸铁 CuSO4 BaSO4 CaSO4 KSO4 MgSO4 FeSO4 Fe2 (SO4)3 硫酸铝硫酸氢钠硫酸氢钾亚硫酸钠硝酸钠硝酸钾硝酸银 Al2(SO4)3 NaHSO4 KHSO4 NaSO3 NaNO3 KNO3 AgNO3 硝酸镁硝酸铜硝酸钙亚硝酸钠碳酸钠碳酸钙碳酸镁 MgNO3 Cu(NO3)2 Ca(NO3)2 NaNO3 Na2CO3 CaCO3 MgCO3 碳酸钾(常见的盐) K2CO3 氢氧化钠氢氧化钙氢氧化钡氢氧化镁氢氧化铜氢氧化钾氢氧化铝 NaOH Ca(OH)2 Ba(OH)2 Mg(OH)2 Cu(OH)2 KOH Al(OH)3 氢氧化铁氢氧化亚铁(常见的碱) Fe(OH)3 Fe(OH)2 甲烷乙炔甲醇乙醇乙酸(常见有机物) CH4 C2H2 CH3OH C2H5OH CH3COOH 碱式碳酸铜石膏熟石膏明矾绿矾 Cu2(OH)2CO3 CaSO4?2H2O 2 CaSO4?H2O KAl(SO4)2?12H2O FeSO4?7H2O 蓝矾碳酸钠晶体(常见结晶水合物)
初中化学教案:分子
初中化学教案:分子 初中化学教案 教学目标 知识目标: 1.学生认识分子的真实存在及分子是构成物质的一种粒子; 2.了解分子的概念和基本性质; 3.学会用分子的观点来区别物理变化和化学变化; 4.理解纯净物和混合物的概念并会判断典型的纯净物和混合物。 能力目标: 培养学生查阅资料、观察及抽象思维能力。 情感目标: 通过实验和讨论激发学生的学习兴趣,培养学生团结协作精神。 教学建议 教材分析 本节教材分成"分子"和"混合物和纯净物"两部分。 前一部分着重于描述物质由分子等粒子所构成,讨论分子的基本性质。教材一开始从人们所熟悉的一些日常现象入手,如:人经过花圃或酒店,会嗅到花或酒的香气;湿的衣服经过晾晒就会干燥;糖块放在水里,会逐渐消失,而水却有了甜味等。通过对这些日常生活现象的思考,使学生自然而然的建立起物质是由人们看不见、摸不着的粒子构成的结论(分子是构过成物质的一种粒子)。通过酒精和水混合后总体积缩小,及晶体碘的升华与凝华等实验现象,使学生在建立起分子是构成物质的一种粒子的结论基础上进一步得出分子是运动的及分子之间有间隔的推论(即分子的性质)。之后,教材以水变成水蒸气,蔗糖溶于水及硫或碳在氧气中燃烧生成二氧化硫或二氧化碳几个典型的物理变化和化学变化,运用初步介绍的分子知识对物质发生变化时分子本身是否发生改变对物理变化、化学变化进行了实质性的分析。从而给分子下一个比较准确的定义。 教材为了进一步让学生确信分子存在的客观性,展示了用扫描隧道显微镜拍摄的苯分子照片,同时用生动的比喻、引导读者去想象分子的大小和运动状态。使学生在感性和理性上都建立起对分子的认识。
教材的第二部分首先以空气的组成及硫粉和铁粉混合实验为基础从宏观上对混合物和 纯净物两个概念做了区分。然后从微观上-用初步掌握的有关分子知识进一步区分纯净物 和混合物,使学生能初步建立纯与不纯的相对概念。 教学建议 本节重点研究的是有关分子知识。分子看不见也摸不着,对于它的存在学生很难相信,接受起来远不如第一章知识来的快。教材第一章重点研究的是氧气的制法及性质。对于氧 气学生比较熟悉,在学生的头脑中已经建立起人吸进的是氧气,呼出的是二氧化碳的概念。氧气尽管也看不见,摸不着,但学生能凭生活经验确信氧气真实存在着。鉴于此,建议在 教学过程中也从生活实际中遇到的问题入手,例如:人经过花圃或酒店,为什么能闻到花 或酒的香气;湿的衣服经过晾晒为什么能干;糖块放在水里,为什么会逐渐消失,而水却 有了甜味等。将宏观现象做为纽带,诱发学生进行想象-人能嗅到花或酒的香气,是因为 花或酒中有香气的分子(或粒子)扩散到空气中,接触到人的嗅觉细胞而使人嗅到了香气。湿衣服能晾干,是由于水的分子扩散到空气中去了。糖块放在水中溶解,而水有了甜味, 是由于糖的分子扩散到水的分子中间去了。以生活实际中的问题让学生感知分子的真实存在。将宏观现象与微观结构建立起了联系。教学过程中将学生实验(氨分子扩散实验、品 红扩散实验并补充酒精与水混合实验)融入在课堂教学中,通过学生实验让学生进一步感 知分子的真实存在,同时也便于学生学习分子性质时,树立起分子是运动的,不同物质分 子大小不同和分子间都有间隔距离的想象。为了使学生更加确信分子的真实存在,除向学 生展示用扫描隧道显微镜拍摄的苯分子照片外,还可让学生通过网络或图书馆查找其它分 子的照片。 对于分子概念的建立,是本节知识的一个重点。教师首先可用多媒体向学生展示第一 章中涉及的几个物质变化(如:水变成水蒸气,硫在氧气中燃烧生成二氧化硫)的微观过程,然后让学生用初步掌握的分子知识以小组的形式从物质发生物理变化或化学变化时分 子本身是否发生改变,对物理变化、化学变化进行实质性的分析,从而给分子一个比较准 确的定义。 本节教材的另一个重点,是使学生树立分子既有可分性又有不可分性的辨证观 点?quot;分子是保持物质化学性质的最小粒子"从保持原物质化学性质来说分子是不可分 的整体粒子,因为分子再分就不是原来物质的分子,也不能保持原来物质的化学性质。同 种物质的分子性质相同,不同种物质的分子性质不同。分子可以再分是说它在化学反应过 程中分子起了变化,变成别种物质的粒子了。通过对分子的可分性与不可分性的认识,逐 步培养学生辨证地思考问题。分子概念中还强调了"化学性质"是因为通常讨论的物理性质 是一种宏观现象,是该物质大量分子聚集在一起表现出来的,而不是每一个单个分子所能 表现的,如:颜色、状态、熔点、沸点、密度等。本节知识不仅应让学生了解分子的概念,也应让学生弄清概念的内在含义。 在学生对分子概念有了了解之后,师生应对分子的基本性质有一个比较全面的概括。 除能指出分子是保持物质化学性质的最小粒子外,还应认识到分子非常微小,分子都在不
九年级化学元素、元素符号、化学式、相对分子质量人教版知识精讲
初中化学元素以及化学式相对分子质量的计算 【同步教育信息】 一. 本周教学内容: (一)元素元素符号 1. 了解元素概念 2. 元素、原子、单质之间的区别和联系 3. 运用元素概念区分单质和化合物 4. 了解元素符号的意义,学会元素符号的正确书写 5. 熟记常见的元素符号 (二)化学式相对分子质量 1. 理解化学式和相对分子质量概念 2. 掌握化学式的书写和读法 3. 理解化学式前和化学式中有关数字的意义 4. 掌握根据化学式的有关计算 二. 重点、难点: 1. 元素、单质、化合物、氧化物的概念 2. 物质的简单分类 3. 元素符号的涵义和书写方法 4. 化学式的写法和读法 4. 有关化学式的计算 三. 教学过程 (一)元素元素符号 1. 元素的概念 世界是由物质组成的。人类已知物质有一千多万种,而这么多物质是由一百多种元素组成。元素的概念是:元素是具有相同核电荷数(即质子数)的同一类原子的总称。元素只有一百多种,物质有一千多万种,说明一种元素能形成许多种物质,或者说许多种物质里可以含有同一种元素。例如水、二氧化碳、氧化汞、氧气里都含有氧元素。比如,英文字母有26个,而英文单词有成千上万个。元素是宏观概念,是同一类原子的总称,只讲种类,不讲个数。决定元素种类的是质子数。原子是具体的微观粒子,既讲种类,又讲个数。如同人类和人。我们不能说几个人类,但可以说几个人。我们可以说鸟类、人类等等,不能说几个鸟类,我们可以说几只鸟或几个人。元素用于描述物质宏观组成,原子用于描述物质的微观组成。如二氧化碳是由碳元素和氧元素组成,一个二氧化碳分子是由一个碳原子和二个氧原子构成。氧气是由氧元素组成,一个氧分子由两个氧原子构成。 元素与原子的比较
九年级上册化学 分子和原子知识点梳理
分子和原子知识点梳理 课题1、分子和原知识点梳理 知识点一:物质是由分子和原子构成的。 1.认识分子 1、分子的基本性质 (1)分子是构成物质的一种粒子,其质量、体积都非常小。 自然界中大多数的物质是由分子构成的。 (2)分子在不断地做无规则运动。 温度越高,分子的运动速度就越快。 (3)分子之间有一定的间隔:气态>液态>固态 (4)同种分子的化学性质相同;不同种分子的化学性质不同 2、分子的概念:保持物质化学性质的最小粒子 3、应用分子的观点认识: (1)纯净物、混合物: 纯净物混合物
由分子构成的物质中,由同一种分子构成的是纯净物。如冰、水共存物实际为纯净物,因为其中的构成粒子只有一种——水分子,由不同种分子构成的是混合物,如红磷和白磷的混合体为混合物,区分纯净物和混合物的关键是把握“物质的种类”或“分子的种类”是否相同。 (2)物理变化、化学变化 水蒸发是发生了物理变化,而水分解是发生了化学变化 水蒸发时,水分子本身没有变化,变化的只是分子间的间隔。水的化学性质也没有改变。水分解时,水分子变成了氢分子和氧分子。分子变了,生成的氢分子和氧分子不具有水分子的化学性质。 注意:在化学变化中,分子的组成一定改变,分子的数目可能改变。 二)认识原子 1、原子定义:化学变化中的最小微粒 2、化学反应的实质:化学变化中分子分裂成原子,原子重新组合成新分子。 3、分子、原子的主要区别:在化学反应中,分子可分,原子不可分 4、分子、原子的相互关系: 5、原子的基本性质: (1)原子也是构成物质的一种粒子,其质量、体积都非常小。 (2)原子同分子一样,也是时刻不停地做高速的无规则运动。 温度越高,能量越大,运动速度就越快。 (3)原子之间也有一定的间隔 原子: 分子:
初三化学:分子和原子知识点汇总二
初三化学:分子和原子知识点汇总二 二、考点清单 1、认识物质的微粒性,知道分子、原子的区别与联系 2、能用分子的观点解释某些常见的现象 3、认识原子的构成。初步了解相对原子质量 三、全面突破 知识点1:分子和原子 一)认识分子 1、分子的基本性质 (1)分子是构成物质的一种粒子,其质量、体积都非常小。 自然界中大多数的物质是由分子构成的。 (2)分子在不断地做无规则运动。 温度越高,分子的运动速度就越快。
(3)分子之间有一定的间隔:气态>液态>固态 (4)同种分子的化学性质相同;不同种分子的化学性质不同 2、分子的概念:保持物质化学性质的最小粒子 3、应用分子的观点认识: (1)纯净物、混合物: 纯净物混合物 由分子构成的物质中,由同一种分子构成的是纯净物。如冰、水共存物实际为纯净物,因为其中的构成粒子只有一种——水分子,由不同种分子构成的是混合物,如红磷和白磷的混合体为混合物,区分纯净物和混合物的关键是把握“物质的种类”或“分子的种类”是否相同。 (2)物理变化、化学变化 水蒸发是发生了物理变化,而水分解是发生了化学变化 水蒸发时,水分子本身没有变化,变化的只是分子间的间隔。水的化学性质也没有改变。水分解时,水分子变成了氢分子和氧分子。分子变了,生成的氢分子和氧分子不具有水分子的化学性质。 注意:在化学变化中,分子的组成一定改变,分子的数目可能改变。
二)认识原子 1、原子定义:化学变化中的最小微粒 2、化学反应的实质:化学变化中分子分裂成原子,原子重新组合成新分子。 3、分子、原子的主要区别:在化学反应中,分子可分,原子不可分 4、分子、原子的相互关系: 5、原子的基本性质: (1)原子也是构成物质的一种粒子,其质量、体积都非常小。 (2)原子同分子一样,也是时刻不停地做高速的无规则运动。 温度越高,能量越大,运动速度就越快。 (3)原子之间也有一定的间隔 原子: 分子:
初中化学分子的性质(提高) 知识讲解
分子的性质(提高) 责编:熊亚军 【学习目标】 1.掌握分子的性质;掌握用粒子的观点解释某些常见的现象。 2.认识分子是保持物质化学性质的最小粒子。 3.能用分子的观点来区别物理变化和化学变化、纯净物和混合物。 【要点梳理】 要点一、分子 1.分子是真实存在的: (1)能闻到花香酒香及品红的扩散等现象,充分说明物质是由分子等微粒构成的,分子在不断地运动。(2)运用现代科学技术手段已观察到了一些分子和原子,也充分证明分子是真实存在的。 2.分子的定义:分子是保持物质化学性质的最小粒子。 (1)构成物质的每一个分子与该物质的化学性质是一致的,分子保持的是物质的化学性质,如氧气的化学性质由氧分子保持,二氧化碳的化学性质由二氧化碳分子保持。 (2)分子不保持物质的物理性质。物质的物理性质(如颜色、状态)是由大量分子聚集在一起才能表现出来的,是宏观现象,不是单个分子能表现出来的。 3.分子的性质:(高清课堂《分子和原子》一) (1)分子的质量和体积都很小。 (2)分子在不断地运动。温度越高分子运动的速率越快,如阳光下湿衣物干得快。 (3)分子之间有间隔。气体的分子之间间隔较大,液体和固体的分子之间间隔较小。气体比液体和固体容易压缩,不同液体混合后的总体积小于二者的原体积之和,都说明分子之间有间隔。 (4)同种物质的分子性质相同,不同种物质的分子性质不同。我们都有这样的生活体验:若口渴了,可以喝水解渴,吃几块冰块也可以解渴,这就说明:水和冰都具有相同的性质,因为水和冰都是由水分子构成的,同种物质的分子,性质是相同的。 【要点诠释】 1.构成物质的微粒具有质量小、体积小、不断运动、有间隔等基本特征。 2.分子是构成物质的一种粒子,而不是唯一的微粒,构成物质的微粒还有原子、离子。 3.分子是由原子构成的,不同分子的构成是不同的。如1个水分子是由两个氢原子和一个氧原子构成的,而1个氢分子是由两个氢原子构成的。 要点二、从分子的观点理解有关概念 1.物理变化和化学变化:由分子构成的物质,发生物理变化时,分子本身没有发生变化,即没有生成新物质。如水的三态变化,只是水分子的聚集状态改变了,水分子本身并没有变。 当物质发生化学变化时,分子本身发生了改变,生成了其他物质的分子。如水在通电条件下分解生成氢气和氧气,这时水分子就变成了氧分子和氢分子,即在化学变化中分子本身发生了改变。
相对原子质量表大全
氢气H2 2 五氧化二磷P2O5142 氧气O232 氢氧化钙(熟石灰)Ca(OH)274 氯气Cl271 氢氧化铜Cu(OH)298 氨气NH317 氢氧化钠NaOH 40 氮气N228 过氧化氢(双氧水)H2O234 一氧化碳CO 28 碱式碳酸铜(绿)Cu2(OH)2CO3222 二氧化碳CO244 盐酸(氯化氢)HCl 36.5 一氧化硫SO 48 氯化钙CaCl2111 二氧化硫SO264 氯化钾KCl 74.5 三氧化硫SO380 氯化铁(淡黄 FeCl3162.5 溶) 二氧化锰MnO287 氯酸钾KClO3122.5 碳酸H2CO362 高锰酸钾(灰锰氧)KMnO4158 碳酸钙CaCO3100 硫酸铜(白固蓝 CuSO4160 溶) 碳酸氢铵NH4HCO379 硫酸钠Na2SO4142 硝酸HNO363 硝酸铵NH4NO380 硫酸H2SO498 甲烷CH416 亚硫酸H2SO382 尿素CO(NH2)260 磷酸H3PO498 甲醇CH3OH 32 水H2O 18 乙醇(酒精)C2H5OH 46 氧化铜(黑)CuO 80 乙炔C2H226 氧化镁(白)MgO 40 乙酸(醋酸)CH3COOH 60 氧化钙(白)CaO 56 四氧化三铁(黑)Fe3O4232 氧化铁(红)Fe2O3160 氧化亚铁(黑)FeO 72
硫酸亚铁(淡绿)FeSO4152 硫酸锌(白/无)ZnSO4161 初中化学常用计算公式 一. 常用计算公式: (1)相对原子质量= 某元素一个原子的质量/ 一个 碳原子质量的1/12 (2)设某化合物化学式为AmBn ①它的相对分子质量=A的相对原子质量×m+B的相 对原子质量×n ②A元素与B元素的质量比=A的相对原子质量×m: B的相对原子质量×n ③A元素的质量分数ω=A的相对原子质量×m /AmBn 的相对分子质量
化学分子式
酸 硫酸H2SO4 亚硫酸H2SO3 盐酸HCl 硝酸HNO3 硫化氢H2S 碳酸H2CO3 初中常见物质的化学式 氢气碳氮气氧气磷硫氯气(非金属单质) H2 C N2 O2 P S Cl2 钠镁铝钾钙铁锌铜钡钨汞(金属单质) Na Mg Al K Ga Fe Zn Cu Ba W Hg 水一氧化碳二氧化碳五氧化二磷氧化钠二氧化氮二氧化硅 H2O CO CO2 P2O5 Na2O NO2 SiO2 二氧化硫三氧化硫一氧化氮氧化镁氧化铜氧化钡氧化亚铜 SO2 SO3 NO MgO CuO BaO Cu2O 氧化亚铁三氧化二铁(铁红)四氧化三铁三氧化二铝三氧化钨FeO Fe2O3 Fe3O4 Al2O3 WO3 氧化银氧化铅二氧化锰(常见氧化物) Ag2O PbO MnO2 氯化钾氯化钠(食盐) 氯化镁氯化钙氯化铜氯化锌氯化钡氯化铝KCl NaCl MgCl2 CaCl2 CuCl2 ZnCl2 BaCl2 AlCl3 氯化亚铁氯化铁氯化银(氯化物/盐酸盐) FeCl2 FeCl3 AgCl 硫酸盐酸硝酸磷酸硫化氢溴化氢碳酸(常见的酸) H2SO4 HCl HNO3 H3PO4 H2S HBr H2CO3 硫酸铜硫酸钡硫酸钙硫酸钾硫酸镁硫酸亚铁硫酸铁 CuSO4 BaSO4 CaSO4 KSO4 MgSO4 FeSO4 Fe2 (SO4)3 硫酸铝硫酸氢钠硫酸氢钾亚硫酸钠硝酸钠硝酸钾硝酸银 Al2(SO4)3 NaHSO4 KHSO4 NaSO3 NaNO3 KNO3 AgNO3 硝酸镁硝酸铜硝酸钙亚硝酸钠碳酸钠碳酸钙碳酸镁 MgNO3 Cu(NO3)2 Ca(NO3)2 NaNO3 Na2CO3 CaCO3 MgCO3 碳酸钾(常见的盐) K2CO3 氢氧化钠氢氧化钙氢氧化钡氢氧化镁氢氧化铜氢氧化钾氢氧化铝NaOH Ca(OH)2 Ba(OH)2 Mg(OH)2 Cu(OH)2 KOH Al(OH)3 氢氧化铁氢氧化亚铁(常见的碱) Fe(OH)3 Fe(OH)2 甲烷乙炔甲醇乙醇乙酸(常见有机物) CH4 C2H2 CH3OH C2H5OH CH3COOH 碱式碳酸铜石膏熟石膏明矾绿矾
初中化学知识点汇总(分子组成与结构)
初中化学知识点汇总(分子组成与结构) 1、分子是保持物质化学性质的最小粒子(由原子、离子构成的物质,原子、离子也能保持物质的化学性质)。 原子是化学变化中的最小粒子。 例如:保持氯气化学性质的最小粒子是D(氯分子)(A、lB、l-、2lD、l2)。保持2化学性质的最小粒子是2分子;保持水银的化学性质的最小粒子是汞原子。 在电解水这一变化中的最小粒子是氢原子和氧原子。 分子的特点: 1)分子的质量和体积都很小。 2)分子总是在不断运动着。(受热的情况下,分子能量增大,运动速率加快。) 3)分子间是有间隔的。(热胀冷缩现象就是物质分子间的间隔受热时增大,遇冷时缩小的缘故。) 4)分子是由原子构成的。 )同种分子化学性质相同,不同种分子化学性质不同。 例:从微观的角度看,水的蒸发与水的电解两种变化有什么不同? 例:试从微观的角度分析,酒精挥发和酒精燃烧两种变化有什么不同? 原子中:核电荷数(带正电)=质子数=核外电子数 相对原子质量=质子数+中子数
原子是由原子核和核外电子构成的,原子核是由质子和中子构成的,构成原子的三种粒子是:质子(正电)、中子(不带电)、电子(带负电)。一切原子都有质子、中子和电子吗?(错!一般的氢原子无中子)。 某原子的相对原子质量=某原子的质量/原子质量的1/12。相对原子质量的单位是"1",它是一个比值。相对分子质量的单位是"1"。 由于原子核所带电量和核外电子的电量相等,电性相反,因此整个原子不显电性(即电中性)。 2、①由同种元素组成的纯净物叫单质(由一种元素组成的物质不一定是单质,也可能是混合物,但一定不可能是化合物。如:金刚石和石墨、氧气和臭氧、红磷和白磷。) ②由一种分子构成的物质一定是纯净物。 ③由不同种元素组成的纯净物一定是化合物;化合物一定是由不同种元素组成的。 纯净物与混合物的区别是物质的种类不同。单质和化合物的区别是元素的种类不同。 ④由两种元素组成的化合物,其中一种是氧元素的叫做氧化物。氧化物一定是含氧化合物,但含氧化合物不一定是氧化物。 ⑤元素符号的意义:表示一种元素,表示这种元素的一个原子。有些还可以表示一种物质。
初中常用相对分子质量及常用化学计算公式
初中常见分子量总结(根据颜色和可溶性,可以组合分离和除杂题自测) 氢气(无无)H2 2 硝酸HNO363 氧气(无无)O232 硝酸根离子团NO3-62 氨气(刺透)NH317 硝酸铵(白/无)NH4NO380 硝酸银Ag NO3170 水H2O 18 盐酸(氯化氢)HCl 36.5 二氧化碳(无无)CO244 两个氯化氢分子 2 HCl73 氧化钙(生石灰)白CaO 56 氯离子Cl1-35.5 一氧化碳(无无)CO 28 氯化钠(食盐)白NaCl 58.5 氧化镁(白)MgO 40 氯化铁(淡黄溶)FeCl3162.5 氧化铁(红)Fe2O3160 氯化钙(白/无)CaCl2111 氧化铜(黑)CuO 80 氯化钡(白/无)BaCl2208 四氧化三铁(黑)Fe3O4232 氯化银AgCl 143.5 氧化亚铁(黑)FeO 72 二氧化锰(黑)MnO287 二氧化硫(刺透)SO264 硫酸H2SO498 硫酸根离子团SO42-96 碳酸H2CO362 硫酸铜(白固蓝溶)CuSO4160 碳酸根CO32—60 硫酸钠(白/无)Na2SO4142 碳酸钙(白沉酸溶)CaCO3100 硫酸钡(白不溶沉)BaSO4233 碳酸钠(白/无)Na2CO3106 硫酸镁(白/无)MgSO4120 碳酸钡(白沉酸溶)BaCO3197 硫酸亚铁(淡绿)FeSO4152 碳酸氢铵(白/无)NH4HCO379 硫酸锌(白/无)ZnSO4161 碱式碳酸铜(绿)Cu2(OH)2CO3222 五水硫酸铜(蓝固蓝溶)Cu SO4 5H2O 250 ? 氯酸钾KClO3122.5 氢氧化钠NaOH 40 高锰酸钾(灰锰氧)KMnO4158 氢氧化钙(熟石灰微溶)Ca(OH)274 甲烷CH416 氢氧根 OH17 尿素CO(NH 2)260 氢氧化镁(白/无)Mg(OH)258 乙醇(酒精)C2H5OH 46 氢氧化铜(蓝沉酸溶)Cu(OH)298 乙酸(醋酸)CH3COOH 60 氨水NH3 H2O35 蔗糖C6H12O6180 ?
