有关官能团的保护

有机合成中的基团保护、导向基(咼考必备)
(一)基团保护
在有机合成中,些不希望起反应的官能团,在反应试剂或反应条件的影响下 而产生副反应,这样就不能达到预计的合成目标, 因此,必须采取对这些基团进 行保护,完成合成后再除去保护基,使其复原。
对保护措施一定要符合下列要求:①只对要保护的基团发生反应,而对其他 基团不反应;②反应较容易进行,精制容易;③保护基易脱除,在除去保护基时, 不影响其他基团。
下面只简略介绍要保护的基团的方法。 1、羟基的保护
在进行氧化反应或某些在碱性条件进行的反应, 往往要对羟基进行保护。女口 防止羟基受碱的影响,可用成醚反应。
-OH A - OR
2、对氨基的保护
氨基是个很活泼的基团,在进行氧化、烷基化、磺化、硝化、卤化等反应时 往往要对氨基进行保护。
防止羟基氧化可用酯化反应。
-OH -------- - O
OC
(1)乙酰化
-NH 2C 或酸OC 1 O
-NH 2— C —
CH 3
(2)对NR 可以加H +质子化形成季铵盐,-NH 也可加H +成-NHr 而保护。 3、对羰基的保护
羰基,特别是醛基,在进行氧化反应或遇碱时,往往要进行保护。对羰基的 保护一般采用缩醛或缩酮反应。+
_ H
-CHO + 2ROH
-CH(OR )2
o
CHjOH II + I
R —0—R
CH 2CH
f
化反应
4、对羧基的保护
羧基在高温或遇碱性试剂时,有时也需要保护,对羧基的保护最常用的是酯 -COOR
-COOH + R -OH
c\
o O
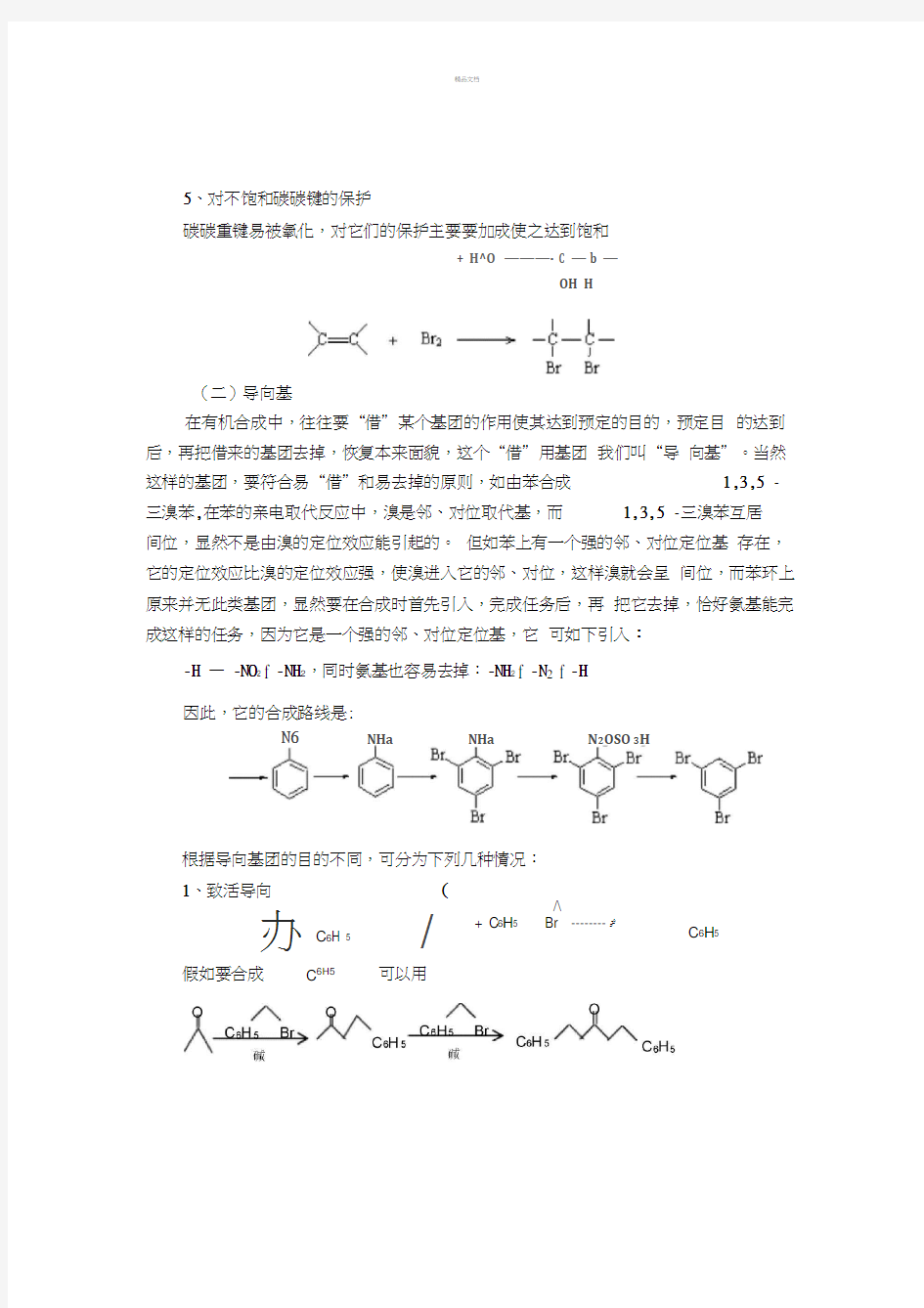
5、对不饱和碳碳键的保护
碳碳重键易被氧化,对它们的保护主要要加成使之达到饱和
(二)导向基
在有机合成中,往往要“借”某个基团的作用使其达到预定的目的,预定目 的达到后,再把借来的基团去掉,恢复本来面貌,这个“借”用基团 我们叫“导 向基”。当然这样的基团,要符合易“借”和易去掉的原则,如由苯合成 1,3,5 -
三溴苯,在苯的亲电取代反应中,溴是邻、对位取代基,而
1,3,5 -三溴苯互居
间位,显然不是由溴的定位效应能引起的。 但如苯上有一个强的邻、对位定位基 存在,它的定位效应比溴的定位效应强,使溴进入它的邻、对位,这样溴就会呈 间位,而苯环上原来并无此类基团,显然要在合成时首先引入,完成任务后,再 把它去掉,恰好氨基能完成这样的任务,因为它是一个强的邻、对位定位基,它 可如下引入:
-H — -NO 2 f -NH 2,同时氨基也容易去掉:-NH 2 f -N 2 f -H 因此,它的合成路线是:
根据导向基团的目的不同,可分为下列几种情况: 1、致活导向
(
办
/
假如要合成
C 6H5
可以用
C 6H 5
/\
+ C 6H 5
Br -------- 扌
C 6H
5
+ H^O ———- C — b —
OH H
N6 NHa
NHa N 2OSO 3H
但在丙酮的一个甲基上导入一个致活基团,使两个甲基上的氢的活性有显著差别,这可用一个乙酯基(-COOC5 )导入丙酮的一个甲基上,则这个甲基的氢有较大的活性,使这个碳成为苄基溴进攻的部位,因此,利用乙酰乙酸乙酯而不用丙酮,完成任务后,把乙酯基水解成羧基,利用1 -酮酸易于脱羧的特性将导向基去掉,于是得出合成路线为:
2、致钝导向
活化可以导向,有时致钝也能导向,如合成N「
_Br
氨基是很强的邻、对位定位基,进行取代反应时容易生成多元取代物:
冒 2 NH2
「+ Br2 —Br_" Br
T
Br
如只在苯胺环上的氨基的对位引入一个溴,必须将氨基的活性降低,这可通过乙酰化反应来达到,同时乙酰氨基是一个邻、对位定位基,而此情况下对位产物是主要产物:
3、利用封闭特定位置来导向
例如合成“
NO,用苯胺为起始原料,用混酸硝化,一方面苯胺易被
?
硝酸氧化,另-NH3SO4H
硝化时得到
NHCOCH 3
6
Br 2〉
NHCOCH 3
6
I
Br
一方面,苯胺与硫酸还会生成硫酸盐,而是一个间位定位基,
2欢迎下载
Br
,所以苯胺硝化时,要把苯胺乙酰化后,再硝化
微量
NHCOCH 3 一
d
NO 2
3
欢迎下载
(90%)
NHCOCH 3 [^J^NO 2
NO 2
(主要)
微量
由于乙酰基此时主要是对位产物,所以仍不能达到目的。如果导向一个磺酸 基,先把氨基的对位封闭,再硝化,可以得到满意结果:
SO 3H
SO 3H
2
NHCOCH 3
I
「-NO 2
精品文档
欢迎您的下载,
资料仅供参考!
致力为企业和个人提供合同协议,策划案计划书,学习资料等等
打造全网一站式需求
