中考化学实验探究题

【实验探究题】
1、控制变量,设计对比实验是实验探究的重要方法。
实验编号一、探究人体呼出气体中二
氧化碳含量比空气中的高
二、探究影响品红扩散快慢
的因素
三、铁钉锈蚀条件的探究
实验设计
实验
分析
本实验条件除了要控
制两个盛装气体样品的集
气瓶大小规格相同外,还要
控制__________________
相同。
发现两杯水都变红,且
整杯热水变红时间比冷水
要短。由此说明:①分子在
不断运动;②影响分子运动
快慢的因素有
______________________。
一周后,左边试管中铁
钉生锈,右边试管中铁钉无
明显变化。上述实验
___________
(填“能”或“不能”)得出
铁钉生锈的条件。
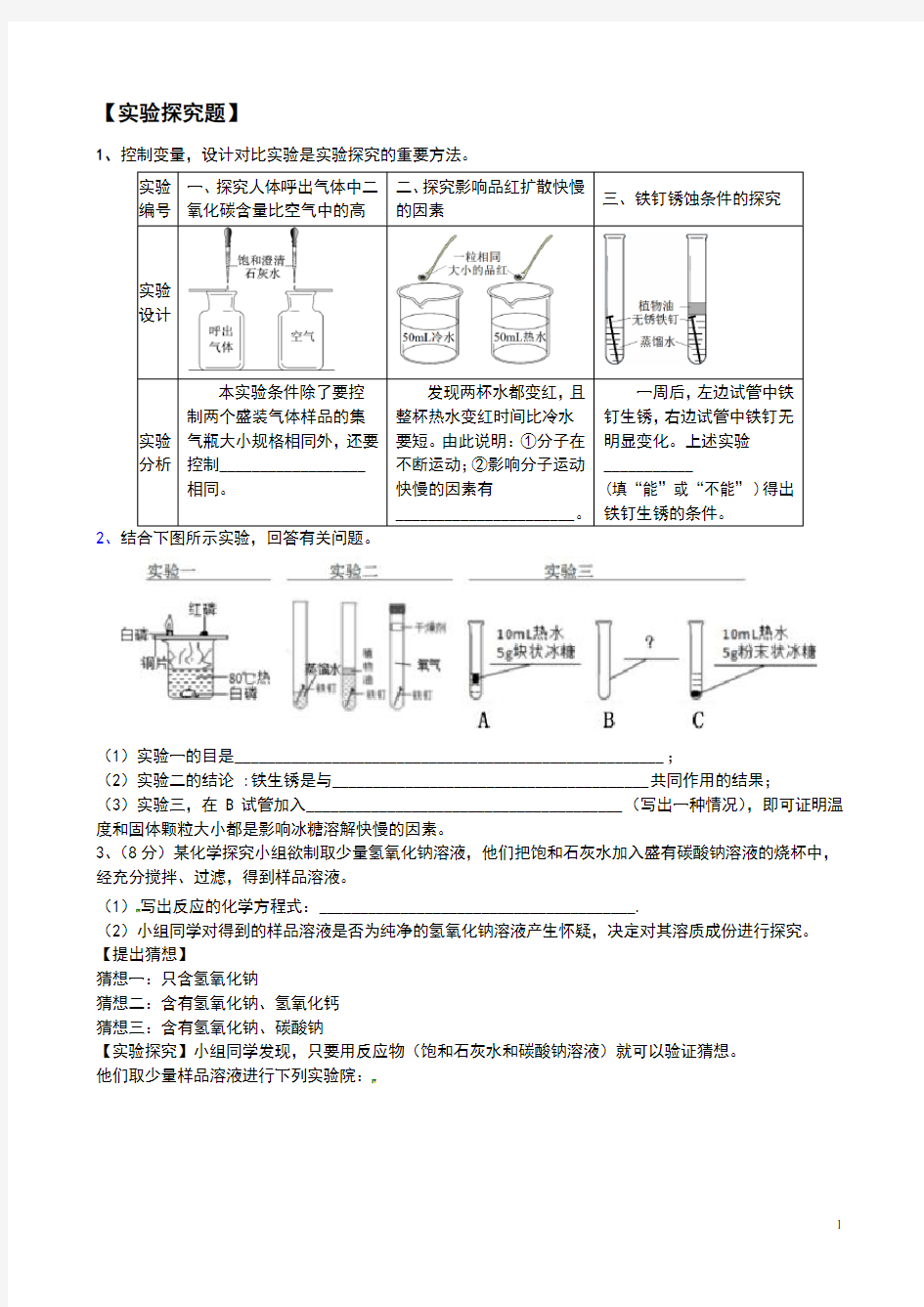
2、结合下图所示实验,回答有关问题。
(1)实验一的目是_____________________________________________________;
(2)实验二的结论 :铁生锈是与_______________________________________共同作用的结果;
(3)实验三,在 B试管加入_______________________________________(写出一种情况),即可证明温度和固体颗粒大小都是影响冰糖溶解快慢的因素。
3、(8分)某化学探究小组欲制取少量氢氧化钠溶液,他们把饱和石灰水加入盛有碳酸钠溶液的烧杯中,经充分搅拌、过滤,得到样品溶液。
(1)写出反应的化学方程式:_______________________________________.
(2)小组同学对得到的样品溶液是否为纯净的氢氧化钠溶液产生怀疑,决定对其溶质成份进行探究。【提出猜想】
猜想一:只含氢氧化钠
猜想二:含有氢氧化钠、氢氧化钙
猜想三:含有氢氧化钠、碳酸钠
【实验探究】小组同学发现,只要用反应物(饱和石灰水和碳酸钠溶液)就可以验证猜想。
他们取少量样品溶液进行下列实验院:
【交流讨论】甲同学认为要验证猜想二不正确,也可往样品溶液入___________;
受该同学的启发,小组同学认为要验证猜想三正确,也可在样品溶液中滴加盐酸。
【实验评价】乙同学往样品溶液中滴入盐酸,刚开始并没有观察到明显现象,试分析原因
_______________________________________________________________。
4、(8分)某化学兴趣小组围绕“酸和碱的反应”,做了如下图所示的两个实验。
(1)实验一:向CuSO4溶液中滴入NaOH溶液,观察到的现象为 ________________ ,该反应的化学方程式为_______________________________________,继续滴加稀盐酸,通过稀盐酸与___________反应的现象,证明了酸和碱能发生反应。
(2)实验二:向NaOH溶液中滴入几滴酚酞溶液,振荡,继续加入稀盐酸,观察到溶液由________色变为无色,由此现象也证明了酸和碱能发生反应。
实验结束后,小组同学对实验二中试管的无色溶液成分展开了讨论。
【提出问题】试管中无色溶液的溶质除酚酞外还有什么?
【猜想假设】猜想一:NaCl和HCl
猜想二:
【实验设计】若要证明猜想一成立,下列试剂中不能达到实验目的的是_________________。
A.紫色石蕊溶液 B.Cu C.AgNO3 D.Na2CO3
【讨论交流】小莹同学认为滴入NaOH溶液,也能证明猜想一成立,你认为小莹同学的方案是否可行并说明理由________________________________________________________________。
5、某化学兴趣小组的同学在实验室发现以前用的一瓶氢氧化钠溶液忘记了盖瓶塞,他们取这种氢氧化钠溶液少量于试管中,再逐滴加入稀盐酸,观察到有气泡产生。小组中有同学断定,这瓶氢氧化钠溶液已经变质。辅导老师肯定了该同学的看法,又有同学提出:所用氢氧化钠溶液是否完全变质?兴趣小组的同学在辅导老师的鼓励下又进行了如下的实验探究:
【提出问题】氢氧化钠溶液是否完全变质?
【进行猜想】(1)该氢氧化钠溶液部分变质;(2)该氢氧化钠溶液全部变质。
【查阅资料】氯化钡溶液呈中性。
说明原溶液中一定有碳酸钠
【结论】该小组同学所用的氢氧化钠溶液是(填“部分”或者“全部”
【反思】氢氧化钠溶液露置于空气中容易变质,反应的化学方程式为:。
6、实验室有一瓶长期放置的氢氧化钠固体,某兴趣小组同学欲对该固体变质情况进行探究。
Ⅰ固体的成分分析
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO3;
②CaCl2溶液的pH=7,碳酸钠溶液的pH ?7
③CaCl2+Na2CO3=CaCO3↓+2NaCl Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
④碱石灰是CaO和NaOH的混合物
【提出猜想】猜想Ⅰ:固体未变质猜想Ⅱ:固体全部变质猜想Ⅲ:固体部分变质
【原因分析】氢氧化钠在空气中变质的原因是______________________________________(用化学方程式表示)。
【进行实验】小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是______________________________,为了进一步得出结论,组其他三位同学分别取小聪实验后的溶液于试管中,进行如下表所示实验。
【实验结论】小红、小美的实验中都观察到有白色沉淀生成且溶液仍是红色,于是他们都得出猜想Ⅲ正确。【反思评价】(一)老师指出,仅凭小红的实验操作和现象无法确定猜想Ⅲ正确,理由是___________________________________________________________________。
(二)根据小美的结论推测小伍实验现象是_________________________________________。
Ⅱ固体中各成分含量
【提出问题】如何测定变质的氢氧化钠固体中碳酸钠的质量分数?
【进行实验】化学小组同学设计了如下实验装置。
①小明同学认为通过测定装置 I中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组同学通过讨论认为不可以,其理由可能是__________________________________________;
②小刚同学在大家讨论的基础上,设计了装置II。请分析:装置II中A的作用_________________________;若无装置C,对测定结果造成的影响是_________________(填“偏大”、“偏小”或“无影响”);
【实验结论】称取10g样品于圆底烧瓶中,实验结束后,测得装置D增重2.2g,请你计算出样品中Na2CO3质量分数。(写出计算过程)
【反思评价】①联想到空气中有CO2,所以实验室中的氢氧化钠应__________________保存。
②若将上述5g氢氧化钠固体全部溶解在45g水中,得到的溶液中氢氧化钠质量分数
___________________10%(填“大于”、“小于”或“等于”)。
7.某不纯的碳酸钠固体样品,含有的杂质可能是硫酸钠、硫酸铜、氯化钠、氯化钙中的一种或几种。为确定其杂质的成分,进行如下实验探究。请你参与探究,并填写空格:
【实验、记录与分析】
8、甲和乙两位同学在实验室中进行化学实验.甲将CO2通入澄清的石灰水中;乙向盛有少量NaOH溶液的试管中滴入几滴酚酞溶液,再倒入一定量的稀盐酸.
小冉小海
(1)小冉同学观察到的现象______,该反应的化学方程式为_________________________________;(2)小海同学实验后发现试管溶液为无色,认为氢氧化钠和盐酸恰好完全反应.你认为他的观点是否正确______ (填“是”或“否”),你的理由是:____________________________________________;(3)实验结束后,两名同学将反应后的剩余物同时倒入废液缸中,发现有气泡产生,废液仍然为无色.请你和两名同学一起对废液缸中废液的组成进行探究.
【提出问豫】废液中的溶质除指示剂外,还有什么?
【进行猜想】①两位同学一致认为溶质为CaCl2和NaCl:
②你认为溶质的组成还可能为_____________.
【实验验证】向废液中加入_____________________,出现_________现象.
【实验结论】说明猜想______ (填①或②)正确.
【实验反思】为减少废液对环境的污染,可采取的方法是___________________.
【拓展延伸】通过酚酞溶液由红色变无色,说明NaOH已与盐酸完全反应,你认为还可以向反应后的溶液中加入___________ (不使用紫色石蕊试液和pH试纸)来证明NaOH确已完全反应.
