GCP资料-药物临床试验英文词汇及缩写
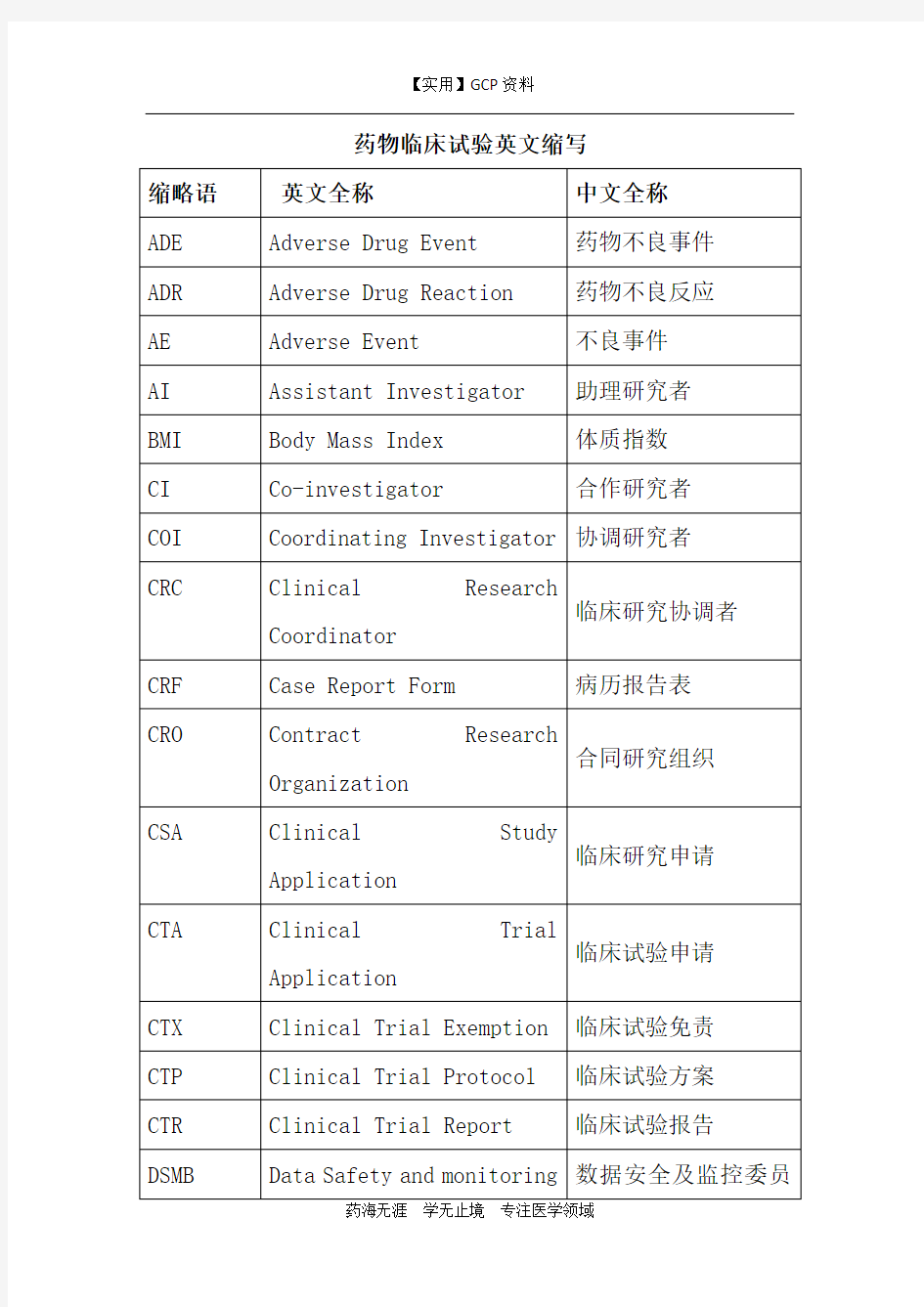
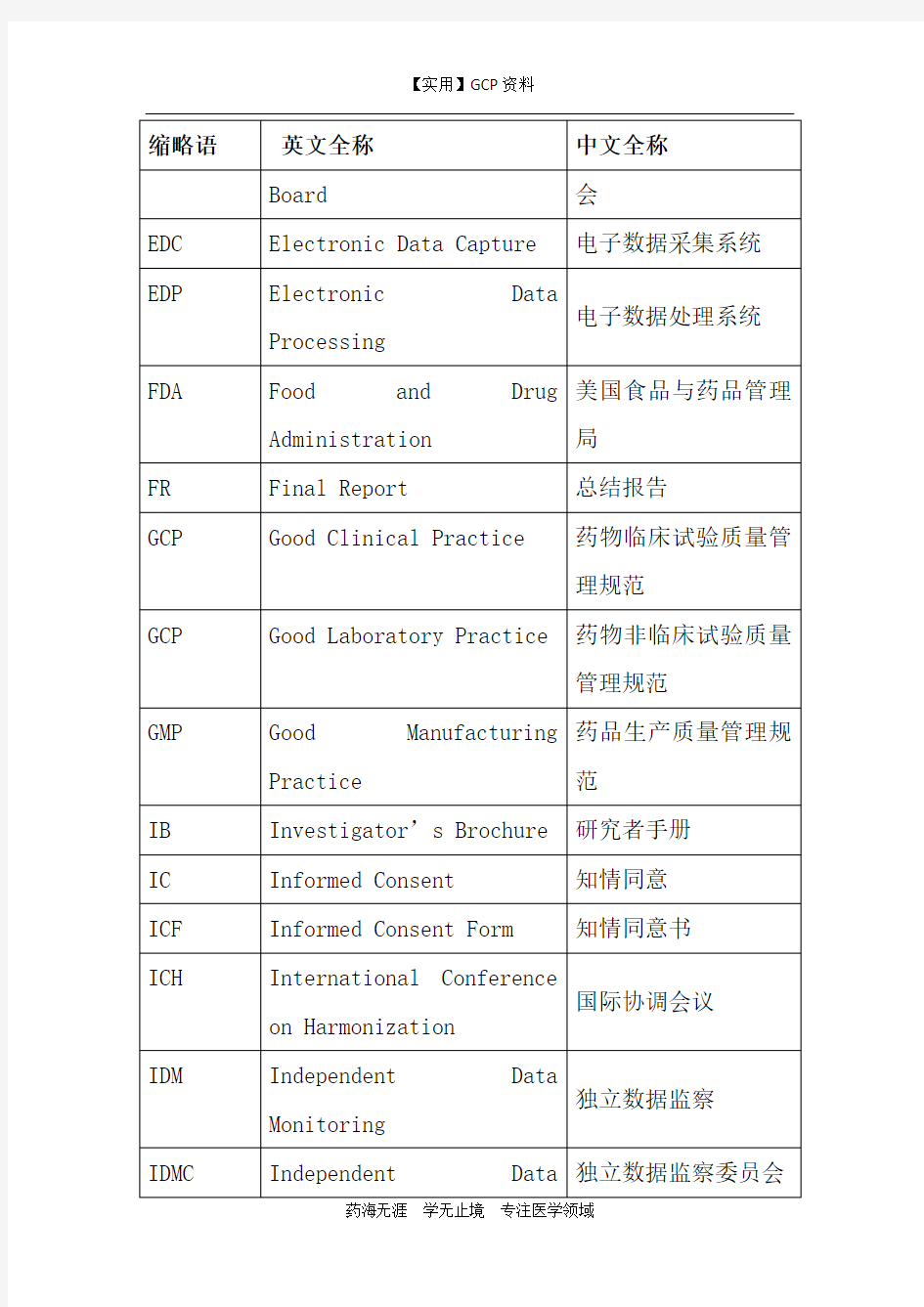
药物临床试验英文缩写
药物临床试验英文缩写
湖北省药物临床评价高峰论坛暨GCP理论教(学)案实践培训班_最终版
湖北省药物临床评价高峰论坛暨GCP理论与实践培训班答题卡 一、单项选择题 二、多项选择题 三、名词解释 1. 2.
3. 4. 四、问答题
湖北省药物临床评价高峰论坛暨GCP理论与实践培训班考题 一、单项选择(共15题,每题2分,合计30分) 1.《药物临床试验质量管理规范》的目的是什么?() A、保证药物临床的过程规范,结果科学可靠,保护受试者的权益及保障其安全 B、保证药物临床试验在科学上具有先进性 C、保证临床试验对受试者无风险 D、保证药物临床试验的过程按计划完成 2.2013年9月6日,国家食品药品监督管理总局通过其官网发布了2013年第28号公告: “关于药物临床试验信息平台的公告”,强制要求凡获国家食品药品监督管理总局临床试验批件并在我国进行临床试验(含生物等效性试验、PK试验、I、Ⅱ、Ⅲ、Ⅳ期试验等)的,均应在该平台进行登记与信息公示。登记药物临床试验信息并对公众公示的目的不包括:() A、保障公众知情权 B、调动公众主动性以及发挥其社会监督作用 C、促进试验质量和效率的提高、促进信息共享、避免资源浪费以及充分整合珍贵的 试验证据 D、促进我国临床试验信息化管理发展 3.有关临床试验方案,下列哪项规定不需要?() A、对试验用药做出规定 B、对疗效评价做出规定 C、对试验结果做出规定 D、对中止或撤除临床试验做出规定 4.关于知情同意书内容的要求,下列哪项不正确?() A、须写明试验目的 B、须使用受试者能理解的语言 C、不必告知受试者可能被分配到试验的不同组别 D、须写明可能的风险和受益 5.关于试验药物的储存,哪一项描述是错误的?() A、及时登记试验药物的出入库记录 B、定期检查药物的库存和药物保质期 C、及时向申办方反应任何在药物存储中出现的问题,如温度超标 D、发现有问题的药物须立即销毁,避免误发给受试者
临床试验常用的英文缩写
专业术语 缩略语英文全称中文全称 DCF data clarification form 数据澄清表,用于纸质query SDV source data verification 原始数据核对 ADE Adverse Drug Event药物不良事件 ADR Adverse Drug Reaction药物不良反应 AE Adverse Event不良事件 AI Assistant Investigator助理研究者 ? BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRAClinical Research Associate 临床监查员(临床监察员)CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表
CRO Contract Research Organization 合同研究组织CSAClinical Study Application 临床研究申请 CTAClinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMBData Safety and monitoring Board数据安全及监控委员会EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCPGood Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规范GMPGood Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on Harmonization国际协调会议
药物临床评价与gcp
1、药物临床评价:是指所有在人体进行的有关药物的任何系统性研究,是证实或揭示药物 作用,不良反应及药物在人体内的吸收、分布、代谢和排泄的过程,目的是确定药物的经济性、有效性与安全性及合理用药方案 2、药物临床评价的主要内容:药物体内过程评价、药物临床有效安全性评价、药物临床给 药方案评价、药物上市后在评价、药物利用评价、药物经济性评价。 3、药物上市后在评价:研究药物根据医药学的最新学术水平,从药理学、药剂学、临床药 学、药物流行病学、药物经济学、药物决策等方面,对已批准上市的药物在社会人群中的疗效、不良反应、用药方案稳定性及费用是否符合安全、有效、经济合理用药的原则作出科学评价。 4、临床药物评价的主要任务:研究药物与人体的相互作用、为起草临床使用说明书提供人 体试验依据、为政府医疗决策提供依据。 5、流行病学 ①定义:流行病学是研究人群中疾病与健康状况的分布及影响因素,并研究防治疾病及 促进健康的策略和措施的科学。 ②临床流行病学:应用流行病学的原理和方法,通过对疾病的诊断、治疗、愈后和病因 的研究,为临床决策提供科学依据的学科。临床流行病学常应用于临床诊断、疗效评价、愈后研究、研究疾病自然史、临床决策分析等领域。 ③《临床流行病学》: 临床医务人员是临床流行病学的主要实践者、研究对象的患者群体、内容是各种临床问题、研究主线是设计、测量与评价 6、循证医学 ①定义:整合最佳临床证据、临床经验和患者价值观的一门学科。 ②核心思想:医疗决策(即病人的处理、治疗指南个医疗政策的制定等)应在现有的最 好的临床研究依据基础上作出,同时也重视结合医生个人的临床经验以及患者的实际状况和意愿。 ③研究方法:有证查证用证、无证创证用证 7、病例对照研究:将具有某一特征或患有某一疾病的人群做为病例组,以不具有这一特征或不患有这一疾病且与病例组人群具有可比性(除了这一特征或疾病以外,其他因素基本一致)的人群做为对照组,收集这两组人群既往可能与这一特征或疾病有关的暴露史,通过两组间暴露因素的统计学分析结合专业解释,从而判断这些暴露因素与研究特征或疾病之间的关系。 8、涉及到的基本法规: 人体实验法规《细伦堡法案》 伦理的法规:《赫尔辛基宣言》 法律:《药品管理法》 行政法规:《品管理法实施条例》,《药品种保护条例》 规范性文件:药品进口药材管理办法、药品标签和说明书管理规定、药物非临床研究质量管理规范 9、药品临床定位方法:选择优势病种、阶段→现代科学技术方法→文献→药理→临床(三联分析法) 临床定位的重要性:有利于中药疗效充分发挥 中药特点的真实体现 有利于创新药物的产生 有利于政策的制定与企业的发展
完整word版,临床试验常见英文缩写
临床试验常见英文缩写 ADR(Adverse drug reaction)不良反应 AE(Adverse event)不良事件 SAE(Serious Adverse Event)严重不良事件 CRF(Case report form/case record form)病例报告表 CRO(Contract research organization)合同研究组织 EC(Ethics Committee)伦理委员会 GCP(Good clinical practice)药品临床试验管理规范 EDC(Electronic data capture)电子数据采集 IB(Investigator's Brochure)研究者手册 ND (Not Done) 未做 NA (Not Applicable) 不适用 UK (Unknown) 未知 PI(Principal investigator )主要研究者 Sub-I(Sub-investigator) 助理研究者 QA(Quality assurance) 质量保证 QC(Quality control) 质量控制 SDV(Source data verification)原始资料核对 SD(Source data)原始数据 SD(Source document ) 原始文件 SFDA 国家食品药品监督管理局 SOP(Standard operating procedure) 标准操作规程 IRB 机构审查委员会 ICF(Informed Consent Form) 知情同意书 TMF(trial master file)研究管理文件夹 临床试验常见英文单词 A ?Active control ,AC 阳性对照,活性对照阳性对照,活性对照?Adverse drug reaction ,ADR 药物不良反应药物不良反应?Adverse event ,AE 不良事件 ?Approval 批准 ?Assistant investigator 助理研究者 ?Audit 稽查 ?Audit report 稽查报告 ?Auditor 稽查员 B ?Bias 偏性,偏倚 ?Blank control 空白对照 ?Blinding/masking 盲法,设盲 ?Block 层 C ?Case history 病历 ?Case report form/case record form ,CRF 病例报告表,病例记录表?Clinical study 临床研究
药物临床试验英文缩写汇编
药物临床试验英文缩写汇编
药物临床试验英文缩写号 1 ADE 药物不良事件Adverse Drug Event 2 ADR 药物不良反应Adverse Drug Reaction 3 AE 不良事件Adverse Event 4 AI 助理研究者Assistant Investigator 5 BMI 体质指数Body Mass Index 6 CI 合作研究者Co-investigato r 7 COI 协调研究者Coordinating Investigator
Research Organization 11 CSA 临床研究申请Clinical Study Application 12 CTA 临床试验申请Clinical Trial Application 13 CTX 临床试验免责Clinical Trial Exemption 14 CTP 临床试验方案Clinical Trial Protocol 15 CTR 临床试验报告Clinical Trial Report 16 DSM 数据安全及监控 Data Safety and
18 EDP 电子数据处理系 统Electronic Data Processing 19 FDA 美国食品与药品 管理局Food and Drug Administration 20 FR 总结报告Final Report 21 GCP药物临床试验质 量管理规范Good Clinical Practice 22 GLP 药物非临床试验 质量管理规范Good Laboratory Practice 23 GMP 药品生产质量管 理规范Good Manufacturing Practice
药物临床试验与GCP_二_
[讲座] 药物临床试验与GCP(二) 徐国柱 (北京大学中国药物依赖性研究所,北京,100083) (续2001年第4期) 5多中心临床试验 多中心临床试验是指由多个研究者按照统一的试验方案在不同的地点、不同的单位同时进行的临床试验。各个中心同期开始、同期结束。多中心试验由一位或几位主要研究者负责,负责单位称组长单位或牵头单位。组长单位的责任很重,要通过各种管理措施保证试验按照统一的方案进行、监控质量、掌握和协调试验进度、进行数据统计、新药审评时负责答辩等。一个好的多中心试验应具备下列条件。 5.1组长单位必须是临床研究基地,牵头人应该在本专业领域有一定的威望,有丰富的临床试验经验,能够熟练处理和解决临床试验过程中出现的各种复杂问题,很好地控制质量,有较好的组织协调能力。熟悉国家对新药临床试验有关法规的要求,能对临床试验结果进行全面技术负责。在临床试验过程中应完成以下各项任务:与申办单位共同制定或帮助申办单位制定试验方案,临床试验病例报告表,建立标准化评价方法。请各参加单位共同讨论,并征得申办者同意。报请伦理委员会批准。 5.2成立协调委员会并召开协调会议。大规模的多中心试验,比如试验周期较长或参加单位比较多,样本量很大,或操作难度、技术难度比较大的临床试验,需要成立协调委员会,由几个主要参加单位的课题负责人组成,负责对试验当中出现的问题进行集体讨论、决策,研究制定解决办法,然后通知各个试验单位付诸实施。比较小的临床试验,由组长单位全面协调即可,但召开协调会议是必须的。一般情况,在试验开始、中期和结束时分别召开研究者协调会议。试验开始时召开的协作组会议是为了统一认识、统一标准、统一步调、统一行动。中期会是为了及时解决试验当中存在的问题,协调进度。试验结束后的会议是为统一结果,统一结论,总结经验,写好总结报告和小结报告而开。 5.3严格的质量控制。试验进行期间组长单位与监查单位必须经常派人前往各个中心,严格按照临床试验方案的要求进行认真仔细的检查,对每一位受试者的观察表记录的数据与原始记录进行核对,做到准确无误。要求各位研究者必须遵从方案,对违背方案操作的要及时发现及时纠正,如到试验后期或试验结束时才发现这样或那样的问题,将非常棘手,影响整个进度和结果。对违背方案操作又不改正者应终止其参加试验。 5.4建立药物分发、储藏、登记管理制度。制定试验用药发放登记表,不同中心以相同程序管理试验用药。 5.5组长单位在制定和分配临床试验各中心的样本量时必须符合统计学要求,对照试验设计应不低于30对,给各中心分配病例数时要考虑分段随机因素。按我国新药审批办法的规定,每个中心完成的病例数至少不低于20例。数据资料由组长单位或另请数据统计部门集中管理与统计分析,建立数据传递与查询程序。 多中心临床试验组长单位的责任固然重要,但参加单位的水平、责任心、通力合作与紧密配合的协作精神非常关键。因此选择好的合作伙伴是完成好多中心试验的前提。 6对试验操作步骤的要求 临床试验具体操作者是临床医生,他们每日承担大量的门诊或病房工作,教学医院需要带实习学生,承担讲课任务,有的医生还承担科研课题或研究生课题等,工作非常繁忙。临床试验需要检查和观察的内容和项目要比一般性常规治疗复杂而烦琐,为了避免遗漏检查项目和观察记录内容,要制定和使用临床试验流程图,流程图内将试验前、试验期间、试验结束时和随访期间所需要做的工作一一列出,提醒研究者。 7监查 监查是为了在临床试验中使受试者的权益受到保障,保证试验记录与报告的数据准确、完整无误,保证试验遵循已批准的方案、临床试验管理规范和有关法规。 7.1监查员的条件 监查员是申办者与研究者之间的主要联系人。一项临床试验聘用监查员的人数依试验的复杂程度
临床试验与实验室中常见的中英文名词与缩写
中国创新药咨询与服务先锋CRO 临床试验以及实验室中常见的英文缩写
药物临床试验英文缩写 缩略语英文全称中文全称 ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范GCP Good Laboratory Practice 药物非临床试验质量管理规范GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on Harmonization 国际协调会议 IDM Independent Data Monitoring 独立数据监察 IDMC Independent Data Monitoring Committee 独立数据监察委员会 IEC Independent Ethics Committee 独立伦理委员会 IND Investigational New Drug 新药临床研究 IRB Institutional Review Board 机构审查委员会 IVD In Vitro Diagnostic 体外诊断 IVRS Interactive Voice Response System 互动语音应答系统 MA Marketing A pproval/Authorization 上市许可证 MCA Medicines Control Agency 英国药品监督局 MHW Ministry of Health and Welfare 日本卫生福利部 NDA New Drug Application 新药申请 NEC New Drug Entity 新化学实体 NIH National Institutes of Health 国家卫生研究所(美国)
临床试验GCP
第九章 一、数据管理的目的是什么? 答:把试验数据迅速、完整、无误的纳入报告,所有涉及数据管理的各种步骤均需记录在案,以便对数据质量及试验实施进行检查。 二、什么叫盲态审核? 答:盲态审核(blind review)是指在最后一份病例报告表输入数据库后,第一次揭盲之前对数据保持盲态的预分析审核,以便对统计分析计划作最后的决定。 三、什么叫质疑表?由谁传送?能不能通过电话传达质疑表的内容? 答:质疑表( query list,query form)是数据管理员再次检查病例报告表发现任何问题后,及时通知检查员,要求研究者作出回答的文件。检查员、研究者、数据管理员之间的各种疑问及解答的交换都由质疑表完成。质疑表应保存备查。质疑表必须由检查员亲自传送给研究者,不能通过电话传达。 四、什么叫结果锁定? 答:结果锁定指在盲态审核认为所建立的数据库正确无误后,由主要研究者、药物注册申请人、生物统计学专业人员和保存盲底的有关人员对数据库进行锁定。此后,对数据库的任何改动只有在以上几方人员同意(可书面形式)的情况下才能进行。 五、临床试验统计分析中常用那两种分析方法? 答:1.PP分析(合格病例分析)对完成治疗方案,且依从性好的病例分析。 2.ITT分析(意向性分析)对所有的病例进行分析,包括合格、脱落,出现不良反应的病例的分析。 六、什么是ITT?什么是FAS? 答:ITT是Intention-To=Treat的缩写,即意向性。指所有经随机化分组,分配了随机号的全部病例,也称为愿意治疗人群。意向性分析时其中未能观察到全部治疗过程的病例资料,用最后一次观察数据接转到试验最终结果,对疗效和不良事件发生二进行意向性分析。ITT 的误差较大。 FAS是全分析集(Full Analysis Set)指尽可能接近符合ITT原则的理想的受试者人群。它应包括几乎所有的随机化后的受试者。只有在导入期中被排除而未入组或者入组后没有任何的随访数据才能从FAS人群中排除。即只要服用了一次药,做了一次有效检测的受试者都应入FAS。 七、什么是PP? 答:PP是Pet-Protocol的缩写,即符合方案集。指所有符合试验方案、依从性好(如接受治疗、主要指标可以测定等)、试验期间未服禁止用药、完成CRF规定填写内容的病例,对其疗效统计分析。 八、ITT和PP有何关系? 答:在确证性试验中,对药物的有效性评价时,宜同时用ITT和PP进行统计分析。当以上两种数据集的分析结论一致时,可以
常用临床试验缩写
临床监查员专业术语、缩略语中英对照表 缩略语英文全称中文全称 ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRA Clinical Research Associate 临床监查员(临床监察员)CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范GLP Good Laboratory Practice 药物非临床试验质量管理规范GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on Harmonization 国际协调会议 IDM Independent Data Monitoring 独立数据监察 IDMC Independent Data Monitoring Committee 独立数据监察委员会IEC Independent Ethics Committee 独立伦理委员会 IND Investigational New Drug 新药临床研究 IRB Institutional Review Board 机构审查委员会 IVD In Vitro Diagnostic 体外诊断 IVRS Interactive Voice Response System 互动语音应答系统
临床试验常用的英文缩写
专业术语 缩略语 英文全称 中文全称 数据澄清表,用于纸质 query 原始数据核对 DCF SDV data clarification form source data verification ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRA Clinical Research Associate 临床监查员(临床监察员) CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规范 GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator's Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on Harmonization 国际协调会议
药物临床试验英文缩写
药物临床试验英文缩写 缩略语英文全称中文全称 ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范GCP Good Laboratory Practice 药物非临床试验质量管理规范GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on 国际协调会议 Harmonization IDM Independent Data Monitoring 独立数据监察 IDMC Independent Data Monitoring Committee 独立数据监察委员会 IEC Independent Ethics Committee 独立伦理委员会 IND Investigational New Drug 新药临床研究 IRB Institutional Review Board 机构审查委员会 IVD In Vitro Diagnostic 体外诊断 IVRS Interactive Voice Response System 互动语音应答系统 MA Marketing Approval/Authorization 上市许可证 MCA Medicines Control Agency 英国药品监督局 MHW Ministry of Health and Welfare 日本卫生福利部 NDA New Drug Application 新药申请 NEC New Drug Entity 新化学实体
临床试验常用术语缩写
专业术语 CRA Clinical Research Associate 临床监查员(临床监察员) CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 ECRF 电子化病历报告表 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规 GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator's Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ECG Electrocardiogram 心电图 ICH International Conference on Harmonization 国际协调会 IDM Independent Data Monitoring 独立数据监察 IDMC Independent Data Monitoring Committee 独立数据监察委员会 IEC Independent Ethics Committee 独立伦理委员会 IND Investigational New Drug 新药临床研究 IRB Institutional Review Board 机构审查委员会 IVD In Vitro Diagnostic 体外诊断 MA Marketing Approval/Authorization 上市许可证 IVRS Interactive Voice Response System 互动语音应答系统 MCA Medicines Control Agency 英国药品监督局 MHW Ministry of Health and Welfare 日本卫生福利部 NDA New Drug Application 新药申请 NEC New Drug Entity 新化学实体 NIH National Institutes of Health 国家卫生研究所(美国) PI Principal Investigator 主要研究者 PL Product License 产品许可证 PMA Pre-market Approval (Application ) 上市前许可(申请) PSI Statisticians in the Pharmaceutical Industry 制药业统计学家协会 QA Quality Assurance 质量保证 QC Quality Control 质量控制 RA Regulatory Authorities 监督管理部门 SA Site Assessment 现场评估 SAE Serious Adverse Event 严重不良事件 SAP Statistical Analysis Plan 统计分析计划 SAR Serious Adverse Reaction 严重不良反应 SD Source Data/Document 原始数据 /文件 SD Subject Diary 受试者日记 Subject identification code (SIC )受试者识别代码 SFDA State Food and Drug Administration 国家食品药品监督管理局 SDV Source Data Verification 原始数据核准 SEL Subject Enrollment Log 受试者入选表 SI Sub-investigator 助理研究者 SI Sponsor-Investigator 申办研究者 SIC Subject Identification Code 受试者识别代码 pd pharmacodynamics 药物效应动力学 SOP Standard 缩略语 英文全称 中文全称 ADE Adverse Drug Event 药物不良事件 AE Adverse Event 不良事件 BMI Body Mass Index 体质指数 COI Coordinating Investigator 协调研究者 ADR Adverse Drug Reaction 药物不良反应 AI Assistant Investigator 助理研究者 CI Co-investigator 合作研究者
药物临床试验GCP试题精编WORD版
药物临床试验G C P试 题精编W O R D版 IBM system office room 【A0816H-A0912AAAHH-GX8Q8-GNTHHJ8】
药物临床试验GCP培训考核试题 第一部分单选题(每题2分) 1 保障受试者权益的主要措施是:C A有充分的临床试验依据 B试验用药品的正确使用方法 C伦理委员会和知情同意书 D保护受试者身体状况良好 2 下列哪一类人员不必熟悉和严格遵守《赫尔辛基宣言》?D A临床试验研究者 B临床试验药品管理者 C临床试验实验室人员 D非临床试验人员 3 下列哪一项不是伦理委员会的组成要求?D A至少有一人为医学工作者 B至少有5人参加 C至少有一人应从事非医学专业 D至少有一人来自药政管理部门4 伦理委员会的工作应:D A接受申办者意见 B接受研究者意见 C接受参试者意见 D是独立的,不受任何参与试验者的影响 5 经过下列哪项程序,临床试验方可实施?D A向伦理委员会递交申请 B已在伦理委员会备案 C试验方案已经伦理委员会口头同意 D试验方案已经伦理委员会同意并签发了赞同意见
6 伦理委员会做出决定的方式是:C A审阅讨论作出决定 B传阅文件作出决定 C讨论后以投票方式作出决定 D讨论后由伦理委员会主席作出决定7 在伦理委员会讨论会上,下列什么人能够参加投票?A A参加会议的伦理委员会委员 B非医学专业委员 C非委员的专家 D非委员的稽查人员 8 伦理委员会书面签发其意见时,不需附带下列哪一项?C A出席会议的委员名单 B出席会议的委员的专业情况 C出席会议委员的研究项目 D出席会议委员的签名 9 伦理委员会从下列哪个角度审阅试验方案?A A保护受试者权益 B研究的严谨性 C主题的先进性 D疾病的危害性 10 下列哪项不是知情同意书必需的内容?C A试验目的 B试验可能的受益和可能发生的危险 C研究者的专业资格和经验 D说明可能被分配到不同组别 11 下列哪项不是受试者的权利?C A自愿参加临床试验 B自愿退出临床试验 C选择进入哪一个组别 D有充分的时间考虑参加试验 12 受试者在任何阶段有权退出试验,但退出后无权要求下列哪一项?D
临床试验常用的英文缩写
专业术语 缩略语英文全称中文全称ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRA Clinical Research Associate 临床监查员(临床监察员) CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案CTR Clinical Trial Report 临床试验报告DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规范GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书
(完整版)药物临床试验GCP试题2
药物临床试验GCP培训考核试题 第一部分单选题(每题2分) 1 保障受试者权益的主要措施是:C A有充分的临床试验依据B试验用药品的正确使用方法 C伦理委员会和知情同意书D保护受试者身体状况良好 2 下列哪一类人员不必熟悉和严格遵守《赫尔辛基宣言》?D A临床试验研究者B临床试验药品管理者 C临床试验实验室人员D非临床试验人员 3 下列哪一项不是伦理委员会的组成要求?D A至少有一人为医学工作者B至少有5人参加 C至少有一人应从事非医学专业D至少有一人来自药政管理部门 4 伦理委员会的工作应:D A接受申办者意见B接受研究者意见 C接受参试者意见D是独立的,不受任何参与试验者的影响 5 经过下列哪项程序,临床试验方可实施?D A向伦理委员会递交申请 B已在伦理委员会备案 C试验方案已经伦理委员会口头同意 D试验方案已经伦理委员会同意并签发了赞同意见 6 伦理委员会做出决定的方式是:C A审阅讨论作出决定B传阅文件作出决定 C讨论后以投票方式作出决定D讨论后由伦理委员会主席作出决定 7 在伦理委员会讨论会上,下列什么人能够参加投票?A A参加会议的伦理委员会委员B非医学专业委员 C非委员的专家D非委员的稽查人员 8 伦理委员会书面签发其意见时,不需附带下列哪一项?C A出席会议的委员名单B出席会议的委员的专业情况 C出席会议委员的研究项目D出席会议委员的签名 9 伦理委员会从下列哪个角度审阅试验方案?A A保护受试者权益B研究的严谨性 C主题的先进性D疾病的危害性 10 下列哪项不是知情同意书必需的内容?C A试验目的B试验可能的受益和可能发生的危险 C研究者的专业资格和经验D说明可能被分配到不同组别 11 下列哪项不是受试者的权利?C A自愿参加临床试验B自愿退出临床试验 C选择进入哪一个组别D有充分的时间考虑参加试验 12 受试者在任何阶段有权退出试验,但退出后无权要求下列哪一项?D A不受到歧视B不受到报复 C不改变医疗待遇D继续使用试验药品 13 关于签署知情同意书,下列哪项不正确?D A 受试者在充分了解全部试验有关情况后同意并签字 B 受试者的合法代表了解全部试验有关情况后同意并签字 C见证人在见证整个知情过程后,受试者或其合法代表口头同意,见证人签字D无行为能力的受试者,必须自愿方可参加试验
临床试验常用的英文缩写
专业术语缩略语?英文全称?????????????????????????中文全称 DCFdataclarificationform数据澄清表,用于纸质query SDVsourcedataverification原始数据核对 ADE AdverseDrugEvent 药物不良事件 ADR AdverseDrugReaction 药物不良反应 AE AdverseEvent 不良事件 AI AssistantInvestigator 助理研究者 BMI BodyMassIndex 体质指数 CI Co-investigator 合作研究者 COI CoordinatingInvestigator 协调研究者 CRA ClinicalResearchAssociate 临床监查员(临床监察员) CRC ClinicalResearchCoordinator 临床研究协调者 CRF CaseReportForm 病历报告表 CRO ContractResearchOrganization 合同研究组织 CSA ClinicalStudyApplication 临床研究申请
CTA ClinicalTrialApplication 临床试验申请 CTX ClinicalTrialExemption 临床试验免责 CTP ClinicalTrialProtocol 临床试验方案 CTR ClinicalTrialReport 临床试验报告 DSMB DataSafetyandmonitoringBoard 数据安全及监控委员会EDC ElectronicDataCapture 电子数据采集系统 EDP ElectronicDataProcessing 电子数据处理系统 FDA FoodandDrugAdministration 美国食品与药品管理局 FR FinalReport 总结报告 GCP GoodClinicalPractice 药物临床试验质量管理规范GLP GoodLaboratoryPractice 药物非临床试验质量管理规范GMP GoodManufacturingPractice 药品生产质量管理规范 IB Investigator’sBroch ure 研究者手册 IC InformedConsent 知情同意 ICF InformedConsentForm 知情同意书 ICH InternationalConferenceonHarmonization 国际协调会议 IDM IndependentDataMonitoring 独立数据监察 IDMC IndependentDataMonitoringCommittee 独立数据监察委员会IEC IndependentEthicsCommittee 独立伦理委员会 IND InvestigationalNewDrug 新药临床研究
