高考化学复习-原电池-部分经典题型整理
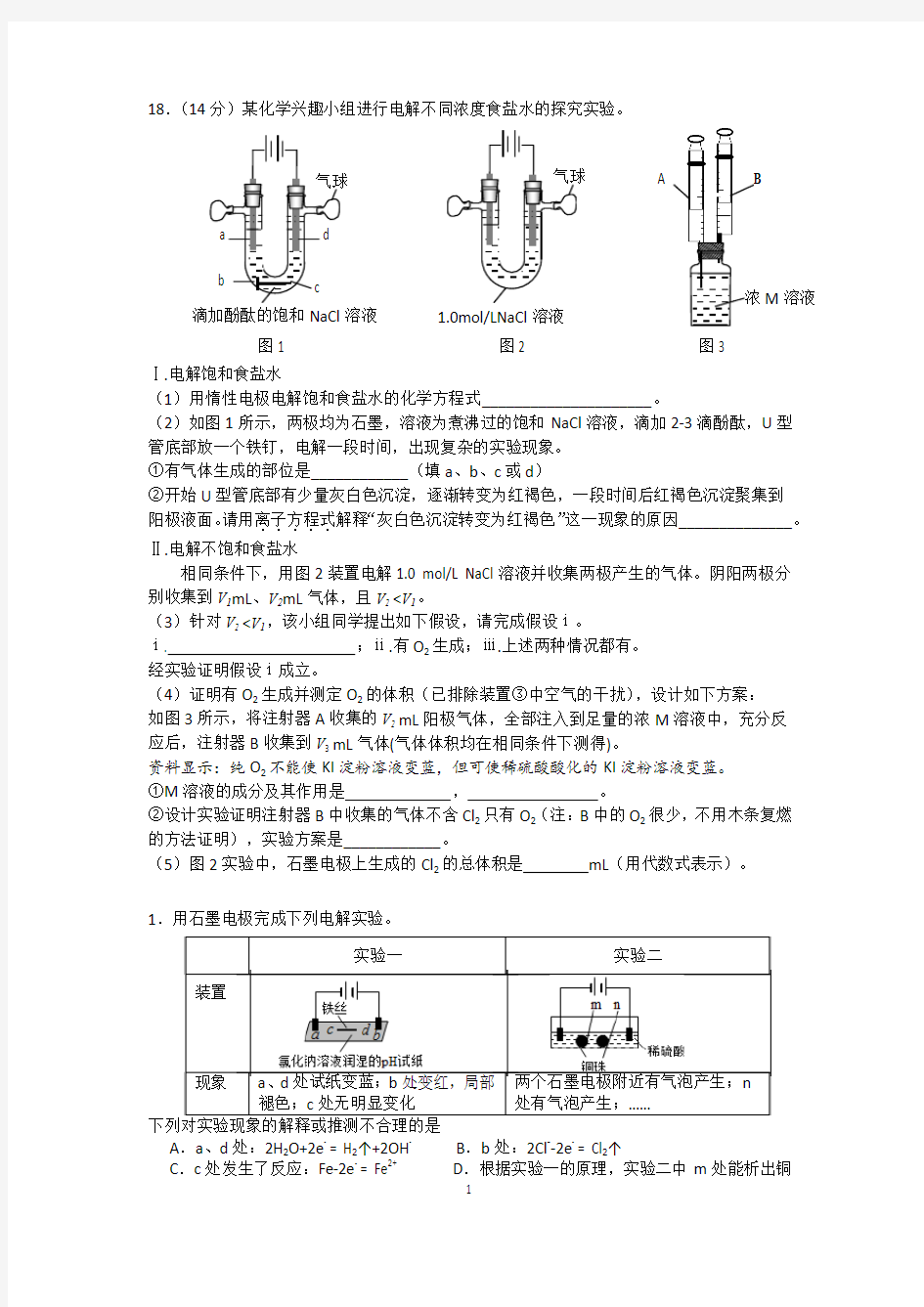

18.(14分)某化学兴趣小组进行电解不同浓度食盐水的探究实验。
Ⅰ.电解饱和食盐水
(1)用惰性电极电解饱和食盐水的化学方程式_____________________。
(2)如图1所示,两极均为石墨,溶液为煮沸过的饱和NaCl 溶液,滴加2-3滴酚酞,U 型管底部放一个铁钉,电解一段时间,出现复杂的实验现象。 ①有气体生成的部位是____________(填a 、b 、c 或d )
②开始U 型管底部有少量灰白色沉淀,逐渐转变为红褐色,一段时间后红褐色沉淀聚集到阳极液面。请用离子方程式.....解释“灰白色沉淀转变为红褐色”这一现象的原因______________。 Ⅱ.电解不饱和食盐水
相同条件下,用图2装置电解1.0 mol/L NaCl 溶液并收集两极产生的气体。阴阳两极分别收集到V 1mL 、V 2mL 气体,且V 2 (3)针对V 2 ⅰ. ;ⅱ.有O 2生成;ⅲ.上述两种情况都有。 经实验证明假设ⅰ成立。 (4)证明有O 2生成并测定O 2的体积(已排除装置③中空气的干扰),设计如下方案: 如图3所示,将注射器A 收集的V 2 mL 阳极气体,全部注入到足量的浓M 溶液中,充分反应后,注射器B 收集到V 3 mL 气体(气体体积均在相同条件下测得)。 资料显示:纯O 2不能使KI 淀粉溶液变蓝,但可使稀硫酸酸化的KI 淀粉溶液变蓝。 ①M 溶液的成分及其作用是 , 。 ②设计实验证明注射器B 中收集的气体不含Cl 2只有O 2(注:B 中的O 2很少,不用木条复燃的方法证明),实验方案是____________。 (5)图2实验中,石墨电极上生成的Cl 2的总体积是 mL (用代数式表示)。 1.用石墨电极完成下列电解实验。 a 、d 处试纸变蓝; b 处变红,局部两个石墨电极附近有气泡产生;n A .a 、d 处:2H 2O+2e - = H 2↑+2OH - B .b 处:2Cl --2e - = Cl 2↑ C .c 处发生了反应:Fe-2e - = Fe 2+ D .根据实验一的原理,实验二中m 处能析出铜 图1 图2 图3 1.0mol/LNaCl 溶液 滴加酚酞的饱和NaCl 溶液 M 溶液 A 19.(12分) 电解一段时间时, 体, 变热,溶液由蓝色变为绿色 (1)甲认为电解过程中阳极产生的是溶液变绿的原因,写出产生该物质的电极反应式:。 (2)乙查阅资料,CuCl2溶液中存在平衡:Cu2+ + 4Cl4]2_(黄色) ΔH>0。 据此乙认为:电解过程中,[CuCl4]2_(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。 乙依据平衡移动原理推测在电解过程中[CuCl4]2_浓度增大的原因:。 溶液,对溶液变色现象继续探究。 电解相同时间时, 蓝色; 色; 丙通过对现象分析证实了甲和乙的观点均不是溶液变绿的主要原因。丙否定甲的依 据是,否定乙的依据是。 (4)丙继续查阅资料: i. 电解CuCl2溶液时可能产生[CuCl2]_,[CuCl2]_掺杂Cu2+后呈黄色 ii. 稀释含[CuCl2]_的溶液生成CuCl白色沉淀 据此丙认为:电解过程中,产生[CuCl2]_掺杂Cu2+后呈黄色,与CuCl2蓝色溶液混合呈绿色。 丙进行如下实验: a.取电解后绿色溶液2 mL,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。 b. 另取少量氯化铜晶体和铜粉,向其中加2 mL浓盐酸,加热获得含[CuCl2]_的黄色溶液。 c. 冷却后向上述溶液…… d. 取c中2 mL溶液,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。 ① a的目的是。 ②写出b中生成[CuCl2]_的离子方程式:。 ③补充c中必要的操作及现象:。 丙据此得出结论:电解时阴极附近生成[CuCl2]_是导致溶液变绿的原因。 17.(20分)乙醇是生活中常见的物质,用途广泛,其合成方法和性质也具有研究价值。 Ⅰ.乙醇可以作为燃料燃烧。 已知化学键的键能是指气态原子间形成1mol 化学键时释放出的能量。应用表中数据(25℃、101 kPa ),写出气态乙醇完全燃烧生成CO 和水蒸气的热化学方程式 。 Ⅱ.直接乙醇燃料电池(DEFC )具有很多优点,引起了人们的研究兴趣。现有以下三种 乙醇燃料电池。 碱性乙醇燃料电池 酸性乙醇燃料电池 熔融盐乙醇燃料电池 (1)三种乙醇燃料电池中正极反应物均为 。 (2)碱性乙醇燃料电池中,电极a 上发生的电极反应式为 ,使用空气 代替氧气,电池工作过程中碱性会不断下降,其原因是 。 (3)酸性乙醇燃料电池中,电极b 上发生的电极反应式为 , 通过质子交换膜的离子是 。 (4)熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,CO 32- 向电极 (填“a ”或“b ”)移动,电极b 上发生的电极反应式为 。 Ⅲ.已知气相直接水合法可以制取乙醇:H 2O(g) + C 2H 4(g) CH 3CH 2OH(g)。当n (H 2O) ︰n (C 2H 4)=1︰1时,乙烯的平衡转化率与温度、压强的关系如下图: (1 ) 图中压强P 1、P 2、P 3、P 4的大小顺序为: ,理由是: 。 (2)气相直接水合法采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290 ℃,压 强6.9MPa ,n (H 2O)︰n (C 2H 4)=0.6︰1。该条件下乙烯的转化率为5℅。若要进一步提高乙烯的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有 、 。 a (Pt) b (Pt) 乙醇 2. 下列说法不合理... 的是 A. 生铁片发生吸氧腐蚀 B. 中心区:Fe – 2e —==== Fe 2+ C. 边缘处:O 2 + 2H 2O +4e —==== 4OH — D. 交界处:4Fe 2+ + O 2 + 10H 2O ==== 4 Fe(OH)3 + 8H + 3.2016年我国科研人员研制出一种室温“可呼吸”Na?CO 2电池。放电时该电池“吸入”CO 2,充电时“呼出”CO 2。吸入CO 2时,其工作原理如右图所示。吸收的全部CO 2中,有2/3转化为Na 2CO 3固体沉积在多壁碳纳米管(MWCNT )电极表面。下列说法正确的是: A .“吸入”CO 2时,钠箔为正极 B .“呼出”CO 2时,Na +向多壁碳纳米管电极移动 C .“吸入”CO 2时的正极反应:4Na + + 3CO 2 + 4e —==== 2Na 2CO 3 + C D .标准状况下,每“呼出”22.4 L CO 2,转移电子数为0.75 mol 1. B 2. D 3. C 17.(21分)Ⅰ.C 2H 5OH(g) +3O 2(g)2CO 2 (g)+ 3H 2O(g)H = -1253kJ/mol (2分) Ⅱ.(1)氧气(1分)(2)C 2H 5OH+16OH --12e -2CO 32- +11H 2O (1分) 空气中的CO 2会与KOH 溶液反应,降低溶液的碱性,同时反应中也会消耗KOH 。(2分) (3)3O 2+12H + +12e - 6H 2O (1分),H +(1分) (4)a (1分)O 2+ 2CO 2 +4e - 2CO 32- (1分) Ⅲ.(1)P 4>P 3>P 2>P 1(1分) 反应为气体体积减小的反应,增大压强平衡正向移动,乙烯的转化率增大,所以相同条件下,转化率越大的代表压强越大。(1分) (2)增加H 2O(g)的量、移出生成物。(各1分) 18.(14分)(1)2NaCl + 2H 2O 2NaOH+ H 2↑ +Cl 2↑ (2)①a b d (3分)②2Fe(OH)2 + Cl 2 + 2H 2O === 2Fe(OH)3 +2Cl - +2H + 或:2Fe(OH)2 + Cl 2 + 2OH - === 2Fe(OH)3 +2Cl - 或:6Fe(OH)2 +3Cl 2 === 4Fe(OH)3 +2Fe 3+ +6Cl - (其它合理答案均给分) (3)部分Cl 2溶解 (4)①NaOH 溶液(1分) 吸收Cl 2(1分) ②将B 中气体分别注入KI 淀粉溶液和稀硫酸酸化的KI 淀粉溶液中,前者不变蓝,后者变蓝,则证明不含Cl 2只含O 2。 (5)V 1-2V 3(1分) 19.(1)Cl 2 (1分) 2Cl - -2e - === Cl 2↑ (2)电解过程放热导致温度升高,Cu 2+ + 4Cl 4]2- 正向移动 (1分) (3)阳极附近溶液仍为蓝色 (1分) U 型管冷却后阴极附近溶液仍为绿色 (1分) (4)① 证明在上述实验条件下,电解后的绿色溶液中存在[CuCl 2]- ② Cu 2+ + 4Cl - + Cu === 2[CuCl 2]- ③ 加入CuCl 2蓝色溶液,直至溶液颜色与电解后绿色溶液基本相同 电解 2021届新高考化学模拟试卷 一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意) 1.能促进水的电离平衡,并使溶液中的c(H+)>c(OH﹣)的操作是() A.将水加热煮沸B.将明矾溶于水 C.将NaHSO4固体溶于水D.将NaHCO3固体溶于水 2.N A是阿伏加德罗常数的值。下列说法正确的是 A.1mol葡萄糖和果糖的混合物中含羟基数目为5N A B.500 mL1 mol .L -1(NH4)2SO4溶液中NH4+数目小于0.5 N A C.标准状况下,22.4 L1,2-二溴乙烷含共价键数为7 N A D.19.2 g铜与硝酸完全反应生成气体分子数为0. 2 N A 3.联合制碱法中的副产品有着多种用途,下列不属于其用途的是 A.做电解液B.制焊药C.合成橡胶D.做化肥 4.下列实验操作、现象及结论均正确的是 选 项 实验操作和现象实验结论 A 向Na2SO3溶液中加入足量的Ba(NO3)2溶液,出现白色沉淀;再加入足量 稀盐酸,沉淀溶解 BaSO3溶于稀盐酸 B 向KI溶液中加入CCl4,振荡后静置;液体分层,下层呈紫红色碘易溶于CCl4,难溶于水C 将AgCl与AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,析 出沉淀的物质的量AgCl多于AgBr K SP(AgCl)>K SP(AgBr) D 室温下,同浓度的Na2A溶液的pH比NaB溶液的pH大说明酸性H2A<HB A.A B.B C.C D.D 5.下列物质中所有的碳原子均处在同一条直线上的是() A.B.H3C-C≡C-CH3C.CH2=CH-CH3D.CH3-CH2-CH3 6.常温下,将NaOH溶液滴加到HA溶液中,测得混合溶液的pH与p - c(A) c(HA) 转化关系如图所示[已知: p - c(A) c(HA) =-lg - c(A) c(HA) ]。下列叙述错误的是() 1998年全国普通高等学校招生统一考试(全国化学) 一、选择题(本题包括5小题,每小题3分,共15分。每小题只有一个选项符合题意) 1.1998年山西朔州发生假酒案,假酒中严重超标的有毒成份主要是 A.HOCH2CHOHCH2OH B.CH3OH C.CH3COOCH2CH3D.CH3COOH 2.向下列溶液滴加稀硫酸,生成白色沉淀,继续滴加稀硫酸,沉淀又溶解的是 A.Na2SiO3B.BaCl2C.FeCl3D.NaAlO2 3.按下列实验方法制备气体,合理又实用的是 A.锌粒与稀硝酸反应制备氢气 B.向饱和氯化钠溶液中滴加浓硫酸制备HCl C.亚硫酸钠与浓硫酸反应制备SO2 D.大理石与浓硫酸反应制备CO2 4.起固定氮作用的化学反应是 A.氮气与氢气在一定条件下反应生成氨气 B.一氧化氮与氧气反应生成二氧化氮 C.氨气经催化氧化生成一氧化氮 D.由氨气制碳酸氢铵和硫酸铵 5.300毫升某浓度的NaOH溶液中含有60克溶质。现欲配制1摩/升NaOH溶液,应取原溶液与蒸馏水的体积比约为 A.1:4 B.1:5 C.2:1 D.2:3 二、选择题(本题包括12小题,每小题3分,共36分。若正确答案包括两个选项,只选一个且正确的给1分)6.氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的最初生成物是 A.HI和HClO B.HCl和HIO C.HClO3和HIO D.HClO和HIO 7.X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的化学式可表示为 A.XY B.XY2 C.XY3D.X2Y3 8.反应4NH3(气)+5O2(气) 4NO(气)+6H2O(气)在2升的密闭容器中进行,1 分钟后,NH3减少了0.12摩尔, 则平均每秒钟浓度变化正确的是 A.NO:0.001摩/升B.H2O:0.002摩/升 C.NH3:0.002摩/升D.O2:0.00125摩/升 9.用水稀释0.1摩/升氨水时,溶液中随着水量的增加而减小的是 A. ] [ ] [ 2 3 O H NH OH ? - B. ] [ ] [ 2 3 - ? OH O H NH C.[H+]和[OH-]的乘积D.OH-的物质的量 10.下列关于铜电极的叙述正确的是 A.铜锌原电池中铜是正极 B.用电解法精炼粗铜时铜作阳极 C.在镀件上电镀铜时可用金属铜作阳极 D.电解稀硫酸制H2.O2时铜作阳极 11.等体积等浓度的MOH强碱溶液和HA弱酸溶液混和后,混和液中有关离子的浓度应满足的关系是A.[M+]>[OH-]>[A-]>[H+] B.[M+]>[A-]>[H+]>[OH-] C.[M+]>[A-]>[OH-]>[H+] D.[M+]>[H+] =[OH-]+[A-] 12.下列分子中所有原子都满足最外层8电子结构的是 A.光气(COCl2)B.六氟化硫 C.二氟化氙D.三氟化硼 13.下列叙述正确的是 A.同主族金属的原子半径越大熔点越高 B.稀有气体原子序数越大沸点越高 C.分子间作用力越弱分子晶体的熔点越低 D.同周期元素的原子半径越小越易失去电子14.将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是 A.硫酸B.氯水C.硝酸锌D.氯化铜 15.有五瓶溶液分别是①10毫升0.60摩/升NaOH水溶液②20毫升0.50摩/升硫酸水溶液③30毫升0.40摩/升HCl溶液④40毫升0.30摩/升HAc水溶液⑤50毫升0.20摩/升蔗糖水溶液。以上各瓶溶液所含离子.分子总数的大小顺序是 A.①>②>③>④>⑤B.②>①>③>④>⑤ C.②>③>④>①>⑤D.⑤>④>③>②>① 16.依照阿佛加德罗定律,下列叙述正确的是 电功率经典练习题 1.一台电动机正常工作时线圈两端电压为380V ,线圈电阻为2Ω,线圈中电流为10A ,这台电动机正常工作1s 消耗的电能为W 和产生的热量为Q 分别为A A.3800J 、200J . B.3800J 、3800J C.72200J 、200J D.72200J 、3800J 2.一个标有“6V 3W”的灯泡,欲接到9V 的电源上能正常发光,应给它C A.串联一个3Ω的电阻 B.并联一个3Ω的电阻 C.串联一个6Ω的电阻 D.并联一个6Ω的电阻 3.一只标有“6V 1.5W”的灯泡L 1和另一只“6V 3W”的灯泡L 2串联后接在电源上,通电后有一只灯泡正常发光,另一只灯泡较暗,其中能正常发光的是灯泡 L1 ,此时电路中的电流是 0.25 A ,电源电压是 9 V 。 4. 图所示电路,电源中电源两端的电压保持不变,R 0为定值电阻,R 为滑动变 阻器.闭合开关S 后,在滑动变阻器滑片P 向右滑动的过程中,下列说法正确 的是 C A .电流表A 1的示数变小 B .电流表A 2的示数变大 C .电压表V 的示数不变 D .小灯泡L 的亮度变暗 5.如图所示电路,电源电压保持不变,L 是标有“6V 3W ”的小灯泡,R 是滑 动变阻器。闭合开关S 3,断开开关S 1、S 2,滑片P 位于中点时,灯泡L 恰好正常发光,电压表V 的示数为U 1;当S 1、S 2都闭合,滑片P 滑至b 端时,电流表 示数为1.5A ,电压表V 的示数为U 2;U 1:U 2=1:2,下列选项正确的是B A .滑动变阻器的变化范围是0~12Ω B .滑动变阻器的变化范围是0~24Ω C .当S 1、S 2 、S 3都闭合,滑片P 位于a 端时,灯泡L 仍能正常工作 6.小敏同学在做电学实验时按照如图7所示的电路将电学器材连接,她使用的 电流表量程为0~0.6A ,电压表的量程为0~3V ,电源两端的电压为6V 且保持不变,电阻R 的阻值为10Ω,允许消耗的最大电功率为0.9W 。滑动变阻器R 0的最大阻值为20Ω,允许通过的最大电流为0.5A 。将开关S 闭合后,要保证电路中各个元件正常工作,以 下说法正确的是 B A .通过电阻R 的电流最大值为0.4A B .滑动变阻器接入电路的最小值为5Ω C .电压表示数最大的变化量为1V D .滑动变阻器R 0消耗的最大功率为1.2W 7.图所示电路中电源两端电压不变。当①和②均为电压表时,开关S 闭合后,电压表V 1、V 2的示数之比为7∶12,电阻R 1消耗的电功率为P 1。当①和②均为电流表 时,开关S 闭合后,电流表A 1、A 2的示数之比为16∶21,此时电阻R 2消耗 的电功率为P 2'。则P 1∶P 2'等于D A .1∶12 B.1∶16 C .3∶64 D.9∶16 8.如图所示电路中,电压U 保持不变,电流表的示数为1A 。如果R 1与R 2的等效电阻为R ,并且R 1:R=5:3,电阻R 2消耗的电功率为2.4W ,则电阻R 1=___12.8__Ω。 9.如图所示电路,R 是定值电阻,灯泡L 1L 2分别标有“8V 8W ”和“12V 24W ”,电路两 R 0 高考总复习原电池和化学电源 【考纲要求】 1.了解原电池的工作原理。 2.能写出原电池的电极反应式和反应的总方程式。 3.能根据氧化还原反应方程式设计简单的原电池。 4.能根据原电池原理进行简单计算。 5.熟悉常见的化学电源(一次电池、二次电池和燃料电池),能分析常见化学电池工作原理,了解废旧电池回收的意义。 【考点梳理】 考点一、原电池的概念 1.能量的转化 原电池:将化学能转变为电能的装置。 电能是现代社会应用最广泛、使用最方便、污染最小的一种二次能源,又称电力。2.工作原理 设计一种装置,使氧化还原反应所释放的能量直接转变为电能,即将氧化反应和还原反应分别在两个不同的区域进行,并使电子转移经过导线,在一定条件下形成电流。 电子从负极(较活泼金属)流向正极(较不活泼金属或碳棒),负极发生氧化反应,正极发生还原反应。 电极电极材料反应类型电子流动方向 负极还原性较强的金属氧化反应负极向外电路提供电子 正极还原性较弱的金属还原反应正极从外电路得到电子 以下是锌铜原电池装置示意图: 要点诠释:盐桥的作用 a.组成:将热的饱和KCl或NH4NO3琼胶溶液倒入U形管中(不能产生裂隙),即可得到盐桥。将冷却后的U形管浸泡在KCl饱和溶液或NH4NO3饱和溶液中备用。 b.作用:(1)使整个装置构成通路,代替两溶液直接接触。(2)平衡电荷。 在整个装置的电流回路中,溶液中的电流通路是靠离子迁移完成的。Zn失去电子形成的Zn2+进入ZnSO4溶液,ZnSO4溶液因Zn2+增多而带正电荷。同时,CuSO4则由于Cu2+变为Cu,使得SO42-相对较多而带负电荷。溶液不保持电中性,这两种因素均会阻止电子从锌片流向铜片,造成电流中断。 由于盐桥(如KCl)的存在,其中阴离子Cl-向ZnSO4溶液扩散和迁移,阳离子K+则向CuSO4溶液扩散和迁移,分别中和过剩的电荷,保持溶液的电中性,因而放电作用不间断地进行,一直到锌片全部溶解或CuSO4溶液中的Cu2+几乎完全沉淀下来。若电解质溶液与KCl溶液反应产生沉淀,可用NH4NO3代替KCl作盐桥。 -- 《电功、电功率》经典练习题 一、基础题(直接应用公式) 1.有一种用于220V 电路中的节能灯,额定功率仅为1W,则通过它的电流为____A 0.0045A 2.1度电可供两盏100W 电灯正常工作_______h. 5h 3.一个“220V 800W ”的电炉,正常工作时电阻丝的电阻是______Ω。 60.5Ω 4.一个灯泡上印着“PZ 220 25”,它正常工作时的电阻是______Ω,如果把它接入一个110V 电压的电路中,它实际消耗的电功率是________,与接在220V电路上相比,这时他发光的亮度___________ (1936Ω,6.25W , 暗些。) 5.某次雷电的电流约2?410A,电压约8 110?V,放电时间约0.001s 。这次雷电的电功率约________千瓦,释放_________J 的能量。(2×109 KW , 2×109 J ) 6.某工厂共有电灯1000盏,都用60W 的普通照明灯泡,平均每天用电12h 。如果都改用40W 的日光灯,不但可以省电,而且比原来更亮了。该厂一年(365天)可节约多少千瓦时的电?(87600KW ·h) 7. 某导体的电阻是2Ω,通过2 A 的电流时,1min 产生多少焦耳的热量?480J 8. 一只额定功率是450W的电饭锅,在220V 的额定电压下使用,每分钟产生________J 的热量.27000J 9. 一只电烙铁的额定电压是220V ,在额定电压下工作时的电阻是1210Ω,它的额定功率是________W,在额定电压下通电10min 产生___________J的热量。40W,24000J 10. 某校师生自制了一台电烘箱。电烘箱的电阻丝通过5A的电流时,每分钟可产生 46.610?J 的热量。求这台电烘箱的电功率和电阻丝工作时的电阻。1.1×103W ,4 4Ω 18. 某型号电冰箱主要技术参数如表所示,此电冰箱连续使用一个月(按30天计)消耗的电能为 。20.7kW ·h 19.一个灯泡的灯丝烧断了,把断了的灯丝搭在一起,灯泡会更亮。怎么解释这个现象? 答:灯丝烧断后再搭在一起,由于灯丝的长度变短而使其电阻变小,在灯泡两端电压 不变的情况下,通过灯丝的电流会变大,根据P=U I可知,灯泡的实际功率会变大,所以灯泡会变亮。 二、电功率练习 1.将标有“12V,3W ”的甲灯和“6V ,3W ”的乙灯串联在15V 的电源上,那么能正常发光的是( )A A .甲灯 B .乙灯 C.甲、乙两灯均能正常发光 D.无法判断 2.有两个额定功率相同的甲、乙灯炮,当它们并联接入某一电路时,甲灯比乙灯亮,则它们的额定电压( )B A.U 甲>U 乙 B. U 甲<U 乙 C. U 甲=U 乙 D.无法判断 3.将“12V 8W ”和“6V 3W”的灯泡并联接在电压是6V的电路上,则它们消耗的实际功率之比是 ( )B A 、2:1 B 、2:3 C 、3:8 D、8:3 4. 两个用电器电阻之比R1:R 2=3:1,分别接在两个电路上, 通过它们的电流之比I 1:I2=2:3,则在相等的时间内电流对它们所做功之比W 1:W 2= . 4:3 5.如图1所示,电源电压保持不变。当开关S 1 合、S 2断开时,电流表的示数为0.2A ;当开关S 1、S 2都闭合时,电流表的示数为0.8A 。则电阻R1与R2的比值为( )A A 、1∶3 B 、 3∶l C 、 2∶3 D 、 3∶2 6.如图8所示,电源电压恒定,定值电阻的阻值R =1 0Ω,滑动变阻器R ′的规格为“20Ω 1A ”。闭合开关S,当滑动变阻器接入电路的阻 值在0~10Ω范围内变化时,电流表的示数在0.3A ~0.6A 的范围内变化,则电源电压为 V。从当滑动 图2 R a b A R ′ S 原电池与电解池测试题 构成原电池的一般条件 ①有氧化还原反应②两个活泼性不同的电极负极:较活泼的电极(氧化反应, 电子流出) 正极:较不活泼的金属、石墨等(还原反应, 电子流入) ③同时与电解质溶液接触④形成闭合回路 构成电解池的条件: (1)外加直流电源 (2)两个固体电极 阴极:发生还原反应的电极。 与电源“-”相连的电极, 得到电子的电极, ' 阳离子移到的电极 阳极:发生氧化反应的电极。 与电源“+”相连的电极, 失去电子的电极, 阴离子移到的电极。 (3)电解质溶液或熔融电解质 (4)构成闭合的电路 阴极:阳离子得电子顺序: ; Ag+>Hg2+> Fe3+>Cu2+> H+(酸)>Pb2+>Sn2+>Fe2+>Zn2+> H+(水)Al3+>Mg2+>Na + >Ca2+> K+ 阳极:阴离子失电子顺序:活性电极﹥阴离子。即:Cu>Hg >Ag>S2>I>Br>Cl>OH>(NO3、SO42含氧酸根)>F- 一、选择题(每题4分,共64分) 1.钢铁发生吸氧腐蚀时,正极上发生的电极反应是 ++2e == H2↑++2e == Fe +O2+4e == 4OH-++e == Fe2+ 2.以下现象与电化腐蚀无关的是 A 黄铜(铜锌合金)制作的铜锣不易产生铜绿 B 生铁比软铁芯(几乎是纯铁)容易生锈 C 锈质器件附有铜质配件,在接触处易生铁锈 D 银质奖牌久置后表面变暗 , 3.A、B、C是三种金属,根据下列①、②两个实验,确定它们的还原性强弱顺序为 ①将A与B浸在稀硫酸中用导线相连,A上有气泡逸出,B逐渐溶解 ②电解物质的量浓度相同的A、C盐溶液时,阴极上先析出C(使用惰性电极) >B>C >C>A >A>B >A>C 4.下列关于实验现象的描述不正确 ...的是 A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 2019年高考理综化学经典例题解析 例题1、在一定体积的密闭容器中充入3L气体R和5L气体Q,在一定条件下发生反应2R(g)+5Q(g)=4X(g)+nY(g)反应完全后,容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中的n值是() A、2 B、3 C 、4 D、5 思维:我们知道87.5%比1小,所以左边系数相加必须大于右边系数相加,满足条件只有A. 例题2、已知二氯苯的同分异构体有3种,则四氯苯的同分异构体有() A、2种 B、3种 C、4种 D、5种 思维:苯环有6个取代位置,四氯苯相当于二氯苯,也是3个 例题3、38.4g铜跟适量的浓HNO3反应,铜全部作用后,共收集到气体22.4L(标况),反应消耗的HNO3的物质的量可能是() A、1.0mol B、1.6mol C、2.2mol D、2.4mol 思维:因为气体有可能是NO和NO2,正常的解法是,列出两个反应式,然后列方程组计算。其实不必,我们完全可以假定全部生成的是NO计算出消耗量,假定全部是NO2,计算出消耗量,答案就在两个数值之间。选C.或者直接列总方程式计算,也快捷的多。 例题4、一定温度下,向足量的饱和Na2CO3溶液中加入1.06g 无水Na2CO3,搅拌后静置,最终所得晶体的质量() A、等于1.06g B、大于1.06g,小于2.86g C、等于2.86g D、大于 2.86g 思维:无水Na2CO3放入溶液会夺取溶液中的水,形成 Na2CO3·10H2O晶体,原溶液为饱和溶液,所以被夺走一部分水后必然过饱和,也就会析出更多的晶体,所以晶体质量必然大于 Na2CO3·10H2O质量,Na2CO3质量为1.06g,Na2CO3·10H2O质量= 286 * 1.06g / 106 = 2.86g 例题5、某烷烃和炔烃的混合气体1L,完全燃烧生成CO2 1.4L,水蒸气1.6L(均同温同压下测得),该混合气体是() A、乙烷和乙炔 B、甲烷和丙炔 C、甲烷和乙炔 D、无法判断 思维:用平均值计算:由产物知混合物的平均化学式为C1.4H3.2,必然有碳原子数小于1.4的烃,只能为甲烷。得出甲烷后,就能迅速解题,选项C. 例题6、甲、乙两种气态化合物都只含X、Y两元素,甲、乙中X 元素的百分含量分别为30.4%和25.9%,若已知甲的分子式是XY2,则乙的分子式可能是() A、XY B、X2Y C、X2Y3 D、X2Y5 思路:本题估算即可得出,没有必要精确计算。乙中X 元素的百分含量比在甲中的小,所以X和Y原子的个数比小于1:2(甲的分子式是XY2),选D. 例题7、有两种气态不饱和烃的混合物1体积,完全燃烧可得3.8体积的CO2和3.6体积的水蒸气(均在相同条件下测定),则这两种烃是() 电功、电功率典型题型(含答案) 【正确认识电功】 1.在家庭电路中,电能表所测量的物理量是( )A.电功B.电功率C.电压D.电流2.关于电功,下列说法中正确的是( )A.电功是表示电流做功快慢的物理量B.电流越大,电流做的功就越多C.电流做功越多,消耗的电能不一定越多D.电功是表示电流做功多少的物理量3.关于电流做功,下列说法中正确的是( )A.导体两端的电压越大,通电时间越长,电流做功就越多B.通过导体的电流越大,通电时间越长,电流做的功就越多C.电流做功是电能转化为其他形式的能的过程D.电流做功是电能转化为内能的过程4.一台洗衣机工作0、5h,电流做功3、6106J,这台洗衣机消耗的电能是 J。5.某次雷电的电流是 2104A,电压约为1108V,放电时间约为0、001s,这次雷电释放的能量是___________J 题型二 【电能的测量和电能表】 电压220V电流规格10(20)A电流频率50Hz每千瓦时的转数3000revs/(kW?h)6.为测量某电热杯的电功率,小明同学把家中其余用电器均从电源上断开,只将该电热杯接入电路,观察 电能表,发现在1min内电能表转盘转动15圈.电能表的部分技术参数如表,该电热杯的电功率是( )A.300W B.30WC.150W D.200W7.小明观察家中的电能表(如图),下列说法正确的是( )A.此电能表应该接在220V的电路中使用B.电能表的额定功率是220WC.小明家已经消耗的电能为107JD.此电能表转盘每小时转过3000转8.如图所示,是感应式电能表的示意图,与其技术参数有关的说法正确的是( )A.正常工作时额定功率为220VB.每转2圈电路耗电为 1kW?hC.正常运行的最大电流为10AD.电路消耗的电能是 2486kW?h9.一只家用电能表标有“1500re vs/(kWh)”的字样,今只让一台收录机工作,测得电能表转盘转过一周的时间恰为100S,则这台收录机的功率为 W。10.如图,这是小明家1个月的电能表月初和月末的两次示数,则小明家本月耗电度,合kW?h,消耗的电能是 J。 题型三 【电功率】 11.下列关于申功率的说法正确的是()A.用电器的电功率越大,它消耗的电能越多B.用电器的电功率越大,消耗电能越快C.用电器工作时间越长,它的电功率越大D.用电器的电能,只与通电时间有关12.小明家有一台家庭用节能台灯,其灯泡亮度相当于40W的普通白炽灯的亮度。在相同的工作时间内,节能 原电池 编稿:宋杰审稿:张灿丽 【学习目标】 1、进一步了解原电池的工作原理; 2、能够写出原电池的电极反应式和原电池的总反应方程式。 【要点梳理】 要点一、原电池 1、概念:将化学能转化为电能的装置叫原电池。 【高清课堂:原电池#原电池的组成条件】 2、原电池的构成条件 ①两个活泼性不同的电极(材料可以是金属或导电的非金属),分别发生氧化和还原反应。 负极:活泼性强,失去电子发生氧化反应。 正极:活泼性弱,溶液中阳离子得到电子发生还原反应。 ②电解质溶液,电解质中阴离子向负极方向移动,阳离子向正极方向移动,阴阳离子定向移动形成内电路。 ③导线将两电极连接,形成闭合回路。 ④有能自发进行的氧化还原反应。 要点诠释:a.原电池中,电极材料可能与电解质反应,也可能与电解质不反应。如图: b.形成闭合回路的方式有多种,可以是用导线连接两个电极,也可以是两电极直接接触。如图: 要点二、原电池工作原理的实验探究 【高清课堂:原电池#原电池的工作原理】 1、实验设计 ①按照图示装置进行实验。请观察两个金属片插入溶液后电流表指针位置的变化、金属电极表面的变化以及溶液温度的变化,分析是否有电流产生。 ②按照下图组装实验装置,注意最后将盐桥插入两种电解质溶液中。请观察反应过程中电流表指针位置的变化,判断是否有电流产生,并观察电极表面以及溶液温度的变化情况。 要点诠释:盐桥的作用及优点 a.组成:将热的饱和KCl或NH4NO3琼胶溶液倒入U形管中(不能产生裂隙),即可得到盐桥。将冷却后的U形管浸泡在KCl饱和溶液或NH4NO3饱和溶液中备用。 b.作用:使两个半电池中的溶液连成一个通路。 c.优点:使原电池中的氧化剂和还原剂近乎完全隔离,并在不同区域之间实现了电子的定向移动,使原电池能持续、稳定地产生电流。 电流产生情况电极表面变化情况温度变化情况能量变化情况 (Ⅰ) 有电流产生锌片质量减小,同时铜片上有红色 物质析出,铜片质量增加溶液温度升高化学能转化为电能、 热能 (Ⅱ) 有电流产生锌片质量减小,铜片上有红色物质 析出,铜片质量增加 溶液温度不变化学能转化为电能 3、实验分析 ①对于图甲装置 Zn片:Zn-2e-=Zn2+ Cu片:Cu2++2e-=Cu 同时在Zn片上,Zn可直接与CuSO4溶液反应,生成Cu与ZnSO4,因此该装置中既有化学能转化为电能,同时也有化学能转化为热能。 ②对于图乙所示原电池 锌片:负极,Zn-2e-=Zn2+(氧化反应) 铜片:正极,Cu2++2e-=Cu(还原反应) 总化学方程式:Zn+Cu2+=Cu+Zn2+ 4、实验原理分析:(如图所示) 1、中学化学中很多“规律”都有适用范围,下列根据有关“规律”推出的结论正确的是 反应物浓度 结构和组 2、室温下,下列溶液中粒子浓度大小关系正确的是 A.Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) B.Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) C.Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-) D.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) 3、为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是 仪器 4、下列有关Fe2(SO4)3溶液的叙述正确的是 A.该溶液中K+、Fe2+、C6H5OH、Br-可以大量共存 B.和K I溶液反应的离子方程式:Fe3++2I- Fe2++I2 C.和Ba(OH)2溶液反应的离子方程式:Fe3++SO42—+Ba2++3OH- Fe(OH)3+ Ba SO4 D.1 L0.1 mol·L—1该溶液和足量的Zn充分反应,生成11.2 g Fe 5、CO2的的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰胺的反应:NH3+CO2→ +H2O 下列有关三聚氰胺的说法正确的是 A.分子式为C3H6N3O3 B.分子中既含极性键,又含非极性键 C.属于共价化合物 D.生成该物质的上述反应为中和反应 6、某原电池装置如右图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是 A.正极反应为AgCl +e-=Ag +Cl- B.放电时,交换膜右侧溶液中有大量白色沉淀生成 C.若用NaCl溶液代替盐酸,则电池总反应随之改变 D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子 7、下列关于0.10 mol·L-1 NaHCO3溶液的说法正确的是 电功率专题 范围专题 1.如图所示的电路中,电源电压不变,移动滑动变阻器R1的滑片P,当电流表的示数变化范围为1A~时,电压表的示数变化了3V,则该定值电阻R2所消耗功率的变化范围是() A.3W~B.3W~C.~10W D.10W~ 2.如图所示,电源电压恒为6V,定值电阻R1=10Ω,滑动变阻器R2的最大阻值为20Ω,电压表接入电路的量程为0~3V,电流表接入电路的量程为0~.当开关S闭合,滑动变阻器的滑片P从b端向a端移动过程中,在保证电压表和电流表安全的情况下,下列说法正确的是() A.电压表的示数变小,电流表的示数变大B.电流表的示数变化范围为~ C.电阻R2的两端电压由4V减小到3V D.电阻R1消耗的功率的变化范围为~ 2.如图所示,电源电压为,电压表量程为“0~3V”,滑动变阻器规格为“20Ω 1A”,小灯泡标有“”(灯丝电阻不变).电流表量程为“0~”,在保证电路元件安全的情况下,下列说法正确的是() A.小灯泡的灯丝电阻为5ΩB.该电路功率变化范围是~ C.滑动变阻器连入电路的阻值变化范围是4~10ΩD.电流表最大示数为 3.某同学在做“调节灯泡亮度”的电学实验时,电路如图所示,电源电压恒为6V,电流表的量程为“0~”,电压表量程“0~3V”,滑动变阻器的规格为“20Ω 2A”,灯泡L标有“3V ”字样(忽略灯丝电阻变化).在实验中为了保证所有元件的安全,下列判断正确的是() A.该电路中,变阻器R接入电路的阻值变化范围为0~20Ω B.该电路消耗的总功率的变化范围为~ C.该电路中,电流表示数的变化范围为~ D.该电路中,电灯消耗功率的变化范围为~ 4.如图所示,电源电压为12V,R0=60Ω,滑动变阻器的规格为“50Ω 2A”,电流表的量程为“0~”,小灯泡上标有“6V 3W”字样.不考虑灯丝电阻变化,并保证电路安全.则() 化学能与电能的转化—原电池专题 1、概念:把化学能直接转化为电能的装置叫做原电池。 2、原电池的工作原理:通过氧化还原反应(有电子的转移)把化学能转变为电能。 3、构成原电池的条件:(1)电极为导体且活泼性不同;(2)两个电极接触(导线连接或直接接触);(3)两个相互连接的电极插入电解质溶液构成闭合回路。 【例题分析】 例1、在如图所示的8个装置中,属于原电池的是() A.①④ B.③④⑤C.④⑧D.②④⑥⑦ 4、电极名称及发生的反应: 负极:较活泼的金属作负极,负极发生氧化反应, 电极反应式:较活泼金属-ne-=金属阳离子 负极现象:负极溶解,负极质量减少。 正极:较不活泼的金属或石墨作正极,正极发生还原反应, 电极反应式:溶液中阳离子+ne-=单质 正极的现象:一般有气体放出或正极质量增加。 5、原电池正负极的判断方法: ①依据原电池两极的材料: 较活泼的金属作负极(K、Ca、Na太活泼,不能作电极); 较不活泼金属或可导电非金属(石墨)、氧化物(MnO2)等作正极。 ②根据电流方向或电子流向:(外电路)的电流由正极流向负极;电子则由负极经外电路 流向原电池的正极。 ③根据内电路离子的迁移方向:阳离子流向原电池正极,阴离子流向原电池负极。 ④根据原电池中的反应类型: 负极:失电子,发生氧化反应,现象通常是电极本身消耗,质量减小。 正极:得电子,发生还原反应,现象是常伴随金属的析出或H2的放出。 6、原电池电极反应的书写方法: (i)原电池反应所依托的化学反应原理是氧化还原反应,负极反应是氧化反应,正极反应是还原反应。因此书写电极反应的方法归纳如下: ①写出总反应方程式。②把总反应根据电子得失情况,分成氧化反应、还原反应。 ③氧化反应在负极发生,还原反应在正极发生,反应物和生成物对号入座,注意酸碱 介质和水等参与反应。 (ii)原电池的总反应式一般把正极和负极反应式相加而得。 电功电功率典例精析 电功和电功率基础知识 1. 电功(W):电流对用电器做的功(电能转化成其他形式能的多少)叫电功。 ①电功的国际单位:焦耳(J)。常用:度(千瓦时)KW.h,1度=1千瓦时=3.6×106焦耳。 ②测量电功的工具:电能表(电度表) ③电功公式:W=Pt=UIt(式中单位W→焦(J);U→伏(V);I→安(A);t→秒)。 ④利用W=UIt计算时注意:①式中的W、U、I、t必须对于同一导体(同一段电路)的同一过程,才能代入公式计算,即要满足“同一性”;②计算时单位要统一;③已知任意的三个量都可以求出第四个量; ⑤其他计算公式:W=I2Rt(多用于串联电路),W=U2t/R(多用于并联电路) 2. 电功率(P):表示电流做功的快慢。国际单位:瓦特(W)。常用单位:千瓦(KW) ①计算公式:P=W/t=UI(式中单位P→瓦(w);W→焦(J);t→秒(s);U→伏(V);I→安(A)) ②利用公式计算时单位要统一: a.如果W用焦(J),t用秒(s),则P的单位是瓦(w); b.如果W用千瓦时(KW.h),t用小时(h),则P的单位是千瓦(KW)。 c.公式中各物理量必须满足“同一性”才能代入公式计算。 ③其他计算公式:P=I2R (多用于串联电路),P=U2/R(多用于并联电路) ④额定电压(U额):用电器正常工作的电压。另有:额定电流 ⑤额定功率(P额):用电器在额定电压下的功率。 ⑥实际电压(U实):实际加在用电器两端的电压。另有:实际电流 ⑦实际功率(P实):用电器在实际电压下的功率。 ⑧用电器消耗的实际功率随加在它两端的实际电压而改变。实际电压升高,实际功率增大;反之则减小。 a.当U 实> U额时,则P 实> P额;(灯很亮,将缩短灯泡寿命,且易烧坏)。 b.当U实< U额时,则P实< P额;(灯很暗)。 c.当U实= U额时,则P实= P额;(正常发光)。 ⑨同一个电阻,接在不同的电压下使用,则有,如:当实际电压是额定电压的一半时,则实际功率就是额定功率的1/4。(即同一用电器消耗的实际功率跟它两端的实际电压的平方成正比,P1/P2=U12/U22) 原电池化学电源 题组一原电池工作原理的考查 1.下列装置中能构成原电池产生电流的是( ) 答案 B 解析A项,电极相同不能构成原电池;C项,酒精不是电解质溶液,不能构成原电池;D项,锌与电解质溶液不反应,无电流产生。 2.有关电化学知识的描述正确的是( ) A.CaO+H2O===Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能B.某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液C.原电池的两极一定是由活动性不同的两种金属组成 D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 答案 D 解析CaO+H2O===Ca(OH)2不是氧化还原反应,KCl和AgNO3反应生成AgCl沉淀易阻止原电池反应的发生;作电极的不一定是金属,如石墨棒也可作电极。 题组二原电池正、负极的判断 3.下列有关原电池的说法中正确的是( ) A.在电路中,电子由正极流向负极 B.在原电池中,相对较活泼的金属作负极,不活泼的金属作正极 C.原电池工作时,正极表面一定有气泡产生 D.原电池工作时,可能会伴随着热能变化 答案 D 解析A项,电路中不存在电子的移动;B项,若是由铝、镁、氢氧化钠溶液构 成的原电池,则负极是铝;C项,若是由锌、铜、硫酸铜溶液构成的原电池,则正 极表面析出铜,没有气泡产生。 4.分析下图所示的四个原电池装置,其中结论正确的是( ) A.①②中Mg作负极,③④中Fe作负极 B.②中Mg作正极,电极反应式为6H2O+6e-===6OH-+3H2↑ C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+ D.④中Cu作正极,电极反应式为2H++2e-===H2↑ 答案 B 解析②中Mg不与NaOH溶液反应,而Al能和NaOH溶液反应失去电子,故Al是负极;③中Fe在浓硝酸中易钝化,Cu和浓HNO3反应失去电子作负极,A错,C错。②中电池总反应为2Al +2NaOH+2H2O===2NaAlO2+3H2↑,负极电极反应式为2Al+8OH--6e-===2AlO-2+4H2O,二者相减得到正极电极反应式为6H2O+6e-===6OH-+3H2↑,B正确。④中Cu是正极,电极反应式为O2+2H2O+4e-=== 4OH-,D错。 题组训练原电池原理的应用 1.电工经常说的一句口头禅:“铜接铝,瞎糊弄”,所以电工操作上规定不能把铜导线与铝导线连接在一起使用,说明原因:_______________________________________________。 答案铜、铝接触在潮湿的环境中形成原电池,加快了铝的腐蚀,易造成电路断路 2.请运用原电池原理设计实验,验证Cu2+、Fe3+氧化性的强弱。请写出电极反应式,负极_______________,正极____________________, 并在方框画出实验装置图,要求用烧杯和盐桥,并标出外电路电子流向。 答案Cu-2e-===Cu2+2Fe3++2e-===2Fe2+ 3.有A、B、C、D、E五块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4 (备战2019年高考)近六年化学经典真题精选训练 物质的组成、性质和分类 一.选择题(共7小题) 1.中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝.关于Lv的叙述错误的 是() A.原子序数116 B.中子数177 C.核外电子数116 D.相对原子质量293 2.在CO2中,Mg燃烧生成MgO和C.下列说法正确的是() A.元素C的单质只存在金刚石和石墨两种同素异形体 B.Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg) C.在该反应条件下,Mg的还原性强于C的还原性 D.该反应中化学能全部转化为热能 3.下列关于物质分类的说法正确的是() A.金刚石、白磷都属于单质 B.漂白粉、石英都属于纯净物 C.氯化铵、次氯酸都属于强电解质 D.葡萄糖、蛋白质都属于高分子化合物 4.230Th和232Th是钍的两种同位素,232Th可以转化成233U.下列有关Th的说法正确的是()A.Th元素的质量数是232 B.Th元素的相对原子质量是231 C.232Th转化成233U是化学变化 D.230Th和232Th的化学性质相同 5.重水(D2O)是重要的核工业原料,下列说法错误的是() A.氘(D)原子核外有1个电子 B.1H与D互称同位素 C.H2O与D2O互称同素异形体 D.1H218O与D216O的相对分子质量相同 6.下列物质分类正确的是() A.SO2、SiO2、CO均为酸性氧化物 B.稀豆浆、硅酸、氯化铁溶液均为胶体 C.烧碱、冰醋酸、四氯化碳均为电解质 D.福尔马林、水玻璃、氨水均为混合物 7.下列叙述正确的是() A.乙酸与丙二酸互为同系物 B.不同元素的原子构成的分子只含极性共价键 2019年普通高等学校招生全国统一考试 理科综合能力测试化学2019-6-9 H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl Ar 40 Fe 56 I 127 一、选择题:在每小题给出的四个选项中,只有一项是符合题目要求的。7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。下列说法错误的是 A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁 B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成 C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐 D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点 8.关于化合物2?苯基丙烯(),下列说法正确的是 A.不能使稀高锰酸钾溶液褪色 B.可以发生加成聚合反应 C.分子中所有原子共平面 D.易溶于水及甲苯 9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是 A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K B.实验中装置b中的液体逐渐变为浅红色 C.装置c中的碳酸钠溶液的作用是吸收溴化氢 D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯 10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。下列叙述错误的是 A.冰表面第一层中,HCl以分子形式存在 B.冰表面第二层中,H+浓度为5×10?3 mol·L?1(设冰的密度为g·cm?3)C.冰表面第三层中,冰的氢键网格结构保持不变 D.冰表面各层之间,均存在可逆反应HCl H++Cl? 11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H 2A的K a1 =×10?3 ,K a2 =×10?6) 溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。 下列叙述错误的是 A.混合溶液的导电能力与离子浓度和种类有关 B.Na+与A2?的导电能力之和大于HA?的 C.b点的混合溶液pH=7 D.c点的混合溶液中,c(Na+)>c(K+)>c(OH?) 12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是 A.相比现有工业合成氨,该方法条件温和,同时还可提供电能 B.阴极区,在氢化酶作用下发生反应H 2 +2MV2+2H++2MV+ C.正极区,固氮酶为催化剂,N 2发生还原反应生成NH 3 D.电池工作时质子通过交换膜由负极区向正极区移动 13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周 “电功率及电功”专题复习 电功率概念辨析 1、 标有“PZ220-40”字样的灯泡正常工作10h ,消耗的电能是_________kW·h ,合_________J 。 2、 现有两个灯泡L1、L2,分别标有“10V 10W”和“9V 5.4W”的字样.当将它们串联使用时,电路两端 允许加的最大电压是______V ;当将他们并联使用时,干路允许通过的最大电流是______A ,电路消耗的最大功率是_______W . 3、 如图5—3所示,当S 闭合,甲、乙两表为电压表时,两表示数比为U 甲︰U 乙=5︰3;当S 断开,甲、 乙两表为电流表时,两表示数比为I 甲︰I 乙=______,此时R 1和R 2消耗的功率之比P 甲︰P 乙=________。 4、 下列说法中,正确的是 ( ) A . 电功率是表示电流做功多少的物理量 B .电功率是表示电流做功快慢的物理量 C .用电器的电功率越大,做功越多 D .相同时间,消耗功率大的用电器耗电一定多 5、下列电器正常工作时,每秒做功为几十焦耳的是 ( ) A .电饭锅 B .教室里的一只日光灯 C .家用手电筒里的灯泡 D .空调器 6、额定电压相同的甲、乙两只白炽灯串联接入电路,发现甲灯比乙灯亮,则下列说法中正确的是 ( ) A.甲灯额定功率和实际功率都比乙灯大 B.甲灯额定功率大,但实际功率小 C.甲灯额定功率和实际功率都比乙灯小 D.甲灯额定功率小,但实际功率大 7、生活中下列用电的做法,正确的是( ) A .用粗铜线代替保险丝 B .开关串联在零线上 C .使用测电笔时手指不接触笔尖金属部位 D .使用洗衣机不接地 8、如图2所示,电源电压保持不变,R 1=2R 2,开关S断开时,电流表的示数为I1,R 1消耗的功率为P 1;开关S 闭合时,电流表示数为电流表的示数为I2,R1消耗的功率为P2,则( ) A .I1∶I2=1∶1,P 1∶P 2=3∶1 B .I1∶I2=1∶3,P 1∶P 2=1∶1 C .I1∶I2=3∶1,P 1∶P 2=1∶1 D .I1∶I2=1∶1,P 1∶P 2=1∶3 9、右图所示的电路中,电源电压为30V ,定值电阻为30Ω,滑动变阻器标有"60Ω,1.5A"字样,在该电路正常使用的情况下,则( ) A .电路消耗的最大功率为75W B.电流表的最大示数为1.5 A C .滑动变阻器消耗的最小功率为45W D.电路总电阻的变化围为0Ω~20Ω 10、如图所示,电源电压不变.闭合开关S 后,当滑动变阻器的 滑片P 向右移动时,下列判断正确的是 ( ) A.电流表示数变小,电压表示数变小,R 1功率变小 B.电流表示数变小,电压表示数变大,R 1功率变大 C.电流表示数变大,电压表示数不变,R 1功率变大 D.电流表示数变小,电压表示数不变,R 1功率变小 11、如图所示电路中,设电源电压不变,灯电阻不变.闭合开关S,在滑动变阻器滑片移动的过程中,电流表的最小示数是0.2A,电压表的最大示数是4V ,灯L 的 最大功率与最小功率之比为9:4,则 ( ) A.电源电压是6V B.灯的电阻是40Ω C.电源电压是4V D.电路消耗的最大功率是2.4W 第9题图 第10题图 A R 1 R 2 P S V V A 11题图 P L S R2020浙江省名校高考化学经典试题
1998年全国高考化学试题
电功率经典练习题(附标准答案)
2021高考化学考点原电池和化学电源(提高)
《电功、电功率》经典练习题+答案
原电池和电解池经典测试题
高考理综化学经典例题解析
电功、电功率典型题型(含答案)
知识讲解_原电池_基础
高考化学选择专题练习经典总结带答案
电功率各专题经典题型及答案
2018年人教版化学必修二原电池知识点与经典练习
初三物理电功电功率典型例题解析(免费)
原电池.doc化学电源.doc电化学.doc经典习题及解析
近六年高考化学经典真题精选训练:物质的组成、性质和分类(含解析)
高考化学试题及答案
初三电功率专题训练经典题目
