常见无机物有机物性质归纳
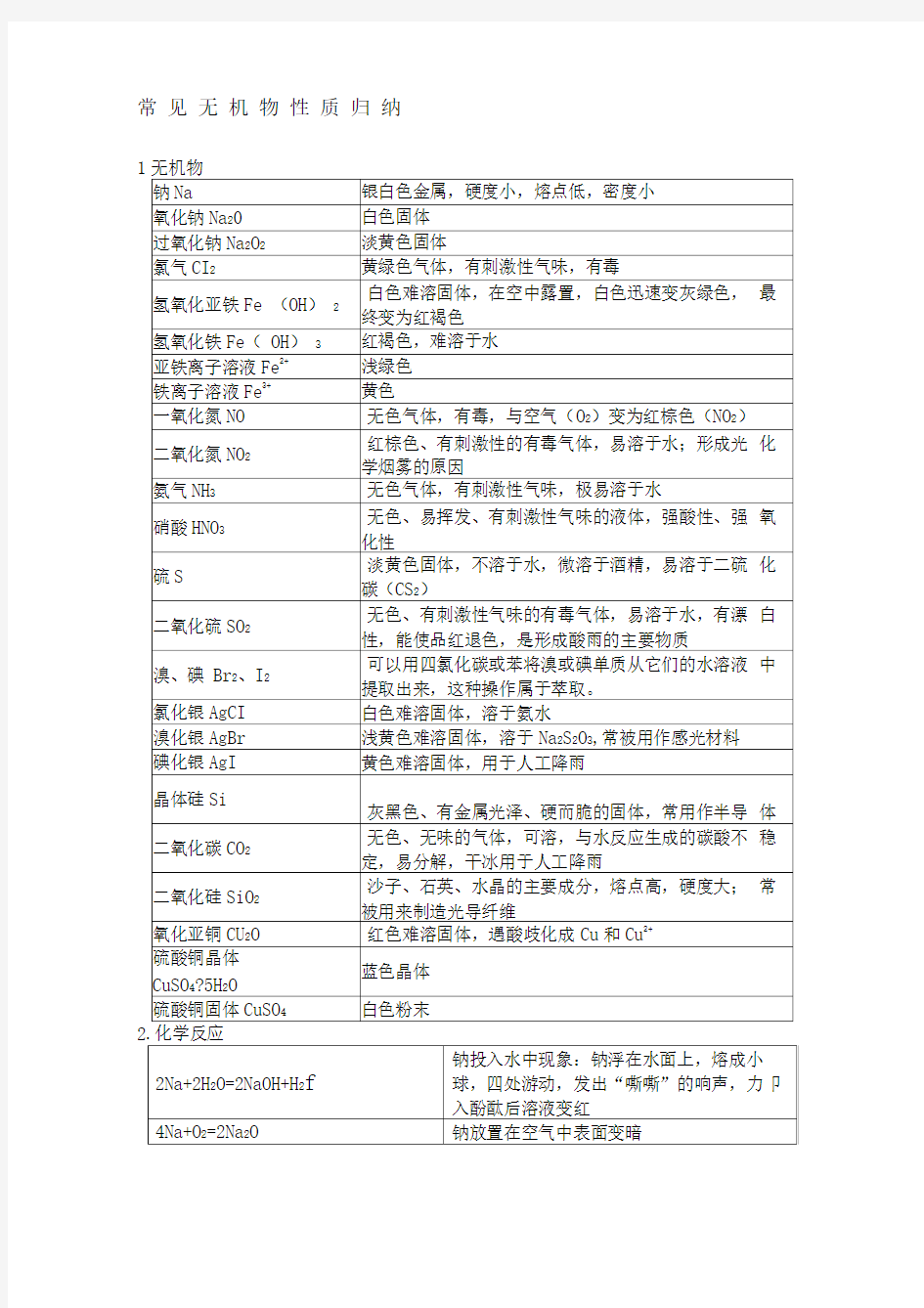
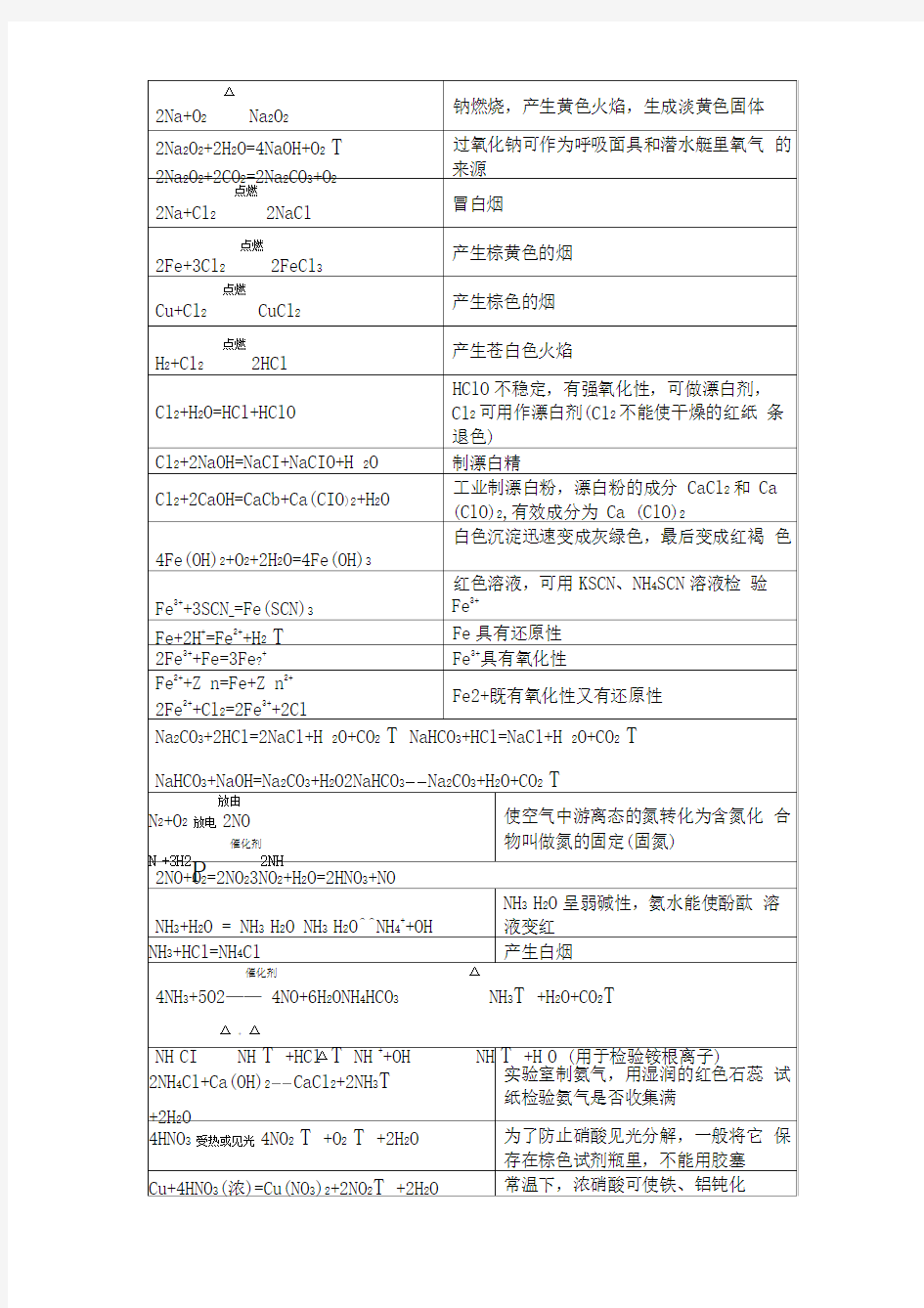
常见无机物性质归纳1无机物
2.化学反应
有机物1?有机物
2.化学反应
有机溶剂分类
有机溶剂分类 一、烃类溶剂 1.烃 只含有碳氢两种元素的有机化合物叫烃。根据结构将烃类分为脂肪烃和芳香烃。脂肪烃包括脂肪链烃和脂环烃。开链结构的脂肪烃根据结构的饱和程度分为饱和链烃(烷烃)和不饱和链烃(烯烃和炔烃)。芳香烃是含有苯环特殊结构的烃类。根据具体结构分为单环芳烃、多环芳烃和稠环芳烃。 烃类溶剂根据来源分为两类:由石油分馏得到的烃类混合物溶剂叫石油溶剂油,简称溶剂油;由化工原料合成或精制得到的成分单一烃类溶剂是烃的纯溶剂。纯溶剂价格较高,通常只用于一些特殊用途中。 2.溶剂油 石油是由多种烃类组成的混合物,经过分馏处理得到不同沸点范围的产品。根据沸,抿范围通常把石油产品分为石油醚、汽油、煤油、柴油、润滑油、石蜡和沥青。其中沸点范围在30~90℃以戊烷和己烷为主要成分的石油醚和沸点范围在40~200℃烃分子含碳数在4~12的汽油,有很好的溶解性能。在工业生产中常做溶剂使用,称为溶剂油或溶剂汽油。近年来还开发出相当于煤油乃至轻柴油馏分做高沸点溶剂油,拓宽了溶剂油的概念。煤油是石油分馏时,沸点在175~325℃范围的馏分,由于馏程长所包含的烃类成分复杂。在一定情况下也可以做溶剂使用,如美国干洗业使用的干洗溶剂汽油(stoddard solvent)实际上是一种不易燃的煤油溶剂。因此广义上溶剂油包括多种沸程范围的烃类混合物以及己烷、苯、甲苯、二甲苯纯烃类溶剂。为了叙述上的方便,本书介绍的溶剂油是指由石油分馏得到的烃类混合物溶剂。 (1)溶剂油按沸程分类根据分馏过程的沸程,溶剂油大致分为三类:把沸程在100℃凋以下的称为低沸点溶剂油,如工业上的6号抽提溶剂油,沸程为60~90℃;把沸程在100~150℃的称为中沸点溶剂油,如橡胶溶剂油,沸程在80~120℃;把沸程高于150℃的称为高调沸点溶剂油,如油漆溶剂油,沸程为140—200℃,油墨溶剂油干点达360℃都属于高沸点溶剂油。从沸程范围看,溶剂油大多数属于汽油馏分。 (2)溶剂油的化学成分溶剂油是各种烃类的混合物,主要成分有开链烷烃、烯烃、环烷烃和芳香烃。由于烯烃化学性质活泼、安定性差,不适合作溶剂使用,所以一般溶剂油中含烯烃很少,成分以其他三类烃为主。 低沸程溶剂油,如6号抽提溶剂油,120号橡胶溶剂油,200号油漆溶剂油中主要成分是烷烃和环烷烃。有时称为脂肪烃类溶剂,脂肪烃溶剂油成分有直链烷烃、支链烷烃、环烷烃。由于不同结构烷烃的溶解性能不同,所以又可以根据其主要成分进一步分类,如以支链烷烃为主要成分的溶剂油,称为异构烷烃溶剂油,它的溶解性能优于一般脂肪烃溶剂油而高沸程溶剂油中甲苯、二甲苯等芳烃含量较大称为芳烃类溶剂油,如近年兴起的高沸点芳烃溶剂油主要成分就是分子中含9个碳原子的芳烃。 溶剂油的性能与其化学成分有密切关系,由于烃类的溶解能力顺序为:芳烃>环烷烃>链烷烃。所以相同沸程的溶剂油中含链烷烃、环烷烃多的比含芳烃较多的溶剂油苯胺点高、贝壳松脂丁醇值低,溶解能力差。 纯芳香烃溶剂油虽然溶解能力强,但毒性也大,因此目前工业上出现用高芳香烃溶剂油和低芳香烃溶剂油来代替苯、甲苯、二甲苯等纯芳香烃溶剂使用的趋势。这样虽然溶解能力稍有降低,但降低了溶剂油的毒性,也降低了生产成本。而且为降低溶剂油的毒性,各国对溶剂油中的芳香烃含量都作出限制,如油漆溶剂油中芳香烃的含量要求在15%以下。
有机化学中各种物质的转换
CH4+2O2→CO2+2H2O(条件为点燃) 甲烷隔绝空气高温分解 甲烷分解很复杂,以下是最终分解。CH4→C+2H2(条件为高温高压,催化剂) 甲烷和氯气发生取代反应 CH4+Cl2→CH3Cl+HCl CH3Cl+Cl2→CH2Cl2+HCl CH2Cl2+Cl2→CHCl3+HCl CHCl3+Cl2→CCl4+HCl (条件都为光照。) 实验室制甲烷 CH3COONa+NaOH→Na2CO3+CH4(条件是CaO 加热) 乙烯燃烧 CH2=CH2+3O2→2CO2+2H2O(条件为点燃) 乙烯和溴水 CH2=CH2+Br2→CH2Br-CH2Br 乙烯和水 CH2=CH2+H20→CH3CH2OH (条件为催化剂) 乙烯和氯化氢 CH2=CH2+HCl→CH3-CH2Cl 乙烯和氢气 CH2=CH2+H2→CH3-CH3 (条件为催化剂) 乙烯聚合 nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂) 氯乙烯聚合 nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂) 实验室制乙烯 CH3CH2OH→CH2=CH2↑+H2O (条件为加热,浓H2SO4) 乙炔燃烧 C2H2+3O2→2CO2+H2O (条件为点燃)
C2H2+2Br2→C2H2Br4 乙炔和氯化氢 两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl2 乙炔和氢气 两步反应:C2H2+H2→C2H4→C2H2+2H2→C2H6 (条件为催化剂) 实验室制乙炔 CaC2+2H2O→Ca(OH)2+C2H2↑ 以食盐、水、石灰石、焦炭为原料合成聚乙烯的方程式。 CaCO3 === CaO + CO2 2CaO+5C===2CaC2+CO2 CaC2+2H2O→C2H2+Ca(OH)2 C+H2O===CO+H2-----高温 C2H2+H2→C2H4 ----乙炔加成生成乙烯 C2H4可聚合 苯燃烧 2C6H6+15O2→12CO2+6H2O (条件为点燃) 苯和液溴的取代 C6H6+Br2→C6H5Br+HBr 苯和浓硫酸浓硝酸 C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸) 苯和氢气 C6H6+3H2→C6H12 (条件为催化剂) 乙醇完全燃烧的方程式 C2H5OH+3O2→2CO2+3H2O (条件为点燃) 乙醇的催化氧化的方程式 2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)(这是总方程式) 乙醇发生消去反应的方程式 CH3CH2OH→CH2=CH2+H2O (条件为浓硫酸170摄氏度) 两分子乙醇发生分子间脱水 2CH3CH2OH→CH3CH2OCH2CH3+H2O (条件为催化剂浓硫酸140摄氏度)
最全的常用有机溶剂参数表
溶剂危害性分类 一类溶剂:应避免 致癌物;备受怀疑的致癌物;环境危害物 二类溶剂:设定残余量,限量使用 非基因性动物致癌物;可能导致不可逆中毒,比如神经性中毒,畸形;可能导致其他可逆性中毒 三类溶剂: 低毒 对人体有潜在毒性,可以接触,但不超过50mg/day。 Solvent Other Names Structure Class Acetic acid Ethanoic acid CH3COOH三类溶剂 2-Propanone Acetone CH3COCH3三类溶剂 Propan-2-one Acetonitrile CH3CN二类溶剂 Anisole Methoxybenzene三类溶剂 Benzene Benzol一类溶剂 n-Butyl alcohol 1-Butanol CH3(CH2)3OH三类溶剂 Butan-1-ol sec-Butyl alcohol 2-Butanol CH3CH2CH(OH)CH3三类溶剂 Butan-2-ol Butyl acetate Acetic acid butyl ester CH3COO(CH2)3CH3三类溶剂 tert-Butylmethyl ether2-Methoxy-2-methyl- propane(CH3)3COCH3三类溶剂Carbon tetrachloride Tetrachloromethane CCl4一类溶剂 Chlorobenzene二类溶剂Chloroform Trichloromethane CHCl3二类溶剂 Isopropylbenzene Cumene 三类溶剂 (1-Methyl)ethylbenzene Cyclohexane Hexamethylene二类溶剂 1,2-Dichloroethane sym-Dichloroethane CH2ClCH2Cl一类溶剂
常见有机物的性质及应用
第11题常见有机物的结构与性质 题组一常见有机物的性质及应用 [解题指导] 1.掌握两类有机反应类型 (1)加成反应:主要以烯烃和苯为代表,碳碳双键、苯环可以发生加成反应。 (2)取代反应:烷烃、苯、乙醇和乙酸均容易发生取代反应。 2.区分三个易错问题 (1)不能区分常见有机物发生反应的反应类型。如塑料的老化发生的是氧化反应,不是加成反应,单糖不能发生水解反应等。 (2)不能灵活区分有机反应的反应条件。如苯与溴水不反应,只与纯液溴反应。 (3)不能准确地对有机物进行分类。如油脂不是高分子化合物。 3.牢记三种物质的特征反应 (1)葡萄糖:在碱性、加热条件下与银氨溶液反应析出银;在碱性、加热条件下与新制氢氧化铜悬浊液反应产生砖红色沉淀。 (2)淀粉:在常温下遇碘变蓝。 (3)蛋白质:浓硝酸可使蛋白质变黄,发生颜色反应。 4.同分异构体判断时必记的三个基团 丙基(C3H7—)有2种,丁基(C4H9—)有4种,戊基(C5H11—)有8种。 [挑战满分](限时10分钟) 1.下列涉及有机物的性质的说法错误的是() A.乙烯和聚氯乙烯都能发生加成反应 B.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了 D.HNO3能与苯、甲苯、甘油、纤维素等有机物发生反应,常用浓硫酸作催作剂 2.下列说法中不正确的是() A.有机化合物中每个碳原子最多形成4个共价键 B.油脂、淀粉、蛋白质在一定条件下都能发生水解反应 C.用溴水既可以鉴别甲烷和乙烯,也可以除去甲烷中的乙烯 D.乙烯和苯均能发生氧化反应,说明乙烯和苯分子中均有碳碳双键
常用有机溶剂
常用有机溶剂 Prepared on 22 November 2020
常用有机溶剂 一、乙醇(ethylalcohol,ethanol) 1.理化性质: (1)分子式C2H6O (2)相对分子质量 (3)结构式CH3CH2OH (4)外观与性状:无色液体,有酒香。 (5)熔点(℃): (6)沸点(℃): (7)相对密度(水=1): (8)相对密度(空气=1): (9)溶解性:与水混溶,可混溶于醚、氯仿、甘油等多数有机溶剂。(10)禁忌物:强氧化剂、酸类、酸酐、碱金属、胺类。 危险类别: (1)燃烧性:易燃 (2)闪点(℃):12 (3)引燃温度(℃):363 (4)爆炸下限(%): (5)爆炸上限(%): 二、甲醇(methylalcohol,Methanol) 1.理化性质:
(1)分子式CH4O (2)相对分子质量32 (3)结构式CH3OH (4)外观与性状:无色澄清液体,有刺激性气味。 (5)熔点(℃): (6)沸点(℃): (7)相对密度(水=1): (8)相对密度(空气=1): (9)溶解性:与水混溶,可混溶于醇、醚等多数有机溶剂。(10)禁忌物:强氧化剂、酸类、酸酐、碱金属。 危险类别: (1)燃烧性:易燃 (2)闪点(℃):11 (3)引燃温度(℃):385 (4)爆炸下限(%): (5)爆炸上限(%): 乙酸乙酯,醋酸乙酯(ethylacetate,aceticester) 1.理化性质: (1)分子式:C4H8O2 (2)相对分子质量 (3)结构式 CH3-C-OCH2CH3 (4)外观与性状:无色澄清液体,有芳香气味,易挥发。
种常见有机溶剂
种常见有机溶剂
————————————————————————————————作者:————————————————————————————————日期:
77种常见有机溶剂 溶剂名沸点溶解性毒性 *液氨 -33.35℃ 特殊溶解性:能溶解碱金属和碱土金 属剧毒性、腐蚀性 液态二氧化硫-10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒?*甲胺 -6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃?二甲胺 7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性 石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似 *乙醚34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性?戊烷36.1与乙醇、乙醚等多数有机溶剂混溶低毒性 二氯甲烷 39.75与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,麻醉性强 *二硫化碳46.23 微溶于水,与多种有机溶剂混溶麻醉性,强刺激性?*溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大?*丙酮56.12 与 1,1-二氯水、醇、醚、烃混溶低毒,类乙醇,但较大? 乙烷 57.28与醇、醚等大多数有机溶剂混溶低毒、局部刺激性 *氯仿61.15 与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性?*甲醇 64.5 与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性, 四氢呋喃66 优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒己烷 68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。麻醉性,刺激性 三氟代乙酸71.78 与水,乙醇,乙醚,丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物 ?1,1,1-三氯乙烷 74.0 与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶低毒类溶剂 *四氯化碳76.75 与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强 *乙酸乙酯 77.112 与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,麻醉性?*乙醇 78.3 与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,麻醉性?丁酮79.64 与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性
高中化学 常见有机物的结构与性质 -学生版
第10题常见有机物的结构与性质 题组一常见有机物的性质及应用 [解题指导] 1.掌握两类有机反应类型 (1)加成反应:主要以烯烃和苯为代表,碳碳双键、苯环可以发生加成反应。 (2)取代反应:烷烃、苯、乙醇和乙酸均容易发生取代反应。 2.区分三个易错问题 (1)不能区分常见有机物发生反应的反应类型。如塑料的老化发生的是氧化反应,不是加成反应,单糖不能发生水解反应等。 (2)不能灵活区分有机反应的反应条件。如苯与溴水不反应,只与纯液溴反应。 (3)不能准确地对有机物进行分类。如油脂不是高分子化合物。 3.牢记三种物质的特征反应 (1)葡萄糖:在碱性、加热条件下与银氨溶液反应析出银;在碱性、加热条件下与新制氢氧化铜悬浊液反应产生砖红色沉淀。 (2)淀粉:在常温下遇碘变蓝。 (3)蛋白质:浓硝酸可使蛋白质变黄,发生颜色反应。 4.同分异构体判断时必记的三个基团 丙基(C3H7—)有2种,丁基(C4H9—)有4种,戊基(C5H11—)有8种。 [挑战满分](限时10分钟) 1.下列涉及有机物的性质的说法错误的是() A.乙烯和聚氯乙烯都能发生加成反应 B.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了 D.HNO3能与苯、甲苯、甘油、纤维素等有机物发生反应,常用浓硫酸作催作剂 2.下列说法中不正确的是() A.有机化合物中每个碳原子最多形成4个共价键 B.油脂、淀粉、蛋白质在一定条件下都能发生水解反应
C.用溴水既可以鉴别甲烷和乙烯,也可以除去甲烷中的乙烯D.乙烯和苯均能发生氧化反应,说明乙烯和苯分子中均有碳碳双键 3.有机化合物与我们的生活息息相关,下列说法正确的是() A.甲苯的硝化、油脂的皂化均可看作取代反应 B.蛋白质水解生成葡萄糖,放出热量,提供生命活动的能量C.石油裂解的目的是为了提高轻质液体燃料的产量和质量 D.棉花和合成纤维的主要成分是纤维素 4.下列说法正确的是() A.糖类、油脂、蛋白质在一定条件下都能发生水解反应 B.植物油的主要成分是高级脂肪酸 C.棉、麻、羊毛完全燃烧都只生成CO2和H2O D.乙烷的二氯取代物有两种同分异构体 5.下列说法正确的是() A.乙烷与氯气在光照条件下发生加成反应 B.将石蜡油(液态烷烃混合物)加强热分解生成的气体都是烷烃C.甲苯能够使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色 D.乙醇能够被酸性的高锰酸钾溶液直接氧化成乙酸 6.下列与有机物的结构、性质有关的叙述正确的是() A.苯、油脂均不能使酸性KMnO4溶液褪色 B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应C.葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体D.乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同 7.下列关于苯的叙述正确的是()
常见有机溶剂的性质大全
溶剂的定义 溶剂(solvent)这个词广义指在均匀的混合物中含有的一种过量存在的组分。狭义地说,在化学组成上不发生任何变化并能溶解其他物质(一般指固体)的液体,或者与固体发生化学反应并将固体溶解的液体。溶解生成的均匀混合物体系称为溶液。在溶液中过量的成分叫溶剂;量少的成分叫溶质。 溶剂也称为溶媒,即含有溶解溶质的媒质之意。但是在工业上所说的溶剂一般是指能够溶解油脂、蜡、树脂(这一类物质多数在水中不溶解)而形成均匀溶液的单一化合物或者两种以上组成的混合物。这类除水之外的溶剂称为非水溶剂或有机溶剂,水、液氨、液态金属、无机气体等则称为无机溶剂。 溶解现象 溶解本来表示固体或气体物质与液体物质相混合,同时以分子状态均匀分散的一种过程。事实上在多数情况下是描述液体状态的一些物质之间的混合,金与铜、铜与镍等许多金属以原子状态相混合的所谓合金也应看成是一种溶解现象。所以严格地说,只要是两种以上的物质相混合组成一个相的过程就可以称为溶解,生成的相称为溶液。一般在一个相中应呈均匀状态,其构成成分的物质可以以分子状态或原子状态相互混合。 溶解过程比较复杂,有的物质在溶剂中可以以任何比例进行溶解,有的部分溶解,有的则不溶。这些现象是怎样发生的,其影响的因素很多,一般认为与溶解过程有关的因素大致有以下几个方面: ⑴相同分子或原子间的引力与不同分子或原子间的引力的相互关系(主要是范德华引力); ⑵分子的极性引起的分子缔合程度; ⑶分子复合物的生成; ⑷溶剂化作用; ⑸溶剂、溶质的相对分子质量; ⑹溶解活性基团的种类和数目。 化学组成类似的物质相互容易溶解,极性溶剂容易溶解极性物质,非极性溶剂容易溶解非极性物质。例如,水、甲醇和乙醇彼此之间可以互溶;苯、甲苯和乙醚之间也容易互溶,但水与苯,甲醇与苯则不能自由混溶。而且在水或甲醇中易溶的物质难溶于苯或乙醚;反之在苯或乙醚中易溶的却难溶于水或甲醇。这些现象可以用分子的极性或者分子缔合程度大小进行判断。纤维素衍生物易溶于酮、有机酸、酯、醚类等溶剂,这是由于分子中的活性基团与这类溶剂中氧原子相互作用的结果。有的纤维素衍生物在纯溶剂中不溶,但可溶于混合溶剂。例如硝化纤维素能溶于醇、醚混合溶剂;三乙酸纤维素溶于二氯乙烷、甲醇混合溶剂。这可能是由于在溶剂之间,溶质与溶剂之间生成分子复合物,或者发生溶剂化作用的结果。总之,溶解过程能够发生,其物质分子间的内聚力应低于物质分子与溶剂分子之间的吸引力才有可能实现。 溶液浓度的表示方法 溶质在溶剂中溶解的多少,彼此间存在着相对量的关系,通常用以下几种方法表示:⑴质量分数 即混合物中某一物质的质量与混合物的质量之比,符号为ω。 物质B的质量分数(ωB)=物质B的质量(mB)/溶液的质量(m) 例如:氯化钠的质量分数ω(NaCl)=15%,即表示100g该溶液中含有NaCl 15g。 ⑵体积分数 通常用于表示溶质为液体的溶液浓度(略) ⑶物质的量的浓度
常用有机溶剂的物化性质
推荐答案 2006-3-4 00:20 【中文名称】甲苯;甲基苯;苯基甲烷 【英文名称】toluene;toluol;methylbenzene 【结构或分子式】 【相对分子量或原子量】92.14 【密度】0.866 【熔点(℃)】-95 【沸点(℃)】110.8 【闪点(℃)】4.4(闭式) 【蒸气压(Pa)】907(0℃);2920(20℃);74194(100℃) 【折射率】1.4967 【性状】 无色易挥发的液体,有芳香气味。 【溶解情况】 不溶于水,溶于乙醇、乙醚和丙酮。 【用途】 用于制造糖精、染料、药物和炸药等,并用作溶剂。 【制备或来源】 由分馏煤焦油的轻油部分或由催化重整轻汽油馏分而制得。 【其他】 化学性质与苯相像。蒸气与空气形成爆炸性混合物,爆炸极限为1.2~7.0%(体积)。
二甲苯分子量106.16。无色透明液体,芳香气味。有三种异构体:邻二甲苯(o-Xylene),相对密度(25℃/4℃)0.87599,凝固点-25.3℃,沸点144.4℃,折射率1.50295,闪点(闭口)17.4℃,燃点500℃,粘度(25℃)0.75mPa·s;间二甲苯(m-xy1ene),相对密度(25℃/4℃)0.8599,凝固点-47.87℃,沸点139.1℃,闪点(开口)25℃,燃点527.8℃。折射率1. 4946;对二甲苯(p=xy1ene),相对密度(25℃/4℃)0.8567,凝固点13.26℃,沸点138.35℃,闪点(闭口)25℃.折射率1.49325。 一般的二甲苯是混合二甲苯.为邻二甲苯(10%一15%)、间二甲苯(45%-70%)、对二甲苯(15%-25%)及少量乙苯的混合物,相对密度(20 ℃/4℃)约为0.86,溶解度参数δ=8.8-9.0。溶于乙醇、乙醚,不溶于水。易燃,蒸气与空气形成爆炸性混合物,爆炸极限1. 09%-6.6%(vol)。有毒,毒性比苯和甲苯为小,空气中最高容许浓度为100mg /m3。 二甲苯可用作溶剂和稀释剂。贮存于阴凉、通风的库房内,远离火种、热源。 二甲苯根据来源和制法分为石油二甲苯和焦化二甲苯。石油二甲苯是石油轻馏分经予加氢精制,催化重整和分离所得;焦化二甲苯是粗苯经过洗涤、分馏所得。 乙酸乙酯 化学式CH3COOC2H5。又称“醋酸乙酯”,无色、有芬芳气味的液体,沸点77℃,熔点-83.6℃,密度0.901g/cm3,溶于乙醇、氯仿、乙醚和苯等。易起水解和皂化反应。可燃,其蒸气和空气形成爆炸混合物。在香料和油漆工业中用作溶剂,也是有机合成的重要原料。 (CH3COOC2H5) 无色液体,有水果香味。沸点77℃。与醇醚互溶,微溶于水,比水轻。易燃,与水在一定条件下水解成对应的醇和酸,在稀硫酸条件下加热,发生可逆反应生成乙醇和乙酸,反应不够完全。在氢氧化钠溶液中加热,水解相当完全,生成乙酸钠和乙醇。主要用作油漆、涂料、硝酸纤维素、树脂等的溶剂。实验室里用乙醇与乙酸在浓硫酸的吸水和催化作用下加热制取。反应器常用烧瓶或试管,并有回流装置,并用冷凝管蒸出乙酸乙酯。接受器里放有饱和碳酸钠溶液,以除去酯中杂入的乙酸并降低酯在水里的溶解度。工业上还用乙醛缩合法制取。需催化剂、助催化剂,使2分子乙醛生成1分子乙酸乙酯。 无色、易挥发、中性的可燃性液体,带有果香气味。熔点为-83.6℃,沸点为77.06℃,相对密度为0.9003,微溶于水。 乙酸乙酯具有酯的一般性质。它主要由乙醇与乙酸、乙酸酐等合成。乙醇与乙酸的酯化反应为可逆平衡反应,速率很慢,加入少量酸作催化剂可加快达成平衡的
有机物的物理性质规律
有机物物理性质的主要规律 河北省宣化县第一中学栾春武 一、密度 物质的密度是指单位体积里所含物质的质量,它与该物质的相对分子质量、分子半径等因素有关。一般来说,有机物的密度与分子中相对原子质量大的原子所占质量分数成正比。例如,烷、烯、炔及苯的同系物等物质的密度均小于水的密度,并且它们的密度均随分子中碳原子数的增加和碳元素的质量分数的增大而增大;而一卤代烷、饱和一元醇随分子中碳原子数的增加,氯元素、氧元素的质量分数降低,密度逐渐减小。 二、溶解性 有机物一般不易溶于水,而易溶于有机溶剂,这是因为有机物分子大多数是非极性分子或弱极性分子,含有憎水基。根据“相似相溶”原理,水是极性分子,只有当某有机物分子中含有亲水基团时,则该有机物就可能溶于水。 亲水基一般包括:-OH、-CHO、COOH等;憎水基一般包括:-R、-NO2、-X、-COOR等。 1. 能溶于水的有机物: ① 小分子醇:CH3OH、C2H5OH、CH2OHCH2OH、甘油等; ②小分子醛:HCHO、CH3CHO、CH3CH2CHO等; ③小分子羧酸:HCOOH、CH3COOH、CH3CH2COOH等; ④低糖:葡萄糖(C6H12O6)、果糖(C6H12O6)、蔗糖(C12H22O11); ⑤氨基酸:CH3CH(NH2)COOH等。 一般来说,低级醇、低级醛、低级酸,单糖和二糖水溶性好,即亲水基占得比重相对较大,憎水基占得比重相对较小,故能溶于水。
2. 不易溶于水的有机物: ① 烷、稀、炔、芳香烃等烃类均不溶于水,因为其分子内不含极性基团; ② 卤代烃:CH3Cl、CHCl3、CCl4、CH3CH2Br、等均不溶于水; ③ 硝基化合物:硝基苯、TNT等; ④ 酯:CH3COOC2H5、油脂等; ⑤ 醚:CH3OCH3、C2H5OC2H5等; ⑥ 大分子化合物或高分子化合物:如高级脂肪酸、塑料、橡胶、纤维等。 一般来说,液态烃、一氯代烃、苯及其同系物、酯类物质不溶于水且密度比水小;硝基苯、溴苯、四氯化碳、氯仿、溴代烃、碘代烃不溶于水且密度比水大。 3. 有机物在汽油、苯、四氯化碳等有机溶剂中的溶解性与在水中的相反: 如乙醇是由较小憎水基团C2H5和亲水基团-OH构成,所以乙醇易溶于水,同时因含有憎水基团,所以必定也溶于四氯化碳等有机溶剂中。其它醇类物质由于都含有亲水基团-OH,小分子都溶于水,但在水中的溶解度随着憎水基团的不断增大而逐渐减小,在四氯化碳等有机溶剂中的溶解度则逐渐增大。 4. 特殊物质(苯酚)在常温时,在水里溶解度不大,当温度高于65℃ 时,能和水以任意比例互溶。 三、熔、沸点 熔、沸点是物质状态变化的标志,有机物熔、沸点的高低与分之间的相互作用、分子的几何形状等因素有关。 1. 结构相似的有机物,相对分子质量越大,分子间作用力越大,其熔、沸点越高。如链烃同系物的沸点,随着相对分子质量的增大而升高,状态由气态(分子中碳原子数小于等于4者及新戊烷通常为气态)到液态,最后变为固态。
各类有机物的通式
各类有机物的通式、及主要化学性质 烷烃CnH2n+2 仅含C—C键与卤素等发生取代反应、热分解、不与高锰酸钾、溴水、强酸强碱反应 烯烃CnH2n 含C==C键与卤素等发生加成反应、与高锰酸钾发生氧化反应、聚合反应、加聚反应 炔烃CnH2n-2 含C≡C键与卤素等发生加成反应、与高锰酸钾发生氧化反应、聚合反应苯(芳香烃)CnH2n-6与卤素等发生取代反应、与氢气等发生加成反应 (甲苯、乙苯等苯的同系物可以与高锰酸钾发生氧化反应) 卤代烃:CnH2n+1X 醇:CnH2n+1OH或CnH2n+2O 苯酚:遇到FeCl3溶液显紫色醛:CnH2nO 羧酸:CnH2nO2 酯:CnH2nO2 有机反应类型: 取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。 加成反应:有机物分子里不饱和的碳原子跟其他原子或原子团直接结合的反应。 聚合反应:一种单体通过不饱和键相互加成而形成高分子化合物的反应。 加聚反应:一种或多种单体通过不饱和键相互加成而形成高分子化合物的反应。 消去反应:从一个分子脱去一个小分子(如水.卤化氢),因而生成不饱和化合物的反应。 氧化反应:有机物得氧或去氢的反应。 还原反应:有机物加氢或去氧的反应。 酯化反应:醇和酸起作用生成酯和水的反应。 水解反应:化合物和水反应生成两种或多种物质的反应(有卤代烃、酯、糖等) 甲烷燃烧 CH4+2O2→CO2+2H2O(条件为点燃) 甲烷隔绝空气高温分解 甲烷分解很复杂,以下是最终分解。CH4→C+2H2(条件为高温高压,催化剂) 甲烷和氯气发生取代反应 CH4+Cl2→CH3Cl+HCl CH3Cl+Cl2→CH2Cl2+HCl CH2Cl2+Cl2→CHCl3+HCl CHCl3+Cl2→CCl4+HCl (条件都为光照。)
最新常用有机溶剂的物化性质
常用有机溶剂的物化 性质
推荐答案 2006-3-4 00:20 【中文名称】甲苯;甲基苯;苯基甲烷 【英文名称】toluene;toluol;methylbenzene 【结构或分子式】 【相对分子量或原子量】92.14 【密度】0.866 【熔点(℃)】-95 【沸点(℃)】110.8 【闪点(℃)】4.4(闭式) 【蒸气压(Pa)】907(0℃);2920(20℃);74194(100℃)【折射率】1.4967 【性状】 无色易挥发的液体,有芳香气味。 【溶解情况】
不溶于水,溶于乙醇、乙醚和丙酮。 【用途】 用于制造糖精、染料、药物和炸药等,并用作溶剂。 【制备或来源】 由分馏煤焦油的轻油部分或由催化重整轻汽油馏分而制得。 【其他】 化学性质与苯相像。蒸气与空气形成爆炸性混合物,爆炸极限为1.2~7.0%(体积)。 二甲苯分子量106.16。无色透明液体,芳香气味。有三种异构体:邻二甲苯(o-Xylene),相对密度(25℃/4℃)0.87599,凝固点-25.3℃,沸点144.4℃,折射率1.50295,闪点(闭口)17.4℃,燃点500℃,粘度(25℃)0.75mPa·s;间二甲苯(m-xy1ene),相对密度(25℃/4℃)0.8599,凝固点-47.87℃,沸点139.1℃,闪点(开口)25℃,燃点527.8℃。折射率1. 4946;对二甲苯(p=xy1ene),相对密度(25℃/4℃)0.8567,凝固点13.26℃,沸点138.35℃,闪点(闭口)25℃.折射率1.49325。 一般的二甲苯是混合二甲苯.为邻二甲苯(10%一15%)、间二甲苯(45%-70%)、对二甲苯(15%-25%)及少量乙苯的混合物,相对密度(20 ℃/4℃)约为0.86,溶解度参数δ=8.8-9.0。溶于乙醇、乙醚,不溶于水。易燃,蒸气与空气形成爆炸性混合物,爆炸极限1. 09%-6.6%(vol)。有毒,毒性比苯和甲苯为小,空气中最高容许浓度为100mg/m3。 二甲苯可用作溶剂和稀释剂。贮存于阴凉、通风的库房内,远离火种、热源。 二甲苯根据来源和制法分为石油二甲苯和焦化二甲苯。石油二甲苯是石油轻馏分经予加氢精制,催化重整和分离所得;焦化二甲苯是粗苯经过洗涤、分馏所得。
有机物的物理性质规律
有机物的物理性质规律 有机物的物理性质与化学性质同等重要,且“结构决定性质,性质反映结构”不仅表现在化学性质中,同时也体现在某些物理性质上。有机物一些物理性质存在着内在规律,如果抓住其中的规律,可以更好地认识有机物。 一、熔沸点 有机物微粒间的作用是分子间作用力,分子间的作用力比较小,因此烃的熔沸点比较低。对于同系物,随着相对分子质量的增加,分子间作用力增大,因此同系物的熔沸点随着相对分子质量的增大而升高。 1. 烃、卤代烃及醛 各种烃的同系物、卤代烃及醛的熔沸点随着分子中碳原子数的增加而升高。如:4CH 、1048362H C H C H C 、、都是烷烃,熔沸点的高低顺序为:10483624H C H C H C CH <<<;846342H C H C H C 、、都是烯烃,熔沸点的高低顺序为:846342H C H C H C <<;再有Cl CH CH Cl CH 233<,CHO CH HCHO 3<等。 同类型的同分异构体之间,主链上碳原子数目越多,烃的熔沸点越高;支链数目越多,空间位置越对称,熔沸点越低。如4332233323)CH (C CH CHCH )CH (CH )CH (CH >>。 2. 醇 由于分子中含有—OH ,醇分子之间存在氢键,分子间的作用力较一般的分子间作用力强,因此与相对分子质量相近的烃比较,醇的熔沸点高的多,如OH CH CH 23的沸点为78℃,323CH CH CH 的沸点为-42℃,23CH CH CH =的沸点为-48℃。 影响醇的沸点的因素有: (1)分子中—OH 个数的多少:—OH 个数越多,沸点越高。如乙醇的沸点为78℃,乙二醇的沸点为179℃。 (2)分子中碳原子个数的多少:碳原子数越多,沸点越高。如甲醇的沸点为65℃,乙醇的沸点为78℃。 3. 羧酸 羧酸分子中含有—COOH ,分子之间存在氢键,不仅羧酸分子间羟基氧和羟基氢之间存在氢键,而且羧酸分子间羰基氧和羟基氢之间也存在氢键,因此羧酸分子之间形成氢键的机会比相对分子质量相近的醇多,因此羧酸的沸点比相对分子质量相近的醇的沸点高,如1-
常用有机溶剂按毒性大小分类表
常用有机溶剂按毒性大小分类表 一、第一类有机溶剂: 1、三氯甲烷 2、1,1,2,2,-四氯乙烷 3、四氯化碳 4、1,2二氯乙烯 5、1,2二氯乙烷 6、二硫化碳 7、三氯乙烯 8、苯 9、由以上溶剂组成的混合物 二、第二类有机溶剂: 1、丙酮 2、异戊醇 3、异丁醇 4、异丙醇 5、乙醚 6、乙二醇乙醚 7、乙二醇乙醚乙酸酯 8、乙二醇丁醚 9、乙二醇甲醚 10、邻—二氯苯 11、二甲苯 12、甲酚 13、氯苯 14、乙酸戊酯 15、乙酸异戊酯
16、乙酸异丁酯 17、乙酸异丙酯 18、乙酸乙酯 19、乙酸丙酯 20、乙酸丁酯 21、乙酸甲酯 22、苯乙烯 23、1,4—二氧杂环己烷 24、四氯乙烯 25、环己醇 26、环己酮 27、1—丁醇 28、2—丁醇 29、甲苯 30、二氯甲烷 31、甲醇 32、甲基异丁基甲酮 33、甲基环己醇 34、甲基环己酮 35、甲丁酮 36、1,1,1—三氯乙烷 37、1,1,2—三氯乙烷 38、丁酮 39、二甲基甲酰胺 40、四氢呋喃 41、正己烷 42、由以上溶剂组成的混合物
三、第三类有机溶剂 1、汽油 2、煤焦油精 3、石油醚 4、石油精 5、轻油精 6、松节油 7、矿油精 8、由以上溶剂组成的混合物 四、有机溶剂按其化学结构可分为10大类: 1、芳香烃类:苯、甲苯、二甲苯等; 2、脂肪烃类:戊烷、己烷、辛烷等; 3、脂环烃类:环己烷、环己酮、甲苯环己酮等; 4、卤化烃类:氯苯、二氯苯、二氯甲烷等; 5、醇类:甲醇、乙醇、异丙醇等; 6、醚类:乙醚、环氧丙烷等; 7、酯类:醋酸甲酯、醋酸乙酯、醋酸丙酯等; 8、酮类:丙酮、甲基丁酮、甲基异丁酮等; 9、二醇衍生物:乙二醇单甲醚、乙二醇单乙醚、乙二醇单丁醚等; 10、其他:乙腈、吡啶、苯酚等。 经常使用有机溶剂,如,乙醇、苯乙烯、全氯乙烯、三氯乙烯、乙烯乙二醇醚和三乙醇胺。 五、常用有机溶剂对人体的危害 1、液氨:剧毒性、腐蚀性 2、液态二氧化硫:剧毒
常见有机溶剂极性表
有机溶剂是能溶解一些不溶于水的物质的一类有机化合物,其特点是在常温常压下呈液态,具有较大的挥发性,在溶解过程中,溶质与溶剂的性质均无改变。 有机溶剂的种类较多,按其化学结构可分为10大类:①芳香烃类:苯、甲苯、二甲苯等; ②脂肪烃类:戊烷、己烷、辛烷等;③脂环烃类:环己烷、环己酮、甲苯环己酮等;④卤化烃类:氯苯、二氯苯、二氯甲烷等;⑤醇类:甲醇、乙醇、异丙醇等;⑥醚类:乙醚、环氧丙烷等;⑦酯类:醋酸甲酯、醋酸乙酯、醋酸丙酯等;⑧酮类:丙酮、甲基丁酮、甲基异丁酮等;⑨二醇衍生物:乙二醇单甲醚、乙二醇单乙醚、乙二醇单丁醚等;⑩其他:乙腈、吡啶、苯酚等。 有机溶剂具有脂溶性,因此除经呼吸道和消化道进入机体内外,尚可经完整的皮肤迅速吸收,有机溶剂吸收入人体后,将作用于富含脂类物质的神经、血液系统,以及肝肾等实质脏器,同时对皮肤和粘膜也有一定的刺激性。不同有机溶剂其作用的主要靶器官和作用的强弱也不同,这决定于每一种有机溶剂的化学结构、溶解度、接触浓度和时间,以及机体的敏感性。 常用溶剂的极性顺序: 水(极性最大) > 甲酰胺 > 乙腈 > 甲醇 > 乙醇 > 丙醇 > 丙酮 > 二氧六环 > 四氢呋喃 > 甲乙酮 > 正丁醇 > 醋酸乙酯 > 乙醚 > 异丙醚 > 二氯甲烷 > 氯仿 > 溴乙烷 > 苯 > 氯丙烷 > 甲苯 > 四氯化碳 > 二硫化碳 > 环己烷 > 己烷 > 庚 烷 > 煤油(极性最小) 有机溶剂的极性根据官能团和对称性可初步判断,具体的需参照极性参数,如下
表示有机溶剂的极性,关系到其物理化学性质、如介电常数、偶极矩或折射率。这种表示方法把所有的溶剂看作是连续作用的介质,而不是看作由各个分子组成的非连续统一体,并且未考虑到溶剂和溶质之间的特殊的相互作用。
常见有机溶剂地溶解性汇总
常用溶剂的沸点、溶解性和毒性 溶剂名称沸点(101.3kPa)溶解性毒性 液氨-33.35℃特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性 液态二氧化硫-10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒 甲胺-6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐 易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃 二甲胺7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性 石油醚不溶于水,与丙酮、***** 、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似 ***** 34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶***** 性 戊烷36.1 与乙醇、***** 等多数有机溶剂混溶低毒性员?婷疋0? 二氯甲烷39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,***** 性强 二硫化碳46.23 微溶与水,与多种有机溶剂混溶***** 性,强刺激性 溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大 丙酮56.12 与水、醇、醚、烃混溶低毒,类乙醇,但较大 1,1-二氯乙烷57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性 氯仿61.15 与乙醇、***** 、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强***** 性 甲醇64.5 与水、***** 、醇、酯、卤代烃、苯、酮混溶中等毒性,***** 性 四氢呋喃66 优良溶剂,与水混溶,很好的溶解乙醇、***** 、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒己烷68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。***** 性,刺激性 三氟代乙酸71.78 与水,乙醇,*****, 丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物 1,1,1-三氯乙烷74.0 与丙酮、、甲醇、***** 、苯、四氯化碳等有机溶剂混溶低毒类溶剂 四氯化碳76.75 与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强 乙酸乙酯77.112 与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,***** 性 乙醇78.3 与水、***** 、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,***** 性 丁酮79.64 与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮 苯80.10 难溶于水,与甘油、乙二醇、乙醇、氯仿、***** 、、四氯化碳、二硫化碳、丙酮、甲苯、二 甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性 乙睛81.60 与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃 混溶,但是不与饱和烃混溶中等毒性,大量吸入蒸气,引起急性中毒 异丙醇82.40 与乙醇、***** 、氯仿、水混溶微毒,类似乙醇 1,2-二氯乙烷83.48 与乙醇、***** 、氯仿、四氯化碳等多种有机溶剂混溶高毒性、致癌 乙二醇二甲醚85.2 溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶。能溶解各种树脂, 还是二氧化硫、氯代甲烷、乙烯等气体的优良溶剂吸入和经口低毒 三氯乙烯87.19 不溶于水,与乙醇.***** 、丙酮、苯、乙酸乙酯、脂肪族氯代烃、汽油混溶有机有毒品_ 三乙胺89.6 水:18.7 以下混溶,以上微溶。易溶于氯仿、丙酮,溶于乙醇、***** 易爆,皮肤黏膜刺 激性强 丙睛97.35 溶解醇、醚、DMF 、乙二胺等有机物,与多种金属盐形成加成有机物高度性,与氢氰 酸相似 庚烷98.4 与己烷类似低毒,刺激性、***** 性
常用有机溶剂
一、乙醇(ethyl alcohol,ethanol) 1.理化性质: (1)分子式C2H6O (2)相对分子质量46.07 (3)结构式CH3CH2OH (4)外观与性状:无色液体,有酒香。 (5)熔点(℃):-114.1 (6)沸点(℃):78.3 (7)相对密度(水=1):0.79 (8)相对密度(空气=1):1.59 (9)溶解性:与水混溶,可混溶于醚、氯仿、甘油等多数有机溶剂。(10)禁忌物:强氧化剂、酸类、酸酐、碱金属、胺类。 危险类别: (1)燃烧性:易燃 (2)闪点(℃):12 (3)引燃温度(℃):363 (4)爆炸下限(%):3.3 (5)爆炸上限(%):19.0 二、甲醇(methyl alcohol,Methanol) 1. 理化性质: (1)分子式CH4O (2)相对分子质量32 (3)结构式CH3OH (4)外观与性状:无色澄清液体,有刺激性气味。 (5)熔点(℃):-97.8 (6)沸点(℃):64.8 (7)相对密度(水=1):0.79 (8)相对密度(空气=1):1.11 (9)溶解性:与水混溶,可混溶于醇、醚等多数有机溶剂。 (10)禁忌物:强氧化剂、酸类、酸酐、碱金属。 危险类别: (1)燃烧性:易燃 (2)闪点(℃):11 (3)引燃温度(℃):385 (4)爆炸下限(%):5.5 (5)爆炸上限(%):44.0
乙酸乙酯,醋酸乙酯(ethyl acetate,acetic ester) 1.理化性质: (1)分子式:C4H8O2 (2)相对分子质量88.10 (3)结构式 CH3-C-OCH2CH3 (4)外观与性状:无色澄清液体,有芳香气味,易挥发。 (5)熔点(℃):-83.6 (6)沸点(℃):77.2 (7)相对密度(水=1):0.90 (8)相对密度(空气=1):3.04 (9)溶解性:微溶于水,可混溶于醇、酮、醚、氯仿等多数有机溶剂。(10)禁忌物:强氧化剂、酸类、碱类。 危险类别: (1)燃烧性:易燃 (2)闪点(℃):-4 (3)引燃温度(℃):426 (4)爆炸下限(%):2.0 (5)爆炸上限(%):11.5 二氯甲烷(dichloromethane) 1.理化性质: (1)分子式:CH2Cl2 (2)相对分子质量84.94 (3)结构式H2CCl2 (4)外观与性状:无色透明液体,有芳香气味。 (5)熔点(℃):-96.7 (6)沸点(℃):39.8 (7)相对密度(水=1):1.33 (8)相对密度(空气=1):2.93 (9)溶解性:微溶于水,溶于乙醇、乙醚。 (10)禁忌物:碱金属、铝。 危险类别: (1)燃烧性:可燃 (2)闪点(℃): (3)引燃温度(℃):615 (4)爆炸下限(%):12 (5)爆炸上限(%):19
高中化学常见物质的物理性质归纳
高中化学常见物质的物理性质归纳 1.颜色的规律 (1)常见物质颜色 以红色为基色的物质 红色:难溶于水的Cu,Cu2O,Fe2O3,HgO等 碱液中的酚酞酸液中甲基橙石蕊及pH试纸遇到较强酸时及品红溶液 橙红色:浓溴水甲基橙溶液氧化汞等 棕红色:Fe(OH)3固体Fe(OH)3水溶胶体等 以黄色为基色的物质 黄色:难溶于水的金碘化银磷酸银硫磺黄铁矿黄铜矿(CuFeS2)等 溶于水的FeCl3甲基橙在碱液中钠离子焰色及TNT等 浅黄色:溴化银碳酦银硫沉淀硫在CS2中的溶液,还有黄磷Na2O2氟气 棕黄色:铜在氯气中燃烧生成CuCl2的烟 以棕或褐色为基色的物质 碘水浅棕色碘酒棕褐色铁在氯气中燃烧生成FeCl3的烟等 以蓝色为基色的物质 蓝色:新制Cu(OH)2固体胆矾硝酸铜溶液中淀粉与碘变蓝石蕊试液碱变蓝pH试纸与弱碱变蓝等 浅蓝色:臭氧液氧等 蓝色火焰:硫硫化氢一氧化碳的火焰甲烷氢气火焰(蓝色易受干扰) 以绿色为色的物质 浅绿色:Cu2(OH)2CO3,FeCl2,FeSO4?7H2O 深黑绿色:K2MnO4 绿色:浓CuCl2溶液pH试纸在约pH=8时的颜色黄绿色:Cl2及其CCl4的萃取液以紫色为基色的物质 KMnO4为深紫色其溶液为红紫色碘在CCl4萃取液碘蒸气中性pH试纸的颜色K+离子的焰色等 以黑色为基色的物质 黑色:碳粉活性碳木碳氧化铜四氧化三铁硫化亚铜(Cu2S) 浅黑色:铁粉 棕黑色:二氧化锰 白色物质 难溶于水和稀酸的:AgCl,BaSO3,PbSO4; 难溶于水的但易溶于稀酸:BaSO3,Ba3(PO4)2,BaCO3,CaCO3,Ca3(PO4)2,CaHPO4,Al(OH)3,Al2O3,ZnO,Zn(OH)2,ZnS,Fe(OH)2,Ag2SO3,CaSO3等; 微溶于水的:CaSO4,Ca(OH)2,PbCl2,MgCO3,Ag2SO4; 与水反应的氧化物:完全反应的:BaO,CaO,Na2O;不完全反应的:MgO (2)离子在水溶液或水合晶体的颜色 水合离子带色的: Fe2+:浅绿色;Cu2+:蓝色; Fe3+:浅紫色呈黄色因有[FeCl4(H2O)2] 2-; MnO4-:紫色苯酚与FeCl3的反应开成的紫色主族元素在水溶液中的离子(包括含氧酸根)无色 运用上述规律便于记忆溶液或结晶水合物的颜色 (3)主族金属单质颜色的特殊性 铯:带微黄色钡:带微黄色铅:带蓝白色铋:带微红色
