实验5 大肠杆菌感受态细胞的制备

学院:专业:姓名:学号:
实验5 大肠杆菌感受态细胞的制备、转化和筛选
实验目的
1、了解和掌握大肠杆菌感受态细胞的制备方法的原理和操作方法。
2、了解和掌握质粒DNA转化大肠杆菌细胞的原理和方法。
实验原理
该技术是将外源DNA分子引入大肠杆菌细胞,使之获得新的遗传性状的一种手段,它是微生物遗传、分子遗传、基因工程等研究领域的基本实验技术。细胞经过一些特殊方法(电击法、氯化钙、Rbcl/Kcl等)处理后,细胞膜的通透性发生了暂时性的改变,成为能允许外源DNA分子进入的细胞,即感受态细胞。
在实验室中感受态细胞的制备经常用到的是氯化钙法,该方法的原理是将快速生长中的大肠杆菌置于经低温预处理的低渗氯化钙中,便会造成细胞膨胀(可能局部原生质体化),使细胞处于容易吸收外源DNA 的状态。
质粒DNA转化大肠杆菌目前主要采用的是热激法,其原理是大肠杆菌在0℃氯化钙低渗溶液中,细菌细胞膨胀成球形,转化混合物中的DNA形成抗DNased的羟基-钙磷酸复合物粘附于细胞表面,经42℃短时间热激处理,使处于感受态的大肠杆菌细胞吸收DNA复合物,在未加抗生素的培养基生长一段时间后,大肠杆菌细胞复原并重新开始分裂增殖.由于在被转化的细胞中,重组子基因得到表达,在含有抗生素的培养基平板上可挑选所需的转化子。
在分子生物学技术中的一类用于选择转化细菌的抗性基因,通常是一些抗生素抗性基因,比如对氨卡青霉素、四环素、氯霉素、卡那霉素以及潮霉素等具有抗性基因,这些基因被构建在质粒载体上。这样,通过在培养基中加入特定的抗生素就可以筛选得到转化的基因。
实验步骤
1、感受态细胞制备(小量制备)
(1)从LB平板上挑取新活化的PBluescript菌落,接种培养,直至对数生长后期,,将该菌悬液以1:100~1:50的比例接种于100mlLB液体培养基中,37℃振荡培养2~3h至OD600=0.5左右。
(2)取1ml细菌培养物置于1.5ml的EP管中,冰浴15min,8000r/min,离心1min,收集菌体,冰浴放置。
(3)取1ml的预冷的氯化钙悬浮菌体,8000r/min,离心1min,收集菌体,冰浴放置。
(4)取1ml的预冷的氯化钙悬浮菌体,冰浴30min,8000r/min,离心1min,收集菌体,冰浴放置。
(5)加入200μl预冷氯化钙,即得可用于转化的感受态细胞。
2、质粒在大肠杆菌中的转化
(6)将上述得到的感受态细胞中加入2μl质粒DNA溶液,轻轻摇匀,冰上放置30min.
(7)42℃水浴中热击90s,热击后迅速置于冰上4min.
(8)向管中加入1mlLB液体培养基(不含抗生素),混匀后37℃振荡培养1h,使细菌恢复正常生长状态,并表达质粒编码的抗生素抗性基因(Amp)。(9)将上述菌液摇匀后去100μl涂布于含Amp的筛选平板上,正面向上放置2min,待菌液完全被培养基吸收后倒置培养皿,37℃培养12~16h.
3、设置对照组
(一)受体菌对照(检验受体菌是否含有质粒)
在上述步骤(6)中在感受态细胞中加入2μl的质粒改为加2μl的水,别的如上述步骤操作。
(二)质粒对照组(检验质粒是否受到污染)
在EP管中加入200μl的预冷的氯化钙,再如上述(6)~(9)步骤进行
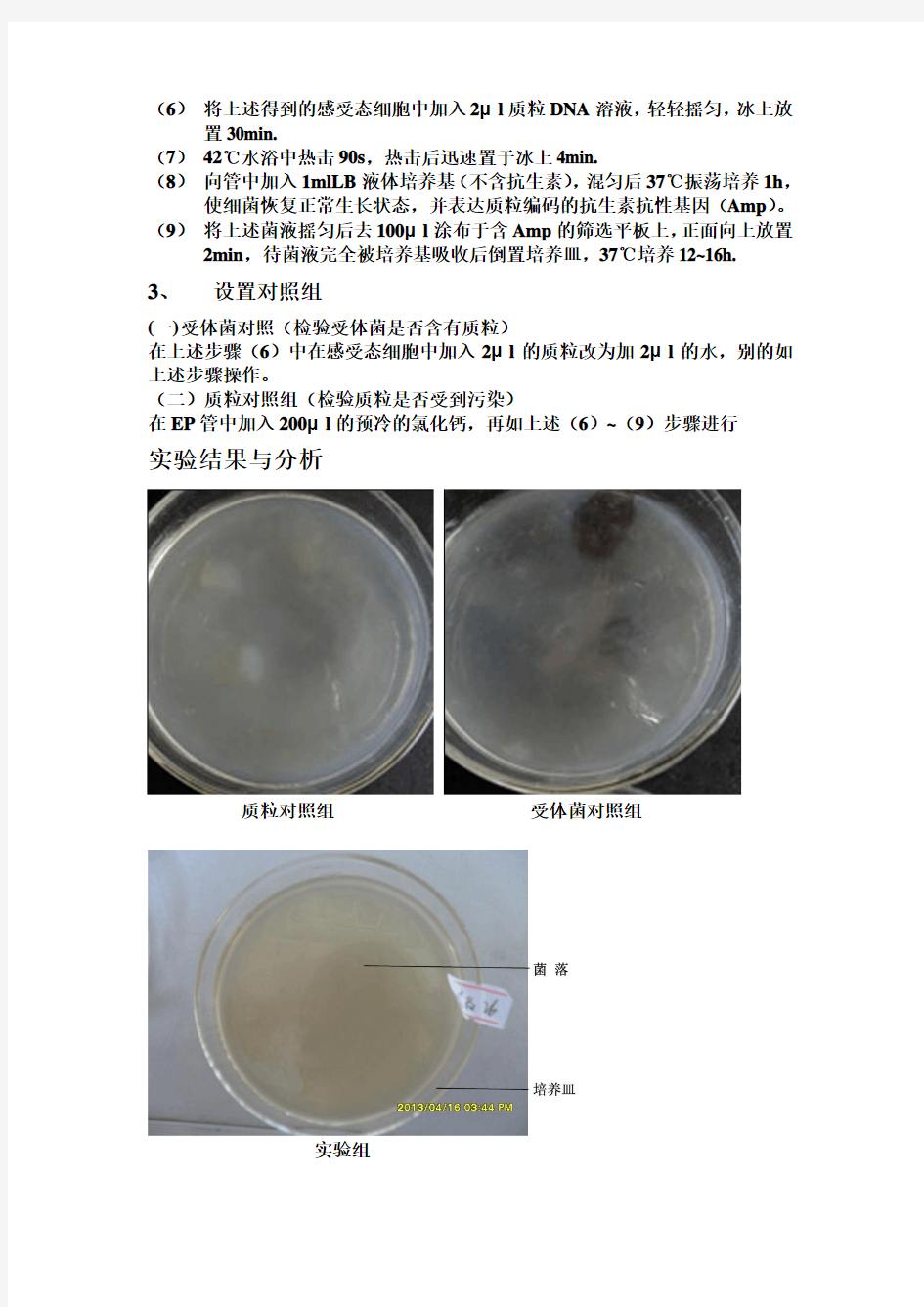
实验结果与分析
质粒对照组受体菌对照组
实验组
实验结果:
此次实验为大肠杆菌感受态细胞的制备、转化和筛选,
步骤主要为用氯化钙法制备感受态细胞以及用热激法来将质粒DNA转化大肠杆菌筛选,从而得到大肠杆菌感受态细胞,我的实验结果如图所示
分析:
一、从质粒对照组以及实验组中无杂菌可知,质粒没有受到污染,在操作
过程中也没受到污染
二、从受体菌对照组无菌可知所用细菌中不含质粒。
三、从实验组图片中可知,在操作过程无杂菌污染,实验比较成功,但是
菌群不多,比较模糊,我觉问题应出现在下列几个方面:
1、应是在步骤(9)中从EP管中所取的量不足或者只取了上层清液,
造成细菌较少;
2、培养的时间较少,细菌还没有完全的长出来;
3、大部分大肠杆菌的转化不完全,没有充分表达质粒编码的抗生素抗
性基因,造成在培养基上不生长。
大肠杆菌感受态细胞的制备实验具体步骤及说明
大肠杆菌感受态细胞的制备实验具体步骤及详细说明 带有外源DNA 的重组质粒,在体外构建后,导入宿主细胞,随着细胞的大量复制、繁殖,才能够有机会获得纯的重组质粒DNA,该过程称之为转化过程。受体细胞经过一些特殊方法(如:CaCl2,RuCl 等化学试剂)的处理后,细胞膜的通透性发生变化,能容许外源DNA 的载体分子通过。 带有外源DNA 的重组质粒,在体外构建后,导入宿主细胞,随着细胞的大量复制、繁殖,才能够有机会获得纯的重组质粒DNA,该过程称之为转化过程。受体细胞经过一些特殊方法(如:CaCl2,RuCl 等化学试剂)的处理后,细胞膜的通透性发生变化,能容许外源DNA 的载体分子通过。 具体步骤 1、从37℃培养16-20 h的平板中挑取一个单菌落(直径2-3 mm),转到一个含有100 ml LB或SOB培养基的1L烧瓶中。于37℃剧烈振摇培养3 h。一般经验,1 OD600约含有大肠杆菌DH5α 109个/mL。 2、将细菌转移到一个无菌、一次性使用的、用冰预冷的50 ml聚丙烯管中,在冰上放置10 min,使培养物冷却至0℃。 3、于4℃用Sorvall GS3特头(或与之相当的转头)以4 100 r/min离心10 min,以回收细胞。 4、倒出培养液,将管倒置1 min以使最后的痕量培养液流尽。
5、每50 ml初始培养液用30 ml预冷的0.1 mol/LCaCl2-MgCl2溶液(80 mmol/L MgCl2,20 mmol/L CaCl2)重悬每份细胞沉淀。 6、于4℃用Sorvall GS3转头(或与之相当的转头)以41 00 r/min离心10 min,以回收细胞。 7、倒出培养液,将管倒置1 min以使最后的痕量培养液流尽。 8、每50 ml初始培养物用2 ml用冰预冷的0.1 mol/L CaCl2(或TFB)重悬每份细胞沉淀。 9、此时,可以用新鲜制备的感受态细胞直接做转化实验,也可以将细胞冻存于- 70℃。 注意事项 1. 为达到高效转化,活细胞数务必少于108个细胞/mL,对于大多散大脑杆菌来说,这相当于OD值为0.4左右。为保证细菌培养物的生长密度不致过高,可每隔15-20 min测定OD600值来监测,用监测的时间及OD值列一个图表,以便预测培养物的OD600值到0.4的时间,当OD600值达到0.35时,收获细菌培养物。 2. 在菌株与菌株之间,OD值与每毫升中活细胞散间的关系变化很大,因此有必要通过漶量特定脑杆菌的生长培养物在生长周期的不同时相的OD600值,并
CaCl2法制备大肠杆菌感受态细胞
CaCl2法制备大肠杆菌感受态细胞 原理: 转化(Transformation):将外源DNA分子引入受体细菌,使之获得新的遗传性状。 受体细菌一般是限制修饰系统缺陷的变异株,不含限制性内切酶和甲基化酶的突变体(R-,M-),可以容忍外源DNA分子进入体内并稳定地遗传给后代。受体细胞经过一些特殊方法,如电击或CaCl2、RbCl/KCl等化学试剂的处理后,细胞膜的通透性增高,成为感受态细胞(Compenent cells),使外源DNA分子得以进入。 目前常用的感受态细胞制备方法有CaCl2和RbCl/KCl法,RbCl/KCl法制备的感受态细胞转化效率较高,但CaCl2法简便易行,且其转化效率完全可以满足一般实验的要求,制备出的感受态细胞暂时不用时,可加入无菌甘油至总体积15%,于-70℃保存半年之久,因此CaCl2法为使用更广泛。 准备: 1、配制0.05mol/L CaCl2-15%甘油(可用0.1mol/L CaCl2和30%甘油等体积混合) 混合溶液,高温高压灭菌; 注:CaCl2必须为分析纯以上。 2、实验中所需的所有试管、培养瓶、离心管等均要用去离子水彻底清洗干净, 高温高压灭菌; 注:最好有制备感受态细菌专用的一套实验器材。 3、受体菌的培养:从非选择性LB平板上挑取E.coli单菌落,接种于3-5ml LB液 体培养基 ( )中,37℃振荡培养过 夜至对数生长中后期。将该菌悬液以1:100的比例接种于50~100ml LB液体培养基中,37℃振荡培养2.5小时至OD600=0.5。注:培养时间不宜超过2.5小时,否则不能达到最高转化效率。 实验步骤: 1、细菌的收获:培养液冰浴5分钟后,4℃5000g离心5分钟。 注:(1)冰浴时间不要超过10分钟;(2)或者4℃8000g离心2分钟,速度太快或时间太长对细菌状态不利,并且不利于下步洗涤。(3)若出现很多黑色沉淀(细菌碎片),说明有多量细菌死亡,此时细菌状态并不好,但若只有少量黑色沉淀,或对转化效率要求不高,亦可继续进行。 2、用预冷的去离子水洗涤沉淀,4℃5000g离心5分钟。 注:(1)洗去细菌碎片和残留的培养液;(2)洗涤时间宜短不宜长。 3、沉淀加入2ml预冷的0.05mol/L CaCl2-15%甘油混合溶液,轻吹散,冰浴5分 钟,4℃5000g离心5分钟。 注:此时可见细菌沉淀为白色,体积也胀大为最初沉淀体积的数倍。 4、沉淀加入2ml预冷的0.05mol/L CaCl2-15%甘油混合溶液,轻吹散,即成为感 受态细胞悬液。分装成50~100μl的小份,贮存于-70℃可保存半年。
农杆菌感受态细胞的制备原理和实验步骤及验证
农杆菌电击感受态的制备及电击转化 表达载体pB-2mb-FRO-1.7A和pB-2mb-1.7A空载体的农杆菌(EHA105)电击转化 (1)抽提纯化pB-2mb-FRO-1.7A和pB-2mb-1.7A空载体的重组质粒 pB-2mb-FRO-1.7A重组载体和pB-2mβ-1.7A空载体的(DH5α)菌种接种于5ml LB(含卡那霉素50mg/L)液体培养基中,37℃,200rpm震荡培养过夜。按V-GENE公司的质粒提取试剂盒提取pB-2mb-FRO-1.7A重组质粒。 (2)取200ml型号的电击杯用无水乙醇浸泡,晾干。 (3)农杆菌EHA105电击预备处理。 I. 接种于5ml YEP(含链霉素Sm50mg/L)液体培养基中,28℃,200rpm震荡培养过夜至OD600值为0.4。EHA105 II. 离心管中收集1ml菌液,4℃,8000rpm,离心30s。1.5ml III. 去残液,沉淀用200μl ddH2O充分悬浮,4℃,8000rpm,离心30s。 IV. 重复步骤ⅲ三次。 V. 去残液,沉淀用200ml ddH2O充分悬浮,即为电击用农杆菌EHA105感受态。加入200μl灭菌甘油混匀后置于-80℃备用。 (4)电击 I. 分别取10ml pB-2mb-FRO1-1.7A和pB-2mb-1.7A重组质粒至200μl EHA105感受态中,轻打混匀,然后转移至电击杯中,置冰上。 II. 准备好电击装置(BioRad),电压为2.5V,用手按住电击按钮,直到啪的一声电击完毕。 III. 室温静置2min后加入800ml YEP培养液,28℃静置1h,然后28℃,200rpm培养2h。IV. 离心30s,收集菌液,沉淀用200ml ddH2O悬浮,用玻璃棒涂布含含卡那霉素50mg/L 和含链霉素Sm50mg/L的YEP固体培养基平板,28℃培养48h。8000rpm 1.制备农杆菌电转感受态 (1)挑取根癌农杆菌EHA 105单菌落,接种于5mlLB〔含利福平(Rif) 50mg/L,;链霉素 100mg/L)液体培养基中,28'C, 220rpm震荡培养过夜。 (2)将2m1过夜培养的菌液加到50ml含同样抗生素的LB培养基中,28'C, 220rpm震荡 3-4小时,至OD560=0.5左右。 (3) 5000rpm离心5分钟,去上清。 (4) 加入40m1 10%甘油悬浮菌体,冰浴30min. (5) 4'C, 5000rpm离心5分钟,去上清。 (6 加入30mL10%甘油重悬浮菌体,4'C, 5000rpm离心5分钟, (7)重复步骤6一次,去上清,加入2ml10%甘油悬浮,分装于1.5ml的离心管中(200 p 1/ 管)备用。 2 农杆菌感受态的电转化 〔I)取2 ul质粒加到200 u I EHA 105感受态细胞中,轻轻混匀,冰浴 30分钟。 (2)把质粒和感受态混合液吸入电极杯,电击转化。 (3)马上加入lml新鲜的LB液体培养基,28'C, 150rpm轻摇4-6小时。 (4)收集菌体涂布于含有链霉素100mg/L),利福平(50mg/L)及质粒所含的抗性的LB固体培
(完整版)大肠杆菌感受态细胞的制备
大肠杆菌感受态细胞的制备 标签: tr..,Ca..,co.. 分类:细胞技术> 感受态细胞 来源: 实验管理实验概要 大肠杆菌感受态细胞的CaCl2法制备及质粒转化 实验原理 处于对数生长期的细菌经CaCl2 处理后接受外源DNA的能力显著增加。细菌处于容易吸收外源DNA的状态叫感受态。 在自然条件下,很多质粒都可通过细菌接合作用转移到新的宿主内,但在人工构建的质粒载体中,一般缺乏此种转移所必需的mob基因,因此不能自行完成从一个细胞到另一个细胞的接合转移。如需将质粒载体转移进受体细菌,需诱导受体细菌产生一种短暂的感受态,以摄取外源DNA。 转化(Transformation)是将外源DNA分子引入受体细胞,使之获得新的遗传性状的一种手段,它是微生物遗传、分子遗传、基因工程等研究领域的基本实验技术。转化过程所用的受体细胞一般是限制修饰系统缺陷的变异株,即不含限制性内切酶和甲基化酶的突变体 (R-,M-),它可以容忍外源DNA分子进入体内并稳定地遗传给后代。受体细胞经过一些特殊方法(如电击法,CaCl2 ,RbCl(KCl)等化学试剂法)的处理后,细胞膜的通透性发生了暂时性的改变,成为能允许外源DNA分子进入的感受态细胞(Compenent cells)。进入受体细胞的DNA分子通过复制、表达实现遗传信息的转移,使受体细胞出现新的遗传性状。将经过转化后的细胞在筛选培养基中培养,即可筛选出转化子(Transformant,即带有异源DNA 分子的受体细胞)。目前常用的感受态细胞制备方法有CaCl2和RbCl(KCl)法,RbCl(KCl)法制备的感受态细胞转化效率较高,但CaCl2法简便易行,且其转化效率完全可以满足一般实验的要求,制备出的感受态细胞暂时不用时,可加入占总体积15%的无菌甘油于-70℃保存(半年),因此CaCl2法使用更广泛。 主要试剂 (1)0.1mol/L CaCl2溶液 (2)LB液体培养基
植物表达载体转化农杆菌操作步骤
植物表达载体转化农杆菌操作步骤 来源:郭庆水的日志 植物表达载体转化农杆菌操作步骤 第一部分:农杆菌介导转化水稻 1、农杆菌选择:LBA4404、EHA105、GV3101 2、农杆菌活化:将保存的农杆菌在固体LB培养基上画线(或加或不加抗生素,LBA4404:Rif 或Str;EHA105:Rif或Str;GV3103:庆大霉素。如果不加抗生素就有可能造成这些菌株的Ti质粒丢失,导致农杆菌缺乏侵染性),抗生素浓度为:50μg/ml。28℃培养。 3、农杆菌感受态细胞的制备: 1)挑取单菌落接种于3ml LB液体培养基中,220rpm 28℃振荡培养至OD600 =0.5。 2)吸取1.5ml菌液于离心管中,冰浴10min; 3)5000(13000)rpm离心30s,弃去上清液; 4)沉淀用1.5 ml 0.5M NaCl悬浮,冰浴20min; 5)5000(13000)rpm离心30s,弃去上清液; 6)每管用100μl 20mMCaCl2悬浮,用于转化; 制备好的感受态细胞可马上使用,也可按每管200ul分装于无菌离心管中,于4℃保存48小时内使用,长期贮存时必须在液氮中速冻后转一70℃保存。使用时从一70℃取出,置冰上融化后使用。 4、DNA直接转化农杆菌: 1)50μl农杆菌感受态细胞中加入质粒DNA 0.1~1μg(5-10ul),之后冰浴30 min; 2)放入液氮中5min(或1min),然后立即放入37℃水浴锅中水浴5min; 3)取出离心管,加入0.5mlLB,28℃、220rpm振荡培养3~5hr; 4)取出菌液于含相应抗生素的LB平板上涂板,在培养箱中28℃条件下倒置培养。2天左右菌落可见。 (pEmu载体:AMP+Rif/Str;pK载体:Kan+Rif/Str;pTCK载体:Kan+Rif/Str) 5、重组农杆菌鉴定: 1)挑取单菌落,接种于含相应抗生素的LB液体培养基中,28℃振荡培养过夜。(pEmu载体:AMP+Rif/Str;pK载体:Kan+Rif/Str;pTCK载体:Kan+Rif/Str) 2)小量提取质粒DNA,加GTE同时加5μL溶菌酶(50μg "ml -1,贮藏浓度为50mg/ml或10mg/ml)。 3)质粒酶切或PCR鉴定。 6、三亲交配法: 参考一: 1)接种含重组质粒的大肠杆菌于含的LB平板,于37℃培养; (pEmu载体:50μg"ml -1AMP;pK载体:50μg"ml -1Kan;pTCK载体:50μg"ml -1Kan)2)接种含动员质粒pRK2013的大肠杆菌于不含抗生素的LB平板上,于37℃培养; 3)接种受体农杆菌EHA105/LBA4404于50μg"mL-1 Rif/Str的LB平板上28 ℃培养; 4)分别挑取上述平板单菌落,分别于LB液体培养基中震荡培养; 5)待三种菌生长到对数期时,各取50μL,混匀,涂布于无抗生素的LB 平板上,28℃培养过夜; 6)挑取长出的小块菌,接种于含相应抗生素的LB液体培养基中,28℃振荡培养24h;(pEmu载体:50μg"ml -1AMP+50μg"mL-1 Rif/Str;pK载体:50μg"ml -1Kan+50μg"mL-1
感受态细胞的制备(DH5α大肠杆菌)
感受态细胞的制备(DH5α) 一、准备工作 所有试剂、容器均需提前预冷。 1、实验器械 4℃离心机(50ml离心管),37℃恒温箱,37℃摇床,超净台(使用前需要紫外消毒15min 至少);0.22μm的滤器2个(过滤灭菌TfB2种溶液),10ml注射器2个;冰盒;高压灭菌的1.5mlEP管1盒,与离心机配套的50ml离心管6个(高压灭菌),高压灭菌的500ml 锥形瓶2个,高压灭菌的100ml玻璃瓶2个,高压灭菌的1ml枪头和200μl枪头各一盒。 2、试剂配制(甘油特别难吸,用蓝枪头慢慢吸吧) ① LB平板:单纯LB平板,加有amp或有kana的(制板时需标注好类型,时间)。 ② SOB培养基(Super Optimal Broth) ③ TfBⅠ:(100ml制备量)分别称取乙酸钾0.294g,MnCl2 0.99g,KCl 0.146g,CaCl2 0.111g,置于200ml烧杯中,加入15ml甘油和85mlDDW,摇晃,使其全部溶解。然后在安全橱中用孔径为0.22μm的滤器过滤混合液,置于高压灭菌的100ml玻璃瓶中,4℃保存,使用前必须预冷。(装在50ml离心管,封口4度保存) ④ TfBⅡ(20ml制备量,每次现用现配,装在50ml离心管):分别称取MOPS 0.046g,CaCl2 0.167g,KCl 0.015g,置于50ml烧杯中,加入3ml甘油和17mlDDW, 摇晃,使其全部溶解。然后在安全橱中用孔径为0.22μm的滤器过滤混合液,使用前必须预冷。
配制量 1 L 配制方法 1.配制250 mM KCl溶液。(50ml离心管分装) 在90 ml的去离子水中溶解l.86 g KCl后,定容至100 ml。 2.配制2 M MgCl2溶液。(50ml离心管分装) 在90 ml去离子水中溶解4.06g MgCl2 6H2O后,定容至100 ml,高温高压灭菌。 5.量取10 m1 250 mM KCl溶液,加入到烧杯中。 6.滴加NaOH小块,调节pH值至 7.0。 7.加入去离子水将培养基定容至l L。 8.高温高压灭菌后,4℃保存。 9.使用前加入5 ml灭菌的2 M MgCl2溶液。 LB培养基 配制量 1 L 配制方法 3.滴加固体NaOH,调节pH值至7.0。 4.加去离子水将培养基定容至1 L。 5高温高压灭菌后,4度保存。
CaCl2感受态细胞的制备实验步骤
CaCl2感受态细胞的制备实验步骤 ?1、从新活化的E.coli DH5α平板上挑取一单菌落,接种于3~5ml LB液 体培养中,37℃振荡培养至对数生长期(12h左右); ? 2、将该菌悬液以1:100~1:50转接于100ml LB液体培养基中,37℃振 荡扩大培养,当培养液开始出现混浊后,每隔20~30min测一次OD600,至OD600为0.3~0.5时停止培养,并转装到1.5 mL离心管中; ? 3、培养物于冰上放置20min; ? 4、 0~4℃,4000g离心10min,弃去上清液,加入1 mL冰冷的 0.1mo1/L CaCl2溶液,小心悬浮细胞, 冰浴20分钟; ?5、0~4℃, 4000g离心10min,倒净上清培养液,再用1.0 mL冰冷的 0.1mo1/L CaCl2溶液轻轻悬浮细胞,冰浴20min; ? 6、 0~4℃, 4000g离心10min,弃去上清液,加入100 μL冰冷的 0.1mo1/L CaCl2溶液,小心悬浮细胞,冰上放置片刻后,即制成了感 受态细胞悬液; ? 7、制备好的感受态细胞悬液可直接用于转化实验,如果在4℃放置 12~24h,其转化效率可以增高4~6倍;也可加入占总体积15%左右 高压灭菌过的甘油,混匀后分装于1.5ml离心管中,置于-70℃条件下, 可保存半年至一年。
CaCl2感受态细胞的制备实验步骤 1.前夜接种受体菌(DH5α或DH10B),挑取单菌落于LB培养基中 37℃摇床培养过夜(约16小时); 2 .取1ml过夜培养物转接于100ml LB培养基中,在37℃摇床上剧烈振 荡培养约2.5-3小时(250-300rpm); 3 .将0.1M CaCl2溶液置于冰上预冷;以下步骤需在超净工作台和冰上 操作; 4 .吸取1.5ml培养好的菌液至1.5ml离心管中,在冰上冷却10分钟; 5 .4℃下3000 g冷冻离心5分钟; 6 .弃去上清,加入100μl预冷0.1M CaCl2溶液,用移液枪轻轻上下吸动 打匀,使细胞重新悬浮,在冰放置20分钟; 7 . 4℃下3000 g冷冻离心5分钟; 8 .弃去上清,加入100μl预冷0.1M CaCl2溶液,用移液枪轻轻上下吸动 打匀,使细胞重新悬浮; 9 .细胞悬浮液可立即用于转化实验或添加冷冻保护剂(15% - 20%甘油)后超 低温冷冻贮存备用(-70℃)。 注意事项 1.细菌的生长状态:实验中应密切注视细菌的生长状态和密度,尽量使 用对数生长期的细胞(一般通过检测OD600来控制。DH5α菌株OD600为0.5时细胞密度是5×107/ml); 2 .所有操作均应在无菌条件和冰上进行; 3 .经CaCl2处理的细胞,在低温条件下,一定的时间内转化率随时间的 推移而增加,24小时达到最高,之后转化率再下降(这是由于总的 活菌数随时间延长而减少造成的); 4 .化合物及无机离子的影响:在Ca2+的基础上联合其他二价金属离子 (如Mn 2+或Co 2+)、DMSO或还原剂等物质处理细菌,可使转化效率大大提高(100-1000倍); 5 .所使用的器皿必须干净。迹量的去污剂或其它化学物质的存在可能 大大降低细菌的转化效率; 6 .质粒的大小及构型的影响:用于转化的应主要是超螺旋的DNA; 7 .一定范围内,转化效率与外源DNA的浓度呈正比;
实验三 大肠杆菌感受态细胞的制备(新)
实验三大肠杆菌感受态细胞的制备 【课前预习】 1、大肠杆菌感受态细胞的制备及转化的基本原理是什么? 2、大肠杆菌感受态细胞的制备可以采用哪些方法? 【目的要求】 1、了解感受态细胞生理特性及制备条件; 2、掌握大肠杆菌感受态细胞制备方法; 【基本原理】 所谓感受态,是指细菌生长过程中的某一阶段的培养物,只有某一生长阶段中的细菌才能作为转化的受体,能接受外源DNA而不将其降解的生理状态。它是由受体菌的遗传性状所决定的,同时也受菌龄、外界环境因子的影响。cAMP可以使感受态水平提高一万倍,而Ca2+也可大大促进转化的作用。细胞的感受态一般出现在对数生长期,新鲜幼嫩的细胞是制备感受态细胞和进行成功转化的关键。感受态形成后,细胞生理状态会发生改变,出现各种蛋白质和酶,负责供体DNA 的结合和加工等。细胞表面正电荷增加,通透性增加,形成能接受外来的DNA 分子的受体位点等。 基因工程技术中最常用的是氯化钙转化技术,虽然对其基本原理仍然不完全清楚,但是比较认同的看法是,细菌处干0℃、CaCl2低渗溶液中,细胞膨胀形成球状,转化混合物中的DNA形成抗DNase的羟基-钙磷酸复合物粘附与细胞表面,经42℃短时间热冲击处理,促进细胞吸收DNA复合物,之后细菌在富含营养的培养基上生长,球状细胞复原并分裂繁殖,重组质粒在转化的细菌中,表达目的基因,因而在选择性培养基平板中,可以选出阳性细菌转化子。Ca2+处理的感受态细胞,一般每微克DNA能转化105-106个细菌、环化的质粒DNA 愈小,转化率愈高。环化的DNA分子比线性DNA分子转化率高1000倍。CaCl2转化法的优点是:简单快速,重复性好,菌株适用范围广。 另外,电击法也可用于转化过程,电击法不需要预先诱导细菌的感受态,依赖短暂的电击,利用瞬时高压电流(数千伏特)处理细胞悬浮液,使微生物细胞膜在高压电作用下发生去极化,产生微孔,悬液中溶解的核酸即可通过细胞膜上的空洞进入细胞内部,转化率最高达109-1010转化子/μg闭环DNA。 制备出的感受态细胞暂时不用时,可加入占总体积15%的无菌甘油或-70℃保存(有效
大肠杆菌和农杆菌感受态的制备
A 大肠杆菌感受态的制备(CaCl2法)(《水稻NR和NIR基因启动子的克隆及功能验证》第38页) 1 材料、设备及试剂 1.1材料 大肠杆菌DH5α、BL21、Rossette、JM109菌株 1.2试剂 LB液体培养基: 蛋白胨10g/L 酵母提取物5g/L NaCl 10g/L NaOH(1mol/L)1mL/L 400mL 0.1M/L预冷的CaCl2溶液(高温高压灭菌) 50%甘油 75%酒精 95%酒精 液氮 1.3 实验设备 接种环、酒精灯,打火机,75%酒精,95%酒精,50mL灭菌三角瓶4个,250mL灭菌的三角瓶4个,移液抢(5mL、200μL,1000μL),灭菌的枪头(5mL、200μL,1000μL),离心管(1.5mL,50mL)恒温摇床,灭菌锅,紫外分光光度计,超净工作台,制冰机,冰盒,高速冷冻离心机。 2 实验步骤 1、从新鲜培养的大肠杆菌DH5α平板上挑取一个单菌落,接种于5mL新鲜LB培液体养基中,于37℃,200rpm振荡培养过夜。 2、培养12~16h,取1ml培养物加入到100mL新鲜LB培液体养基中,于37℃,200rpm振荡培养至OD=0.4~0.6(3~4h) 3、在无菌条件下将菌液转移到250mL离心管中,置于冰上10min. 4、于4℃,3000rpm离心5~10 min,弃上清,收集菌体。 5、加入20mL预冷的0.1M/L CaCl2溶液重新悬沉淀,至于冰上30min(严格) 6、于4℃,3000rpm离心5~10 min,弃上清,收集菌体。 7、加入4 mL0.1M/L CaCl2溶液及15%(最终浓度)甘油(50%的甘油1.71428 mL),重悬沉淀。 8、以100μL每管分装于1.5mL冻存管中保存于液氮。 3 试验结果 4 注意事项
农杆菌感受态的制备方法
农杆菌感受态细胞制备 第一天晚至第三天晚: 1)取-80℃保存的GV3101于含50μg/ml 利福平的LB (千分之一的利福平)平板划线,28℃培养(一般要两天)。 注意:划线的时候要少沾一点原菌株,不必等到菌株融化就可轻轻沾一点,一定要少量,然后轻轻地划在板上。挑得太多不容易长出单菌落,如果太用力也容易伤到菌株。 第三天下午或晚: 2) 挑取单菌落接种于灭菌的50ml 新管子加10ml 50μg/ml (千分之一)利福平的LB 液体培养基中,200rpm 28℃振荡培养12-16 hr (过夜可以)。 注意:管子最好用灭菌过的报纸包一下,摇菌时。 第四天早: 3) 取1-2ml (按1:50或者1:100的比例)菌液转接于含有50μg/ml (千分之一)利福平的100ml LB 液体培养基中(用500 ml 的三角瓶来摇菌28℃,200rpm 振荡培养至OD 600=0.5)。 注意:摇菌的过程可能需要3-4小时,要随时监控菌的浓度,可以平行的摇两瓶,其中一瓶用来测浓度,避免污染;并且为了保证检测菌液与未检测菌液的一致性,平行的两瓶菌液,最好来源于同一个50 ml 管子的菌液。 摇菌的过程中可以预先把NaCl 置于冰上预冷。 4) 转移菌液到新的灭过菌的50 ml 离心管中,冰上30min ; 5) 4℃,5000rpm 离心5min 。 6) 在超净台中弃上清,将管子倒立在灭过菌的吸水纸上,尽量倒干,可以用预冷的NaCl 快速冲洗一遍。 7) 加入10ml 预冷的0.15M 的NaCl 溶液,轻轻悬浮细胞,冰上放置20min 。 注意:要用5ml 枪调到3ml 挡,轻轻抽打。 8) 4℃,5000rpm 离心5min 。 9) 在超净台中弃上清,将管子倒立在灭过菌的吸水纸上,尽量倒干。 10)加入2 ml 预冷的含15%甘油的20mM 的CaCl 2溶液,轻轻悬浮。 注意:要用1ml 枪轻轻抽打。 11)按200ul 的量分装到1.5 ml 无菌Eppendorf tube 中,液氮速冻,-80℃保存,一般不要存放超过2-3个月。
高效感受态细胞的制备
感受态细胞的制备 一、实验原理 受体细胞通过一些特殊方法(如电击法,CaCl2,MnCl2,MgCl2等化学试剂法)的处理后,使细胞膜的通透性发生了暂时性的改变,成为能允许外源DNA分子进入的状态,成为感受态细胞。 本方案介绍的方法为TSS法和KCM转化法。 二、材料及准备工作 一)材料准备
二)试剂配制 1、液体LB培养基(200ml,高压灭菌,4℃保存备用) 蛋白胨 2.0g 酵母提取物 1.0g 氯化钠(NaCl) 2.0g 2、固体LB培养基(2×100ml,高压灭菌) 蛋白胨2×1.0g 酵母提取物2×0.5g 氯化钠(NaCl)2×1.0g 琼脂粉2×1.5g 温度降低到45℃后(不烫手),取其中一瓶加入氨苄至终浓度100μg/ml(100mlLB加100μl 100mg/ml的氨苄)后铺平皿,另一瓶直接铺平皿。4℃保存备用。 3、TSS液(100ml)(有效期2周) 聚乙二醇(PEG8000)10g 终浓度10% DMSO 5ml 终浓度5%
MgCl2(1mol/L)5ml 终浓度50mmol/L LB 85ml 终浓度85% 去离子水补足100ml,0.22μm过滤器过滤后,4℃保存备用 注:聚乙二醇分子量可以为3000-8000 4、5×KCM液(10ml)(可-20℃长期保存备用) KCl(2mol/L) 2.5ml CaCl2(1mol/L) 1.5ml MgCl2(1mol/L) 2.5ml 水补足到10ml, 0.22μm过滤器过滤后,4℃保存备用(不要高压消毒) 5、氨苄青霉素(amp)(100mg/ml) 取0.5g氨苄青霉素,溶解于5ml去离子水中,0.5ml分装,-20℃ 保存备用 三)仪器设备 1、低温大容量离心机 2、恒温水浴锅 3、超净台 4、高压锅 5、37℃孵育箱 6、恒温摇床 7、制冰机 8、分光光度计
农杆菌感受态细胞的制备原理和实验步骤及验证
农杆菌感受态细胞的制备原理和实验步骤发布日期:2010-04-28 发布 人:technew最后更新时间:2010-04-28 浏览次数:889 一、目的及要求 了解和掌握农杆菌感受态细胞制备的原理和方法。 二、实验原理 在利用根癌农杆菌介导的基因转化中,首先要获得含有目的基因的农杆菌工程菌株。 在基因工程操作中,感受态细胞的制备和质粒的转化是一项基本技术。感受态是细菌细胞具有的能够接受外源DNA 的一种特殊生理状态。农杆菌的感受态可用CaCl2 处理而诱导产生。将正在生长的农杆菌细胞在加入到低渗的氯化钙溶液中,0℃下处理便会使细菌细胞膜的透性发生改变,此时的细胞呈现出感受态。 制备好的农杆菌感受态细胞迅速冷冻于70℃可保存相当一段时间而不会对其转化效率有太大影响。 三、实验仪器、材料和试剂 仪器:超净工作台,恒温摇床,冷冻高速离心机,高压灭菌锅,冰箱,70℃超低温冰柜,分光光度计,接种针,10ml 试管,50ml 离心管,1.5ml 离心管,冰浴,微量进样器及吸头。以上玻璃仪器和离心管需在用前灭菌,灭菌条件:120℃,15分钟。 材料:土壤农杆菌LBA4404菌株或其它农杆菌菌株 试剂: YEB液体培养基(1升):酵母提取物1g,牛肉膏5g,蛋白胨5g,蔗糖5g, MgSO4.7H2O 0.5g, pH7.0,高压灭菌; 链霉素(Sm)储液:125mg/ml 0.15 N NaCl,高压灭菌。 20mM CaCl2,高压灭菌。
四、实验步骤 1. 挑取根癌农杆菌LBA4404 单菌落于3ml 的YEB液体培养基(含Sm 125mg/l)中,28°C振荡培养过夜; 2. 取过夜培养菌液0.5ml接种于50mlYEB(Sm 125mg/l)液体培养基中,28°C振荡培养至OD600为0.5; 3. 5000rpm, 离心5min; 4. 加入10ml 0.15N NaCl,使农杆菌细胞充分悬浮,5000rpm, 离心5min; 5. 弃上清,置于冰上,加入1ml预冷的20mM CaCl2,充分悬浮细胞,冰浴中保存,24小时内使用,或分装成每管200ml,液氮中速冻1 分钟,置70°C保存备用。 一.农杆菌感受态细胞的制备 二.双元载体转化农杆菌EHA105 三.杆菌转化子的鉴定 A.农杆菌转化子的PCR鉴定 B.农杆菌转化子的酶切鉴定 关键词:农杆菌感受态细胞转化子 一.农杆菌感受态细胞的制备(同大肠杆菌质粒DNA的提取),然后将其转化大肠杆菌,再提取大肠杆菌的质粒DNA进行酶切鉴定。 取-70℃保存的EHA105于含有50μg/ml链霉素平板划线,28℃培养2天。挑单 菌落接种于5ml YM(0.5g/L KH 2 PO 4 ,10 g/L Mannitol,2 g/L L-Glutamine,0.2 g/L NaCL,0.2 g/L MgSO 4,0.3 g/L Yeast extract,PH 7 .0)液体培养基中,220rpm, 28℃振荡培养18 hr 左右。将5ml菌液转接于100ml YM液体培养基中, 28℃,220rpm,振荡培养至OD 600 =0.5。转入无菌1.5ml的EP管,5000g离心5min, 去上清液。加入1ml预冷的0.1M的CaCl 2 溶液,轻轻悬浮细胞,冰上放置20min, 4℃下,5000g离心5min,去上清。加入200μl预冷的含15%甘油的0.1M的CaCl 2溶液,轻轻悬浮。混匀后立即冻存于-80℃。 二.双元载体转化农杆菌EHA105 取1μg左右的质粒DNA加入到200μl EHA105感受态细胞中,混匀后,冰浴30min;-70℃放置10min ;取出后37℃水浴5min或42℃水浴1min;冰浴2min;加入800μl YM液体培养基,28℃,175rpm摇培3hr;取出后涂在含50μg/ml Kanamycin 的YM平板上,28℃培养到形成单菌落。
烟草农杆菌转化实验步骤1
烟草农杆菌转化实验 实验配方:1L RMOP: 20×大量元素50ml 200×微量元素5ml 200×有机5ml 200×铁盐5ml 3%蔗糖30g 0.8%琼脂(国产)4g/500ml 灭菌后,每500ml培养基加入: 0.1mg/L NAA 1mg/ml NAA 50μL 1mg/L 6-BA 1mg/ml6-BA 500μL YEB: 液体培养基:1L 酵母提取物1g 牛肉膏5g 蛋白胨5g 蔗糖5g MgSO4?7H2O 0.5g pH7.0 高压灭菌。 固体培养基: 每升YEB 液体培养基加15g 琼脂粉,高压灭菌。 卡那霉素(Kan)储液:100mg/ml 利福平(Rif)储液:50mg/ml YEB 固体培养基平板: 灭菌后的YEB 固体培养基待其温度降至50℃时加入卡那霉素(Kan)和利福平(Rif),至终浓度为50mg/l,混匀后立即倒入培养皿,凝固后4℃倒置保存。 一.农杆菌感受态细胞的制备 (1)划线活化农杆菌,挑取农杆菌单菌落于3ml的YEB液体培养基(含Rif 50mg/l)中,28℃振荡培养过夜; (2)取过夜培养菌液1ml接种于50ml YEB(Rif 50mg/l)液体培养基中,28℃振荡培养至OD600为0.5; (3)取2ml菌液,13000rpm,离心30sec, 弃上清; (4)加入10ml 0.1M CaCl2,使农杆菌细胞充分悬浮,冰浴30min;
(5)13000rpm,离心30sec,弃上清,置于冰上,加入2.5ml预冷的0.1M CaCl2,充分悬浮细胞,分装在1.5ml EP管中,液氮中速冻1min,置-80℃冰箱保存备用。二.质粒DNA导入农杆菌 ①电转法: 1.取农杆菌感受态在冰上冻融; 2.加2μL质粒DNA于100μL感受态细胞中,用枪头轻轻搅拌混匀; 3.然后再将其转入电转杯中(不要产生气泡),在2500V高压下电击; 4.取出电转杯,加入500μL预冷的YEB培养基(不含抗生素),轻轻吹打混匀,吸出菌液转入1.5ml离心管中,28℃,200rpm振荡培养5h; 5.取30-40μL菌液涂在含相应抗生素(50mg/l Kan和50mg/l Rif)的YEB平板上,28℃倒置培养1.5-2天; 6.挑选单菌落PCR检测,将阳性菌落保存。 ②冻融法: 1、在200μl感受态细胞中加入2-6μl质粒DNA,冰浴5min,液氮中速冻5min; 2、迅速转入37℃水浴中,热激5min; 3、加入1ml YEB(不含抗生素)液体培养基,28℃慢速振荡培养2-4小时; 4、3000rpm离心4min,去一部分上清,留取200μl菌液涂布于含有50mg/l Kan 和50mg/l Rif的YEB平板; 5、放置约0.5h,待水份干后,28℃培养约24小时至长出菌落。 6、挑选单菌落PCR检测,将阳性菌落保存。 三.烟草遗传转化实验 ①准备农杆菌 (1)将农杆菌在平板上划线,从平板上挑取单菌落,接种到20mL附加相应抗生素(kan 50mg/L, Rif 50mg/L)的YEB液体培养基中,在恒温摇床上,于28℃下以180r/min培养至OD600为0.6~0.8(约需17h)。 (2)将OD600为0.6~0.8的菌液,按1%~2%的比例,转入新配制的无抗生素(含Rif)的YEB液体培养基中,可同时加入100~500μmol/L的乙酰丁香酮。在上述相同的条件下再培养6h左右,待OD600为0.2~0.5时即可用于转化。
大肠杆菌感受态细胞的制备和转化原理
大肠杆菌感受态细胞的制备和转化(原理) 感受态细胞的概念重组DNA分子体外构建完成后,必须导入特定的宿主(受体)细胞,使之无性繁殖并高效表达外源基因或直接改变其遗传性状,这个导入过程及操作统称为重组DNA分子的转化。在原核生物中,转化是一个较普遍的现象,在细胞间转化是否发生,一方面取决于供体菌与受体菌两者在进化过程中的亲缘关系,另一方面还与受体菌是否处于一种感受状态有着很大的关系。 1、感受态细胞的概念 所谓的感受态,即指受体(或者宿主)最易接受外源DNA片段并实现其转化的一种生理状态,它是由受体菌的遗传性状所决定的,同时也受菌龄、外界环境因子的影响。cAMP可以使感受态水平提高一万倍,而Ca2+也可大大促进转化的作用。细胞的感受态一般出现在对数生长期,新鲜幼嫩的细胞是制备感受态细胞和进行成功转化的关键。 制备出的感受态细胞暂时不用时,可加入占总体积15%的无菌甘油或-70℃保存(有效期6个月)。 2、转化的概念及原理 在基因克隆技术中,转化特指将质粒DNA或以其为载体构建的重组DNA导入细菌体内,使之获得新的遗传特性的一种方法。
它是微生物遗传、分子遗传、基因工程等研究领域的基本实验技术之一。 受体细胞经过一些特殊方法(如:电击法,CaCl2等化学试剂法)处理后,使细胞膜的通透性发生变化,成为能容许外源DNA分子通过的感受态细胞。进入细胞的DNA分子通过复制、表达实现遗传信息的转移,使受体细胞出现新的遗传性状。 大肠杆菌的转化常用化学法(CaCl2法),该法最先是由Cohen 于1972年发现的。其原理是细菌处于0℃,CaCl2的低渗溶液中,菌细胞膨胀成球形,转化混合物中的DNA形成抗DNase(DNA酶)的羟基--钙磷酸复合物粘附于细胞表面,经42℃短时间热冲击处理,促使细胞吸收DNA复合物,在丰富培养基上生长数小时后,球状细胞复原并分裂增值。被转化的细菌中,重组子中基因得到表达,在选择性培养基平板上,可选出所需的转化子。 Ca2+处理的感受态细胞,其转化率一般能达到5×106--2×107转化子/质粒DNA,可以满足一般的基因克隆试验。如在Ca2+的基础上,联合其它的二价金属离子(如Mn2+、Co2+)、DMSO或还原剂等物质处理细菌,则可使转化率提高100--1000倍。 化学法简单、快速、稳定、重复性好,菌株适用范围广,感受态细菌可以在-70℃保存,因此被广泛用于外源基因的转化。
实验七 感受态细胞的制备和重组质粒的转化
实验七感受态细胞的制备和重组质粒的转化 【实验目的】 1.掌握用CaCl2法制备感受态细胞的原理和方法。 2.学习和掌握质粒DNA的转化和重组质粒的筛选方法。 【实验原理】 质粒在不同的细菌之间转移是微生物世界中一种普遍的现象,一个细菌品系通过吸收另一个细菌品系的质粒DNA而发生了遗传性状的改变,这种现象叫做转化,获得了外源DNA的细胞称为转化子。 在基因克隆技术中,所谓转化是指质粒或重组质粒被导入受体细胞,表达相应的选择标记基因,并在一定的培养条件下,在选择性培养基上长出转化子的过程。质粒必须通过转化进入细菌细胞内,才能进行扩增和表达,从而获得大量的克隆基因,使我们能够进行进一步的DNA操作,如亚克隆等;或者获得其表达产物。转化效率的高低与受体菌的生理状态有关。细菌吸收外源DNA的能力最高时的状态被称为感受态细胞(competent cell)。有些种类的细菌在其生长的任一阶段都处于感受态,而另一些细菌只有处于某个生长时期时(一般为对数生长早、中期),才会处于感受态,如本实验所用的大肠杆菌。用一定浓度的CaCl2 处理对数生长早中期的细菌可以大大提高细菌吸收周围环境中的DNA分子的能力。对这种现象的一种解释是CaCl2能使细菌细胞壁的通透性增强,从而提高转化率。这种转化方法称为“化学法”。目前还可以使用电激的方法,通过瞬间的高压电流,在细胞上形成孔洞,使外源DNA进入胞内,从而实现细胞的转化。电激转化的效率往往比化学法高出1到2个数量级,达到1 x 108转化子/μg DNA,甚至1 x 109转化子/μg DNA,所以常用于文库构建时的转化或遗传筛选。 微生物转化是基因工程的常用技术,大肠杆菌是基因工程中最常用的受体菌,本实验即是用前面实验获得的重组质粒转化大肠杆菌细胞。 【试剂与器材】 〈一〉试剂 1.LB液体培养基: 参见附录 每组配200mL, 其中100mL分装于500mL三角瓶中,另各取3mL装于2只大试管中,其余装于装于500mL三角瓶中,121℃高压蒸汽灭菌20分钟。 2.LB/Amp/IPTG/X-Gal平板(1): 配1L LB液体培养基,加入20g琼脂粉和1支搅拌棒,同上高压灭菌,趁热取出置搅拌器上冷却,待冷至55℃左右, 加氨苄青霉素(Ampicillin)至终浓度100μg/ml (Amp储存液一般为100mg/mL), 倒平板,每皿倒约15 mL,室温放置过夜至冷凝水挥发干净。使用前半小时在培养基表面加20μL 50mg/mL X-gal 和100μL 0.1mol/L IPTG,涂匀,待这两种化合物渗入琼脂后,即可用于转化菌的涂布。 每组制备LB平板2个,LB/Amp 平板5个,LB/Amp/IPTG/X-Gal平板6个。 3.IPTG储存液(0.1mol/L):1.2g IPTG加水至50ml,过滤除菌,4℃储存。 4.X-gal储存液:50mg/ml溶于二甲基甲酰胺溶剂中,过滤除菌,4℃储存。 5.1 mol/L CaCl2储存液,使用浓度为0.1mol/L,CaCl2应使用分析纯,配100mL,高压灭菌,全班用。6.甘油(灭菌),全班50mL,同上高压灭菌。 7.酸洗无菌玻璃珠,涂布平板用,用50mL三角瓶分装,同上高压灭菌,烘干备用。 〈二〉器材 1. 37℃温箱、水浴锅、恒温振荡器等 2. 高速冷冻离心机 3. 微量移液器等
农杆菌感受态细胞的制备原理和实验步骤(精)
一、目的及要求 了解和掌握农杆菌感受态细胞制备的原理和方法。 二、实验原理 在利用根癌农杆菌介导的基因转化中,首先要获得含有目的基因的农杆菌工程菌株。 在基因工程操作中,感受态细胞的制备和质粒的转化是一项基本技术。感受态是细菌细胞具有的能够接受外源DNA 的一种特殊生理状态。农杆菌的感受态可用CaCl2 处理而诱导产生。将正在生长的农杆菌细胞在加入到低渗的氯化钙溶液中,0℃下处理便会使细菌细胞膜的透性发生改变,此时的细胞呈现出感受态。 制备好的农杆菌感受态细胞迅速冷冻于70℃可保存相当一段时间而不会对其转化效率有太大影响。 三、实验仪器、材料和试剂 仪器:超净工作台,恒温摇床,冷冻高速离心机,高压灭菌锅,冰箱,70℃超低温冰柜,分光光度计,接种针,10ml 试管,50ml 离心管,1.5ml 离心管,冰浴,微量进样器及吸头。以上玻璃仪器和离心管需在用前灭菌,灭菌条件:120℃,15分钟。 材料:土壤农杆菌LBA4404菌株或其它农杆菌菌株 试剂: YEB 液体培养基(1升):酵母提取物1g ,牛肉膏5g ,蛋白胨5g ,蔗糖 5g , MgSO4.7H2O 0.5g, pH7.0,高压灭菌; 链霉素(Sm )储液:125mg/ml
0.15 N NaCl,高压灭菌。 20mM CaCl2,高压灭菌。 四、实验步骤 1. 挑取根癌农杆菌LBA4404 单菌落于3ml 的YEB 液体培养基(含Sm 125mg/l)中,28°C 振荡培养过夜; 2. 取过夜培养菌液0.5ml 接种于50mlYEB(Sm 125mg/l液体培养基中,28°C 振荡培养至OD600为0.5; 3. 5000rpm, 离心5min ; 4. 加入10ml 0.15N NaCl,使农杆菌细胞充分悬浮,5000rpm, 离心5min ; 5. 弃上清,置于冰上,加入1ml 预冷的20mM CaCl2,充分悬浮细胞,冰浴中保存,24小时内使用,或分装成每管200ml ,液氮中速冻1 分钟,置70°C 保存备用。
感受态细胞的制备步骤和原理
感受态细胞的制备步骤和原理 实验目的 为了获得大量的质粒作为克隆载体,我们需要将购买来的质粒通过转化的方法导入细菌的细胞内。制备出感受态的细胞,我们就可以方便的将需克隆的质粒导入其中,使其繁殖,就能获得大量质粒。本次实验的目的就是增加质粒的数量。同时,我们能掌握大肠杆菌感受态细胞的制备及转化的基本原理和实验技术方法。 实验原理及过程 实验步骤 1挑取一个JM109单菌落于3ml LB(无抗生素)培养基中,37℃,180rpm培养过夜。 [让菌复苏,进入对数期的早中期。此时更容易制得感受态细胞。] 2取0.4mL过夜培养物加入到40mL LB(无抗生素)培养基中,37℃250rpm大约2.5小时。 [减少达到所需亮的均所需繁殖的世代数,以减少菌的变 GAGGAGAGGAFFFFAFAF
异。] 3取培养物置于40mL的灭菌离心管中,冰浴10min,4000rpm 4℃离心10min,弃上清。(将所有上清倒光,可以将离心管倒过来) [使细菌的生长停止,代谢减慢。因为这时已经没有培养基了,如果细菌仍有很高的代谢效率,则有大量细菌死亡。] 4菌体重悬于10mL 100mmol/L冰冷CaCl2中,轻吹,4℃30min,4000rpm离心5min弃上清。 [ 细菌处于0度,CaCl2低渗溶液中,菌细胞膨胀成球形,外源DNA形成抗DNA酶的羟基-钙磷酸盐混合物黏附于细胞表面(羟基来源于细胞壁上的糖,磷酸来源于DNA),经短时间420C热激处理,促进细胞吸收DNA复合物。(一定要轻吹,这时细胞壁打开,十分脆弱)] 5菌体重悬于1mL 100mmol/L冰冷的CaCl2中,轻吹,用于转化。 [除去所有的LB以及细胞破损后释放出来的细胞内含物。防止细胞分裂,以致大量细胞死亡。(一定要轻吹,这时细 胞壁打开,十分脆弱)] GAGGAGAGGAFFFFAFAF
