处方药登记表
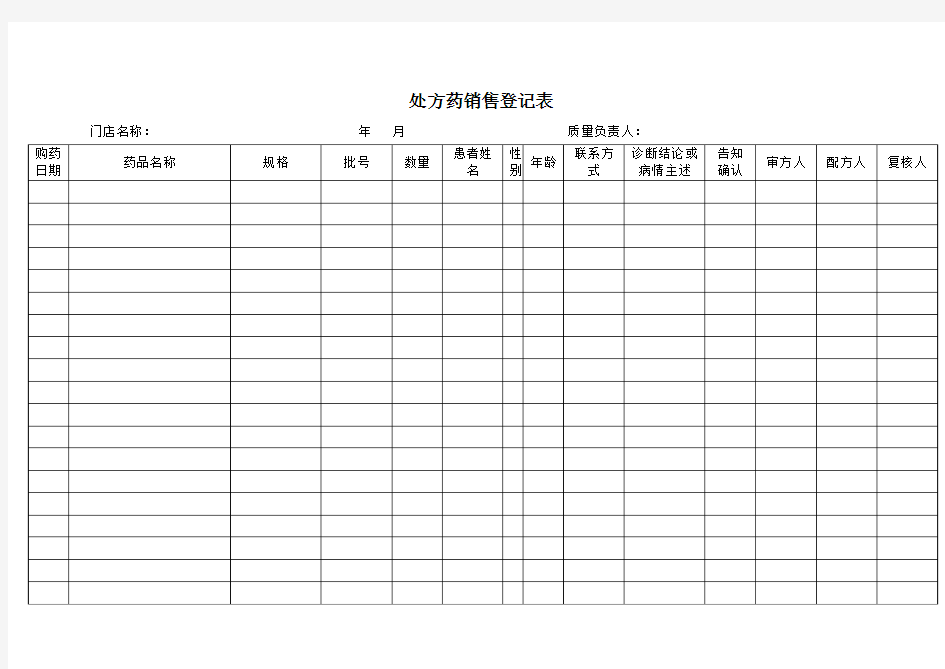
处方药销售登记表
门店名称:年月质量负责人:
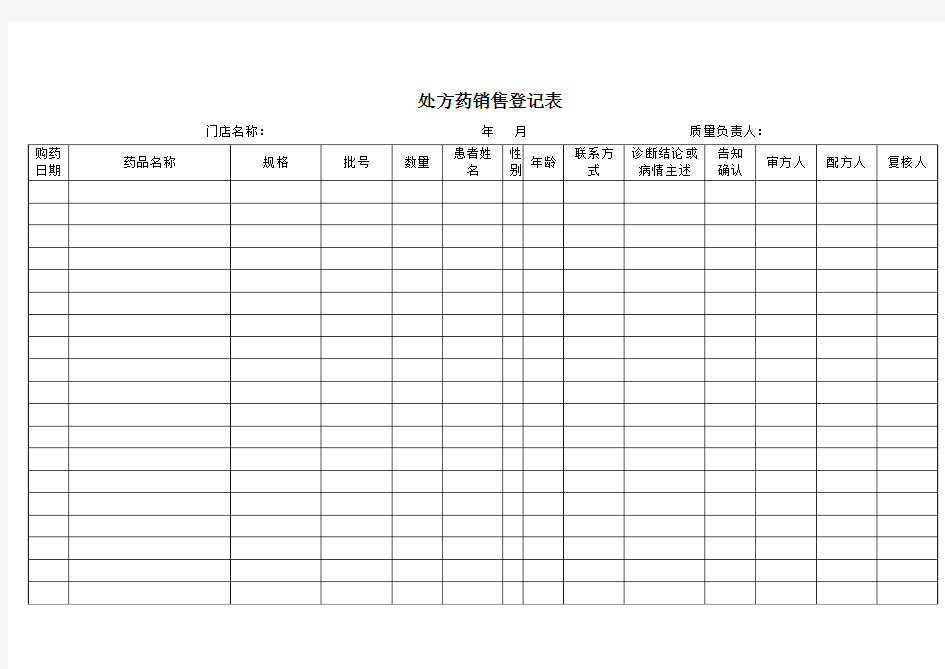
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
处方药销售登记表
门店名称:年月质量负责人:
化学药品非处方药说明书规范细则(国食药监注[2006]540号)
【发布单位】国家食品药品监督管理局 【发布文号】国食药监注[2006]540号 【发布日期】2006-10-20 【生效日期】2006-10-20 【失效日期】 【所属类别】政策参考 【文件来源】国家食品药品监督管理局 化学药品非处方药说明书规范细则 (国食药监注[2006]540号) 各省、自治区、直辖市食品药品监督管理局(药品监督管理局): 根据《药品说明书和标签管理规定》(局令第24号)和《处方药与非处方药分类管理办法》(国家药品监督管理局令第10号),为做好非处方药说明书规范工作,国家局组织制定了《化学药品非处方药说明书规范细则》和《中成药非处方药说明书规范细则》,现予印发。 本通知发布之日起,国家局在《关于对第一批〈国家非处方药目录〉药品进行审核登记工作 的通知》(国药管安〔1999〕425号)中有关“非处方药药品标签、使用说明书和包装指导原则”和在《关于做好第一批非处方药药品审核登记工作的通知》(国药管安〔2000〕278号) 中的“非处方药药品标签、使用说明书和包装指导原则的补充说明”同时废止。 附件:1.化学药品非处方药说明书规范细则 2.中成药非处方药说明书规范细则 国家食品药品监督管理局 二○○六年十月二十日 化学药品非处方药说明书规范细则 一、化学药品非处方药说明书格式 处方药、外用药品标识位置 X X X说明书
请仔细阅读说明书并按说明使用或在药师指导下购买和使用 警示语位置 【药品名称】 【成份】 【性状】 【作用类别】 【适应症】 【规格】 【用法用量】 【不良反应】 【禁忌】 【注意事项】 【药物相互作用】 【贮藏】 【包装】 【有效期】 【执行标准】 【批准文号】 【说明书修订日期】 【生产企业】 如有问题可与生产企业联系 二、化学药品非处方药说明书各项内容书写要求 非处方药、外用药品标识 非处方药、外用药品标识在说明书首页右上角标注。 外用药品专用标识为红色方框底色内标注白色“外”字。药品说明书如采用单色印刷,其说明书中外用药品专用标识亦可采用单色印刷。 非处方药专有标识按《关于公布非处方药专有标识及管理规定的通知》规定使用。 说明书标题 “XXX说明书”中的“XXX”是指该药品的通用名称。 请仔细阅读说明书并按说明使用或在药师指导下购买和使用 该忠告语必须标注,采用加重字体印刷。 警示语 是指需特别提醒用药人在用药安全方面需特别注意的事项。 有该方面内容,应当在说明书标题下以醒目的黑体字注明。无该方面内容的,不列该项。
关于印发中药、天然药物处方药说明书格式、内容书写要求及撰写指导原则的通知
关于印发中药、天然药物处方药说明书格式、内容书写要求及撰写指导原则的通知 (征求意见稿 2006.6.2) 各省、自治区、直辖市食品药品监督管理局(药品监督管理局): 为贯彻实施《药品说明书和标签管理规定》(国家食品药品监督管理局令第24号,以下简称《管理规定》),加强中药、天然药物处方药说明书的规范和管理,我局制定了《中药、天然药物处方药说明书格式》(附件一)、《中药、天然药物处方药说明书内容书写要求》(附件二)以及《中药、天然药物处方药说明书撰写指导原则》(附件三),现予以印发,并就有关事项通知如下: 一、对已批准注册的中药、天然药物处方药,应当按照《中药、天然药物处方药说明书格式》和《中药、天然药物处方药内容书写要求》印制说明书。申请注册中药、天然药物的,以及按补充申请提出说明书修订的,应按照《中药、天然药物处方药说明书撰写指导原则》起草说明书样稿。 二、关于“核准日期”。对于2006年6月日前批准注册的中药、天然药物,其“核准日期”项下的日期应为按照《关于实施<药品说明书和标签管理规定>有关事宜的公告》
提出补充申请后,药品监督管理部门予以核准的日期。 三、关于“外用药”。外用药系指(待定)的药物。 外用药品标识为红色方框底色内标注白色“外”字,样式: 用药品标识可以单色印制。对于既可内服,又可外用的中药、天然药物,可不标注外用药品标识。 四、关于【成份】。对于药品处方已列入国家秘密技术项目的品种,应与原核准并使用的说明书【成份】或【主要成份】项下内容一致,原核准说明书不包括【成份】或【主要成份】项的,可不列此项。 五、关于【功能主治】/【适应症】。对于2006年6月日前批准注册的中药、天然药物,应按原核准使用的说明书中的该项内容表述。 六、关于【规格】。对于2006年6月日前批准注册的中药、天然药物,如该品种所执行的药品标准中无【规格】项,可不列此项。 七、关于【不良反应】、【注意事项】及【禁忌】。生产企业应当密切关注药品使用的安全性问题,并根据药品的临床使用情况、国家药品不良反应监测中心的公告、检索到的相关文献等,及时提出完善【不良反应】、【注意事项】以及【禁忌】等项目内容的补充申请。完善该三项目内容时,不
肠炎宁颗粒非处方药说明书范本
附件2 肠炎宁颗粒等14种非处方药说明书范本 肠炎宁颗粒非处方药说明书范本 请仔细阅读说明书并按说明使用或在药师指导下购买和使用。 [药品名称] 通用名称:肠炎宁颗粒 汉语拼音: [成份] [性状] [功能主治]清热利湿,行气。用于急、慢性胃肠炎,腹泻,小儿消化不良。 [规格]每袋装10克 [用法用量]口服,一次10克,一日3~4次,小儿酌减。 [不良反应] [禁忌]孕妇禁用,糖尿病患者禁服。 [注意事项] 1.饮食宜清淡,忌烟、酒及辛辣、生冷、油腻食物。 2.不宜在服药期间同时服用滋补性中药。 3.有慢性结肠炎、溃疡性结肠炎便脓血等慢性病史者,患泄泻时应去医院就诊。 4.有高血压、心脏病、肝病、肾病等慢性病严重者应在医师指导下服用。 5.症状严重或有里急后重、脓血便的患者应及时去医院就诊。 6.服药3天症状无缓解,应去医院就诊。 7.儿童、哺乳期妇女及年老体弱者应在医师指导下服用。 8.对本品过敏者禁用,过敏体质者慎用。 10.本品性状发生改变时禁止使用。 11.儿童必须在成人监护下使用。 12.请将本品放在儿童不能接触的地方。 13.如正在使用其他药品,使用本品前请咨询医师或药师。 [药物相互作用]如与其他药物同时使用可能会发生药物相互作用,详情请咨询医师或药师。[贮藏] [包装] [有效期] [执行标准] [批准文号] [说明书修订日期] [生产企业]
企业名称: 生产地址: 邮政编码: 电话号码: 传真号码: 网址: 如有问题可与生产企业联系。
达立通颗粒非处方药说明书范本 请仔细阅读说明书并按说明使用或在药师指导下购买和使用。 [药品名称] 通用名称:达立通颗粒 汉语拼音: [成份] [性状] [功能主治]清热解郁,和胃降逆,通利消滞。用于肝胃郁热所致痞满证,症见胃脘胀满、嗳气、纳差、胃中灼热、嘈杂泛酸、脘腹疼痛、口干口苦;运动障碍型功能性消化不良见上述症状者。[规格] 每袋装6克。 [用法用量] 温开水冲服,一次1袋,一日3次。于饭前服用。 [不良反应] 个别患者服药后可能出现腹痛、腹泻、呕吐、皮疹。 [禁忌] [注意事项] 1.饮食宜清淡,忌酒及辛辣、生冷、油腻食物。 2.忌愤怒、忧郁,保持心情舒畅。 3.不宜在服药期间同时服用滋补性中药。 4.脾虚便溏者慎用;胃寒痛者不适用,主要表现为遇凉则胃痛发作或加重,得温暖则胃痛减轻,喜热饮食,或大便溏。 5.孕妇慎用,儿童、哺乳期妇女、年老体弱者应在医师指导下服用。 6.有高血压、心脏病、肝病、糖尿病、肾病等慢性病患者应在医师指导下服用。 7.胃胀或腹痛等症状严重者,应及时去医院就诊。 8.服药3天症状无缓解,应去医院就诊。 9.对本品过敏者禁用,过敏体质者慎用。 10.本品性状发生改变时禁止使用。 11.儿童必须在成人监护下使用。 12.请将本品放在儿童不能接触的地方。 13.如正在使用其他药品,使用本品前请咨询医师或药师。 [药物相互作用] 如与其他药物同时使用可能会发生药物相互作用,详情请咨询医师或药师。[贮藏] [包装] [有效期] [执行标准] [批准文号] [说明书修订日期] [生产企业] 企业名称: 生产地址: 邮政编码: 电话号码: 传真号码:
妇科疾病常用非处方药应用指南
妇科疾病常用非处方药应用指南 主讲人:王璞
前言 非处方药相对安全、使用方便,是日常生活中 用来治疗一些病因较明确、症状较轻疾病的主 要药物,因此其使用广泛,但是由于专业知识 相对不足,致使消费者(患者)在使用非处方 药防治疾病过程中难免存在误区,因此职业药 师,特别是药店药师的指导作用就十分重要。 妇科疾病是应用非处方药治疗较多的一类疾病, 因此本次讲座以妇科疾病常用的非处方药应用 指导为主题,围绕执业药师在非处方药应用中 的指导作用和注意事项展开。
讲座目录 ?一、非处方药简介 ?二、执业药师应用非处方药指导纲要?三、妇科疾病常用非处方药应用指南
一、非处方药简介 ?(一)概念 ?(二)非处方药与处方药的区别?(三)非处方药的特点 ?(四)警示语或忠告语 ?(五)非处方药类别
(一)概念 ?非处方药,简称OTC(over the counter drug ),指为方便公众用药, 在保证用药安全的前提下,经国家卫生行政部门规定或审定后,不需要医师或其它医疗专业人员开写处方即可购买的药品,一般公众凭自我判断,按照药品标签及使用说明就可自行使用。 ?非处方药一般是从上市两年以后的处方药中遴选出来的,而且作为非处 方药使用后,如发现有不妥之处,还会重新回到处方药目录中,故具有疗效明确、质量稳定,副作用小,安全稳定等特点。
(二)非处方药与处方药的区别 项目非处方药处方药疾病诊断者患者自我诊断医生 疾病类型小伤小病解除症状,慢性病 维持治疗 病情较重,需经医生诊断治 疗 取药凭据不需处方医生处方 取药地点医院调剂室、药店、超市 (乙类) 医院调剂室、药店(凭医生 处方) 服药天数短长 给药途径口服、外用为主根据病情和医嘱执行品牌保护方式品牌新药保护、专利保护期宣传对象消费者医生 广告范围大众传播媒介专业性医药报刊 专有标示有无
门店药品销售管理制度
门店药品销售管理制度 1、为确保门店销售药品的合法性和规范性,安全合理为消费者提供放心药品和优质服务,特制定本制度。 2、门店销售药品应按依法批准的经营方式和经营范围经营。 3、凡从不药品零售工作的营业员,上岗前必须经过业务培训考核合格,同时对与药品直接触的工作人员每年定期进行健康检查,体检合格方可上岗工作。 4、药品陈列应清洁美观,摆放时应做到药品与非药品分开,处方药与非处方药分开,内服药与外用药分开。 5、销售药品严格遵守有关法律、法规和制度,正确介绍药品的性能、用途,禁忌及注意事项。 6、销售药品时,处方要经执业药师或具有药师以上职称的人员审核后方可调配和销售。 7、处方药不应用采用开架自选的销售方式。 8、无医师开具的处方,不得销售处方药。 9、对处方所列药品不得擅自更改或代用。 10、对有配伍禁忌或超剂量的处方,应当拒约调配销售,必要时,需经原处方医生更正或重新签字方可调配和销售。 11、处方的审核调配或销售人员均应在处方上签字或盖章,处方按有关规定保存备查。 12、非处方药可凭处方出售。但如顾客要求,执业药师或药师负责对药品的购买和使用进行指导。 13、销售的中药饮片应符合炮制规范,并做到计量准确。 14、药品拆零销售使用的工具,包裹应清洁和卫生,出售时应在药袋上写明药品名称、规格、服法、用量、有效期等到内容。 15、门店应在零店堂内提供咨询服务,为消费者提供用药咨询和指导,指导顾客安全、合理用药。 16、药品不得采用有奖销售、附赠药品或礼品销售等方式销售。 17、结缺货药品要认真登记,及时向业务部或配送中心传递药品信息,以便及时组织货源及时上柜。 18、门店应在店堂明示服务公约,公布监督电话和设置顾客意见簿。 19、门店对顾客反映的问,应认真对待,详细记录、及时处理。 20、门店内进行的广告宣传,应符合国有关规定。 门店处方管理制度 1、为加强门店处方管理,特制定本制度。 2、处方调剂人员必须经专业或岗位培训,考试合格后方可上岗。 3、处方审核人员应具有执业药师或有药师(或中药师)以上的专业技术职称。 4、处方审核人员收到处方后,认真审查处方的姓名、年龄、性别、药品名称、剂量及处方
解毒痤疮丸等4种非处方药说明书
附件2: 解毒痤疮丸等4种非处方药说明书 解毒痤疮丸说明书 请仔细阅读说明书并按说明使用或在药师指导下购买和使用 【药品名称】 通用名称:解毒痤疮丸 汉语拼音: 【成份】 【性状】 【功能主治】清肺胃、解热毒、消痤疮。痤疮属肺胃热盛证,症见皮肤局部粉刺,丘疹,脓疱,以及面红,口渴,口臭,小便短黄,大便秘结,舌红苔黄等。 【规格】每袋装6克 【用法用量】口服,一次6克(1袋),一日3次。4周为一个疗程。 【不良反应】胃脘不适,大便稀溏或腹泻,腹痛。 【禁忌】脾胃虚寒者禁用。 【注意事项】 1.忌烟酒、辛辣、油腻及腥发食物。 2.保持面部卫生,切忌以手挤压患处。不宜滥用化妆品及外涂药物,必要时应在医师或药师指导下使用。 3.不宜在服药期间同时服用滋补性中药。 4.脾虚便溏者慎用。有高血压、心脏病、肝病、糖尿病、肾病等慢性病严重者应在医师指导下服用。 5.孕妇慎用。哺乳期妇女不宜服用。儿童应在医师指导下服用。 6.本品中大黄含有蒽醌类化合物,长期服用可能导致结肠黑变病。 7.服药后大便次数增多且不成形者,应酌情减量。 8.服药期间如出现其他不适应到医院就诊。 9.如有较多囊肿、脓疮、结节等损害者,应去医院就诊。 10.用药2周症状无缓解,应去医院就诊。 11.严格按用法用量服用,本品不宜长期服用。 12.对本品过敏者禁用,过敏体质者慎用。 13.本品性状发生改变时禁止使用。 14.儿童必须在成人监护下使用。 15.请将本品放在儿童不能接触的地方。 16.如正在使用其他药品,使用本品前请咨询医师或药师。 【药物相互作用】如与其他药物同时使用可能会发生药物相互作用,详情请咨询医师或药师。【贮藏】【包装】【有效期】【执行标准】【批准文号】【说明书修订日期】 【生产企业】 企业名称:生产地址:邮政编码:电话号码:传真号码:网址: 如有问题可与生产企业联系 珍牡胶囊说明书 请仔细阅读说明书并按说明使用或在药师指导下购买和使用 【药品名称】
化学药品非处方药说明书格式
附件1: 化学药品非处方药说明书规范细则一、化学药品非处方药说明书格式 非处方药、外用药品标识位置 X X X说明书 请仔细阅读说明书并按说明使用或在药师指导下购买和使用 警示语位置 【药品名称】 【成份】 【性状】 【作用类别】 【适应症】 【规格】 【用法用量】 【不良反应】 【禁忌】 【注意事项】 【药物相互作用】 【贮藏】 【包装】 【有效期】 【执行标准】 【批准文号】
【说明书修订日期】 【生产企业】 如有问题可与生产企业联系 二、化学药品非处方药说明书各项内容书写要求 非处方药、外用药品标识 非处方药、外用药品标识在说明书首页右上角标注。 外用药品专用标识为红色方框底色内标注白色“外”字。药品说明书如采用单色印刷,其说明书中外用药品专用标识亦可采用单色印刷。 非处方药专有标识按《关于公布非处方药专有标识及管理规定的通知》规定使用。 说明书标题 “XXX说明书”中的“XXX”是指该药品的通用名称。 请仔细阅读说明书并按说明使用或在药师指导下购买和使用 该忠告语必须标注,采用加重字体印刷。 警示语 是指需特别提醒用药人在用药安全方面需特别注意的事项。 有该方面内容,应当在说明书标题下以醒目的黑体字注明。无该方面内容的,不列该项。 【药品名称】 按下列顺序列出: 通用名称:属《中国药典》收载的品种,其通用名称应当与药典一致;药典未收载的品种,其名称应当符合药品通用名称命名原则。 商品名称:未批准使用商品名称的药品不列该项。 英文名称:无英文名称的药品不列该项。 汉语拼音: 【成份】 处方组成及各成份含量应与该药品注册批准证明文件一致。成份含量按每一个制剂单位
处方药说明书_药物过量_撰写要点和案例分析
?审评规范? 处方药说明书[药物过量]撰写要点和案例分析 萧惠来 国家食品药品监督管理总局药品审评中心,北京 100038 摘要:处方药说明书是重要的沟通工具,关系到药品的正确使用与患者的用药安全。介绍我国、美国食品药品管理局和欧盟药品管理局对处方药说明书[药物过量]项目撰写要点的有关要求,并从报送到国家食品药品监督管理总局药审中心的说明书样稿中选取11个典型案例,分析目前我国药品注册过程中该项目存在的问题。结果发现基本内容缺失是该项目存在的主要问题,以此为鉴并且避免这些问题的出现对规范药品说明书撰写和有效监管大有裨益。 关键词:处方药;药品说明书;药物过量;药品监管;案例分析 中图分类号:R956.13 文献标志码:A 文章编号:1674 - 6376 (2015) 03 - 0251 - 05 DOI: 10.7501/j.issn.1674-6376.2015.03.004 Writing highlights and case analysis of overdosage section of labeling for prescription drug XIAO Hui-Lai Center for Drug Evaluation, China Food and Drug Administration, Beijing 100038, China Abstract: The labeling for Prescription drug is an important communication tool, that is related to the correct use and drug safety of patients. The writing highlights of overdosage section of labeling for prescription drug required by CFDA, FDA and EMA are described. 11 typical cases are selected from the labeling drafts submitted to CFDA CDE for registration, and current problems of the section in process of drug registration of our country are analyzed. That lack of basic content is the main problem is found. Taking this as a lesson and avoiding these problems is of greater advantage to standardization of drug labeling and itseffective supervision. Key words: prescription drug;labeling; overdosage;drug administration;case analysis 处方药说明书是重要的沟通工具,关系到药品的正确使用与患者的用药安全;需要用清楚而有益的方式,向医护人员提供安全和有效用药必需的详细处方资料[1]。处方药说明书[药物过量]项目主要介绍该药品过量引起的急性毒性反应、中毒剂量和救治措施。药物过量往往会引起严重的毒性反应,甚至危及生命。不言而喻该项目关系到患者的安危,应引起足够重视。本文首先介绍我国、美国食品药品管理局(FDA)和欧盟药品管理局(EMA)对处方药说明书[药物过量]项目撰写要点的要求;然后以此为标准,从报送到国家食品药品监督管理总局药审中心(以下简称“药审中心”)的说明书样稿中选取11个典型案例,分析目前我国药品注册报送的说明书样稿存在的问题,从正反两方面阐述如何写好说明书该项目,期望对说明书撰写者有帮助,也对说明书监管有益。 1[药物过量]撰写要点 1.1我国的要求 我国“化学药品和治疗用生物制品说明书规范细则[2]”规定“[药物过量]详细列出过量应用该药品可能发生的毒性反应、剂量及处理方法。未进行该项实验且无可靠参考文献的,应当在该项下予以说明。” 2004年,药品审评中心曾拟定“化学药品、生物制品说明书指导原则(第二稿)”,该指导原则虽然没有正式公布实施,但有重要参考价值。该指导原则要求:[药物过量] 本项应对急性药物过量的症状、体征和实验室阳性发现进行描述,同时应提供 收稿日期:2015-02-09 作者简介:萧惠来,男,教授,研究方向为药品审评。E-mail: penglai8051@https://www.360docs.net/doc/e79580234.html,
非处方药药品标签、使用说明书和包装指导原则
非处方药药品标签、使用说明书和包装指导原则 为了作好第一批《国家非处方药目录》药品审核登记工作,特制定《非处方药药品标签、使用说明书和包装指导原则》(以下简称《指导原则》),供第一批《国家非处方药目录》药品审核登记使用。 非处方药药品标签、使用说明书及包装应按照《指导原则》,在原批准内容的基础上起草和修改,以达到科学、简明、消费者易懂的要求。 凡《指导原则》中未包括的项目,必须与原批准的药品标签、使用说明书和包装一致。 一、使用说明书内容要求 使用说明书中应包括以下内容: l、药品名称 必须在显著位置标明药品的通用名称、汉语拼音、英文名称、商品名称(如无商品名称,此项可省略)。 2、药物组成 必须注明药品中所有活性成分(中成药应标明处方全部组成)的通用名称及最小服用单位内的各成分含量和所有非活性成分的名称。不允许使用“等”、“……”等缩略语。 3、药理作用 除原有的药理作用外,必须注明此药品为XXX类(如感冒用药、暑湿类药)非处方药药品。对于隶属多类的药品,必须同时注明。
4、适应症(中成药为功能与主治) 描述必须清楚明确,不得超出药品原批准适应症范围,不允许使用“等”、“……”等缩略语。 5、用法用量 使用说明书中必须清楚描述药品的用法用量。用法应与药品原批准的用法相同,用量应以片、丸、支等明确的单位表达;必须标明最大用量,并且不得超过原批准用量。 6、注意事项 (1)对于《国家非处方药目录》中注明使用时间的药品,必须注明“如在XX日内症状未缓解,请找医生咨询”。 (2)原药品使用说明书的药物使用过量警告,必须保留,同时还必须注明“如服用过量,请立即向医务人员求助”。 (3)必须注明“当药品性状发生改变时禁止服用”。 (4)必须注明“儿童必须在成人的监护下使用”及“请将此药品放在儿童不能接触的地方”。 (5)如药品须慎用时,必须注明。 (6)如药品对各种实验室测定指标产生影响,必须注明。 7、不良反应 应包括药品所有已证明的不良反应和潜在的不良反应,原使用说明书中的不良反应内容必须保留。必须注明药品对于儿童、老人、孕妇及其它特殊人群的不良反应,如药品未证明对以上人员的安全性,必须在注意事项中注明。
化学药品处方药转换非处方药申报资料及要求
化学药品处方药转换非处方药申报资料及要求 一、申报分类 第一类:与公布的非处方药处方、锅药途径相同,仅剂型或规格不同的品种 第二类:由己公布非处方药活性成分组成的复方制剂 第三类:不包括在以上两类中的品种 二、申报资料项目 (一)综述资料 1.处方药转换非处方药申请表 2.申报资料目录 3.申报说明 应包括国内外有关该药品研究、生产、销售和使用安全性、有效性情况的综述,在国外是否作为非处方药管理,以及对申报资料来源及文献检索范围的说明。
4.拟使用的非处方药说明书样稿 需附原说明书,如对原说明书中的内容进行调整或补充,须说明理由。 5.现销售的最小销售单位样品一份 6.证明性文件 应包括药品生产批件或进口注册证,代理商还应提供生产企业授权书原件。 (二)药学资料 7.药品制剂及活性成分、非活性成分的法定质量标准应在本项资料中说明制剂及所有成分的标准来源,己列入我国药典的成分可不提供此成分质量标准。 8.药品质量资料 应包括药品质量情况报告及稳定性研究报告。 (三)药品安全性研究 9.毒理研究资料
应包括制剂和活性成分毒理研究资料。己公布非处方药活性成分可不提供本项资料。 10.不良反应(事件)研究资料 应包括制剂及各成分药品不良反应(事件)研究综述和相关临床试验及文献资料、省级以上药品不良反应监测机构检索报告(检索时间应截止到申报前3个月内)。 11.依赖性研究资料 应包括制剂及各成分依赖性研究综述和相关试验及文献资料(无依赖性成分可不提供此成分资料,如药品各成分均无依赖性,可不提供本项资料)。 12.耐受性研究资料 应包括制剂及各成分耐受性研究综述和相关临床试验及文献资料。 13.与其它药物和食物相互作用情况 应包括研究综述和相关试验及文献资料。 14.消费者进行自我诊断、自我药疗情况下的药物安全性研究资料 重点说明患者是否可自我诊断所申报的适应症,是否需要专业人员帮助,用法用量是否可以正确掌握。
中成药非处方药说明书规范细则
附件2: 中成药非处方药说明书规范细则一、中成药非处方药说明书格式 非处方药、外用药品标识位置 X X X说明书 请仔细阅读说明书并按说明使用或在药师指导下购买和使用 警示语位置 【药品名称】 【成份】 【性状】 【功能主治】 【规格】 【用法用量】 【不良反应】 【禁忌】 【注意事项】 【药物相互作用】 【贮藏】 【包装】 【有效期】 【执行标准】 【批准文号】 【说明书修订日期】 【生产企业】 如有问题可与生产企业联系
二、中成药非处方药说明书各项内容书写要求 非处方药、外用药品标识 非处方药、外用药品标识在说明书首页右上角标注。 外用药品专用标识为红色方框底色内标注白色“外”字。药品说明书如采用单色印刷,其说明书中外用药品专用标识亦可采用单色印刷。 非处方药专有标识按《关于公布非处方药专有标识及管理规定的通知》规定使用。 说明书标题 “XXX说明书”中的“XXX”是指该药品的通用名称。 请仔细阅读说明书并按说明使用或在药师指导下购买和使用 该忠告语必须标注,采用加重字体印刷。 警示语 是指需特别提醒用药人在用药安全方面需特别注意的事项。 有该方面内容的,应当在说明书标题下以醒目的黑体字注明。无该方面内容的,不列该项。 【药品名称】 按下列顺序列出: 通用名称:如该药品属《中华人民共和国药典》收载的品种,其通用名称应当与药典一致;药典未收载的品种,其名称应当符合药品通用名称命名原则。 汉语拼音: 【成份】 除《中药品种保护条例》第十三条规定的情形外,必须列出全部处方组成和辅料,处方所含成份及药味排序应与药品标准一致。 处方中所列药味其本身为多种药材制成的饮片,且该饮片为国家药品标准收载的,只需写出该饮片名称。
处方药与非处方药及包装、标签和说明书的管理(三)
[模拟] 处方药与非处方药及包装、标签和说明书的管理 (三) B型题是一组试题(2至4个)公用一组A、B、C、D、E五个备选。选项在前,题干在后。每题只有一个正确答案。每个选项可供选择一次,也可重复选用,也可不被选用。考生只需为每一道题选出一个最佳答案。 [A].酚酞指示剂 [B].甲基橙指示液 [C].永停终点法 [D].自身指示终点法 [E].淀粉指示液 第1题: 高碘酸钾法测定山梨醇及注射液的含量______ 参考答案: E 详细解答: 第2题: 直接酸滴定测定阿司匹林含量______ 参考答案: A 详细解答: 第3题: 双相滴定法测定苯甲酸钠的含量______ 参考答案: B 详细解答: 第4题: 亚硝酸钠滴定法测对氨基水杨酸钠含量______
参考答案: C 详细解答: 第5题: 直接酸碱滴定法测定阿司匹林含量时,氢氧化钠滴定液(0.1mol/L)滴定度的计算式(摩尔比为1:1时)______ 参考答案: D 详细解答: 第6题: 两步滴定法测定阿司匹林片剂含量的计算式______ 参考答案: C 详细解答: 第7题: HPLC测定阿司匹林栓剂含量的计算式______
参考答案: A 详细解答: [A].GC [B].双相滴定法 [C].赭色沉淀 [D].橙红色沉淀 [E].对氯苯氧异丁酸 第8题: 苯甲酸钠中性溶液与三氯化铁试液反应______ 参考答案: C 详细解答: 第9题: 以氢氧化钠滴定液(0.1mol/L)滴定,酚酞指示液指示终点,检查氯贝丁酯的酸度______ 参考答案: E 详细解答: 第10题: 对氨基水杨酸钠中的间氨基酚的检查______ 参考答案: B 详细解答: 第11题: 对氨基水杨酸钠的重氮-偶合呈色反应______ 参考答案: D
非处方药说明书范本
非处方药说明书范本 1.疏清颗粒 疏清颗粒说明书 请仔细阅读说明书并按说明使用或在药师指导下购买和使用。 [药品名称] 通用名称:疏清颗粒 汉语拼音: [成份] [性状] [功能主治]清热解毒,宣泄肺胃。用于小儿急性上呼吸道感染属风热证,证见:发热、鼻塞、咽痛、流涕、口渴、咳嗽、汗出、舌红或苔薄黄。 [规格] 每袋装3克 [用法用量] 开水冲服。1岁以下,一次3克;1~3岁,一次6克;4~6岁,一次9克;7岁以上,一次12克;一日3次。 [不良反应]监测数据显示,本品有恶心、呕吐、腹泻、皮疹等不良反应报告。 [禁忌] 1.肝功能严重损害者禁用。 2.对本品及所含成份过敏者禁用。 [注意事项] 1.本品宜饭后服用,禁与茶及含鞣酸类药合用,忌辛辣生冷油腻食物。 2.风寒感冒者不适用,表现为恶寒发热,无汗、咳嗽、喉痒、流清涕、咽不红。 3.按照用法用量服用,服药3天症状无改善或服药期间症状加重者,应及时就医。 4.体温超过38.5℃应及时就医。 5.脾胃虚弱,大便稀溏者慎用。 6.体弱者慎用。 7.有心脏病、肾病等疾病应在医师指导下服用。 8.对本品及所含成份过敏者禁用,过敏体质者慎用。 9.本品性状发生改变时禁止使用。 10.儿童必须在成人监护下使用。 11.请将本品放在儿童不能接触的地方。 12.如正在使用其他药品,使用本品前请咨询医师或药师。 [药物相互作用]如与其他药物同时使用可能会发生药物相互作用,详情请咨询医师或药师。 [贮藏] [包装] [有效期] [执行标准] [批准文号] [说明书修订日期] [生产企业] 企业名称:
生产地址: 邮政编码: 电话号码: 传真号码: 网址: 如有问题可与生产企业联系。
FDA对处方药说明书儿科资料的要求_黄芳华
?国外信息? FDA对处方药说明书儿科资料的要求 黄芳华,萧惠来 国家食品药品监督管理总局药品审评中心,北京 100038 摘要:美国食品药品监督管理局(FDA)于2013年2月发布了《人用处方药和生物制品说明书儿科资料指导原则(草案)》,该指导原则详细规定了儿科资料在处方药说明书中的合适位置以及内容要求,以指导儿科患者的合理用药。介绍该指导原则的主要内容,包括FDA对处方药说明书儿科资料要求的主要法规依据、儿科年龄分段、决策的儿科资料分类等背景资料,以及儿科资料在说明书中具体要求,以期对我国处方药说明书的撰写和监管工作的开展提供有益的借鉴,以便指导医生和患者合理用药。 关键词:处方药;药品说明书;儿科资料;合理用药;指导原则 中图分类号:R951 文献标志码:A 文章编号:1674 - 6376 (2013) 05 - 0330- 05 DOI: 10.7501/j.issn.1674-6376.2013.05.003 FDA requirements for pediatric data of prescription drug specifications HUANG Fang-hua, XIAO Hui-lai Center for Drug Evaluation, State Food and Drug Administration, Beijing 100038, China Abstract: US Food and Drug Administration (FDA) issued “Guidance for Industry and Review Staff Pediatric Information Incorporated Into Human Prescription Drug and Biological Products Labeling (Draft)” on February 2013. The draft guidance provides the recommendations on placement and content of pediatric data in human prescription drug and biological products specifications, which aims at giving the guidance for the appropriate use of drugs in treating pediatric patients. This article introduces its main content, including the background of FDA main regulatory foundation on the requirement of pediatric data in human prescription drugs specifications, pediatric age categories, and categorise of pediatric data for decision making, as well as the details of requirement on pediatric data in specifications, expecting to provide the useful guidance for writing and supervision of drug specifications in China. Key words: prescription drug; specifications; pediatric data; guidance 美国食品药品监督管理局(FDA)于2013年2月发布了《人用处方药和生物制品说明书儿科资料指导原则(草案)》[1],详细规定了儿科资料在处方药说明书中的合适位置和内容。通过这些规定,以指导儿科患者的合理用药。目前我国还没有类似的指导原则,仅在2006年颁布实施的《化学药品和治疗用生物制品说明书规范细则》的“儿童用药”项有简单的原则规定[2]。本文介绍FDA该指导原则的主要内容,期望对我国处方药说明书的撰写和监管工作的开展提供有益的借鉴,以便指导医生和患者合理用药。 1背景资料 1.1FDA对处方药说明书儿科资料要求的主要法规依据 20世纪90年代早期之前,美国的大部分药品说明书包括很少或者没有儿科应用信息,以告知这些药物用于儿科人群的有效性和安全性。90年代之后,FDA通过一系列的行动来加强对说明书儿科信息的监管。1994年12月FDA通过发布对说明书儿童用药小节的要求修订的规定终稿,来加强药品说明书中的儿科应用信息。1998年10月FDA发布了《关于要求制造商对新药和生物制品在儿科患者中的安全性和有效性评估的规定(儿科规定)》终稿,该儿科规定于2002年10月被暂停使用。 收稿日期:2013-08-15 作者简介:黄芳华,女,博士,副主任药师,主要从事药品技术审评工作。Tel: (010)68585566-447 E-mail: huangfh@https://www.360docs.net/doc/e79580234.html,
非处方药说明书范本
附件2 非处方药说明书范本 板蓝根泡腾片说明书 请仔细阅读说明书并按说明使用或在药师指导下购买和使用 [药品名称] 通用名称:板蓝根泡腾片 汉语拼音: [成份] [性状] [功能主治]清热解毒,凉血利咽,消肿。用于热毒壅盛,咽喉肿痛;扁桃腺炎见上述证候者。[规格]每片重3.5克 [用法用量] 热水泡服,一次1~2 片,一日3~4次。 [不良反应] [禁忌] 本品为泡腾片,禁止吞服。 [注意事项] 1.忌烟酒、辛辣、鱼腥食物。 2.不宜在服药期间同时服用滋补性中药。 3.孕妇及哺乳期妇女慎用,且应在医师指导下使用。 4.儿童、年老体弱、脾虚便溏者应在医师指导下服用。 5.有高血压、心脏病、肝病、糖尿病、肾病等慢性病患者应在医师指导下服用。 6.扁桃体有化脓或发热体温超过38.5℃的患者应去医院就诊。 7.服药3天症状无缓解,应去医院就诊。 8.对本品过敏者禁用,过敏体质者慎用。 9.本品性状发生改变时禁止使用。 10.儿童必须在成人监护下使用。 11.请将本品放在儿童不能接触的地方。 12.如正在使用其他药品,使用本品前请咨询医师或药师。 [药物相互作用]如与其他药物同时使用可能会发生药物相互作用,详情请咨询医师或药师。[贮藏] [包装] [有效期] [执行标准] [批准文号] [说明书修订日期] [生产企业] 企业名称: 生产地址: 邮政编码: 电话号码: —1 —
传真号码: 网址: 如有问题可与生产企业联系—2—
丹芎瘢痕涂膜说明书 请仔细阅读说明书并按说明使用或在药师指导下购买和使用 [药品名称] 通用名称:丹芎瘢痕涂膜 汉语拼音: [成份] [性状] [功能主治] 活血化瘀,软坚止痒。用于减轻和辅助治疗烧烫伤创面愈合后的瘢痕增生。 [规格] 每支装40克。 [用法用量] 外用。深Ⅱ度烧烫伤创面已愈合瘢痕尚未形成、或瘢痕形成初期,按下述方法使用:涂药前先用温水洗净患处,擦干,将本品均匀涂于患处,即形成药膜,次日揭去药膜。一日1次,5 个月为一疗程。每次涂药面积不得超过患者表面积的8%。 [不良反应] 本品有皮疹、瘙痒、水疱等病例报告。 [禁忌] 1.创面未愈合者忌用。 2.孕妇忌用。 3.婴幼儿忌用。 4.硬损性疤痕或感染性疤痕禁用。 5.酒精过敏者禁用。 [注意事项] 1.本品为外用药,禁止内服。 2.本品适用于创面已愈合者。 3.本品为烧烫伤创面愈合后瘢痕增生的辅助治疗药品,应在医生确诊后使用。 4.第一次使用本品前应咨询医生,治疗期间应定期到医院检查。 5.切勿接触眼睛、口腔等黏膜处。皮肤破溃处禁用。 6.瘢痕表面涂药时,药膜要达到一定的厚度(0.3毫米以上),涂膜范围要超出瘢痕面积。 7.发生在非暴露部位、关节活动部位的疤痕,表面涂药、待药成膜不黏手时,外敷纱布固定或用 绷带包扎固定,防止因摩擦或活动时药膜脱落。包扎瘢痕处可2~3 天更换涂膜一次。 8.早期疤痕用药治疗,痛、痒、紧缩症状减轻时,活动量应由少逐渐增加。禁止早期瘢痕用药当 天大量活动,以免水疱发生。 9.揭药时应该轻轻将药膜从边缘揭起取下,重新涂药。禁忌瘢痕局部用力反复摩擦,以免发生水疱。 10.有出血倾向者、经期妇女慎用,且应由医师指导。哺乳期妇女、儿童、年老体弱者应在医师 指导下使用。 11.天花和凹陷疤痕不宜使用。 12.本品不宜大面积使用,用药后皮肤过敏者应停止使用,症状严重者应去医院就诊。 13.对本品及酒精过敏者禁用,过敏体质者慎用。 14.本品性状发生改变时禁止使用。 15.儿童必须在成人监护下使用。 16.请将本品放在儿童不能接触的地方。 —3 —
地衣芽孢杆菌活菌颗粒非处方药说明书范本
地衣芽孢杆菌活菌颗粒非处方药说明书范本 请仔细阅读说明书并按说明使用或在药师指导下购买和使用。[药品名称] 通用名称:地衣芽孢杆菌活菌颗粒 商品名称: 英文名称: 汉语拼音: [成份] [性状] [作用类别]本品为消化类非处方药品。 [适应症]用于细菌或真菌引起的急、慢性肠炎、腹泻。也可用于其他原因引起的肠道菌群失调的防治。 [规格]每袋0.5克(5亿活菌)。 [用法用量]口服,成人,一次1袋;儿童,一次0.5袋;一日3次;首次加倍。服用时将颗粒溶于水或牛奶中混匀后服用。[不良反应]个别患者可见便秘。 [禁忌] [注意事项] 1.本品为活菌制剂,切勿将本品置于高温处,溶解时水温不宜超过40℃。 2.避免与抗菌药同服,必要时需间隔3小时服用。 3.对本品过敏者禁用,过敏体质者慎用。 4.本品性状发生改变时禁止使用。 5.请将本品放在儿童不能接触的地方。
6.儿童必须在成人监护下使用。 7.如果正在使用其他药品,使用本品前请咨询医师或者药师。[药物相互作用] 1.抗菌药与本品合用时可减低其疗效。 2.铋剂、鞣酸、药用炭、酊剂等能抑制、吸附活菌,不能并用。 3.如与其他药物同时使用可能会发生药物相互作用,详情请咨询医生或药师。 [药理作用]本品以活菌进入肠道后,对葡萄球菌、酵母样菌等致病菌有拮抗作用,而对双歧杆菌、乳酸杆菌、拟杆菌、笑话链球菌有促生长作用,从而可调整菌群失调达到治疗目的。本品可促使机体产生抗菌活性物质,杀灭致病菌。此外通过夺氧生物效应使肠道缺氧,有利于大量厌氧菌生长。 [贮藏] [包装] [有效期] [执行标准] [说明书修订日期] [生产企业] 企业名称: 生产地址: 邮政编码: 电话号码: 传真号码: 网址: 如有问题可与生产企业联系。
处方药与非处方药分类管理办法
处方药与非处方药分类管理办法(试行)(局令第10号) 1999年06月18日发布 《处方药与非处方药分类管理办法》(试行)于1999年6月11日经国家药品监督管理局局务会审议通过,现予发布。本办法自2000年1月1日起施行。 一九九九年六月十八日 处方药与非处方药分类管理办法 (试行) 第一条为保障人民用药安全有效、使用方便,根据《中共中央、国务院关于卫生改革与发展的决定》,制定处方药与非处方药分类管理办法。 第二条根据药品品种、规格、适应症、剂量及给药途径不同,对药品分别按处方药与非处方药进行管理。 处方药必须凭执业医师或执业助理医师处方才可调配、购买和使用;非处方药不需要凭执业医师或执业助理医师处方即可自行判断、购买和使用。 第三条国家药品监督管理局负责处方药与非处方药分类管理办法的制定。各级药品监督管理部门负责辖区内处方药与非处方药分类管理的组织实施和监督管理。 第四条国家药品监督管理局负责非处方药目录的遴选、审批、发布和调整工作。 第五条处方药、非处方药生产企业必须具有《药品生产企业许可证》,其生产品种必须取得药品批准文号。 第六条非处方药标签和说明书除符合规定外,用语应当科学、易懂,便于消费者自行判断、选择和使用。非处方药的标签和说明书必须经国家药品监督管理局批准。 第七条非处方药的包装必须印有国家指定的非处方药专有标识,必须符合质量要求,方便储存、运输和使用。每个销售基本单元包装必须附有标签和说明书。
第八条根据药品的安全性,非处方药分为甲、乙两类。 经营处方药、非处方药的批发企业和经营处方药、甲类非处方药的零售企业必须具有《药品经营企业许可证》。 经省级药品监督管理部门或其授权的药品监督管理部门批准的其它商业企业可以零售乙类非处方药。 第九条零售乙类非处方药的商业企业必须配备专职的具有高中以上文化程度,经专业培训后,由省级药品监督管理部门或其授权的药品监督管理部门考核合格并取得上岗证的人员。 第十条医疗机构根据医疗需要可以决定或推荐使用非处方药。 第十一条消费者有权自主选购非处方药,并须按非处方药标签和说明书所示内容使用。 第十二条处方药只准在专业性医药报刊进行广告宣传,非处方药经审批可以在大众传播媒介进行广告宣传。 第十三条处方药与非处方药分类管理有关审批、流通、广告等具体办法另行制定。 第十四条本办法由国家药品监督管理局负责解释。 第十五条本办法自2000年1月1日起施行。
