workbench热力学与结构力学多物理场耦合仿真

Workbench 热应力与结构应力多物理场耦合仿真
这是分析的例子ANSYS实例数据(ANSYS WORKBENCH 14.5版本)
fenxi.rar
自己做的一个小例子,下图所示刚基板受热,热传导到陶瓷上,两种材料热膨胀系数不一样,受热速度不一样,导致温度不一样,热导致两种材料发生热应力
也可以坚固基板的四个螺钉孔,分析热导致的结构应力
ANSYS workbench 中建立瞬时热分析,再建立结构分析,结构分析共用热分析结果。如下图所示:
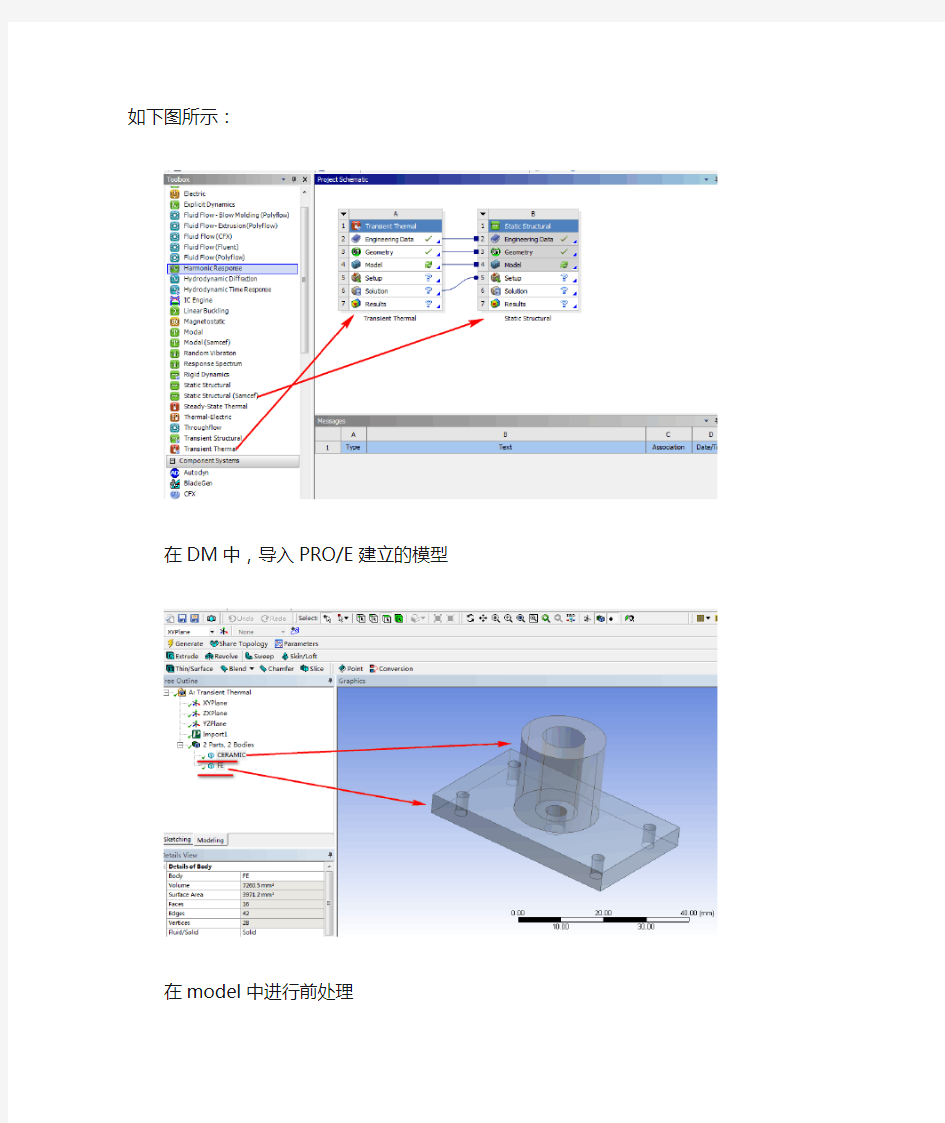
在DM中,导入PRO/E建立的模型
在model中进行前处理
给两个PART 添加材料属性
发现没有陶瓷的材料,所以要添加陶瓷的材料属性。
进入到材料属性中,又发生陶瓷的材料属性太少,只有一点热传导率和比热容,要新加弹性模量才能结构分析,还要增加热膨胀系数
给陶瓷新增热膨胀系数,弹性模量
刷新材料属性
给陶瓷,铁添加材料属性
焊接,在这里假设为绑定接触
接触的类型多,且复杂,最难设置的就是接触边界条件,如果接触没有设置对,仿真结果完全不对,或者不收敛。特别是螺钉的接触设置,带间隙的接触
划分网格,自由划分如下,明显感觉陶瓷划分不好
使用multizone网格
分析时间改为50S后的结果
在一个面加载150度温度,查看50S后的结果
分析后温度场
由于前面已经增加了结构分析,所以分析里面已经有结构的分析项
直接查看不对基板进行约束的,自由状态的结构应力图:
对基板螺钉孔进行固定约束,再查看结果:增加约束
大家关注的是陶瓷的应力,所以可以单独查看陶瓷应力
增加螺钉后,陶瓷与基板的接触应力变大了,肯定是螺钉固定基板,导致基板的形变发生变
化,引起接触区域的变形更大导致。这时需要优化螺钉的固定位置。
物理化学热力学第一定律总结
热一定律总结 一、 通用公式 ΔU = Q + W 绝热: Q = 0,ΔU = W 恒容(W ’=0):W = 0,ΔU = Q V 恒压(W ’=0):W =-p ΔV =-Δ(pV ),ΔU = Q -Δ(pV ) → ΔH = Q p 恒容+绝热(W ’=0) :ΔU = 0 恒压+绝热(W ’=0) :ΔH = 0 焓的定义式:H = U + pV → ΔH = ΔU + Δ(pV ) 典型例题:3.11思考题第3题,第4题。 二、 理想气体的单纯pVT 变化 恒温:ΔU = ΔH = 0 变温: 或 或 如恒容,ΔU = Q ,否则不一定相等。如恒压,ΔH = Q ,否则不一定相等。 C p , m – C V , m = R 双原子理想气体:C p , m = 7R /2, C V , m = 5R /2 单原子理想气体:C p , m = 5R /2, C V , m = 3R /2 典型例题:3.18思考题第2,3,4题 书2.18、2.19 三、 凝聚态物质的ΔU 和ΔH 只和温度有关 或 典型例题:书2.15 ΔU = n C V , m d T T 2 T 1 ∫ ΔH = n C p, m d T T 2 T 1 ∫ ΔU = nC V , m (T 2-T 1) ΔH = nC p, m (T 2-T 1) ΔU ≈ ΔH = n C p, m d T T 2 T 1 ∫ ΔU ≈ ΔH = nC p, m (T 2-T 1)
四、可逆相变(一定温度T 和对应的p 下的相变,是恒压过程) ΔU ≈ ΔH –ΔnRT (Δn :气体摩尔数的变化量。如凝聚态物质之间相变,如熔化、凝固、转晶等,则Δn = 0,ΔU ≈ ΔH 。 101.325 kPa 及其对应温度下的相变可以查表。 其它温度下的相变要设计状态函数 不管是理想气体或凝聚态物质,ΔH 1和ΔH 3均仅为温度的函数,可以直接用C p,m 计算。 或 典型例题:3.18作业题第3题 五、化学反应焓的计算 其他温度:状态函数法 Δ H m (T ) = ΔH 1 +Δ H m (T 0) + ΔH 3 α β β α Δ H m (T ) α β ΔH 1 ΔH 3 Δ H m (T 0) α β 可逆相变 298.15 K: ΔH = Q p = n Δ H m α β Δr H m ? =Δf H ?(生) – Δf H ?(反) = y Δf H m ?(Y) + z Δf H m ?(Z) – a Δf H m ?(A) – b Δf H m ?(B) Δr H m ? =Δc H ?(反) – Δc H ?(生) = a Δc H m ?(A) + b Δc H m ?(B) –y Δc H m ?(Y) – z Δc H m ?(Z) ΔH = nC p, m (T 2-T 1) ΔH = n C p, m d T T 2 T 1 ∫
功能强大的多物理场耦合分析软件
功能强大的多物理场耦合分析软件 COMSOL Multiphysics(原FEMLAB) COMSOL Multiphysics是一个专业有限元数值分析软件包,是对基于偏微分方程的多物理场模型进行建模和仿真计算的交互式开发环境系统。它为所有科学和工程领域内物理过程的建模和仿真提供了一种崭新的技术! CAE软件。 COMSOL Multiphysics是专为描述和模拟各种物理现象而开发的基于有限元分析的软件包,它使得建立各种物理现象的数学模型并进行数值模拟计算变得更为容易和可能。在使用COMSOL Multiphysics软件的过程中,您可以自己建立普通的偏微分方程形式,也可以使用COMSOL Multiphysics提供的特定的物理应用模型。这些特定的物理应用模型包括预先设定好的模块和在一些特殊应用领域内已经通过微分方程和变量建立起来的用户界面。此外,COMSOL Multiphysics软件通过把任意数目的这种物理应用模块整合成对一个单一问题的描述,使得建立耦合问题变得更为容易。 模型库是整个COMSOL Multiphysics软件包的最特色部分,它囊括了各种工程领域内的所有模型。每一个模型都包含了非常完善的相关文档如工程技术背景、结果讨论和一步一步建立模型的每个过程描述。由于这些模型文件都已经包括了网格划分和运行计算的信息,所以您可以自己打开这些文件并试着进行相应的各种后处理操作和显示。另外,您可以应用、扩充或者修改这些工程模型使它们符合您的个人需求。因此,进入这些模型库就给您提供了建立自己模型的基础和起点。而事实上,这些模型库也会给您建立自己的模型提供宝贵的参考。 能够独立于MATLAB运算的COMSOL Multiphysics软件系统为进一步改进软件提供了一个很好的基础和平台。COMSOL Multiphysics提供了与市场上主流的CAD软件进行接口的直接界面。在已有的三角形、四面体网格划分模型基础上,又新增加了四边形、六面体和棱柱体网格模型。为了更好地进行自动求解运算,COMSOL Multiphysics 还提供了强大的运算求解能力。 COMSOL Multiphysics软件系统具备了在Linux、Solaris和HP-UX等系统下的64位处理能力,尤其是可以在AMD64/Linux平台上进行64位计算。在一个系统上加入64位处理能力意味着COMSOL Multiphysics所能处理问题的规模比原来提高了至少10到100倍。 通过COMSOL Multiphysics的多物理场功能,您可以选择不同的模块,同时模拟任意物理场组合进行耦合分析;通过使用相应模块直接定义物理参数创建模型; 使用基于偏微分方程的模型可以自由定义用户自己的方程;
大学物理化学热力学
第三章热力学第二定律 §3.1 自发过程的共同特征 一、自发过程 “自发过程”?在一定条件下能自动进行的过程。?推论: ?一切自发过程都是有方向性的,人类经 验没有发现哪一个自发过程可以自动地 回复原状。二、决定自发过程的方向和限度的因素?从表面上看,各种不同的过程有着不同的决定因素,例如: –i)决定热量流动方向的因素是温度T; –ii)决定气体流动方向的是压力P; –iii)决定电流方向的是电位V; –iv)而决定化学过程和限度的因素是什么呢? 三、自发过程的共同特征 分析: ?根据人类经验,自发过程都是有方向性的(共同特点),即自发过程不能自动回复原状。 1、理想气体向真空膨胀 ?即:当系统回复到 原状时,环境中有 W的功变成了Q (=-W)的热。 ?因此,环境最终能否回复原状(即理气向真空膨胀是否能成为可逆过程),就取决于(环境得到的)热能否全部变为功而没有任何其他变化。 2、热量由高温物体流向低温物体 ?因此,系统回复了原状的同时,环境最终能否回复原状( 即热由高温向低温流动能否成为一可逆过程),取决于(环境得到的) 热能否全部变为功而没有任何其他变化。3、Cd放入PbCl 2 溶液转变成CdCl 2 溶液和Pb ?已知此过程是自发的,在反应进行时有 ∣Q∣的热量放出(放热反应,Q<0) ?欲使系统回复原状,可进行电解反应。 ?若电解时做的电功为W,同时还有∣Q′∣的热量放出,当反应系统回复原状时,环境中损失的功(电功)为W,得到的热为∣Q∣+∣Q′∣
?根据能量守恒原理: ∣W∣=∣Q∣+∣Q′∣ ?所以环境能否回复原状(即此反应能否成为可逆过程),取决于 ?(环境得到的)热(∣Q∣+∣Q′∣) 能否全部转化为功W (=∣Q∣+∣Q′∣)而没有任何其他变化。?自发过程能否成为热力学可逆过程,最终均可归结为: ?“热能否全部转变为功而没有任何其他变化”?然而经验证明:热功转化是有方向性的,即?“功可自发地全部变为热;但热不可能全部转变为功而不引起任何其他变化”。 ?“一切自发过程都是不可逆过程。” ?这就是自发过程的共同特征。 §3.2 热力学第二定律的经典表述 ?一切自发过程的方向,最终都可归结为热功转化的方向问题: ?“功可全部变为热,而热不能全部变为功而不引起任何其他变化”。一、克劳修斯和开尔文对热力学第二 定律的经典表述 1.克劳修斯(Clausius) 表述:?“不可能把热从低温物体传到高温物 体,而不引起任何其他变化。” 2. 开尔文(Kelvin) 表述 ?不可能从单一热源取出热使之完全变为功,而不发生其他变化。 ?也可表达为: ?“第二类永动机是不可能造成的。” *热力学第二定律的克劳修斯表述与开尔文表述等价。二、关于热力学第二定律表述的几点说明 1. 第二类永动机并不违反热力学第一定律。?它究竟能否实现,只有热力学第二定律才能回答。但回答是: ?“第二类永动机是不可能存在的。” 其所以不可能存在,也是人类经验的总结。
化工热力学复习总结材料
第一章、绪论 一、化工热力学的目的和任务 通过一定的理论方法,从容易测量的性质推测难测量的性质、从有限的实验数据获得更系统的物性的信息具有重要的理论和实际意义。 化工热力学就是运用经典热力学的原理,结合反映系统特征的模型,解决工业过程(特别是化工过程)中热力学性质的计算和预测、相平衡和化学平衡计算、能量的有效利用等实际问题。 二、1-2化工热力学与物理化学的关系 化工热力学与物理化学关系密切,物理化学的热力学部分已经介绍了经典热力学的基本原理和理想系统(如理想气体和理想溶液等)的模型,化工热力学将在此基础上,将重点转移到更接近实际的系统。 三、热力学性质计算的一般方法 (1)基于相律分析系统的独立变量和从属变量; (2)由经典热力学原理得到普遍化关系式。特别是将热力学性质与能容易测量的p、V、T及组成性质和理想气体等压热容联系起来; (3)引入表达系统特性的模型,如状态方程或活度系数; (4)数学求解。 第2章流体的P-V-T关系 1.掌握状态方程式和用三参数对应态原理计算PVT性质的方法。 2.了解偏心因子的概念,掌握有关图表及计算方法。 1.状态方程:在题意要求时使用该法。 ①范德华方程:常用于公式证明和推导中。 ②R—K 方程: ③维里方程: 2.普遍化法:使用条件:在不清楚用何种状态方程的情况下使用。 三参数法: ①普遍化压缩因子法 ②普遍化第二维里系数法 3、Redlich-Kwong(RK)方程 3、Soave(SRK)方程
4、Peng-Robinson (PR )方程 () 22 a 0.45724c r c R T T P α= 0.0778 c c RT b P = §2-5高次型状态方程 5、virial 方程 virial 方程分为密度 型: 和压力型: 第3章 纯物质的热力学性质 1、热力学性质间的关系 dU TdS pdV =- H=U+PV dH TdS Vdp =+ A=U-TS dA SdT pdV =-- G=H-TS dG SdT Vdp =-+ Maxwell 关系式 S V T P V S ?????? =- ? ??????? S P T V P S ?????? = ? ??????? V T P S T V ??????= ? ??????? P T V S T P ?????? =- ? ??????? 转换公式: 1Z X Y X Y Z Y Z X ??????? ??=- ? ? ?????????? 3.2计算H ?和S ?的方法 1.状态方程法: P P V dH C dT V T dP T ?? ???=+- ???????? P P C V dS dT dP T T ???=- ???? 2.剩余性质法: ①普遍化压缩因子图 ()()0 1 R R R T C C C H H H RT RT RT ω =+ ()()0 1 R R R T S S S R R R ω = +
最新大学物理化学1-热力学第一定律课后习题及答案说课讲解
热力学第一定律课后习题 一、是非题 下列各题中的叙述是否正确?正确的在题后括号内画“√”,错误的画“?”。 1.在定温定压下,CO 2 由饱和液体转变为饱和蒸气,因温度不变,CO2的热力学能和焓也不变。( ) 2. d U = nC V,m d T这个公式对一定量的理想气体的任何pVT过程均适用。( ) 3. 一个系统从始态到终态,只有进行可逆过程才有熵变。( ) 4. 25℃时H2(g)的标准摩尔燃烧焓等于25℃时H2O(g)的标准摩尔生成焓。( ) 5. 稳定态单质的?f H(800 K) = 0。( ) 二、选择题 选择正确答案的编号,填在各题后的括号内: 1. 理想气体定温自由膨胀过程为:()。 (A)Q > 0;(B)?U < 0;(C)W <0;(D)?H = 0。 2. 对封闭系统来说,当过程的始态和终态确定后,下列各项中没有确定的值的是:( )。 ( A ) Q;( B ) Q+W;(C ) W( Q = 0 );( D ) Q( W = 0 )。 3. pVγ = 常数(γ = C p,m/C V,m)适用的条件是:( ) (A)绝热过程;( B)理想气体绝热过程; ( C )理想气体绝热可逆过程;(D)绝热可逆过程。 4. 在隔离系统内:( )。 ( A ) 热力学能守恒,焓守恒;( B ) 热力学能不一定守恒,焓守恒; (C ) 热力学能守恒,焓不一定守恒;( D) 热力学能、焓均不一定守恒。 5. 从同一始态出发,理想气体经可逆与不可逆两种绝热过程:( )。 ( A )可以到达同一终态;( B )不可能到达同一终态; ( C )可以到达同一终态,但给环境留下不同影响。 6. 当理想气体反抗一定的压力作绝热膨胀时,则:( )。 ( A )焓总是不变;(B )热力学能总是增加; ( C )焓总是增加;(D )热力学能总是减少。 7. 已知反应H2(g) +1 2 O2(g) ==== H2O(g)的标准摩尔反应焓为?r H(T),下列说法中不 正确的是:()。 (A)?r H(T)是H2O(g)的标准摩尔生成焓; (B)?r H(T)是H2O(g)的标准摩尔燃烧焓; (C)?r H(T)是负值; (D)?r H(T)与反应的?r U数值不等。 三、计算题 习题1 10 mol理想气体由25℃,1.0 MPa膨胀到25℃,0.1 MPa,设过程为:
《化工热力学》课程标准
《化工热力学》课程标准 英文名称:Chemical Engineering Thermodynamics 课程编号: 适用专业:应用化学本科学分数:2 一、课程性质 所属一级学科——化学工程,二级学科——化学工程基础学科。 《化工热力学》是应用化学专业的重要专业方向课程。该课程包括化工基础理论,热力学案例分析、化工节能创新等化工技能,是化工类专业教学体系和人才培养体系中比较重要的专业课。 先修课程为《高等数学》、《物理化学》、《化工原理》等。 二、课程理念 1、该课程是化学工程的精髓 《化工热力学》课程属于工学学科门类下化学工程学科,是化工过程研究、开发和设计的理论基础,在科研和生产领域具有不可缺少的地位。它是从化学工程的角度,分析并给出化工过程经历的实质性变化,在原理和计算方法上指导各种化工过程的进行和优化。 该课程是应用化学专业的重要专业方向课程,是化学工程的精髓,是所有单元操作的基础,是《化工原理》、《反应工程》、《化工分离过程》等课程的基础和指导。 该课程在化学化工类人才培养中起着重要的承前启后、由基础到专业的桥梁作用,是化工类人才持续深造和研究开发必须打好的知识功底。 2、理论与工程应用相结合,培养学生的工程与开发能力 该课程定位为工程学科专业方向课,故在培养学生科学素质的同时,始终强调工程能力的培养,将化工热力学理论,模型与工程应用融为一体,旨在培养学生能够应用和建立热力学模型解决化学工程和工艺开发中的问题。 3、砸实热力学知识,培养学生扎实的学习能力和创造能力 该课程是以化工热力学、工程热力学和统计热力学为学科基础,以计算机及其技术为工具,培养学生从热力学角度分析解决现代化工技术的复杂工程问题。为了培养创新型高素质人才,既要给学生以干粮——扎实的热力学知识,又要给学生以猎枪——获取和创造知识的能力。 4、重视过程与动态评价 采用平时表现与考试成绩相结合的评价理念。学生在完成课后作业、课堂讨论、口试等内容和环节后,获得参加考试资格。知识和能力之间应树立一种内在联系,多看重教学过程中学生的参与程度和提高程度,不把期末考试作为教学评价的唯一标准,坚持“过程评价”和“动态评价”。 三、课程目标 总目标: 通过介绍化工热力学的起源、现状和发展,使学生了解热力学在化工过程中的主要实际应用;引导学生构建化工热力学课程的知识网络,使学生掌握化工热力学的基本概念和基本原理,利用化工热力学的方法对化工中物系的热力学性质和其它化工物性进行关联及推算,利用化工热力学的原理和模型进行化工过程能量、相平衡分析和研究;训练学生理论联系实际的思维,使学生具备利用热力学知识分析解决化工领域中有关实际问题的初步能力,形成基本知识扎实、应用能力突出的专业素养。 分目标:
物理化学热力学章节测试练习答案-201X
物理化学热力学章节测试练习(2010.4)答案 一、选择题 1、下列过程ΔH≠0的是: (A) 理想气体恒温膨胀过程; (B) 恒压、恒熵和不做非体积功的可逆过程; (C) 真实气体的节流膨胀过程; (D)任一个绝热且不做非体积功的过程。 D 2、下列说法正确的是: (A) 物体的温度越高,其热量越多; (B) 物体的温度越高,其热力学能越大; (C) 体系的焓等于恒压热; (D)体系的焓就是体系所含的热量。 B 3、封闭体系在不可逆循环中,热温商之和Σ(Q/T): (A) 大于零(B) 等于零 (C) 小于零(D) 不可能小于零 C 4、对于孤立体系中发生的实际过程,下式中不正确的是: (A) W = 0 (B) Q = 0 (C) ΔS > 0 (D) ΔH = 0 D 5、恒压下纯物质体系,当温度升高时其吉布斯自由能: (A) 上升(B) 下降 (C) 不变(D) 无法确定 B 6、体系的状态改变了,其内能值 (A)必定改变(B)必定不变 (C)不一定改变(D)状态与内能无关 C 7、体系进行一次循环过程 (A)W=0 (B)|Q|=|W|(C)Q=0 (D)U=0 B 8、理想气体绝热向真空膨胀,则 (A) ΔS = 0,W = 0 (B) ΔH = 0,ΔU = 0 (C) ΔG = 0,ΔH = 0 (D) ΔU = 0,ΔG = 0
B 9、下述说法哪一个错误? (A) 封闭体系的状态与其状态图上的点一一对应 (B) 封闭体系的状态即是其平衡态 (C) 封闭体系的任一变化与其状态图上的实线一一对应 (D) 封闭体系的任一可逆变化途径都可在其状态图上表示为实线 C 10、下述说法中哪一个错误? (A) 体系放出的热量一定等于环境吸收的热量 (B) 体系温度的降低值一定等于环境温度的升高值 (C) 热力学平衡时体系的温度与环境的温度相等 (D) 若体系1与体系2分别与环境达成热平衡,则此两体系的温度相同 B 11、A,B,C 三种物质组成的溶液,物质 C 的偏摩尔量为 (A)()A B C ,,,T p n n n μ? (B)()A B C ,,,T p n n G n ?? (C)()A B A ,,,T p n n A n ?? (D)C A n n p T B n H ,,,)/(?? B 12、下列各式中哪个是化学势? (a) C B ,,T S n H n ?? ? ? ??? (b) C B ,,T p n A n ?? ? ? ??? (c) C B ,,T V n G n ?? ? ? ??? (d) C B ,,S V n U n ?? ? ? ??? D 13、饱和理想溶液中溶质的化学势μ与纯溶质的化学势μ*的关系式为 (A )μμ=* (B )μμ>* (C )μμ<* (D )不能确定 A 14、在一定温度压力下,对于只有体积功的任一化学反应,能用于判断其反应方向的是: (A )r m G ? (B ) K (C ) m r G ? (D ) m r H ? C 15、实际气体在节流过程中:(B) (A) ΔH=0,ΔA=0 (B) Q=0,ΔH=0
622物理化学考试大纲汇总
硕士研究生入学统一考试《物理化学Ⅰ》科目大纲 (科目代码:622) 学院名称(盖章):化学化工学院 学院负责人(签字): 编制时间:2014年8月20日
《物理化学Ⅰ》科目大纲 (科目代码:622) 一、考核要求 物理化学主要内容包括气体、化学热力学(统计热力学)、化学动力学、电化学、界面化学与胶体化学等。要求考生熟练掌握物理化学的基本概念、基本原理及计算方法。 二、考核目标 物理化学考试在考查基本知识、基本理论的基础上,注重考查考生灵活运用这些基础知识观察和解决实际问题的能力。它的评价标准是高等学校优秀毕业生能达到及格或及格以上水平,以保证被录取者具有较扎实的物理化学基础知识。 三、考核内容 第一章气体 §1.1 气体分子运动论 §1.2 摩尔气体常数 §1.3 理想气体的状态图 §1.4 气体运动的速率分布 §1.5 气体平动能分布 §1.6 气体分子在重力场中的分布 §1.7 分子的碰撞频率与平均自由程 §1.8 实际气体 §1.9 气液间的转变 §1.10 压缩分子图 掌握理想气体状态方程和混合气体的性质(组成的表示、分压定律、分容定律)。了解分子碰撞频率、平均自由程和实际气体概念,特别要了解实际气体的状态方程(范德华方程)以及实际气体的液化、临界性质、应状态原理与压缩因子图等。 第二章热力学第一定律及其应用 §2.1 热力学概论 §2.2 热平衡与热力学第零定律-温度的概念 §2.3 热力学的一些基本概念 §2.4 热力学第一定律 §2.5 准静态过程和和可逆过程 §2.6 焓 §2.7 热容 §2.8 热力学第一定律对理想气体的应用 §2.9 Carnot循环 §2.10 实际气体
物理化学第二章 热力学第一定律
第二章 热力学第一定律 一.基本要求 1.掌握热力学的一些基本概念,如:各种系统、环境、热力学状态、系 统性质、功、热、状态函数、可逆过程、过程和途径等。 2.能熟练运用热力学第一定律,掌握功与热的取号,会计算常见过程中 的, , Q W U ?和H ?的值。 3.了解为什么要定义焓,记住公式, V p U Q H Q ?=?=的适用条件。 4.掌握理想气体的热力学能和焓仅是温度的函数,能熟练地运用热力学 第一定律计算理想气体在可逆或不可逆的等温、等压和绝热等过程中, , , , U H W Q ??的计算。 二.把握学习要点的建议 学好热力学第一定律是学好化学热力学的基础。热力学第一定律解决了在恒 定组成的封闭系统中,能量守恒与转换的问题,所以一开始就要掌握热力学的一 些基本概念。这不是一蹴而就的事,要通过听老师讲解、看例题、做选择题和做 习题等反反复复地加深印象,才能建立热力学的概念,并能准确运用这些概念。 例如,功和热,它们都是系统与环境之间被传递的能量,要强调“传递”这 个概念,还要强调是系统与环境之间发生的传递过程。功和热的计算一定要与变 化的过程联系在一起。譬如,什么叫雨?雨就是从天而降的水,水在天上称为云, 降到地上称为雨水,水只有在从天上降落到地面的过程中才被称为雨,也就是说, “雨”是一个与过程联系的名词。在自然界中,还可以列举出其他与过程有关的 名词,如风、瀑布等。功和热都只是能量的一种形式,但是,它们一定要与传递 的过程相联系。在系统与环境之间因温度不同而被传递的能量称为热,除热以外, 其余在系统与环境之间被传递的能量称为功。传递过程必须发生在系统与环境之 间,系统内部传递的能量既不能称为功,也不能称为热,仅仅是热力学能从一种 形式变为另一种形式。同样,在环境内部传递的能量,也是不能称为功(或热) 的。例如在不考虑非膨胀功的前提下,在一个绝热、刚性容器中发生化学反应、 燃烧甚至爆炸等剧烈变化,由于与环境之间没有热的交换,也没有功的交换,所 以0, 0, 0Q W U ==?=。这个变化只是在系统内部,热力学能从一种形式变为
大学物理化学1-热力学第一定律课后习题及答案资料
大学物理化学1-热力学第一定律课后习题 及答案
热力学第一定律课后习题 一、是非题 下列各题中的叙述是否正确?正确的在题后括号内画“√”,错误的画“?”。 1.在定温定压下,CO2由饱和液体转变为饱和蒸气,因温度不变,CO2的 热力学能和焓也不变。( ) 2. d U = nC V,m d T这个公式对一定量的理想气体的任何pVT过程均适用。( ) 3. 一个系统从始态到终态,只有进行可逆过程才有熵变。 ( ) 4. 25℃时H2(g)的标准摩尔燃烧焓等于25℃时H2O(g)的标准摩尔生成焓。( ) 5. 稳定态单质的?f H(800 K) = 0。 ( ) 二、选择题 选择正确答案的编号,填在各题后的括号内: 1. 理想气体定温自由膨胀过程为:()。 (A)Q > 0;(B)?U < 0;(C)W <0;(D)?H = 0。 2. 对封闭系统来说,当过程的始态和终态确定后,下列各项中没有确定的 值的是:( )。 ( A ) Q; ( B ) Q+W; (C ) W( Q = 0 ); ( D ) Q( W = 0 )。 3. pVγ = 常数(γ = C p,m/C V,m)适用的条件是:( ) (A)绝热过程; ( B)理想气体绝热过程; ( C )理想气体绝热可逆过程; (D)绝热可逆过程。 4. 在隔离系统内:( )。
( A ) 热力学能守恒,焓守恒; ( B ) 热力学能不一定守恒,焓守恒; (C ) 热力学能守恒,焓不一定守恒; ( D) 热力学能、焓均不一定守恒。 5. 从同一始态出发,理想气体经可逆与不可逆两种绝热过程:( )。 ( A )可以到达同一终态; ( B )不可能到达同一终态; ( C )可以到达同一终态,但给环境留下不同影响。 6. 当理想气体反抗一定的压力作绝热膨胀时,则:( )。 ( A )焓总是不变; (B )热力学能总是增加; ( C )焓总是增加; (D )热力学能总是减少。 O2(g) ==== H2O(g)的标准摩尔反应焓为?r H(T),下 7. 已知反应H2(g) +1 2 列说法中不正确的是:()。 (A)?r H(T)是H2O(g)的标准摩尔生成焓; (B)?r H(T)是H2O(g)的标准摩尔燃烧焓; (C)?r H(T)是负值; (D)?r H(T)与反应的?r U数值不等。 三、计算题 习题1 10 mol理想气体由25℃,1.0 MPa膨胀到25℃,0.1 MPa,设过程为: ( 1 )自由膨胀; ( 2 )对抗恒外压力0.1 MPa膨胀; ( 3 )定温可逆膨胀。试计算三种膨胀过程中系统对环境作的功。
化工热力学
天津市高等教育自学考试课程考试大纲 课程名称:化工热力学课程代码:0708 第一部分课程性质与目标 一、课程性质与特点化工热力学是高等教育自学考试化学工程专业所开设的专业基础课程之一。它是化学工程学的一个重要分支,也是化工过程研究、开发与设计的理论基础。本课程系统地介绍了将热力学原理应用于化学工程技术领域的研究方法。它以热力学第一、第二定律为基础,研究化工过程中各种能量的相互转化及其有效利用,深刻阐述了各种物理和化学变化过程达到平衡的理论极限、条件和状态。它是一门理论性与应用性均较强的课程。 二、课程目标与基本要求 设置本课程,为了使考生能够掌握化工热力学的基本概念、理论和专业知识;能利用化工热力学的原理和模型对化工中涉及到的化学反应平衡原理、相平衡原理等进行分析和研究;能利用化工热力学的方法对化工中涉及的物系的热力学性质和其它化工物性进行关联和推算;并学会利用化工热力学的基本理论对化工中能量进行分析等。 通过本课程学习,要求考生: 1、正确理解化工热力学的有关基本概念和理论; 2、理解各个概念之间的联系和应用; 3、掌握化工热力学的基本计算方法; 4、能理论联系实际,灵活分析和解决实际化工生产和设计中的有关问题。 三、与本专业其它课程的关系化工热力学是化工类专业必修的专业基础课程,它与化学工程专业的许多其它课程有着十分密切的关系。物理化学是本课程的基础,同时本课程又是化工原理、化工设计、反应工程、化工分离过程等课程的基础和指导。 第二部分考核内容与考核目标 第一章绪论 一、学习目的与要求通过本章学习,正确认识“热”的概念及人们对于“热”的认识发展过程;了解化工热力学的主要内容及研究方法。 二、考核知识点与考核目标 (一)什么是“热” (一般)识记:人们对于“热”的几种认识;“热”概念的发展过程 (二)化工热力学的主要内容(次重点)识记:化工热力学的主要内容理解:“化工热力学”与“物理化学”的主要区别 (三)化工热力学的研究方法(一般)识记:化工热力学的研究方法有经典热力学方法和分子热力学方法。 第二章流体的p-V-T 关系 、学习目的与要求 通过本章的学习,能熟练掌握流体(特别是气体)的各种类型的p、V、T 关系(包括 状态方程法和对应状态法)及其应用、优缺点和应用范围。 二、考核知识点与考核目标 (一)维里方程(重点)理解:维里方程的几种形式维里系数的物理意义应用:二阶舍项的维里方
多物理场耦合技术的研究进展与发展趋势10页
多物理场耦合技术的研究进展与发展趋势 一、数值计算概述 现代科学技术问题通常有三种研究方法:理论推导、科学实验和科学计算。科学技术可以帮助科学家揭示用物质实验手段尚不能表现的科学奥秘和 科学规律,同时,它也是工程科学家的研究成果——理论、方法和科学数据的归总,成为推动工程和社会进步的最新生产力。数值计算方法则是科学计算核心。 数值计算技术诞生于上个世纪五十年代初,Bruce, G. H.和Peaceman, D. W.模拟了一维气相不稳定径向和线形流。受当时计算机能力及解法限制,数值计算技术只是初步应用于求解一维问题。随着计算机技术和计算方法的发展,复杂的工程问题也可以采用离散化的数值计算方法并借助计算机得到满足工程要求的数值解。 数值计算可理解为用计算机来做实验,比如某一特定LED(发光二极管)工作过程中内部电流密度、温度及热应力问题,通过计算并显示其计算结果。我们可以看到LED 内部电流密度是否存在拥挤现象,内部温度分布的各个细节,以及由于温度的变化引起的应力集中是否存在,它的位置、大小及其随时间的变化等。 我们可以将数值计算分为以下几个步骤:
首先要建立反映问题本质的数学模型。具体说就是要建立反映问题中各物理量之间的偏微分方程及其相应的定解条件,这是数值计算的出发点。比如牛顿型流体流动的数学模型就是著名的纳维—斯托克斯方程及其相应的定解条件。 数学模型建立之后,接下来就是求解这个模型。需要寻求高效、高准确度的计算方法。求解科学问题就是求解偏微分方程。 在确定了计算方法后,就可以开始编制程序并进行计算。实践表明这一部分工作是整个工作的主体,会占据整个工程的绝大部分时间。随着软件技术的发展,出现了应用于各领域的商业软件,运用这些软件使得这部分工作得到大大简化,缩短了模拟过程的周期。这样,科研人员能够将自己的时间和精力更多的投入到自己研究的问题上,而不是编写计算代码。 通过上述描述,用数值计算方法解决科学计算问题的一般过程可以用如下流程来形象地描述: 实际问题→数学模型→计算方法→计算程序→计算机计算→结果分析 在计算工作完成后,需要处理大量的计算结果数据。计算结果的图形后处理也是一项十分重要的工作。现在很多模拟工具已经能将图形编辑成连贯动画进行播放。 数值计算具有很多优点,但是它也有自己的局限性:
大学物理化学23热力学练习题
热力学 一、判断题: 1、在定温定压下,CO2由饱和液体转变为饱和蒸气,因温度不变,CO2的热力学能和焓也不变。 2、25℃时H2(g)的标准摩尔燃烧焓等于25℃时H2O(g)的标准摩尔生成焓。 3、稳定态单质的Δf H mΘ(800K)=0 。 4、d U=nC v,m d T公式对一定量的理想气体的任何pVT过程都适用。 5、系统处于热力学平衡态时,其所有的宏观性质都不随时间而变。 6、若系统的所有宏观性质均不随时间而变,则该系统一定处于平衡态。 7、隔离系统的热力学能是守恒的。 8、隔离系统的熵是守恒的。 9、一定量理想气体的熵只是温度的函数。 10、绝热过程都是定熵过程。 11、一个系统从始态到终态,只有进行可逆过程才有熵变。 12、系统从同一始态出发,经绝热不可逆过程到达的终态,若经绝热可逆过程,则一定达不到此终态。 13、热力学第二定律的克劳修斯说法是:热从低温物体传到高温物体是不可能的。 14、系统经历一个不可逆循环过程,其熵变> 0。 15、系统由状态1经定温、定压过程变化到状态2,非体积功W’<0,且有W G和G <0,则此状态变化一定能发生。 16、绝热不可逆膨胀过程中S >0,则其相反的过程即绝热不可逆压缩过程中S <0。 17、临界温度是气体加压液化所允许的最高温度。 18、可逆的化学反应就是可逆过程。 19、Q和W不是体系的性质,与过程有关,所以Q + W也由过程决定。 20、焓的定义式H = U + pV是在定压条件下推导出来的,所以只有定压过程才有焓变。 21、焓的增加量?H等于该过程中体系从环境吸收的热量。 22、一个绝热过程Q = 0,但体系的?T不一定为零。 23、对于一定量的理想气体,温度一定,热力学能和焓也随之确定。 24、某理想气体从始态经定温和定容两过程达终态,这两过程的Q、W、?U及?H是相等的。 25、任何物质的熵值是不可能为负值和零的。 26、功可以全部转化为热,但热不能全部转化为功。 27、不可逆过程的熵变是不可求的。 28、某一过程的热效应与温度相除,可以得到该过程的熵变。 29、在孤立体系中,一自发过程由A→B,但体系永远回不到原来状态。 30、绝热过程Q = 0,即,所以d S = 0。 31、可以用一过程的熵变与热温熵的大小关系判断其自发性。 32、绝热过程Q = 0,而由于?H = Q,因而?H等于零。 33、按Clausius不等式,热是不可能从低温热源传给高温热源的。 34、在一绝热体系中,水向真空蒸发为水蒸气(以水和水蒸气为体系),该过程W>0,?U>0。 35、体系经过一不可逆循环过程,其?S体>0。 36、对于气态物质,C p-C V = n R。 37、在一绝热体系中有一隔板,两边分别是空气和真空,抽去隔板,空气向真空膨胀,此时Q = 0,所以?S=0。 二、填空题: 1、一定量的理想气体由同一始态压缩至同一压力p,定温压缩过程的终态体积为V,可逆绝热压缩过程的终
(物理化学)第二章 热力学基础概念题1
第二章 热力学基础概念题 一、填空题 1、一定量的N 2气在恒温下增大压力,则其吉布斯自由能变 。(填增大,不变,减小) 2、物理量,,,,,,Q W U H V T p 属于状态函数的有 ;属于途径函数的有 ;状态函数中属于强度性质的有 ;属于容量性质的有 。 3、对组成不变的均相封闭系统,T S p ???= ???? ;对理想气体T S p ???= ???? 。 4、21 ln V W nRT V =的适用条件是 ; 1TV γ-=常数的适用条件是 ; p H Q ?=的适用条件是 。 5、1摩尔理想气体经恒温膨胀,恒容加热和恒压冷却三步完成一个循环回到始态,此过程吸热20.0kJ 。则U ?= ,H ?= ,W = 。 6、体积功的通用计算公式是W = ;在可逆过程中,上式成为W = ;在等压过程中,上式成为W = 。 7、给自行车打气时,把气筒内的空气作为体系,设气筒、橡皮管和轮胎均不导热,则该过程中Q 0,W 0 。 8、273.15K 、101.325kPa 下,固体冰融化为水,其Q 0,W 0, U ? 0,H ? 0 。 二、选择题 1、水在可逆相变过程中: (1)0U ?=,0H ?=; (2)0T ?=,0p ?=; (3)0U ?=,0T ?=; (3)以上均不对。 2、理想气体,p m C 与,V m C 的关系为:
(1),p m C =,V m C ;(2),p m C >,V m C ;(3),p m C <,V m C ;(4)无法比较。 3、液态水在100℃及101.325Pa 下汽化成水蒸气,则该过程的: (1) △H=0; (2) △S=0; (3) △A=0; (4) △G=0 。 4、理想气体从状态Ⅰ等温自由膨胀到状态Ⅱ,可用那个状态函数的变量来判断过程的自发性: (1)△G ; (2)△U; (3) △S; (4) △H 。 5、公式dG SdT Vdp =-+可适用下述那一过程: (1)在298K, 101.325kP 下水蒸气凝结成水的过程; (2)理想气体膨胀过程; (3)电解水制H 2(g)和O 2(g)的过程; (4) 在一定温度压力下,由()()223N g H g +合成()3NH g 的过程。 6、对封闭的单组分均相系统,且'0W =时,T G p ??? ????的值应是: (1)<0 ; (2) >0 ; (3)=0 ; (4)前述三种情况无法判断。 7、理想气体等温自由膨胀过程为: (1)0Q <; (2)0U ?<; (3)0W >; (4)0H ?=。 8、一封闭系统,当状态从A 到B 发生变化时,经历两条任意的不同途径,则下列四式中正确的是: (1)12Q Q =; (2)12W W =; (3)1122Q W Q W +=+; (4)12U U ?=?。 9、反应热公式p r Q H =?除应满足“封闭系统,不做非体积功”外,还应满足: (1)21p p ==定值; (2) e p =定值; (3) 外p=p ; (4) 21e p p p ===定值。 三、是非题 (正确地打“√”,错误的打“×”) 1、 理想气体在恒定的外压下绝热膨胀到终态,因为是恒压,所以H Q ?=,又 因为是绝热,0Q =,故0H ?=,对吗? ( ) 2、 气体经不可逆绝热膨胀后,因为Q =0,固其熵变等于零。是不是?( ) 3、在-10℃,101.325kPa 下过冷的H 2O(l)凝结为冰是一个不可逆过程,故此过程的熵变大于零。是不是?( ) 4、热力学第二定律的克劳修斯说法是:热从低温物体传给高温物体是不可能的。是不是?( ) 5、绝热过程都是等熵过程。是不是?( )
物理化学课后答案解析_热力学第一定律
第二章热力学第一定律 【复习题】 【1】判断下列说法是否正确。 (1)状态给定后,状态函数就有一定的值,反之亦然。 (2)状态函数改变后,状态一定改变。 (3)状态改变后,状态函数一定都改变。 (4)因为△U=Q v, △H =Q p,所以Q v,Q p是特定条件下的状态函数。 (5)恒温过程一定是可逆过程。 (6)汽缸内有一定量的理想气体,反抗一定外压做绝热膨胀,则△H= Q p=0。 (7)根据热力学第一定律,因为能量不能无中生有,所以一个系统若要对外做功,必须从外界吸收热量。 (8)系统从状态Ⅰ变化到状态Ⅱ,若△T=0,则Q=0,无热量交换。 (9)在等压下,机械搅拌绝热容器中的液体,使其温度上升,则△H = Q p = 0。 (10)理想气体绝热变化过程中,W=△U,即W R=△U=C V△T,W IR=△U=C V△T,所以W R=W IR。(11)有一个封闭系统,当始态和终态确定后; (a)若经历一个绝热过程,则功有定值; (b)若经历一个等容过程,则Q有定值(设不做非膨胀力); (c)若经历一个等温过程,则热力学能有定值; (d)若经历一个多方过程,则热和功的代数和有定值。 (12)某一化学反应在烧杯中进行,放热Q1,焓变为△H1,若安排成可逆电池,使终态和终态都相同,这时放热Q2,焓变为△H2,则△H1=△H2。 【答】(1)正确,因为状态函数是体系的单质函数,体系确定后,体系的一系列状态函数就确定。相反如果体系的一系列状态函数确定后,体系的状态也就被惟一确定。(2)正确,根据状态函数的单值性,当体系的某一状态函数改变了,则状态函数必定发生改变。 (3)不正确,因为状态改变后,有些状态函数不一定改变,例如理想气体的等温变化,内能就不变。 (4)不正确,ΔH=Qp,只说明Qp 等于状态函数H的变化值ΔH,仅是数值上相等,并不意味着Qp 具有状态函数的性质。ΔH=Qp 只能说在恒压而不做非体积功的特定条件下,Qp
大学物理化学4-多组分体系热力学课后习题及答案
多组分体系热力学课后习题 一、是非题 下述各题中的说法是否正确?正确的在题后括号内画“√”,错的画“?” 1. 二组分理想液态混合物的总蒸气压大于任一纯组分的蒸气压。( ) 2. 理想混合气体中任意组分B 的逸度B ~p 就等于其分压力p B ~。( ) 3. 因为溶入了溶质,故溶液的凝固点一定低于纯溶剂的凝固点。( ) 4. 溶剂中溶入挥发性溶质,肯定会引起溶液的蒸气压升高。( ) 5. 理想溶液中的溶剂遵从亨利定律;溶质遵从拉乌尔定律。( ) 6. 理想液态混合物与其蒸气达成气、液两相平衡时,气相总压力p 与液相组成x B 呈线性关系。( ) 7. 如同理想气体一样,理想液态混合物中分子间没有相互作用力。( ) 8. 一定温度下,微溶气体在水中的溶解度与其平衡气相分压成正比( ) 9. 化学势是一广度量。( ) 10. 只有广度性质才有偏摩尔量( ) 11. ) B C C,(,,B ≠???? ????n V S n U 是偏摩尔热力学能,不是化学势。( ) 二、选择题 选择正确答案的编号,填在各题题后的括号内 1. 在α、β两相中都含有A 和B 两种物质,当达到相平衡时,下列三种情况, 正确的是:( )。 (A)ααμ=μB A ; (B) βαμ=μA A ; (C) β αμ=μB A 。 2. 理想液态混合物的混合性质是:( )。 (A)Δmix V =0,Δmix H =0,Δmix S >0,Δmix G <0; (B)Δmix V <0,Δmix H <0,Δmix S <0,Δmix G =0; (C)Δmix V >0,Δmix H >0,Δmix S =0,Δmix G =0; (D)Δmix V >0,Δmix H >0,Δmix S <0,Δmix G >0。 3. 稀溶液的凝固点T f 与纯溶剂的凝固点*f T 比较,T f <*f T 的条件是:( )。 (A )溶质必需是挥发性的; (B )析出的固相一定是固溶体; (C )析出的固相是纯溶剂; (D )析出的固相是纯溶质。 4. 若使CO 2在水中的溶解度为最大,应选择的条件是:( )。 (A )高温高压; (B )低温高压; (C )低温低压; (D )高温低压。
化工热力学_Chapter7-01
May 27, 2011
背景 两相接触时,相间将发生物质、能量的交换,直至相的性质如温度、压力、组成等保持恒定,即处于相平衡。掌握相平衡时体系的温度、压力、各相的体积和组成以及其它热力学函数间的关系较为重要。 相平衡是化工分离技术与分离设备开发、设计的理论基础,工业上应用广泛的精馏、吸收、萃取、吸附、结晶等就是分别以汽-液、气-液、液-液、气-固、液-固平衡为设计依据。 本章主要论述相平衡理论及平衡数据的计算,重点讨论汽-液平衡。
进行混合物相平衡计算时,需将混合物的相平衡准则与反映混合物特征的模型(状态方程+混合规则或活度系数模型)结合起来。 Gibbs-Duhem方程反映了混合物中各组分的偏摩尔性质的约束关系,它不仅在检验偏摩尔性质模型时非常 有用,而且因某些偏摩尔性质,例如, ,等,与混合物的相平衡紧密联系,在相平衡数据的检验和推算中也有非常重要的应用。ln i γ?ln i φ1)确定平衡状态; 2)计算互成平衡状态下各个相的性质。 相平衡热力学性质计算包括两个部分:
重点内容: ?平衡性质与判据,混合物的汽液相平衡及其表达?混合物相平衡关系(温度T、压力p、与各相的组成)的确定 ?汽液相平衡计算类型与方法 ?汽-液平衡计算 ?Gibbs-Duhem方程应用于汽液平衡数据的热力学一致性校验
主要内容 7.1 相平衡的判据与相律7.2 汽液平衡相图 7.3 汽液平衡计算
7.1.1 相平衡的判据 7.1 相平衡的判据与相律 等温等压的封闭体系达到平衡的判据: ,()0 T p dG =(7-1) 相平衡指的是溶液中形成若干相,这些相之间保持着物理平衡而处于多相共存状态。一切自发过程必引起体系的自由焓减少,达到平衡时,体系的自由焓最小。
