pGEX-4T-1-USP原核表达载体构建
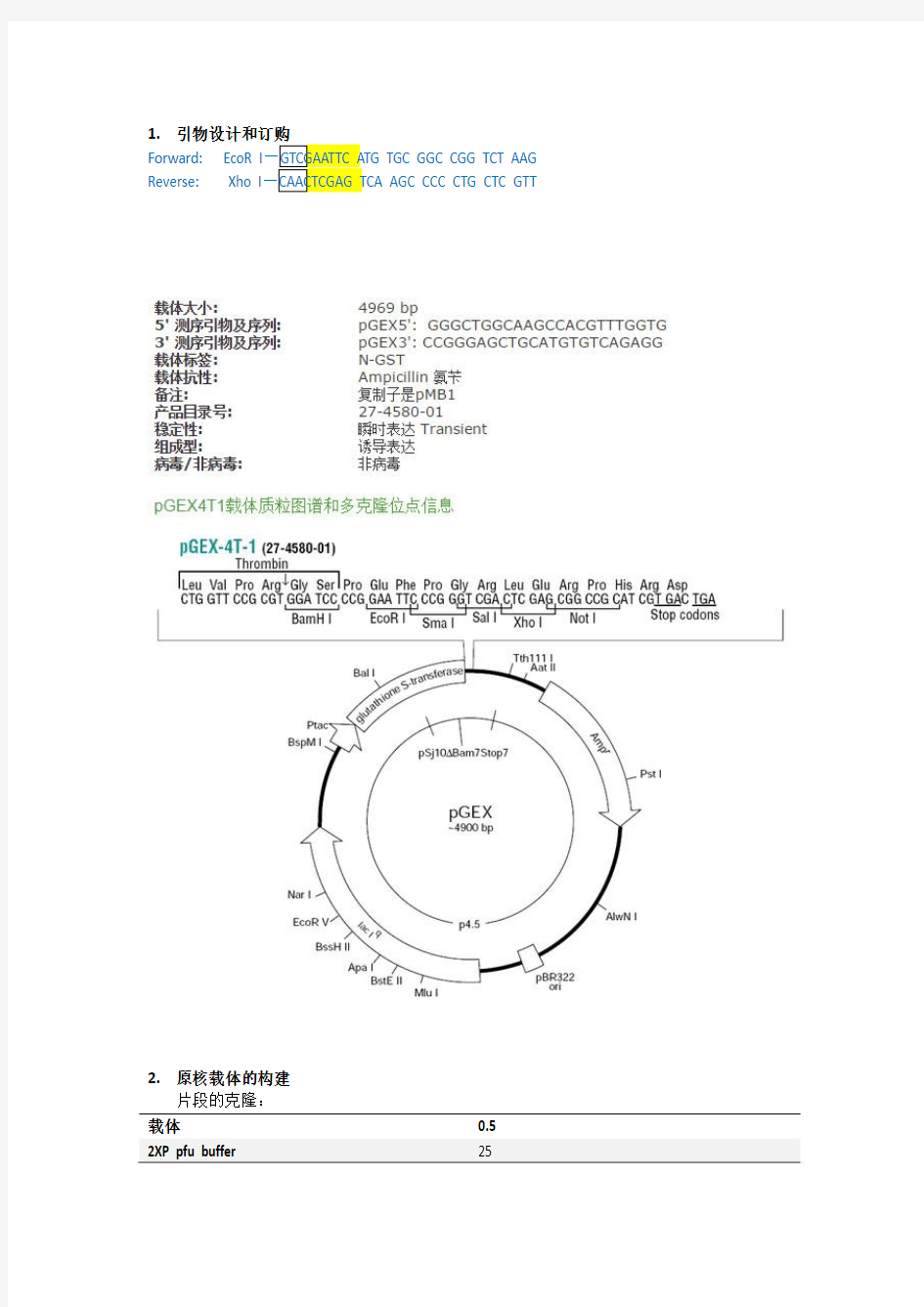

1.
Forward: EcoR I
Reverse: Xho I
2.原核载体的构建
片段的克隆:
载体0.5 2XP pfu buffer 25
Dntps (2.5mM ) 8 Primer-f 1 Primer-R 1 KOD E
1 酶切: dd water 24 10X buffer 4 DNA 10 EcoR I 1
dd water 32.5 10X buffer 4 DNA 2 ug EcoR I 1 Xho I 1 Total
40 ul
37℃,2 h 。做两个单酶切位点,加上一个未酶切的载体做对照,一起跑胶。
回收。 连接: Vector DNA 2 Insert DNA 6 10X buffer 1.5 T4 DNA ligase
1 For 22℃,
2 h
取7.5 ul 转化涂板。同时取空载和感受态涂板做对照。 小提鉴定。测序。
{
⑴冰上20分钟-→热激:42℃、90秒-→冰上2
分钟 ⑵图板(相应抗性的LB 固体平板)
⑶12-16h 后收板,挑单克隆,小提摇菌。
图为:取500 ul菌液,离心加入1Xcracking buffer,13000rpm,离心15min,然后取15ul上样检测,得到如上图,其中L11,L22和L32分子量明显比其他的大,猜测为连接成功的质粒。
然后小提,酶切检测,片段大小为1700bp左右。确认载体片段插入成功(第四道为空载)。
然后取10ul质粒送测序。
原核&真核表达载体构建
原核、真核表达载体构建 真核表达载体和原核表达载体的区别:主要是因为原核和真核表达系统所需的表达元件不同。 比如说启动子,终止子在两种表达系统中是不一样的。 带有真核表达元件的是真核载体,能在真核生物内表达; 带有原核表达元件的是原核载体,能在原核生物内表达。两者都具有的为穿梭载体。 ㈠原核表达载体指:能携带插入的外源核酸序列进入原核细胞中进行复制的载体。 原核表达载体调控原件 1.启动子 启动子是DNA链上一段能与RNA聚合酶结合并起始RNA合成的序列,它是基因表达不可缺少的重要调控序列。没有启动子,基因就不能转录。由于细菌RNA聚合酶不能识别真核基因的启动子,因此原核表达载体所用的启动子必须是原核启动子。原核启动子是由两段彼此分开且又高度保守的核苷酸序列组成,对mRNA的合成极为重要。在转录起始点上游5~10 bp处,有一段由6~8个碱基组成,富含A和T的区域,称为Pribnow 盒,又名TATA 盒或-10区。来源不同的启动子,Pribnow 盒的碱基顺序稍有变化。在距转录起始位点上游35 bp 处,有一段由10 bp组成的区域,称为-35区。转录时大肠杆菌RNA聚合酶识别并结合启动子。-35区与RNA聚合酶s亚基结合,-10区与RNA聚合酶的核心酶结合,在转录起始位点附近DNA被解旋形成单链,RNA聚合酶使第一和第二核苷酸形成磷酸二酯键,以后在RNA聚合酶作用下向前推进,形成新生的RNA 链。原核表达系统中通常使用的可调控的启动子有Lac(乳糖启动子)、Trp(色氨酸启动子)、Tac(乳糖和色氨酸的杂合启动子) 、lPL (l噬菌体的左向启动子)、T7噬菌体启动子等。 2. SD序列 1974年Shine和Dalgarno首先发现,在mRNA上有核糖体的结合位点,它们是起始密码子AUG和一段位于AUG上游3~10 bp处的由3~9 bp组成的序列。这段序列富含嘌呤核苷酸,刚好与16S rRNA 3¢末端的富含嘧啶的序列互补,是核糖体RNA的识别与结合位点。以后将此序列命名为Shine-Dalgarno序列,简称SD序列。它与起始密码子AUG之间的距离是影响mRNA转录、翻译成蛋白的重要因素之一,某些蛋白质与SD序列结合也会影响mRNA与核糖体的结合,从而影响蛋白质的翻译。另外,真核基因的第二个密码子必须紧接在ATG 之后,才能产生一个完整的蛋白质。 3.终止子 在一个基因的3¢末端或是一个操纵子的3'末端往往有特定的核苷酸序列,且具有终止转录功能,这一序列称之为转录终止子,简称终止子(terminator)。转录终止过程包括:RNA聚合酶停在DNA模板上不再前进,RNA的延伸也停止在终止信号上,完成转录的RNA从RNA聚合酶上释放出来。对RNA聚合酶起
原核表达遇到瓶颈怎么办(终审稿)
原核表达遇到瓶颈怎么 办 TPMK standardization office【 TPMK5AB- TPMK08- TPMK2C- TPMK18】
我想表达遇到的第一个瓶颈估计就是为什么我的外源片段插到载体里面,PCR鉴定没问题,双酶切也OK,可是就是不见表达。一般我们是如何判断没有表达呢?大多都是首先进行SDS-PAGE。在跑胶的时候一定要设对照,比较严谨的电泳对照,应该是:Marker,标准品阳性对照(如果有,且打算做Western的话),以及空白载体(诱导)和重组载体(不诱导)2个阴性对照,再加上诱导不同时间的表达结果。Marker用于判断条带大小,标准品用于判断Western体系包括抗体显色剂和操作的可靠性,以及精确判断大小;空白载体(诱导)负对照有助于判断在非诱导条件下的本底表达;而重组载体(不诱导)负对照则有助于判断诱导的效果以及排除诱导剂对宿主菌潜在的干扰,或者是区分细菌内源和外源表达产物——偷懒可不是好习惯,会影响结果判断。注意,接种表达和接种做感受态都类似,一定要用挑单克隆、加足量抗生素、过夜培养的新鲜菌液转种最好,在筛选压力下生长旺盛的种子液远比经过4℃保存的菌液要好得多,也许是因为保存时间长会导致抗生素失效部分细菌丢失质粒或者其他变化。反正就是一种经验做法。 跑SDS-PAGE的话可以用考马斯亮兰染,它灵敏度在100ng左右;但是不能跟着做Western了。银染的灵敏度在0.1~1 ng;有钱还可以用Sypro Red,灵敏度高还可以继续做Western。WesternBlot是蛋白质定性和半定量的最通用的技术,具体细节可参考生物通WesternBlot技术专题,我们有详细介绍的。 在做过Western Blot仍没有检测到表达带,那么就要开始进行下一步的分析了。首先,看看载体的多克隆位点和片断插入的序列,是否有因为酶切连接而意外引入了转录终止信号。有时载体几经多个实验人员的周转,反复插入片断,或者是粘端
重组表达质粒的构建——原核表达载体选择
重组表达质粒的构建——原核表达载体选择质粒载体是重组蛋白表达的关键工具,其结构如下图。重组蛋白表达,我们首先要将基因插入到表达载体上,插入的位置为多克隆位点。质粒载体上有很多的功能元件,这些元件对于蛋白的表达都是至关重要的。尽管我们经过系统的分析和预测,但是仍有很多蛋白不能顺利表达、表达量很低或者表达状态不好。这个时候我们需要尝试构建不同的表达载体以期得到最好的效果,这些载体的主要区别是启动子和融合标签的差异。 蛋白表达优化主要工作也就是尝试构建不同融合表达标签,使用不同的宿主表达菌,测试不同的表达条件,筛选出最优表达体系。常用的融合标签有GST、MBP、Trx、6His、SUMO等,这些标签主要功能是促表达、促可溶、信号标记或助纯化。福因德生物可以提供以下系列载体以供科研表达研究。 1)促表达/促溶标签 2)信标标签
3)纯化标签 我们选择表达载体的时候不但要考虑蛋白怎么表达成功,更要考虑蛋白怎么纯化出来,纯化的问题主要是考虑纯化标签和酶切位点的选择,下表我们列举了常见的纯化标签和酶切位点。 4)酶切位点 以上为原核表达常用的标签和酶切位点,其性质也都作了简要的介绍,各专业网站或专业书籍已对此做详尽解释,科研工作者可根据具体实验设计方案,组合设计以上标签和酶切位点的使用。特别值得注意的是,选用和设计蛋白酶切位点的时候首要考虑的是序列内部有没有蛋白酶位点,同时要考虑酶切的效率和蛋白酶试剂成本。一般商业化载体,在标签蛋白与载体多克隆位点之间都设计有酶切位点。 标签可设计在N-端也可在C-端,设计在N-端的优势是,可通过标签高效翻译起始位点带动插入蛋白的表达,可溶性标签的高效表达更可促进蛋白的可溶性表达;同时,大部分的蛋白内切酶的切割位点在C-端,所以标签设计在N-端可将标签切割完全。 在设计标签序列与酶切位点的时候还要考虑N-端稳定性原则,也就是所谓宿主细胞的N-端规则(N-end rule),这个要避免;同时,还应该检查是否引入了可与别的蛋白相互作用的序列或者蛋白酶切位点。
表达载体的构建方法及步骤
表达载体的构建方法及步骤 令狐采学 一、载体的选择及如何阅读质粒图谱 目前,载体主要有病毒和非病毒两大类,其中质粒DNA 是一种新的非病毒转基因载体。 一个合格质粒的组成要素: (1)复制起始位点Ori 即控制复制起始的位点。原核生物DNA 分子中只有一个复制起始点。而 真核生物DNA 分子有多个复制起始位点。 (2)抗生素抗性基因可以便于加以检测,如Amp+ ,Kan+ (3)多克隆位点MCS 克隆携带外源基因片段 (4)P/E 启动子/增强子 (5)Terms 终止信号 (6)加poly(A)信号可以起到稳定mRNA 作用 选择载体主要依据构建的目的,同时要考虑载体中应有合适的限制酶切位点。如果构建的目 的是要表达一个特定的基因,则要选择合适的表达载体。 载体选择主要考虑下述3点: 【1】构建DNA 重组体的目的,克隆扩增/基因表达,选择合适的克隆载体/表达载体。 【2】.载体的类型:
(1)克隆载体的克隆能力-据克隆片段大小(大选大,小选小)。如<10kb 选质粒。 (2)表达载体据受体细胞类型-原核/真核/穿梭,E.coli/哺乳类细胞表达载体。 (3)对原核表达载体应该注意:选择合适的启动子及相应的受体菌,用于表达真核蛋白质时注意克服4个困难和阅读框错位;表达天然蛋白质或融合蛋白作为相应载体的参考。 【3】载体MCS 中的酶切位点数与组成方向因载体不同而异,适应目的基因与载体易于链接,不能产生阅读框架错位。 综上所述,选用质粒(最常用)做载体的5点要求: (1)选分子量小的质粒,即小载体(1-1.5kb)→不易损坏,在细菌里面拷贝数也多(也有大载 体); (2)一般使用松弛型质粒在细菌里扩增不受约束,一般10个以上的拷贝,而严谨型质粒<10个。 (3)必需具备一个以上的酶切位点,有选择的余地; (4)必需有易检测的标记,多是抗生素的抗性基因,不特指多位Ampr(试一试)。 (5)满足自己的实验需求,是否需要包装病毒,是否需要加入荧光标记,是否需要加入标签蛋白,是否需要真核抗性(如Puro、G418)等等。 无论选用哪种载体,首先都要获得载体分子,然后采用适当的限制酶将载体DNA 进行切割,获得线性载体分子,以便于与
原核表达载体的重要调控元件
原核表达载体的重要调控元件 启动子 启动子是DNA链上一段能与RNA聚合酶结合并起始RNA合成的序列,它是基因表达不可缺少的重要调控序列。没有启动子,基因就不能转录。由于细菌RNA聚合酶不能识别真核基因的启动子,因此原核表达载体所用的启动子必须是原核启动子。 原核启动子是由两段彼此分开且又高度保守的核苷酸序列组成,对mRNA的合成极为重要。在转录起始点上游5~10 bp处,有一段由6~8个碱基组成,富含A和T的区域,称为Pribnow 盒,又名TATA 盒或-10区。来源不同的启动子,Pribnow 盒的碱基顺序稍有变化。在距转录起始位点上游35 bp处,有一段由10 bp组成的区域,称为-35区。转录时大肠杆菌RNA聚合酶识别并结合启动子。-35区与RNA聚合酶s 亚基结合,-10区与RNA聚合酶的核心酶结合,在转录起始位点附近DNA被解旋形成单链,RNA聚合酶使第一和第二核苷酸形成磷酸二酯键,以后在RNA聚合酶作用下向前推进,形成新生的RNA链。 原核表达系统中通常使用的可调控的启动子有Lac(乳糖启动子)、Trp(色氨酸启动子)、Tac(乳糖和色氨酸的杂合启动子) 、lP L (l噬菌体的左向启动子)、T7噬菌体启动子等。 (1)Lac启动子:它来自大肠杆菌的乳糖操纵子,是DNA分子上一段有方向的核苷酸序列,由阻遏蛋白基因(LacI)、启动基因(P)、操纵基因(O)和编码3个与乳糖利用有关的酶的基因结构所组成。Lac启动子受分解代谢系统的正调控和阻遏物的负调控。正调控通过CAP(catabolite gene activation protein)因子和cAMP 来激活启动子,促使转录进行。负调控则是由调节基因产生LacZ阻遏蛋白,该阻遏蛋白能与操纵基因结合阻止转录。乳糖及某些类似物如IPTG可与阻遏蛋白形成复合物,使其构型改变,不能与O基因结合,从而解除这种阻遏,诱导转录发生。 (2)trp启动子:它来自大肠杆菌的色氨酸操纵子,其阻遏蛋白必须与色氨酸结合才有活性。当缺乏色氨酸时,该启动子开始转录。当色氨酸较丰富时,则停止转录。b-吲哚丙烯酸可竞争性抑制色氨酸与阻遏蛋白的结合,解除阻遏蛋白的活性,促使trp启动子转录。 (3)Tac启动子:Tac启动子是一组由Lac和trp启动子人工构建的杂合启动子,受Lac阻遏蛋白的负调节,它的启动能力比Lac和trp都强。其中Tac 1是由Trp启动子的-35区加上一个合成的46 bp DNA片段(包括Pribnow 盒)和Lac操纵基因构成,Tac 12是由Trp的启动子-35区和Lac启动子的-10区,加上Lac 操纵子中的操纵基因部分和SD序列融合而成。Tac启动子受IPTG的诱导。
原核表达步骤
1.将已经成功转有重组表达载体pET-28a-CYP83A1的表达菌 E. coli.BL21(DE3)在LB固体培养基(50μg/mL Kan)上划线接种培 2.挑取单菌落,接种于5mL的LB液体培养基(50μg/mL Kan)中,37℃,180r/min振荡培养过夜。 3.取500μL过夜培养的菌液转接入100mL新的LB液体培养基(50μg/mL Kan)中,37℃,190r/min振荡培养到菌液OD600 =0.6~0.8。 4.分组培养:实验组加入终浓度为1mmol/L的IPTG,对照组不加IPTG,37℃,190r/min诱导培养6h。 5.8000r/min离心2min,收集细菌,用1×PBS(0.01mol/L)缓冲液悬浮。 6.冰上超声波破碎,功率30w,工作5s,间歇5s,总时间2min。 7.4℃、12000r/min离心10min,分离上清与沉淀,取100μL上清与等体积的2×上样缓冲液混合;用200μL1×上样缓冲液悬浮沉淀,沸水浴5min后,对上清和沉淀进行SDS-PAGE检测。
重组质粒在大肠杆菌中的诱导表达及SDS-PAGE分析 挑测序正确的单克隆接种到3mLLB(50μg·mL-1Kan)培养基中,振荡培养12h后,将菌液按1﹕100的比例加入到300mL LB(50μg·mL-1Kan)培养基中200r/min37℃振荡培养至OD600为0.5—0.6时,加入IPTG(使终浓度为1mmol·L-1)进行诱导表达,分别在37℃诱导4h,4℃保存备用。未加IPTG诱导的pET-28a-CsFOMT收集作为阴性对照。诱导全部完成后,各取50mL 菌液离心收集细菌,加入SDS上样缓冲液,悬浮混匀,100℃3min,12000r/min离心1min,取上清4℃保存备用。另取50mL菌液离心收集菌体后用1×PBS(PH7.4)将沉菌悬起,经过超声波细胞破碎(20mm的变幅杆,400W,超声2s,间隔5s,重复60次),10000r/min离心10min分离上清和沉淀,上清和沉淀样品中分别加入SDS上样缓冲液,混匀,沸水浴,取上清和沉淀分别进行SDS-PAGE(5%浓缩胶,12%分离胶),然后分析蛋白表达结果
原核表达步骤
原核表达步骤
Chi l 原核表达基本试验步骤 将克隆化基因插入合适载体后导入大肠杆菌用于表达大量蛋白质的方法一般称为原核表达。这种方法在蛋白纯化、定位及功能分析等方面都有应用。大肠杆菌用于表达重组蛋白有以下特点:易于生长和控制;用于细菌培养的材料不及哺乳动物细胞系统的材料昂贵;有各种各样的大肠杆菌菌株及与之匹配的具各种特性的质粒可供选择。但是,在大肠杆菌中表达的蛋白由于缺少修饰和糖基化、磷酸化等翻译后加工,常形成包涵体而影响表达蛋白的生物学活性及构象。 表达载体在基因工程中具有十分重要的作用,原核表达载体通常为质粒,典型的表达载体应具有以下几种元件: (1)选择标志的编码序列; (2)可控转录的启动子; (3)转录调控序列(转录终止子,核糖体结合位点); (4)一个多限制酶切位点接头; (5)宿主体内自主复制的序列。 原核表达一般程序如下:获得目的基因-准备表达载体-将目的基因插入表达载体中(测序验证)-转化表达宿主菌-诱导靶蛋白的表达-表达蛋白的分析-扩增、纯化、进一步检测,其中包括: 一、试剂准备 (1)LB培养基。 (2)1M IPTG(异丙基硫代-β-D-半乳糖苷):2.38g IPTG溶于10ml ddH2O
中,0.22μm滤膜抽滤,-20℃保存。 CCY的IPTG是1M的,用时进行1000倍稀释。 二、操作步骤 (一)获得目的基因 1、通过PCR方法:以含目的基因的克隆质粒为模板,按基因序列设计一对引物(在上游和下游引物分别引入不同的酶切位点),PCR循环获得所需基因片段。 2、通过RT-PCR方法:用TRIzol法从细胞或组织中提取总RNA,以mRNA 为模板,逆转录形成cDNA第一链,以逆转录产物为模板进行PCR循环获得产物。 (二)构建重组表达载体 1、载体酶切:将表达质粒用限制性内切酶(同引物的酶切位点)进行双酶切,酶切产物行琼脂糖电泳后,用胶回收Kit或冻融法回收载体大片段。 2、PCR产物双酶切后回收,在T4DNA连接酶作用下连接入载体。我们用Soultion I连接。 (三)获得含重组表达质粒的表达菌种 1、将连接产物转化大肠杆菌BL21,根据重组载体的标志(抗Amp或蓝白斑)作筛选,挑取单斑,碱裂解法小量抽提质粒,双酶切初步鉴定。 2、测序验证目的基因的插入方向及阅读框架均正确,进入下步操作。否则应筛选更多克隆,重复亚克隆或亚克隆至不同酶切位点。 3、以此重组质粒DNA转化表达宿主菌的感受态细胞。
想和大家讨论讨论原核表达载体
【建议】想和大家讨论讨论原核表达载体 原核表达载体,如pet系列,型号从小到大,那么多,往往让新手选择起来不知所措。所以希望和大家讨论讨论到底他们是怎么演变的,每个的优缺点,是不是号越大的就越好等新手们往往困惑不已的问题。 希望下面的讨论分系列进行,如pet系列、pgex系列等 这篇文章是我从网上找的关于pet载体的介绍,只要你耐心的看完,相信能有个基本的了解关于pet载体及应用。更详细的内容请高手进行补充 pET,原核表达金标准(转) pET 载体中,目标基因克隆到T7 噬菌体强转录和翻译信号控制之下,并通过在宿主细胞提供T7 RNA 聚合酶来诱导表达。Novagen 的pET 系统不断扩大,提供了用于表达的新技术和选择,目前共包括36 种载体类型、15 种不同宿主菌和设计用于有效检测和纯化目标蛋白的许多其它相关产品。 优点 ·是原核蛋白表达引用最多的系统 ·在任何大肠杆菌表达系统中,基础表达水平最低 ·真正的调节表达水平的“变阻器”控制 ·提供各种不同融合标签和表达系统配置 ·可溶性蛋白生产、二硫键形成、蛋白外运和多肽生产等专用载体和宿主菌 ·许多载体以LIC 载体试剂盒提供,用于迅速定向克隆PCR 产物 ·许多宿主菌株以感受态细胞形式提供,可立即用于转化 阳性pFORCE TM 克隆系统具有高效克隆PCR 产物、阳性选择重组体和高水平表达目标蛋白等特点。 pET 系统概述 pET 系统是在大肠杆菌中克隆和表达重组蛋白的最强大系统。根据最初由Studier 等开发的T7 启动子驱动系统,Novagen 的pET 系统已用于表达成千上万种不同蛋白。 控制基础表达水平 pET 系统提供6 种载体- 宿主菌组合,能够调节基础表达水平以优化目标基因的表达。没有单一策略或条件适用于所有目标蛋白,所以进行优化选择是必要的。 宿主菌株 质粒在非表达宿主菌中构建完成后,通常转化到一个带有T7 RNA 聚合酶基因的宿主菌(λ DE3 溶原菌)中表达目标蛋白。在λ DE3 溶原菌中,T7 RNA 聚合酶基因由lacUV5 启动子控制。未诱导时便有一定程度转录,因此适合于表达其产物对宿主细胞生长无毒害作用的一些基因。而宿主菌带有pLysS 和pLyE 时调控会更严紧。pLys 质粒编码T7 溶菌酶,
如何做原核表达
如何做原核表达 人们合成与生物相关的物质是从尿素开始的,1828年,德国化学家维勒人工合成了存在于生物体的这种有机物。在1960年我国科学家采用化学方法首次成功地合成了具有生物活性的蛋白质——胰岛素。随着内切酶的发现和基因工程技术的发展,人们发现用各种不同的载体在原核、真核系统中进行蛋白表达更为行之有效。而这其中大肠杆菌表达系统发展得最为迅速、成熟。原核表达具有操作方便、快捷,需时较短,表达量大,适合工业化生产等优点。虽然也有缺少糖基化和表达后加工等问题,当有了其它多种表达系统后,原核系统仍是我们合成外源蛋白的首选。 在网上看到有人把原核表达技术分成四个等级:初次尝试扫盲、乱棍打枣入门、系统优化中级和自成一体高手,觉得十分有意思。但是根据笔者自己的经验以及耳闻目睹的一些经历告诉我:做表达?那是谋事在人,成事在天。有时候你把克隆做出来了,双酶切鉴定没问题,测序没问题,可是就是看不到表达带。原因当然可以分析,实验也是可以改进,但是窜改一下戈尔泰的话:“成功的实验都是一样的,失败的实验各有各的不幸。”在实验遇到瓶颈的时候要如何进行分析,找到问题的症结是我们的实验关键所在。在准备进行原核表达的时候需要考虑的因素很多,市面上可供选择的载体、菌株也很多,要如何进行正确的选择,找到适合自己的载体是十分重要的。所以,现在要对目前常用的一些载体进行介绍,让我们对其相关产品及其表达原理进行了解,以方便实验设计。 首先来一些大肠杆菌表达的基本概念:一个完整的表达系统通常包括配套的表达载体和表达菌株,如果是特殊的诱导表达还包括诱导剂,如果是融合表达还包括纯化系统或者Tag检测等等。选择表达系统通常要根据实验目的来考虑,比如表达量高低,目标蛋白的活性,表达产物的
原核表达步骤
Chi l 原核表达基本试验步骤 将克隆化基因插入合适载体后导入大肠杆菌用于表达大量蛋白质的方法一般称为原核表达。这种方法在蛋白纯化、定位及功能分析等方面都有应用。大肠杆菌用于表达重组蛋白有以下特点:易于生长和控制;用于细菌培养的材料不及哺乳动物细胞系统的材料昂贵;有各种各样的大肠杆菌菌株及与之匹配的具各种特性的质粒可供选择。但是,在大肠杆菌中表达的蛋白由于缺少修饰和糖基化、磷酸化等翻译后加工,常形成包涵体而影响表达蛋白的生物学活性及构象。 表达载体在基因工程中具有十分重要的作用,原核表达载体通常为质粒,典型的表达载体应具有以下几种元件: (1)选择标志的编码序列; (2)可控转录的启动子; (3)转录调控序列(转录终止子,核糖体结合位点); (4)一个多限制酶切位点接头; (5)宿主体内自主复制的序列。 原核表达一般程序如下:获得目的基因-准备表达载体-将目的基因插入表达载体中(测序验证)-转化表达宿主菌-诱导靶蛋白的表达-表达蛋白的分析-扩增、纯化、进一步检测,其中包括: 一、试剂准备 (1)LB培养基。 (2)1M IPTG(异丙基硫代-β-D-半乳糖苷):2.38g IPTG溶于10ml ddH2O
中,0.22μm滤膜抽滤,-20℃保存。 CCY的IPTG是1M的,用时进行1000倍稀释。 二、操作步骤 (一)获得目的基因 1、通过PCR方法:以含目的基因的克隆质粒为模板,按基因序列设计一对引物(在上游和下游引物分别引入不同的酶切位点),PCR循环获得所需基因片段。 2、通过RT-PCR方法:用TRIzol法从细胞或组织中提取总RNA,以mRNA 为模板,逆转录形成cDNA第一链,以逆转录产物为模板进行PCR循环获得产物。 (二)构建重组表达载体 1、载体酶切:将表达质粒用限制性内切酶(同引物的酶切位点)进行双酶切,酶切产物行琼脂糖电泳后,用胶回收Kit或冻融法回收载体大片段。 2、PCR产物双酶切后回收,在T4DNA连接酶作用下连接入载体。我们用Soultion I连接。 (三)获得含重组表达质粒的表达菌种 1、将连接产物转化大肠杆菌BL21,根据重组载体的标志(抗Amp或蓝白斑)作筛选,挑取单斑,碱裂解法小量抽提质粒,双酶切初步鉴定。 2、测序验证目的基因的插入方向及阅读框架均正确,进入下步操作。否则应筛选更多克隆,重复亚克隆或亚克隆至不同酶切位点。 3、以此重组质粒DNA转化表达宿主菌的感受态细胞。
表达载体的构建方法及步骤
表达载体的构建方法及步骤 一、载体的选择及如何阅读质粒图谱 目前,载体主要有病毒和非病毒两大类,其中质粒DNA 是一种新的非病毒转基因载体。一个合格质粒的组成要素: (1)复制起始位点Ori 即控制复制起始的位点。原核生物DNA 分子中只有一个复制起始点。而 真核生物DNA 分子有多个复制起始位点。 (2)抗生素抗性基因可以便于加以检测,如Amp+ ,Kan+ (3)多克隆位点MCS 克隆携带外源基因片段 (4)P/E 启动子/增强子 (5)Terms 终止信号 (6)加poly(A)信号可以起到稳定mRNA 作用 选择载体主要依据构建的目的,同时要考虑载体中应有合适的限制酶切位点。如果构建的目 的是要表达一个特定的基因,则要选择合适的表达载体。 载体选择主要考虑下述3点: 【1】构建DNA 重组体的目的,克隆扩增/基因表达,选择合适的克隆载体/表达载体。【2】.载体的类型: (1)克隆载体的克隆能力-据克隆片段大小(大选大,小选小)。如<10kb 选质粒。(2)表达载体据受体细胞类型-原核/真核/穿梭,E.coli/哺乳类细胞表达载体。
(3)对原核表达载体应该注意:选择合适的启动子及相应的受体菌,用于表达真核蛋白质时注意克服4个困难和阅读框错位;表达天然蛋白质或融合蛋白作为相应载体的参考。【3】载体MCS 中的酶切位点数与组成方向因载体不同而异,适应目的基因与载体易于链接,不能产生阅读框架错位。 综上所述,选用质粒(最常用)做载体的5点要求: (1)选分子量小的质粒,即小载体(1-1.5kb)→不易损坏,在细菌里面拷贝数也多(也有大载 体); (2)一般使用松弛型质粒在细菌里扩增不受约束,一般10个以上的拷贝,而严谨型质粒<10个。 (3)必需具备一个以上的酶切位点,有选择的余地; (4)必需有易检测的标记,多是抗生素的抗性基因,不特指多位Ampr(试一试)。(5)满足自己的实验需求,是否需要包装病毒,是否需要加入荧光标记,是否需要加入标签蛋白,是否需要真核抗性(如Puro、G418)等等。 无论选用哪种载体,首先都要获得载体分子,然后采用适当的限制酶将载体DNA 进行切割,获得线性载体分子,以便于与目的基因片段进行连接。 如何阅读质粒图谱 第一步:首先看Ori 的位置,了解质粒的类型(原核/真核/穿梭质粒) 第二步:再看筛选标记,如抗性,决定使用什么筛选标记。 (1)Ampr 水解β-内酰胺环,解除氨苄的毒性。 (2)tetr 可以阻止四环素进入细胞。 (3)camr 生成氯霉素羟乙酰基衍生物,使之失去毒性。 (4)neor(kanr)氨基糖苷磷酸转移酶使G418(长那霉素衍生物)失活
原核表达操作步骤及注意事项
原核表达操作步骤及注意事项 时间:2010-03-03 14:05:01 来源:作者:点击:1046次 将克隆化基因插入合适载体后导入大肠杆菌用于表达大量蛋白质的方法一般称为原核表达。这种方法在蛋白纯化、定位及功能分析等方面都有应用。大肠杆菌用于表达重组蛋白有以下特点: 易于生长和控制;用于细菌培养的材料不及哺乳动物细胞系统的材料昂贵;有各种各样的大肠杆菌菌株及与之匹配的具各种特性的质粒可供选择。但是,在大肠杆菌中表达的蛋白由于缺少修饰和糖基化、磷酸化等翻译后加工,常形成包涵体而影响表达蛋白的生物学活性及构象。 表达载体在基因工程中具有十分重要的作用,原核表达载体通常为质粒,典型的表达载体应具有以下几种元件: (1)选择标志的编码序列; (2)可控转录的启动子; (3)转录调控序列(转录终止子,核糖体结合位点); (4)一个多限制酶切位点接头; (5)宿主体自主复制的序列。 原核表达一般程序如下: 获得目的基因-准备表达载体-将目的基因插入表达载体中(测序验证)-转化表达宿主菌-诱导靶蛋白的表达-表达蛋白的分析-扩增、纯化、进一步检测 一、试剂准备 1、LB培养基。 2、100mM IPTG(异丙基硫代-β-D-半乳糖苷):2.38g IPTG溶于100ml ddH2O中,0.22μm滤膜抽滤,-20℃保存。 二、操作步骤 (一)获得目的基因 1、通过PCR方法:以含目的基因的克隆质粒为模板,按基因序列设计一对引物(在上游和下游引物分别引入不同的酶切位点),PCR循环获得所需基因片段。 2、通过RT-PCR方法:用TRIzol法从细胞或组织中提取总RNA,以mRNA为模板,逆转录形成cDNA 第一链,以逆转录产物为模板进行PCR循环获得产物。 (二)构建重组表达载体 1、载体酶切:将表达质粒用限制性切酶(同引物的酶切位点)进行双酶切,酶切产物行琼脂糖电泳后,用胶回收Kit或冻融法回收载体大片段。 2、PCR产物双酶切后回收,在T4DNA连接酶作用下连接入载体。
原核表达步骤总结
原核表达步骤 原核表达先要将基因克隆到原核表达载体上,然后通过转化到 JM109或BL21等菌株中,诱导表达蛋白,然后进行蛋白纯化。本实验方案的前提是,目的基因已克隆到载体,并已转进入JM109菌株中。 1.鉴定目的蛋白是否在大肠杆菌JM109或BL21中大量表达 (1)制样 1 . 挑取经过双酶切鉴定的单克隆菌落于700ul LB培养基,加入0.7ul Amp(100mg/mL),37o C200r/min摇床培养,过夜活化。 2. 以1:50比例(200ul),将活化的过夜培养物加入10mL LB液体培养基中,加入10uLAmp(100mg/ml),37o C200r/min摇床扩大培养2h-3h,期间取样监控菌液的OD值,控制菌液OD600在0.6-1.0之间,以使大肠杆菌处于最适合表达外源蛋白的生长状态。(一般3h时,菌液浓度及达到标准,但是不同的基因对菌的影响不同,所以第一次实验时需要确定这个最佳时间) 3. 从10ml扩大培养物中取3ml菌液作为不加IPTG的空白对照(CK),其余7ml菌液加入7ul IPTG(储存浓度为0.5mol/l),使IPTG 终浓度达到0.5mmol/l。以200r/min的转速,37o C摇床培养3h。 4. 以5000r/min离心2min收集菌体,倾倒上清,每个离心管收集3ml培养物。 5. 加入1ml dH2O,将管底沉淀用振荡器打散以充分洗涤,8000r/min 离心2min,倾倒上清。 6. 重复步骤5。将离心管中的水倒干净。 (二)菌落SDS-PAGE 1. 在收集的菌体中加入200ul 1×SDS PAGE loading buffer(可根据沉淀的量增加或减少loading buffer的量,一般200ul比较合适)。用漩涡器剧烈震荡,确保将管底沉淀震散。 2. 将样品于100℃恒温加热器上开盖加热10min(Marker也要加热)。样品凉后,12000r/min离心3min,取每管的上清点样。上样量一般30ul—40ul,marker 20ul。 (3)SDS-PAGE分析 1. 根据目的片段的大小,制作不同浓度的分离胶 蛋白分子量 (kDa)凝胶浓度 (%) 4-4020
原核表达详细步骤
原核表达详细步骤 PartⅠ选择表达的目的基因 一、基因序列 1. 得到靶基因DNA(cDNA)序列,有几种方式寻找正确的读码顺序: ①利用生物信息学在NCBI上blast同源基因,找到同源蛋白,再在DNA 的ORF中找到正确的读码。 ②实验方法,即得到蛋白,进行测序,然后在DNA上找到正确的读码。 ③利用mRNA的特征,找到启动子,编码区,终止子。在编码区中找到翻译起始密码子与终止密码子(cDNA)。 2. 注意事项: ①区别ORF和CDS→ORF一般在DNA上的定义,寻找原则是翻译起始密码子和终止密码子;CDS可以是DNA上的定义,也可以是mRNA上的定义,分为complete CDS和partial CDS,是从第一个核酸开始读,连续读下去,complete CDS读码是“M、、、、、、、、、*”,partial CDS的读码是相应的AA ②在进行试验设计时,充分利用生物信息学的信息后,在进行试验设计。 二、抗原决定簇的预测 1、原理: 蛋白质表面部分可以使免疫系统产生抗体的区域叫抗原决定簇。一般抗原决定簇是由6-12 氨基酸或碳水基团组成,它可以是由连续序列(蛋白质一级结构)组成或由不连续的蛋白质三维结构组成。变性蛋白只是天然蛋白伸直的了产物,用来免疫动物具有更强的抗原性。只是天然蛋白中被包在内部的抗原决定簇也会暴露出来,如果用该变性抗原制备的抗体来检测变性抗原是可以的,如果用来检测天然蛋白,可能会有假阳性。做单抗也可以,同样道理,筛选出的单抗可能对抗的抗原决定簇处于天然抗原的内部,是否能用还要看将来该单抗用来干什么。 2、选择原则: (1)、亲水性:大部分抗原决定簇是亲水性的。
原核表达步骤
实验方法与步骤 1 表达质粒的构建及测序分析 1.1 cofilin-1的片段的准备 1.1.1 引物设计 根据在GenBank上查找人源cofilin-1的基因序列,用Primer Premier 5.0软件进行上下游引物的设计,并送往上海生物工程技术服务有限公司合成的PCR 引物。引物如下: 引物名称序列 F-cofilin-1 5′-AAGTCGACATATGGCCTCCGGTGTG-3′ R-cofilin-1 5′-TCTCTCGAGGGCTCACAAAGGCTTG-3′将以上引物用灭菌的三蒸水稀释成10μmol/L,分装于Eppendorf管中,-20℃冰箱中保存备用。 1.1.2 cofilin-1片段PCR 1 反应体系: 2.5μl KOD polymerase(3’-5’核酸外 切酶活性) KOD polymerase buffer 5μl MgSO4 2.5μl DMSO(“万能溶剂”) 2.5μl dNTPMixture 5μl PrimerF(底物) 1.5μl PrimerR 1.5μl Template(模板)5μl ddH2O 25μl Total 50μl 2PCR反应条件:
①94℃预变性3min ②94℃退火30s ③65℃延伸40s ④68℃40s ⑤go to②30个循环 ⑥68℃5min ⑦4℃forever 3 琼脂糖凝胶电泳对PCR产物进行检测 (1)配置浓度为1%的凝胶。称取琼脂糖0.3g,加入30ml 1×TAE电泳缓冲液(Tris-乙酸电泳缓冲液)中,用微波炉加热2min,待凝胶稍冷却,加入2μl EB(溴化乙锭,荧光染色剂)混匀后倾入凝胶铸槽中,插入梳子,并用玻璃棒驱除气泡,待凝胶完全凝结后拔除梳子。 (2)把凝胶置于1×TAE电泳缓冲液的电泳槽中,加样孔置于负极一侧,然后依次在加样孔中加入50μl Marker、50μl样品+10μl loading buffer(上样缓冲液,可以显示两条带,前面的蓝色的条带是溴酚蓝,代表的片段大小是300bp,后面的有点绿色的条带是二甲苯青,代表的片段大小在4000bp左右),盖上电泳盖,以100V电压进行电泳。 (3)当Marker条带充分分开后即可停止电泳,将凝胶移至保鲜膜上,置于凝胶自动成像仪中分析。 4 割胶回收PCR反应体系的扩增产物,用Omega Bio-Tek公司的Gel Extrection Kit进行回收: (1)将PCR扩增产物经1%的琼脂糖凝胶电泳,在紫外灯下迅速切取含有目的条带的琼脂糖凝胶,放入灭菌的EP管中。DNA在紫外灯下曝光时间不超过30s。 (2)称量凝胶块重量,以1g=1ml进行计算,加入适量体积的binding buffer,55-65℃加热至凝胶完全融化(约7~10min),每隔2~3min震荡一次。 (3)将Hibind DNA柱子套在2ml的收集管。将上述步骤(2)的溶液转移至Hibind DNA柱子中,10000×g离心1min,弃滤液。 (4)将柱子装回收集管中,加入300μl binding buffer,10000×g离心1min,
DREB基因的原核表达载体的构建及检测
DREB基因原核表达载体的构建及检测 李典鹏1霍凯丽1李政1陈丽萍1刘超2* (1.新疆农业大学草业与环境科学学院,新疆乌鲁木齐 830052; 2.新疆农业大学农学院,新疆乌鲁木齐 830052) 摘要:以从苜蓿基因组获取的DREB基因为目的基因,经过大肠杆菌液体培养基和固体筛选培养基的制备、大肠杆菌工程菌平板培养、PCR扩增目的基因片段、PCR产物回收与纯化、回收产物与PSURE-T载体连接、大肠杆菌液体培养、大肠杆菌感受态细胞制备及转化、筛选重组转化菌落以及通过TPTG的诱导等一系列实验,使DREB基因在原核生物体内表达,最后通过酶切及电泳检测分析,确定了由DREB基因编码翻译蛋白的正常表达,达到了DREB基因在原核体内表达的目的。 关键词:DREB;原核表达;大肠杆菌;PCR 0 引言 高等植物中脱水应答元件结合蛋白(Dehydration-responsive element binding protein,DREB)属于转录因子家族AP2/EREB亚族。在应答脱水、高盐和冷胁迫中具有重要的作用[1,2]。DREB参与了植物胁迫中有ABA 依赖和非ABA 依赖响应的2 种响应途径,研究发现DRE2 结合蛋白DBF1 和DBF2 可以与干旱响应基因的顺式作用元件特异性结合,并在ABA 依赖的小麦水分胁迫反应途径中调节与抗旱相关的rab17 基因的表达[3]提高转基因植物对干旱、高盐和冷胁迫的耐受性[4,5]。通过在模式植物中过表达DREB 基因,已经揭示了许多植物的DREB基因在逆境胁迫应答中的作用[6]。 大肠杆菌DH5α是目前原核细胞表达系统中应用最普遍的基因工程菌之一 [7]。大肠杆菌表达系统的发展历史可追溯到20 年前。科学家分别将酿酒酵母DNA 片段、粗糙链孢霉DNA 片段和哺乳动物cDNA 片段导入大肠杆菌,引起其表型的改变,证明了外源基因在大肠杆菌中可以使现有功能的活性表达[8]。与其他表达系统相比,大肠杆菌表达系统具有遗传背景清楚、目的基因表达水平高、培养周期短、抗污染能力强等特点[9-10],是分子生物学研究和生物技术产业化发展进程中的重要工具[11-12]。本实验通过对大肠杆菌DH5α构建DREB基因的表达载体的构建,为后续试验以及相关研究打下坚实基础。其次,通过对含有DREB基因的大肠杆进行工程培养,也为生物科学专业学生的实验学习提供较为稳定的菌种。 1材料与方法 1.1材料 供试原核表达载体为大肠杆菌菌株DH5α,由新疆农业大学农学院生物技术引论与实践课程组提供。
原核表达综述
[Merck推荐]原核表达秘笈之宿主菌株选择指南 在原核蛋白表达过程中,选择构建一个合适原核表达体系需要综合考虑3大因素:表达载体、宿主菌株、表达诱导条件,以获得最满意的表达效果。 事实上,在平时的实验中,最容易被忽视的就是宿主菌的选择——多数人会直接选择自己实验室曾经用过的表达菌株,或者是载体配套的菌株,而不去追究原因——即使表达结果不佳,大多在表达条件和载体上找原因,也不会考究菌株的选择是否适合。 作为原核表达的宿主,对外源基因的表达会产生一定的影响,是勿庸置疑的。每一个宿主细胞都像一个微观的小工厂,按照细胞固有的程序完成“你给它们安排的生产任务”——因为很难亲眼观察微观世界中表达是如何进行的,当出现问题时,我们需要经验判断问题所在。宿主细胞对原核表达可能会产生哪些影响呢? 知其然还要知其所以然。比如,菌株内源的蛋白酶过多,可能会造成外源表达产物的不稳定,所以一些蛋白酶缺陷型菌株往往成为理想的起始表达菌株。堪称经典的BL21系列就是lon和ompT蛋白酶缺陷型,也是我们非常熟悉的表达菌株。大名鼎鼎的BL21(DE3)融源菌则是添加T7聚合酶基因,为T7表达系统而设计。 真核细胞偏爱的密码子和原核系统有不同,因此,在用原核系统表达真核基因的时候,真核基因中的一些密码子对于原核细胞来说可能是稀有密码子,从而导致表达效率和表达水平很低。改造基因是比较麻烦的做法,Rosetta 2系列就是更好的选择——这种携带pRARE2质粒的BL21衍生菌,补充大肠杆菌缺乏的七种(AUA, AGG, AGA, CUA, CCC, GGA 及CGG)稀有密码子对应的 tRNA,提高外源基因、尤其是真核基因在原核系统中的表达水平。(已经携带有氯霉素抗性质粒) 当要表达的蛋白质需要形成二硫键以形成正确的折叠时,可以选择K–12衍生菌Origami 2系列,thioredoxin reductase (trxB) 和glutathione
重组质粒的原核表达
实验九表达质粒的构建与诱导表达 第一节原核表达概述 基因工程的研究一方面是获得基因的表达产物,另一方面是研究基因结构与功能的关系,最终都涉及目的基因的表达问题。表达载体(express vector)是指本身携带有宿主细胞基因表达所需的调控序列,能使克隆的基因在宿主细胞内进行转录与翻译的载体。也就是说,克隆载体只是携带外源基因,使其在宿主细胞内扩增;表达载体不仅使外源基因扩增,还使其表达。 表达载体在基因工程中具有十分重要的作用。外源基因在宿主(受体)细胞内是否表达以及表达水平受到许多因素(调控元件)的制约: 1.正确的阅读框架 为了获得正确编码的外源蛋白,外源基因编码区在插入表达质粒中原核基因编码区时,阅读框架应保持一致。阅读框架是由每三个核苷酸为一组连接起来的编码序列,外源基因只有在它与载体DNA的起始密码相吻合时,才算处于正确的阅读框架之中,从而表达融合蛋白,使外源蛋白与宿主蛋白相融合。 2.目的基因有效转录的启动子 启动子(promoter) 是DNA链上一段能与RNA聚合酶结合并能起始mRNA合成的序列, 它是基因表达不可缺少的重要调控序列。原核启动子是由两段彼此分开且又高度保守的核苷酸序列组成的,分别称为一35区和一10区。一35区的序列为TTGACA,一10区序列为TATAAT。此两序列之间的最佳间距为17 bp。可与RNA聚合酶结合,并指导该酶在正确的转录部位开始合成mRNA。由于细菌RNA聚合酶不能识别真核基因的启动子,因此原核表达载体必须用原核启动子带动真核基因在原核生物中转录。原核表达载体启动子的转录常常是可以控制的,即一般情况下不转录,而受诱导剂诱导时就能转录,带动外源基因的高效表达。 目前常用的启动子:如大肠杆菌的lac启动子是乳糖操纵子的启动子,受la cⅠ编码的阻遏蛋白调节控制;trp 等启动子是色氨酸操纵子启动子,受trp R编码的阻遏蛋白调节控制;tac启动子,由lac启动子的一l0区和trp 启动子的一35区融合而成,汇合了lac和trp两者优点,是一个很强的启动子,受lacⅠ编码的阻遏蛋白调节;lacUV 5启动子是经紫外线诱变改造后的lac启动子,该启动子失去CAP和cAMP的正调控,只要有乳糖或IPTG 存在时就能够启动转录;噬菌体的λP L、R启动子是λ噬菌体左、右向启动子,是一个温度敏感的阻遏蛋白受温度调控的很强的启动子;T7噬菌体启动子,比大肠杆菌启动子强得多,并且十分专一,只被T7 RNA聚合酶所识别;SV40启动子、多角蛋白启动子以及花椰菜花叶病毒(CaMV)启动子。 3.转录终止子 构建表达载体时,为了稳定载体系统,防止克隆的外源基因干扰表达载体的稳定性,一般要在多克隆位点的下游插入一段很强的核糖体RNA转录终止子(terminator)。否则合成的 mRNA过长,不仅消耗细胞内的底物和能量,而且容易使mRNA形成妨碍翻译的二级结构。原核基因的转录终止序列包括依赖Rho蛋白和不依赖Rho蛋白两种。不依赖Rho的终止信号序列都含发夹结构,末端为一连串T 及YRTCTG。 4.mRNA有效翻译的SD序列 在原核生物中,mRNA分子上有两个核糖体结合位点(ribosome binding site,RBS)也调节着mRNA的翻译,一个是起始密码(AUG或GUG),另一个是位于起始密码上游3~11个核苷酸处的由3~9个核苷酸组成的一段保守序列AGGAGGU,这段序列富含嘌呤核苷酸,称为SD序列。而核糖体和mRNA的结合是由SD序列以及与起始密码子AUG之间的距离决定的。因此,SD序列和它的起始密码子AUG之间的距离是影响外源基因在原核生物中表达量高低的重要因素。SD序列与AUG间隔9个碱基最为合适,其间距离过长或过短都会影响目的基因的表达,有时由于这种距离的影响,蛋白质合成水平会相差2 000倍以上。且SD序列与AUG之间的碱基最好是A或U,一3位最好是A。 5.转录、翻译后的适当修饰和加工 真核生物基因表达的产物往往需要进行适当的修饰加工,但由于大肠杆菌本身的蛋白质翻译后修饰加工系统相当不完善,表达的真核蛋白质不能形成适当的折叠或糖基化修饰。并且不同宿主其修饰系统也不一样,所以选择宿主时应注意。 6.信号序列(signal sequence)
