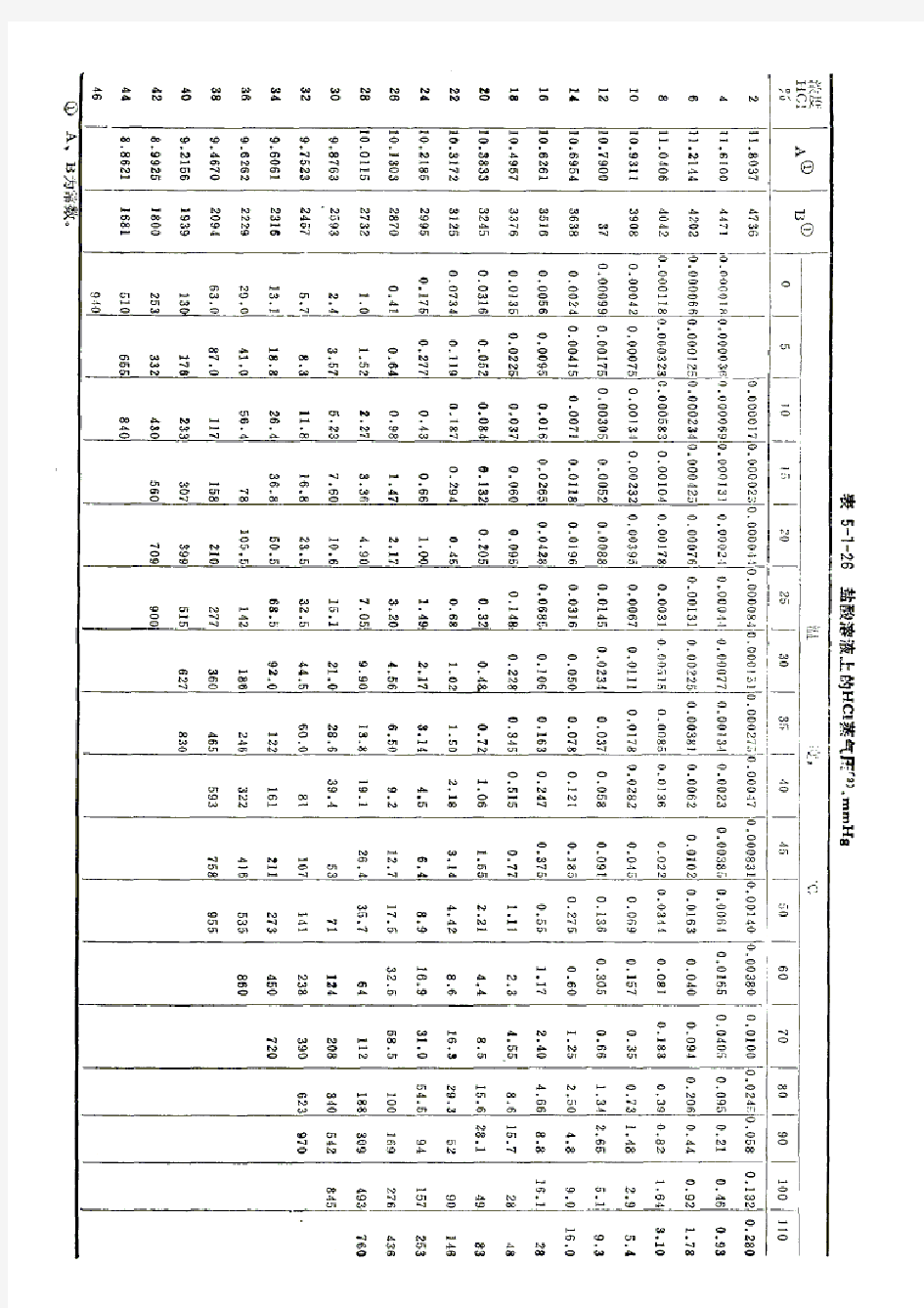
盐酸溶液上的HCl蒸汽压
液氨特性及应急处理
液氨特性及应急处理 2.1氨的理化性质 2.1.1标识 中文名氨;氨气(液氨) 英文名 ammonia 分子式 NH3 相对分子质量 17.03 CAS号 7664-41-7 危险性类别第2.3类有毒气体 化学类别氨 2.1.2理化性质 熔点(℃) -77.7 沸点(℃) -33.5 液体相对密度(水=1)0.82(-79℃) 气体相对密度(空气=1)0.6 饱和蒸汽压(kpa) 506.62 (4.7℃) 临界温度(℃) 132.5 临界压力(Mpa) 11.40 溶解性易溶于水、乙醇、乙醚 2.1.3稳定性和反应活性 稳定性稳定 聚合危害不聚合 避免接触的禁忌物卤素、酰基氯、酸类、氯仿、强氧化剂。 燃烧(分解)产物氧化氮、氨。 在高温时会分解成氮和氢,有还原作用。在催化剂存在时可被氧化成一氧化氮。 2.1.4主要组成与性状 主要成分纯品 外观与性状无色有刺激性恶臭的气体。 主要用途用做制冷剂及制取铵盐和氮肥。 液氨是无色的液体。是一种优良的溶剂。蒸发热很大,在沸点时是每克1369.08焦(327卡)。储于耐压钢瓶或钢槽中。由气态氨液化而得。 2.1.5爆炸特性与消防 燃烧性易燃 闪点(℃)无意义 引燃温度(℃) 651 爆炸下限(%) 15.7 爆炸上限(%) 27.4 最小点火能(mJ)至1000 mJ也不发火(氢气为0.02 mJ) 最大爆炸压力(Mpa) 0.580 2.2危险特性 与空气混合能形成爆炸性混合物。遇明火、高热能引起燃烧爆炸。与氟、氯等接触会发生剧烈反应。若遇高热,容器内压增大,有开裂和爆炸的危险。 2.3灭火方法 消防人员必须穿戴全身防火防毒服。切断气源。若不能立即切断气源,则不允许熄灭正在燃烧的气体。喷水冷却容器,可能的话将容器从火场移至空旷处。 2.4灭火剂: 雾状水、干粉、二氧化碳、砂土。 2.5健康危害 侵入途径吸入 健康危害低浓度氨对粘膜有刺激作用,高浓度可造成组织溶解坏死。
饱和蒸气压计算方法
饱和蒸气压 编辑[bǎo hézhēng qìyā] 在密闭条件中,在一定温度下,与固体或液体处于相平衡的蒸气所具有的压力称为饱和蒸气 压。同一物质在不同温度下有不同的蒸气压,并随着温度的升高而增大。不同液体饱和蒸气 压不同,溶剂的饱和蒸气压大于溶液的饱和蒸气压;对于同一物质,固态的饱和蒸气压小于 液态的饱和蒸气压。 目录 1定义 2计算公式 3附录 ?计算参数 ?水在不同温度下的饱和蒸气压 1定义编辑 饱和蒸气压(saturated vapor pressure) 例如,在30℃时,水的饱和蒸气压为4132.982Pa,乙醇为10532.438Pa。而在100℃时,水的 饱和蒸气压增大到101324.72Pa,乙醇为222647.74Pa。饱和蒸气压是液体的一项重要物理性 质,液体的沸点、液体混合物的相对挥发度等都与之有关。 2计算公式编辑 (1)Clausius-Claperon方程:d lnp/d(1/T)=-H(v)/(R*Z(v)) 式中p为蒸气压;H(v)为蒸发潜热;Z(v)为饱和蒸汽压缩因子与饱和液体压缩因子之差。 该方程是一个十分重要的方程,大部分蒸汽压方程是从此式积分得出的。 (2)Clapeyron 方程: 若上式中H(v)/(R*Z(v))为与温度无关的常数,积分式,并令积分常数为A,则得Clapeyron方 程:ln p=A-B/T 式中B=H(v)/(R*Z(v))。 (3)Antoine方程:lg p=A-B/(T+C) 式中,A,B,C为Antoine常数,可查数据表。Antoine方程是对Clausius-Clapeyron方程最 简单的改进,在1.333~199.98kPa范围内误差小。 3附录编辑 计算参数 在表1中给出了采用Antoine公式计算不同物质在不同温度下蒸气压的常数A、B、C。其公 式如下 lgP=A-B/(t+C)(1) 式中:P—物质的蒸气压,毫米汞柱; t—温度,℃ 公式(1)适用于大多数化合物;而对于另外一些只需常数B与C值的物质,则可采用(2) 公式进行计算 lgP=-52.23B/T+C (2) 式中:P—物质的蒸气压,毫米汞柱; 表1 不同物质的蒸气压 名称分子式范围(℃) A B C 1,1,2-三氯乙烷C2H3Cl3 \ 6.85189 1262.570 205.170 1,1,2一三氯乙烯C2HCl3 \ 7.02808 1315.040 230.000 1,2一丁二烯C4H6 -60~+80 7.16190 1121.000 251.000
水的饱和蒸汽压与温度对应表
水的饱和蒸汽压与温度对应表 一、水的饱和蒸汽压与温度的关系 蒸汽压是一定外界条件下,液体中的液态分子会蒸发为气态分子,同时气态分子也会撞击液面回归液态。这是单组分系统发生的两相变化,一定时间后,即可达到平衡。平衡时,气态分子含量达到最大值,这些气态分子对液体产生的压强称为蒸气压。 水的表面就有水蒸气压,当水的蒸气压达到水面上的气体总压的时候,水就沸腾。我们通常看到水烧开,就是在100摄氏度时水的蒸气压等于一个大气压。蒸气压随温度变化而变化,温度越高,蒸气压越大,当然还和液体种类有关。 一定的温度下,与同种物质的液态(或固态)处于平衡状态的蒸气所产生的压强叫饱和蒸气压,它随温度升高而增加。如:放在杯子里的水,会因不断蒸发变得愈来愈少。如果把纯水放在一个密闭的容器里,并抽走上方的空气。当水不断蒸发时,水面上方气相的压力,即水的蒸气所具有的压力就不断增加。但是,当温度一定时,气相压力最终将稳定在一个固定的数值上,这时的气相压力称为水在该温度下的饱和蒸气压力。当气相压力的数值达到饱和蒸气压力的数值时,液相的水分子仍然不断地气化,气相的水分子也不断地冷凝成液体,只是由于水的气化速度等于水蒸气的冷凝速
度,液体量才没有减少,气体量也没有增加,液体和气体达到平衡状态。所以,液态纯物质蒸气所具有的压力为其饱和蒸气压力时,气液两相即达到了相平衡。饱和蒸气压是物质的一个重要性质,它的大小取决于物质的本性和温度。饱和蒸气压越大,表示该物质越容易挥发。 二、水的饱和蒸汽压与温度对应表 水的饱和蒸汽压与温度对应表
三、水的饱和蒸汽压与温度的换算公式 当10℃≤T≤168℃时,采用安托尼方程计算:lgP=7.07406-(1657.46/(T+227.02)) 式中:P——水在T温度时的饱和蒸汽压,kPa; T——水的温度,℃ 四、水的饱和蒸汽压曲线
15立方米液氨储罐杨砺
153 M液氨储罐设计 杨砺
目录 一、设计条件表---------------------------------------------------------------------------------- 3 二、设计数据表----------------------------------------------------------------------------------- 3 三、焊缝结构及无损检测----------------------------------------------------------------------- 3 四、管口表----------------------------------------------------------------------------------------- 4 五、封头设计-------------------------------------------------------------------------------------- 4 六、筒体长度确定---------------------------------------------------------------------------------5 七、设备的材料及其厚度计算----------------------------------------------------------------- 5 八、卧式容器应力校核---------------------------------------------------------------------------7 九、开孔及开孔补强------------------------------------------------------------------------------8 十、零部件设计----------------------------------------------------------------------------------- 9 1、支座设计---------------------------------------------------------------------------------9 2、人孔其法兰设计-------------------------------------------------------------------------10 3、安全阀接口管及其法兰设计--------------------------------------------------------- 10 4、液氨出口接管及其法兰设计----------------------------------------------------------11 5、放空口接管及其法兰设--------------------------------------------------------------- 11 6、液氨入口接管与其法兰设计------------------------------------------------------- 11 7、压力表接管及其法兰设计----------------------------------------------------------- 12 8、气氨出口接管及其法兰设计-------------------------------------------------------- 12 9、排污管及其法兰设计------------------------------------------------------------------12 10、液位计及其法兰的选择------------------------------------------------------------- 13 十一、焊接接头设计---------------------------------------------------------------------------13 十二、参考资料-----------------------------------------------------------------------------------14 十三、结束语--------------------------------------------------------------------------------------15
1-3 纯液体饱和蒸气压的测定
实验1-3 纯液体饱和蒸气压的测定 【目的要求】 1. 掌握静态法测定液体饱和蒸气压的原理及操作方法。学会由图解法求平均摩尔气化热和正常沸点。 2. 理解纯液体的饱和蒸气压与温度的关系、克劳修斯-克拉贝龙(Clausius -Clapeyron)方程式的意义。 3. 了解真空泵、恒温槽及气压计的使用及注意事项。 【实验原理】 在通常温度下(距离临界温度较远时),纯液体与其蒸气达平衡时的蒸气压称为该温度下液体的饱和蒸气压,简称为蒸气压。蒸发一摩尔液体所吸收的热量称为该温度下液体的摩尔气化热。 液体的蒸气压随温度而变化,温度升高时,蒸气压增大;温度降低时,蒸气压降低,这主要与分子的动能有关。当蒸气压等于外界压力时,液体便沸腾,此时的温度称为沸点,外压不同时,液体沸点将相应改变,当外压为101.325kPa 时,液体的沸点称为该液体的正常沸点。 液体的饱和蒸气压与温度的关系用克劳修斯-克拉贝龙方程式表示: 2m vap d ln d RT H T p ?= (1) 式中,R 为摩尔气体常数;T 为热力学温度;Δvap H m 为在温度T 时纯液体的摩尔气化热。 假定Δvap H m 与温度无关,或因温度范围较小,Δvap H m 可以近似作为常数,积分(1)式得: ln p =C T R H +??-1m vap (2) 其中C 为积分常数。由此式可以看出,以ln p 对1/T 作图,应为一直线,直线的斜率为 R H m vap ?-,由斜率可求算液体的Δvap H m 。 测定液体饱和蒸气压的方法很多。本实验采用静态法,是指在某一温度下,直接测量饱和蒸气压,此法一般适用于蒸气压比较大的液体。实验所用仪器是纯液体饱和蒸气压测定装置,如图2-1所示。 平衡管由A 球和U 型管B 、C 组成。平衡管上接一冷凝管5,以橡皮管与压力计相连。A 内装待测液体,当A 球的液面上纯粹是待测液体的蒸气,而B 管与C 管的液面处于同一水平时,则表示B 管液面上的(即A 球液面上的蒸气压)与加在C 管液面上的外压相等。此时,体系气液两相平衡的温度称为液体在此外压下的沸点。用当时的大气压减去压力计两水银面的高度差,即为该温度下液体的饱和蒸气压。 用静态法测量不同温度下纯液体饱和蒸气压的实验方法,有升温法和降温法二种。 【仪器试剂】 纯液体饱和蒸气压测定装置1套; 放大镜(×5)1只; 直尺1把;真空泵及附件等。。 蒸馏水;无水乙醇 【实验步骤】 升温法测定不同温度下纯液体的饱和蒸气压
液氨密度表
液氨密度表 温度℃密度㎏/L 温度℃密度㎏/L 温度℃密度㎏/L -50 0.701997 -16 0.659846 18 0.613188 -49 0.700807 -15 0.658546 19 0.611726 -48 0.699614 -14 0.657243 20 0.610258 -47 0.698419 -13 0.655936 21 0.608784 -46 0.697221 -12 0.654625 22 0.607303 -45 0.696020 -11 0.653310 23 0.605817 -44 0.694816 -10 0.651991 24 0.604324 -43 0.693610 -9 0.650668 25 0.602824 -42 0.692400 -8 0.649341 26 0.601318 -41 0.691188 -7 0.648009 27 0.599805 -40 0.689973 -6 0.646673 28 0.598285 -39 0.688755 -5 0.645333 29 0.596759 -38 0.687534 -4 0.643989 30 0.595225 -37 0.686309 -3 0.642640 31 0.593684 -36 0.685082 -2 0.641287 32 0.592136 -35 0.683852 -1 0.639929 33 0.590581 -34 0.682618 0 0.638567 34 0.589018 -33 0.681382 1 0.637200 35 0.587447 -32 0.680142 2 0.635828 36 0.585869 -31 0.678899 3 0.634451 37 0.584283 -30 0.677653 4 0.633070 38 0.582688 -29 0.676404 5 0.631684 39 0.581086 -28 0.675151 6 0.630293 40 0.579475 -27 0.673895 7 0.628897 41 0.577855 -26 0.672635 8 0.627496 42 0.576227 -25 0.671372 9 0.626089 43 0.574590 -24 0.670106 10 0.624678 44 0.572945 -23 0.668836 11 0.623261 45 0.571290 -22 0.667562 12 0.621838 46 0.569625 -21 0.666285 13 0.620411 47 0.567951 -20 0.665005 14 0.618978 48 0.566268 -19 0.663721 15 0.617539 49 0.564574 -18 0.662433 16 0.616094 50 0.562871 -17 0.661141 17 0.614644 注:在-50℃至50℃范围内,液氨的相对密度还可按下式计算: d4t= 1+0.424805×√133-t +0.015938×(133-t) 4.2830+0.813055×√133-t -0.008286×(133-t) 资料名称:液氨在不同温度下的密度
纯液体饱和蒸气压的测定
物理化学实验--纯液体饱和蒸汽压的测定 化学化工学院 07应化1W 宋强
Ⅰ目的要求 一.明确纯液体饱和蒸气压的定义和气液两相平衡的概念,深入了解纯液体饱和蒸气压和温度的关系——克劳修斯—克拉贝龙方程式 二.用等压记测定不同温度下环已烷(或正已烷)的饱和蒸气压。初步掌握真空实验技术 三.学会用图解法求被测液体在实验温度范围内的平均摩尔气化热与正常沸点Ⅱ基本原理 在一定温度下,与纯液体处于平衡态时的蒸气压力,称为该温度下的饱和蒸气压。这里的平衡状态是指动态平衡。在某一温度下,被测液体处于密闭真空容器中,液体分子中表面逃逸成蒸气,同时蒸气分子因碰撞而凝结成液相,当两者的速率相等时,就达到了动态平衡,此时气相中的蒸气密度不再改变,因而具有一定的饱和蒸气压。 纯液体的蒸气压是随温度变化而变化的,它们之间的关系可用克劳修斯—克拉贝龙方(Clausius—Clapeyron)方程来表示: dLnp*/dT=△v H m/RT2 (3—1) 式中p*为纯液体温度T时的饱和蒸气压;T为热力学温度;△v H m为液体摩尔气化热;R为气体常数。如果温度变化的范围不大,△v H m视为常数,可当作平均摩尔气化热。将(3—1)式积分得: Lnp*=-△v H m/RT + c (3—2) 式中c为积分常数,此数与压力p*有关。 由(3—2)式可知,在一定温度范围内,测定不同温度下的饱和蒸气压,以Lnp*对1/T作图,可得一条直线。由该直线的斜率可求得实验范围内液体的平均摩尔
气化热。当外压为101.325Kpa时,液体的蒸气压与外压相等时的温度称为该液体的正常沸点。从图中也可求得其正常沸点。 测定饱和蒸气压常用的方法有动态法、静态法、和饱和气流法等。本实验采用静态法,既被测物质放在一个密闭的体系中,在不同温度下直接测量其饱和蒸气压,在不同外压下测量相应的沸点。此法适用于蒸气压比较大的液体。 Ⅲ仪器试剂 蒸气压测定装置1套真空泵1台 数字式气压计1台电加热器1只 温度计2支数字式真空及计1台 磁力搅拌器1台异丙醇(分析纯,沸点82.5℃) 一、仪器装置如图所示: 所有借口必须严密封闭。平衡管由三根相连通的玻璃管a,b和c组成,a管中存储被测液体,b和c中也有液体在底部相连。当a、c管的上部纯粹是待测液体的蒸气,b与c管中的液面在同一水平时,则表示在c管液面上的蒸气压与加在b 管液面上的外压相等,此时液体的温度即体系的气液平衡温度,亦即沸点。 平衡管中的液体可用下法装入:先将平衡管取下洗净,烘干,然后烤烘(可用煤气灯)a管,赶走管内空气,速将液体自b管的管口灌入,冷却a管,液体即被吸入。反复二,三次,使液体灌至a管高度的三分之二为宜,然后接在装置上。
液氨储罐设计
第一章绪论 1. 1 设计任务 设计一液氨贮罐。工艺条件:温度为40 C,氨饱和蒸气压1.55MPa,容积为20m3, 使用年限15 年。 1.2 设计要求及成果 1. 确定容器材质; 2. 确定罐体形状及名义厚度; 3. 确定封头形状及名义厚度; 4. 确定支座,人孔及接管,以及开孔补强情况 5. 编制设计说明书以及绘制设备装配图1 张(A1)。 1.3 技术要求 (一)本设备按GBI50-1998《钢制压力容器》进行制造、试验和验收 (二)焊接材料,对接焊接接头型式及尺寸可按GB985-80中规定(设计焊接接头系数1.0) (三)焊接采用电弧焊,焊条型号为E4303 (四)壳体焊缝应进行无损探伤检 查,探伤长度为100% 第二章设计参数确定 2.1 设计温度 题目中给出设计温度取40 C
2.2设计压力 在夏季液氨储罐经太阳暴晒,随着气温的变化,储罐的操作压力也在不断变化。通过查阅资料可知包头最高气温为40.4 C,通过查表可知,在40C时液氨的饱和蒸汽压(绝对压力)为1.55MPa,密度为580kg/m3,而容器设计时必须考虑在工作情况下可能遇到的工作压力和相对应的温度两者相结合中最苛刻工作压力来确定设计压力。一般是指容器顶部最高压力与相应的设计温度一起作为设计载荷条件,其值不低于工作压力。 此液氨储罐采用安全法,依据《化工设备机械基础》若储罐采用安全法时 设计压力应采用最大工作压力P w的1.05 1.1倍,取设计压力P 1.05P w (已知 P w 1.55MPa表压)所以P 1.05F W 1.6MPa。 2.3腐蚀余量 查《腐蚀数据手册》16MnR耐氨腐蚀,其0.1mm/ y,若设计寿命为15 年,则C215 0.1 1.5mm 2.4焊缝系数 该容器属中压贮存容器,技《压力容器安全技术监察规程》规定,氨属中度 毒性介质,容器筒体的纵向焊接接头和封头基本上都采用双面焊或相当于双面焊 的全焊透的焊接接头,所以取1.0或0.85常见。得选取按下表选择 2.5容器直径 考虑到压制封头胎具的规格及标准件配套选用的需要,容器的筒体和封头的
饱和蒸汽压
饱和蒸汽压
饱和蒸气压 编辑 [bǎo hézhēng qìyā] 饱和蒸汽压即饱和蒸气压。 在密闭条件中,在一定温度下,与固体或液体处于相平衡的蒸气所具有的压力称为饱和蒸气压。同一物质在不同温度下有不同的蒸气压,并随着温度的升高而增大。不同液体饱和蒸气压不同,溶剂的饱和蒸气压大于溶液的饱和蒸气压;对于同一物质,固态的饱和蒸气压小于液态的饱和蒸气压。 蒸汽压指的是在液体(或者固体)的表面存在着该物质的蒸汽,这些蒸汽对液体表面产生的压强就是该液体的蒸汽压。比如,水的表面就有水蒸汽压,当水的蒸汽压达到水面上的气体总压的时候,水就沸腾。我们通常看到水烧开,就是在100摄氏度时水的蒸汽压等于一个大气压。蒸汽压随温度变化而变化,温度越高,蒸汽压越大,当然还和液体种类有关。一定的温度下,与同种物质的液态(或固态)处于平衡状态的蒸汽所产生的压强叫饱和蒸汽压,它随温度升高而增加。如:放在杯子里的水,会因不断蒸发变得愈来愈少。如果把纯水放在一个密闭的容器里,并抽走上方的空气。当水不断蒸发时,水面上方汽相的压力,即水的蒸汽所具有的压力就不断增加。但是,当温度一定时,汽相压力最终将稳定在一个固定的数值上,这时的汽相压力称为水在该温度下的饱和蒸汽压力。当汽相压力的数值达到饱和蒸汽压力的数值时,液相的水分子仍然不断地气化,汽相的水分子也不断地冷凝成液体,只是由于水的气化速度等于水蒸汽的冷凝速度,液体量才没有减少,气体量也没有增加,液体和气体达到平衡状态。所以,液态纯物质蒸汽所具有的压力为其饱和蒸汽压力时,汽液两相即达到了相平衡。饱和蒸汽压是物质的一个重要性质,它的大小取决于物质的本性和温度。饱和蒸汽压越大,表示该物质越容易挥发。 1定义编辑 饱和蒸气压(saturated vapor pressure) 例如,在30℃时,水的饱和蒸气压为4132.982Pa,乙醇为10532.438Pa。而在100℃时,水的饱和蒸气压增大到101324.72Pa,乙醇为222647.74Pa。饱和蒸气压是液体的一项重要物理性质,液体的沸点、液体混合物的相对挥发度等都与之有关。 2计算公式编辑 (1)Clausius-Claperon方程:d lnp/d(1/T)=-H(v)/(R*Z(v)) 式中p为蒸气压;H(v)为蒸发潜热;Z(v)为饱和蒸汽压缩因子与饱和液体压缩因子之差。 该方程是一个十分重要的方程,大部分蒸汽压方程是从此式积分得出的。 (2)Clapeyron 方程: 若上式中H(v)/(R*Z(v))为与温度无关的常数,积分式,并令积分常数为A,则得Clapeyron方程:ln p=A-B/T 式中B=H(v)/(R*Z(v))。 (3)Antoine方程:lg p=A-B/(T+C) 式中,A,B,C为Antoine常数,可查数据表。Antoine方程是对Clausius-Clapeyron方程最简单的改进,在1.333~199.98kPa范围内误差小。 3附录编辑 计算参数 在表1中给出了采用Antoine公式计算不同物质在不同温度下蒸气压的常数A、B、C。其公式如下 lgP=A-B/(t+C)(1) 式中:P—物质的蒸气压,毫米汞柱; t—温度,℃ 公式(1)适用于大多数化合物;而对于另外一些只需常数B与C值的物质,则可采用(2)公式进行计算 lgP=-52.23B/T+C (2)
液氨储罐设计参数的确定设计说明书
液氨储罐设计参数的确定设计说明书第一章绪论 1.1设计符号说明 英文字母 α———容器的设计寿命,y; D———贮罐径,mm; i []tσ———钢板的许用应力,MPa P———液氨的饱和蒸汽压,MPa C———钢板厚度负偏差, mm; 1 C———介质的腐蚀裕量, mm; 2 希腊字母 δ———罐体计算厚度, mm; δ———罐体设计厚度, mm; d δ———罐体的名义厚度, mm; n δ———罐体的有效厚度, mm; e ?———圆整值,mm λ———腐蚀速率,y mm/ φ———焊接接头系数
1.2 设计任务 设计一液氨贮罐。工艺条件:温度为40℃,氨饱和蒸气压MPa 28m。 .1,容积为3 55 1.3 设计思路 综合运用所学的机械基础课程知识,本着认真负责团结合作的态度,对储罐进行详细设计。在设计过程中综合考虑了经济性,实用性,安全可靠性,各项设计参数都正确参考了行业使用标准或国家标准,这样让设计有实际意义,并考虑到结构方面的要求,合理地进行设计,研究出最佳方案。 1.4 设计特点 容器的设计一般由筒体、封头、法兰、支座、接口管及人孔等组成。常、低压化工设备通用零部件大都有标准,设计时可直接选用。本设计书主要介绍了液罐的的筒体、封头的设计计算,低压通用零部件的选用。 各项设计参数都正确参考了行业使用标准或国家标准,这样让设计有章可循,并考虑到结构方面的要求,合理地进行设计。 1.5设计要求及成果 1. 确定容器材质; 2. 确定罐体形状及名义厚度; 3. 确定封头形状及名义厚度; 4. 确定支座,人孔及接管,以及开孔补强情况
5. 编制设计说明书以及绘制设备装配图1(A2)。 1.6技术要求 (一)本设备按GBl50-1998《钢制压力容器》进行制造、试验和验收 (二)焊接材料,对接焊接接头型式及尺寸可按GB985-80中规定(设计焊接接头系φ) 数0.1 = (三)焊接采用电弧焊,焊条型号为E4303 (四)壳体焊缝应进行无损探伤检查,探伤长度为100% 第二章液氨储罐设计参数的确定 2.1.设计温度与设计压力的确定 液氨储罐通常置于室外,罐液氨的温度和压力直接受到大气温度的影响,在夏季液氨储罐经太阳暴晒,随着气温的变化,储罐的操作压力也在不断变化。根据设计任务书的要求,所设计液氨贮罐的最高使用温度为40℃,查表可知40℃时液氨的饱和蒸汽压为1.55MPa。《压力容器安全监察规程》规定液化气体储罐必须安装安全阀,设计压力可取最大操作压力的1.05-1.10倍。取1.10倍最大操作压力为设计压力,所以设计压力p = 1.10×(1.05? 1.1) = 1.595MPa,故取设计压力p=1.6MPa。 2.2.罐体和封头的材料的选择 选择容器用钢必须综合考虑:容器的操作条件,如设计压力、设计温度、介质特性和操作压力等;材料的使用性能,如力学性能、物理性能、化学性能(主要是耐腐蚀性
水在不同温度下的饱和蒸气压
饱和蒸气压(s a t u r a t e d v a p o r p r e s s u r e) 在密闭条件中,在一定温度下,与液体或固体处于相平衡的蒸气所具有的压力称为饱和蒸气压。同一物质在不同温度下有不同的蒸气压,并随着温度的升高而增大。不同液体饱和蒸汽压不同,溶剂的饱和蒸汽压大于溶液的饱和蒸汽压;对于同一物质,固态的饱和蒸汽压小于液态的饱和蒸汽压。例如,在30℃时,水的饱和蒸气压为4132.982Pa,乙醇为10532.438Pa。而在100℃时,水的饱和蒸气压增大到101324.72Pa,乙醇为222647.74Pa。饱和蒸气压是液体的一项重要物理性质,如液体的沸点、液体混合物的相对挥发度等都与之有关。 饱和蒸气压曲线 水在不同温度下的饱和蒸气压 SaturatedWaterVaporPressuresatDifferentTemperatures
编辑本段饱和蒸汽压公式 (1)Clausius-Claperon方程:dlnp/d(1/T)=-H(v)/(R*Z(v)) 式中p为蒸汽压;H(v)为蒸发潜热;Z(v)为饱和蒸汽压缩因子与饱和液体压缩因子之差。 该方程是一个十分重要的方程,大部分蒸汽压方程是从此式积分得出的。 (2)Clapeyron方程: 若上式中H(v)/(R*Z(v))为与温度无关的常数,积分式,并令积分常数为A,则得Clapeyron 方程:lnp=A-B/T 式中B=H(v)/(R*Z(v))。 (3)Antoine方程:lnp=A-B/(T+C)
式中,A,B,C为Antoine常数,可查数据表。Antoine方程是对Clausius-Clapeyron方程最简单的改进,在1.333~199.98kPa范围内误差小。 编辑本段附录 在表1中给出了采用Antoine公式计算不同物质在不同温度下蒸气压的常数A、B、C。其公式如下 lgP=A-B/(t+C)(1) 式中:P—物质的蒸气压,毫米汞柱; t—温度,℃ 公式(1)适用于大多数化合物;而对于另外一些只需常数B与C值的物质,则可采用(2)公式进行计算 lgP=-52.23B/T+C(2) 式中:P—物质的蒸气压,毫米汞柱; 表1不同物质的蒸气压 名称分子式范围(℃)ABC 银Ag1650~1950公式(2)2508.76 氯化银AgCl1255~1442公式(2)185.58.179 三氯化铝AlCl370~190公式(2)11516.24 氧化铝Al2O31840~2200公式(2)54014.22 砷As440~815公式(2)13310.800 砷As800~860公式(2)47.16.692 三氧化二砷As2O3100~310公式(2)111.3512.127 三氧化二砷As2O3315~490公式(2)52.126.513 氩Ar-207.62~-189.19公式(2)7.81457.5741 金Au2315~2500公式(2)3859.853 三氯化硼BCl3……6.18811756.89214.0 钡Ba930~1130公式(2)35015.765 铋Bi1210~1420公式(2)2008.876 溴Br2……6.83298113.0228.0 碳C3880~4430公式(2)5409.596 二氧化碳CO2……9.641771284.07268.432 二硫化碳CS2-10~+1606.851451122.50236.46 一氧化碳CO-210~-1606.24020230.274260.0 四氯化碳CCl4……6.933901242.43230.0 钙Ca500~700公式(2)1959.697 钙960~1100公式(2)37016.240 镉Cd150~320.9公式(2)1098.564 镉500~840公式(2)99.97.897 氯Cl2……6.86773821.107240 二氧化氯ClO2-59~+11公式(2)27.267.893 钴Co2374公式(2)3097.571 铯Cs200~230公式(2)73.46.949 铜Cu2100~2310公式(2)46812.344 氯化亚铜Cu2Cl2878~1369公式(2)80.705.454 铁Fe2220~2450公式(2)3097.482
液氨储蓄罐的机械设计
XX学院 本科课程设计 题目:液氨储蓄罐的机械设计 专业:应用化学 学院:化学XX 学院 班级: XX级XX 班 姓名: XXX 学号:XXX 指导教师: XXX
目录 一、设计条件 (3) 二、设计内容 (3) 1.选择符合要求的材料 (3) 2.确定设计参数 (4) 3.罐体壁厚设计 (5) 4.封头壁厚设计 (5) 5.校核水压实验强度 (5) 6.应力的计算 (6) 7.鞍座的设计 (8) 8.人孔的设计 (10) 9.人孔的补强 (11) 10.接口管的设计 (11) 五、课程设计收获 (13) 六、设计符号说明 (13) 七、参考资料 (14)
液氨储罐的机械设计 一、 设计时间 2016年10月25日-2016年12月25日 二、 设计条件 1.工艺条件;温度40℃,氨的饱和蒸汽压1.55MPa 2.贮罐筒体为圆柱形,封头为标准椭圆封头 3. 贮罐容积V (单位m 3):20 4. 使用地点:XX 三、 设计内容 1.选择符合要求的材料 因为液氨的腐蚀性小,贮罐可选用一般钢材,但由于液氨贮罐属于带压容器,可以考虑20R 和16MnR 这两种钢种。而16MnR 在中温(475℃以下)及低温(-40℃以上)的机械性能优于20R ,是使用十分成熟的钢种,质量稳定,可使用在-40-475℃场合,故在此选择16MnR 钢板作为制造筒体和封头的材料。 2.确定设计参数 (1)设计温度 题目中给出设计温度取40℃。 (2)设计压力 在夏季液氨储罐经太阳暴晒,随着气温的变化,储罐的操作压力也在不断变化。通过查阅资料可知包头最高气温为40℃,通过查表可知,在40℃ 时液氨的饱和蒸汽压(绝对压力)为1.55MPa ,密度为580kg/m 3,而容器设计时必须考虑在工作情况下可能遇到的工作压力和相对应的温度两者相结合中最苛刻工作压力来确定设计压力。一般是指容器顶部最高压力与相应的设计温度一起作为设计载荷条件,其值不低于工作压力。 此液氨储罐采用安全法,依据《化工设备机械基础》若储罐采用安全法时设计压力应采用最大工作压力的倍,取设计压力(已知 w P 1.105.1-w P P 05.1=
饱和蒸汽压计算方法
There is a large number of saturation vapor pressure equations used to calculate the pressure of water vapor over a surface of liquid water or ice. This is a brief overview of the most important equations used. Several useful reviews of the existing vapor pressure curves are listed in the references. Please note the updated discussion of the WMO formulation. 1) Vapor Pressure over liquid water below 0°C ?Goff Gratch equation (Smithsonian Tables, 1984, after Goff and Gratch, 1946): Log10p w = -7.90298 (373.16/T-1) [1] + 5.02808 Log10(373.16/T) - 1.3816 10-7 (1011.344 (1-T/373.16)-1) + 8.1328 10-3 (10-3.49149 (373.16/T-1) -1) + Log10(1013.246) with T in [K] and p w in [hPa] ?WMO (Goff, 1957): Log10p w = 10.79574 (1-273.16/T)[2] - 5.02800 Log10(T/273.16) + 1.50475 10-4 (1 - 10(-8.2969*(T/273.16-1))) + 0.42873 10-3 (10(+4.76955*(1-273.16/T)) - 1) + 0.78614 with T in [K] and p w in [hPa] (Note: WMO based its recommendation on a paper by Goff (1957), which is shown here. The recommendation published by WMO (1988) has several typographical errors and cannot be used. A corrigendum (WMO, 2000) shows the term +0.42873 10-3 (10(-4.76955*(1-273.16/T)) - 1) in the fourth line compared to the original publication by Goff (1957). Note the different sign of the exponent. The earlier 1984 edition shows the correct formula.) ?Hyland and Wexler (Hyland and Wexler, 1983): Log p w = -0.58002206 104 / T [3] + 0.13914993 101
水的饱和蒸汽压与温度对应表
水的饱和蒸汽压与温度对应表 蒸气压蒸气压指的是在液体(或者固体)的表面存在着该物质的蒸气,这些蒸气对液体表面产生的压强就是该液体的蒸气压。比如,水的表面就有水蒸气压,当水的蒸气压达到水面上的气体总压的时候,水就沸腾。我们通常看到水烧开,就是在100摄氏度时水的蒸气压等于一个大气压。蒸气压随温度变化而变化,温度越高,蒸气压越大,当然还和液体种类有关。一定的温度下,与同种物质的液态(或固态)处于平衡状态的蒸气所产生的压强叫饱和蒸气压,它随温度升高而增加。如:放在杯子里的水,会因不断蒸发变得愈来愈少。如果把纯水放在一个密闭的容器里,并抽走上方的空气。当水不断蒸发时,水面上方气相的压力,即水的蒸气所具有的压力就不断增加。但是,当温度一定时,气相压力最终将稳定在一个固定的数值上,这时的气相压力称为水在该温度下的饱和蒸气压力。当气相压力的数值达到饱和蒸气压力的数值时,液相的水分子仍然不断地气化,气相的水分子也不断地冷凝成液体,只是由于水的气化速度等于水蒸气的冷凝速度,液体量才没有减少,气体量也没有增加,液体和气体达到平衡状态。所以,液态纯物质蒸气所具有的压力为其饱和蒸气压力时,气液两相即达到了相平衡。饱和蒸气压是物质的一个重要性质,它的大小取决于物质的本性和温度。饱和蒸气压越大,表示该物质越容易挥
发。 当气液或气固两相平衡时,气相中A物质的气压,就为液相或固相中A物质的饱和蒸气压,简称蒸气压。下面为影响因素: 1.对于放在真空容器中的液体,由于蒸发,液体分子不断进入气相,使气相压力变大,当两相平衡时气相压强就为该液体饱和蒸汽压,其也等于液相的外压;温度升高,液体分子能量更高,更易脱离液体的束缚进入气相,使饱和蒸气压变大。 2.但是一般液体都暴露在空气中,液相外压=蒸气压力+空气压力=101.325KPa),并假设空气不溶于这种液体,一般情况由于外压的增加,蒸气压变大(不过影响比较小) 3.一般讨论的蒸气压都为大量液体的蒸气压,但是当液体变为很小的液滴是,且液滴尺寸越小,由于表面张力而产生附加压力越大,而使蒸气压变高(这也是形成过热液体,过饱和溶液等亚稳态体系的原因)。所以蒸气压与温度,压力,物质特性,在表面化学中液面的曲率也有影响. 不同物质的蒸气压不同,下面总结给出水在不同温度下的饱和蒸气压:
水在不同温度下的饱和蒸气压
饱和蒸气压(saturated vapor pressure) 在密闭条件中,在一定温度下,与液体或固体处于相平衡的蒸气所具有的压力称为饱和蒸气压。同一物质在不同温度下有不同的蒸气压,并随着温度的升高而增大。不同液体饱和蒸汽压不同,溶剂的饱和蒸汽压大于溶液的饱和蒸汽压;对于同一物质,固态的饱和蒸汽压小于液态的饱和蒸汽压。例如,在30℃时,水的饱和蒸气压为,乙醇为。而在100℃时,水的饱和蒸气压增大到,乙醇为。饱和蒸气压是液体的一项重要物理性质,如液体的沸点、液体混合物的相对挥发度等都与之有关。 饱和蒸气压曲线 水在不同温度下的饱和蒸气压 Saturated Water Vapor Pressures at Different Temperatures
编辑本段饱和蒸汽压公式 (1)Clausius-Claperon方程:d lnp/d(1/T)=-H(v)/(R*Z(v)) 式中p为蒸汽压;H(v)为蒸发潜热;Z(v)为饱和蒸汽压缩因子与饱和液体压缩因子之差。 该方程是一个十分重要的方程,大部分蒸汽压方程是从此式积分得出的。 (2)Clapeyron 方程: 若上式中H(v)/(R*Z(v))为与温度无关的常数,积分式,并令积分常数为A,则得Clapeyron 方程:ln p=A-B/T 式中B=H(v)/(R*Z(v))。 (3)Antoine方程:ln p=A-B/(T+C) 式中,A,B,C为Antoine常数,可查数据表。Antoine方程是对Clausius-Clapeyron方
程最简单的改进,在~范围内误差小。 编辑本段附录 在表1中给出了采用Antoine公式计算不同物质在不同温度下蒸气压的常数A、B、C。其公式如下 lgP=A-B/(t+C)(1) 式中:P—物质的蒸气压,毫米汞柱; t—温度,℃ 公式(1)适用于大多数化合物;而对于另外一些只需常数B与C值的物质,则可采用(2)公式进行计算 lgP=T+C (2) 式中:P—物质的蒸气压,毫米汞柱; 表1 不同物质的蒸气压 名称分子式范围(℃) A B C 银Ag 1650~1950 公式(2)250 氯化银AgCl 1255~1442 公式(2) 三氯化铝AlCl3 70~190 公式(2)115 氧化铝Al2O3 1840~2200 公式(2)540 砷As 440~815 公式(2)133 砷As 800~860 公式(2) 三氧化二砷As2O3 100~310 公式(2) 三氧化二砷As2O3 315~490 公式(2) 氩Ar ~ 公式(2) 金Au 2315~2500 公式(2)385 三氯化硼BCl3 …… 钡Ba 930~1130 公式(2)350 铋Bi 1210~1420 公式(2)200 溴Br2 …… 碳 C 3880~4430 公式(2)540 二氧化碳CO2 …… 二硫化碳CS2 -10~+160 一氧化碳CO -210~-160 四氯化碳CCl4 …… 钙Ca 500~700 公式(2)195 钙960~1100 公式(2)370 镉Cd 150~ 公式(2)109 镉500~840 公式(2) 氯Cl2 (240) 二氧化氯ClO2 -59~+11 公式(2) 钴Co 2374 公式(2)309 铯Cs 200~230 公式(2) 铜Cu 2100~2310 公式(2)468 氯化亚铜Cu2Cl2 878~1369 公式(2) 铁Fe 2220~2450 公式(2)309 氯化亚铁FeCl2 700~930 公式(2)
