高中化学四种晶体类型的比较
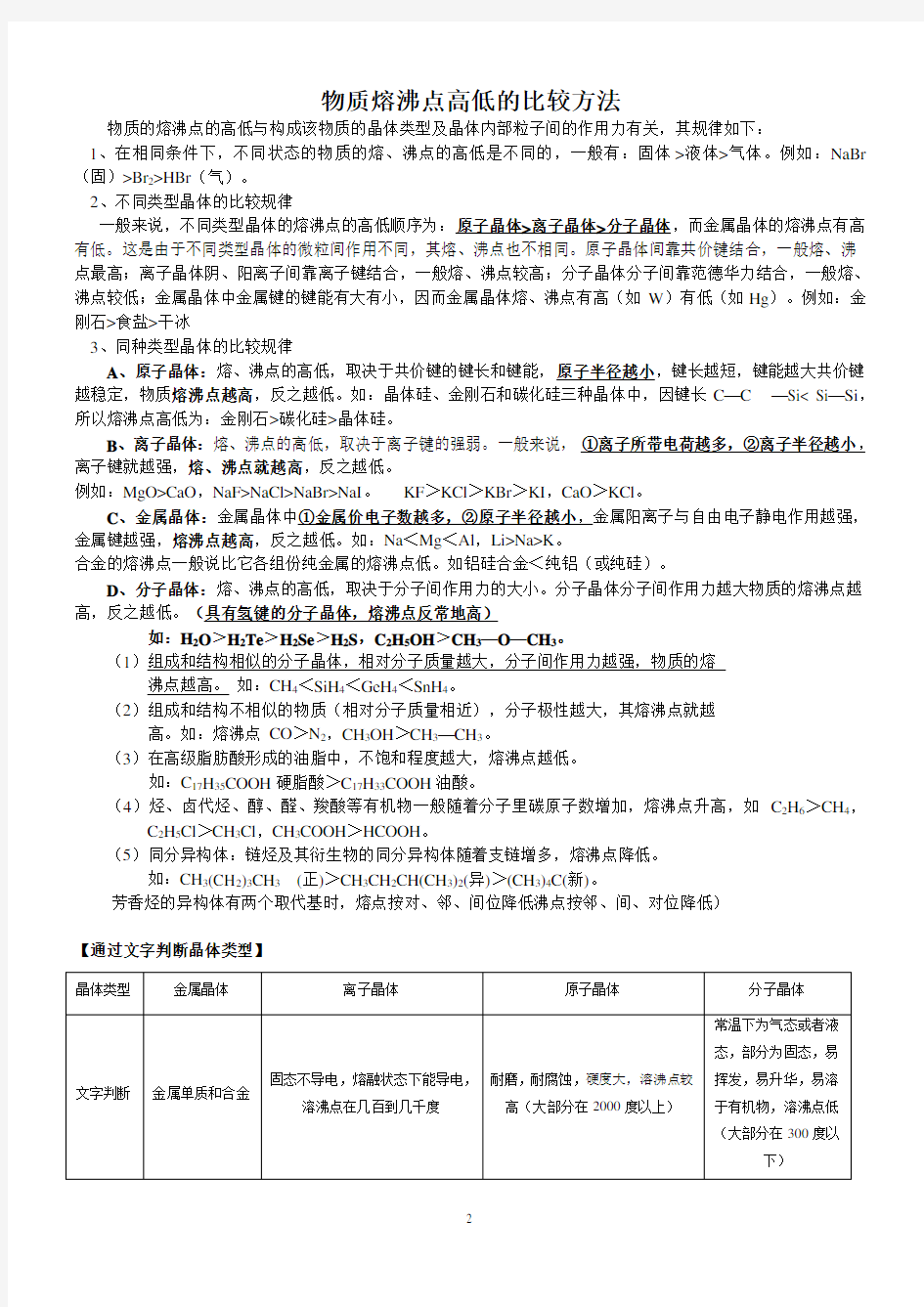
四种晶体类型的比较
物质熔沸点高低的比较方法
物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下:
1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr (固)>Br2>HBr(气)。
2、不同类型晶体的比较规律
一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰
3、同种类型晶体的比较规律
A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,原子半径越小,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
B、离子晶体:熔、沸点的高低,取决于离子键的强弱。一般来说,①离子所带电荷越多,②离子半径越小,离子键就越强,熔、沸点就越高,反之越低。
例如:MgO>CaO,NaF>NaCl>NaBr>NaI。KF>KCl>KBr>KI,CaO>KCl。
C、金属晶体:金属晶体中①金属价电子数越多,②原子半径越小,金属阳离子与自由电子静电作用越强,金属键越强,熔沸点越高,反之越低。如:Na<Mg<Al,Li>Na>K。
合金的熔沸点一般说比它各组份纯金属的熔沸点低。如铝硅合金<纯铝(或纯硅)。
D、分子晶体:熔、沸点的高低,取决于分子间作用力的大小。分子晶体分子间作用力越大物质的熔沸点越高,反之越低。(具有氢键的分子晶体,熔沸点反常地高)
如:H2O>H2Te>H2Se>H2S,C2H5OH>CH3—O—CH3。
(1)组成和结构相似的分子晶体,相对分子质量越大,分子间作用力越强,物质的熔
沸点越高。如:CH4<SiH4<GeH4<SnH4。
(2)组成和结构不相似的物质(相对分子质量相近),分子极性越大,其熔沸点就越
高。如:熔沸点CO>N2,CH3OH>CH3—CH3。
(3)在高级脂肪酸形成的油脂中,不饱和程度越大,熔沸点越低。
如:C17H35COOH硬脂酸>C17H33COOH油酸。
(4)烃、卤代烃、醇、醛、羧酸等有机物一般随着分子里碳原子数增加,熔沸点升高,如C2H6>CH4,C2H5Cl>CH3Cl,CH3COOH>HCOOH。
(5)同分异构体:链烃及其衍生物的同分异构体随着支链增多,熔沸点降低。
如:CH3(CH2)3CH3(正)>CH3CH2CH(CH3)2(异)>(CH3)4C(新)。
芳香烃的异构体有两个取代基时,熔点按对、邻、间位降低沸点按邻、间、对位降低)
【通过文字判断晶体类型】
(完整word版)四种晶体类型的比较
物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr(固)>Br2>HBr(气)。 2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
B 、离子晶体:熔、沸点的高低,取决于离子键的强弱。一般来说,离子半径越小,离子所带电荷越多,离子键就越强,熔、沸点就越高,反之越低。 例如:MgO>CaO ,NaF>NaCl>NaBr>NaI 。 KF >KCl >KBr >KI ,CaO >KCl 。 C 、金属晶体:金属晶体中金属阳离子所带电荷越多,半径越小,金属阳离子与自由电子静电作用越强,金属键越强,熔沸点越高,反之越低。如:Na <Mg <Al ,Li>Na>K 。 合金的熔沸点一般说比它各组份纯金属的熔沸点低。如铝硅合金<纯铝(或纯硅)。 D 、分子晶体:熔、沸点的高低,取决于分子间作用力的大小。分子晶体分子间作用力越大物质的熔沸点越高,反之越低。(具有氢键的分子晶体,熔沸点反常地高) 如:H 2O >H 2Te >H 2Se >H 2S ,C 2H 5OH >CH 3—O —CH 3。 (1)组成和结构相似的分子晶体,相对分子质量越大,分子间作用力越强,物质的熔沸点越高。如:CH 4<SiH 4<GeH 4<SnH 4。 (2)组成和结构不相似的物质(相对分子质量相近),分子极性越大,其熔沸点就越高。如熔沸点 CO >N 2,CH 3OH >CH 3—CH 3。 (3)在高级脂肪酸形成的油脂中,不饱和程度越大,熔沸点越低。 如:C 17H 35COOH >C 17H 33COOH ;硬脂酸 > 油酸 (4)烃、卤代烃、醇、醛、羧酸等有机物一般随着分子里碳原子数增加,熔沸 点升高,如C 2H 6>CH 4, C 2H 5Cl >CH 3Cl ,CH 3COOH >HCOOH 。 (5)同分异构体:链烃及其衍生物的同分异构体随着支链增多,熔沸点降低。如: CH 3(CH 2)3CH 3 (正)>CH 3CH 2CH(CH 3)2(异)>(CH 3)4C(新)。 芳香烃的异构体有两个取代基时,熔点按对、邻、间位降低沸点按邻、间、对位降低) 针对性训练 一、选择题 1.下列性质中,可以证明某化合物内一定存在离子键的是( ) (A )溶于水 (B )有较高的熔点 (C )水溶液能导电 (D )熔融状态能导电 2.下列物质中,含有极性键的离子化合是( ) (A )CaCl 2 (B )Na 2O 2 (C )NaOH (D )K 2S 3.Cs 是IA 族元素,F 是VIIA 族元素,估计Cs 和F 形成的化合物可能是( ) (A )离子化合物 (B )化学式为CsF 2 (C )室温为固体 (D )室温为气体 4.某物质的晶体中含A 、B 、C 三种元素,其排列方式如图所示(其中前后两面心上的B 原子未能画出),晶体中A 、B 、C 的中原子个数之比依次为( ) (A )1:3:1 (B )2:3:1 (C )2:2:1 (D )1:3:3 6.在NaCl 晶体中与每个Na +距离等同且最近的几个Cl -所围成的空间几何构型为( ) (A )正四面体 (B )正六面体 (C )正八面体 (D )正十二面体 7.如图是氯化铯晶体的晶胞(晶体中最小的重复单元),已知晶体中2个最近的Cs +离子核间距为a cm ,氯化铯的式量为M ,NA 为阿伏加德罗常数,则氯化铯晶体的密度为( ) (A )3 8a N m A ?g·cm -3 (B )A N Ma 83 g·cm -3 (C )3 a N M A ?g·cm -3 (D )A N Ma 3 g·cm -3
高中化学四种晶体类型的比较
四种晶体类型的比较
物质熔沸点高低的比较方法 物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr (固)>Br2>HBr(气)。 2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,原子半径越小,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
高中化学选修三_晶体结构与性质
晶体结构与性质 一、晶体的常识 1.晶体与非晶体 得到晶体的途径:熔融态物质凝固;凝华;溶质从溶液中析出 特性:①自范性;②各向异性(强度、导热性、光学性质等) ③固定的熔点;④能使X-射线产生衍射(区分晶体和非晶体最可靠的科学方法) 2.晶胞--描述晶体结构的基本单元.即晶体中无限重复的部分 一个晶胞平均占有的原子数=1 8×晶胞顶角上的原子数+1 4×晶胞棱上的原子+1 2×晶胞面上的粒子数+1×晶胞体心内的原子数 思考:下图依次是金属钠(Na)、金属锌(Zn)、碘(I 2)、金刚石(C)晶胞的示意图.它们分别平均含几个原子? eg :1.晶体具有各向异性。如蓝晶(Al 2O 3·SiO 2)在不同方向上的硬度不同;又如石墨与层垂直方向上的电导率和与层平行方向上的电导率之比为1:1000。晶体的各向异性主要表现在( ) ①硬度 ②导热性 ③导电性 ④光学性质 A.①③ B.②④ C.①②③ D.①②③④ 2.下列关于晶体与非晶体的说法正确的是( ) A.晶体一定比非晶体的熔点高 B.晶体一定是无色透明的固体 C.非晶体无自范性而且排列无序 D.固体SiO 2一定是晶体 3.下图是CO 2分子晶体的晶胞结构示意图.其中有多少个原子?
二、分子晶体与原子晶体 1.分子晶体--分子间以分子间作用力(范德华力、氢键)相结合的晶体 注意:a.构成分子晶体的粒子是分子 b.分子晶体中.分子内的原子间以共价键结合.相邻分子间以分子间作用力结合 ①物理性质 a.较低的熔、沸点 b.较小的硬度 c.一般都是绝缘体.熔融状态也不导电 d.“相似相溶原理”:非极性分子一般能溶于非极性溶剂.极性分子一般能溶于极性溶剂 ②典型的分子晶体 a.非金属氢化物:H 2O、H 2 S、NH 3 、CH 4 、HX等 b.酸:H 2SO 4 、HNO 3 、H 3 PO 4 等 c.部分非金属单质::X 2、O 2 、H 2 、S 8 、P 4 、C 60 d.部分非金属氧化物:CO 2、SO 2 、NO 2 、N 2 O 4 、P 4 O 6 、P 4 O 10 等 f.大多数有机物:乙醇.冰醋酸.蔗糖等 ③结构特征 a.只有范德华力--分子密堆积(每个分子周围有12个紧邻的分子) CO 2 晶体结构图 b.有分子间氢键--分子的非密堆积以冰的结构为例.可说明氢键具有方向性 ④笼状化合物--天然气水合物
四种晶体类型的比较
四种晶体类型的比较 物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr(固)>Br2>HBr(气)。 2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价
键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C —C
高中化学选修三选修物质结构与性质第三章第章常见晶体结构晶胞分析归纳整理总结
个六元环共有。每个六元环实际拥有的碳原子数为 ______个。C-C键夹角:_______。C原子的杂化方式是______ SiO2晶体中,每个Si原子与个O原子以共价键相结合,每个O原子与个Si 原子以共价键相结合,晶体中Si原子与O原子个数比为。晶体中Si原子与Si—O键数目之比为。最小环由个原子构成,即有个O,个Si,含有个Si-O键,每个Si原子被个十二元环,每个O被个十二元环共有,每个Si-O键被__个十二元环共有;所以每个十二元环实际拥有的Si原子数为_____个,O原子数为____个,Si-O键为____个。硅原子的杂化方式是______,氧原子的杂化方式是_________. 知该晶胞中实际拥有的Na+数为____个 Cl-数为______个,则次晶胞中含有_______个NaCl结构单元。 3. CaF2型晶胞中,含:___个Ca2+和____个F- Ca2+的配位数: F-的配位数: Ca2+周围有______个距离最近且相等的Ca2+ F- 周围有_______个距离最近且相等的F——。 4.如图为干冰晶胞(面心立方堆积),CO2分子在晶胞中的位置为;每个晶胞含二氧化碳分子的个数为;与每个二氧化碳分子等距离且最近的二氧化
碳分子有个。 5.如图为石墨晶体结构示意图, 每层内C原子以键与周围的个C原子结合,层间作用力为;层内最小环有 _____个C原子组成;每个C原子被个最小环所共用;每个最小环含有个C原子,个C—C键;所以C原子数和C-C键数之比是_________。C原子的杂化方式是__________. 6.冰晶体结构示意如图,冰晶体中位于中心的一个水分子 周围有______个位于四面体顶角方向的水分子,每个水分子通过 ______条氢键与四面体顶点上的水分子相连。每个氢键被_____个 水分子共有,所以平均每个水分子有______条氢键。 7.金属的简单立方堆积是_________层通过_________对 _________堆积方式形成的,晶胞如图所示:每个金属阳离子的 配位数是_____,代表物质是________________________。 8.金属的体心立方堆积是__________层通过 ________对________堆积方式形成的,晶胞如图: 每个阳离子的配位数是__________.代表物质是 _____________________。
四种晶体类型的比较
四种晶体类型的比较 GE GROUP system office room 【GEIHUA16H-GEIHUA GEIHUA8Q8-
四种晶体类型的比较
物质熔沸点高低的比较方法 物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体> >HBr(气)。 液体>气体。例如:NaBr(固)>Br 2 2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
例如:MgO>CaO ,NaF>NaCl>NaBr>NaI 。 KF >KCl >KBr >KI ,CaO >KCl 。 C 、金属晶体:金属晶体中金属阳离子所带电荷越多,半径越小,金属阳离子与自由电子静电作用越强,金属键越强,熔沸点越高,反之越低。如:Na <Mg <Al ,Li>Na>K 。 合金的熔沸点一般说比它各组份纯金属的熔沸点低。如铝硅合金<纯铝(或纯硅)。 D 、分子晶体:熔、沸点的高低,取决于分子间作用力的大小。分子晶体分子间作用力越大物质的熔沸点越高,反之越低。(具有氢键的分子晶体,熔沸点反常地高) 如:H 2O >H 2Te >H 2Se >H 2S ,C 2H 5OH >CH 3—O —CH 3。 (1)组成和结构相似的分子晶体,相对分子质量越大,分子间作用力越强,物质的熔沸点越高。如:CH 4<SiH 4<GeH 4<SnH 4。 (2)组成和结构不相似的物质(相对分子质量相近),分子极性越大,其熔沸点就越高。如熔沸点 CO >N 2,CH 3OH >CH 3—CH 3。 (3)在高级脂肪酸形成的油脂中,不饱和程度越大,熔沸点越低。 如:C 17H 35COOH >C 17H 33COOH ;硬脂酸 > 油酸
高中化学 常见晶胞模型
离子晶体 氯化钠晶体 (1)NaCl晶胞每个Na+等距离且最近的Cl-(即Na+配位数)为6个 NaCl晶胞每个Cl-等距离且最近的Na+(即Cl-配位数)为6个 (2)一个晶胞内由均摊法计算出一个晶胞内占有的Na+4_个; 占有的Cl-4个。 (3)在该晶体中每个Na+周围与之最接近且距离相等的Na+ 共有12个; 与每个Na+等距离且最近的Cl-所围成的空间几何构型为正八面体 CsCl晶体(注意:右侧小立方体为CsCl晶胞;左侧为8个晶胞) (1) CsCl晶胞中每个Cs+等距离且最近的Cl-(即Cs+配位数) 为8个 CsCl晶胞中每个Cl-等距离且最近的Cs+(即Cl-配位数) 为8个,这几个Cs+在空间构成的几何构型为正方体。 (2)在每个Cs+周围与它最近的且距离相等的Cs+有6个 这几个Cs+在空间构成的几何构型为正八面体。 (3)一个晶胞内由均摊法计算出一个晶胞内占有的Cs+ 1个;占有的Cl- 1个。 CaF 2 晶体 (1)) Ca2+立方最密堆积,F-填充在全部四面体空隙中。 (2)CaF 2 晶胞中每个Ca2+等距离且最近的F-(即Ca2+配位数) 为8个 CaF 2 晶胞中每个F-等距离且最近的Ca2+(即F-配位数)为4个 (3)一个晶胞内由均摊法计算出一个晶胞内占有的Ca2+4个; 占有的F-8个。ZnS晶体: (1)1个ZnS晶胞中,有4个S2-,有4个Zn2+。 (2)Zn2+的配位数为4个,S2-的配位数为 4个。 原子晶体 金刚石金刚石晶胞金刚石晶胞 (1)金刚石晶体 a、每个金刚石晶胞中含有8个碳原子,最小的碳环为6元环,并且不在同一平 面(实际为椅式结构),碳原子为sp3杂化,每个C以共价键跟相邻的_4_个C 结合,形成正四面体。键角109°28’ b、每个碳原子被12个六元环共用,每个共价键被6个六元环共用 c、12g金刚石中有2mol共价键,碳原子与共价键之比为 1:2
高中化学晶体结构知识汇总
1、晶体类型判别: 分子晶体:大部分有机物、几乎所有酸、大多数非金属单质、所有非金属氢化物、部分非金属氧化物。 原子晶体:仅有几种,晶体硼、晶体硅、晶体锗、金刚石、金刚砂(SiC)、氮化硅 (Si3N4)、氮化硼(BN)、二氧化硅(SiO2)、氧化铝(Al2O3)、石英等; 金属晶体:金属单质、合金; 离子晶体:含离子键的物质,多数碱、大部分盐、多数金属氧化物; 2、分子晶体、原子晶体、金属晶体、离子晶体对比表 晶体类型分子晶体原子晶体金属晶体离子晶体 定义分子通过分子间 作用力形成的晶 体 相邻原子间 通过共价键 形成的立体 网状结构的 晶体 金属原子通 过金属键形 成的晶体 阴、阳离子通 过离子键形成 的晶体 组成晶体的粒子分子原子金属阳离子 和自由电子 阳离子和 阴离子 组成晶体粒子间的相互作用范德华力或氢键共价键 金属键(没 有饱和性方 向性) 离子键(没有 饱和性方向 性) 典型实例冰(H2O)、 P4、I2、干冰 (CO2)、S8 金刚石、晶 体硅、 SiO2、SiC Na、Mg、 Al、Fe NaOH、 NaCl、K2SO4 特征熔点、 沸点 熔、沸点较低熔、沸点高 一般较高、 部分较低 熔、沸点较高导热性不良不良良好不良 导电性 差,有些溶 于水可导电 多数差良好 固态不导电, 熔化或溶于水 能导电 机械加 工性能 不良不良良好不良 硬度硬度较小高硬度 一般较高、 部分较低 略硬而脆 溶解性相似相溶不溶 不溶,但有 的反应 多数溶于水, 难溶于有机溶 剂 3、不同晶体的熔沸点由不同因素决定: 离子晶体的熔沸点主要由离子半径和离子所带电荷数(离子键强弱)决定,分子晶体的熔沸点主要由相对分子质量的大小决定,原子晶体的熔沸点主要由晶体中共价键的强弱决定,且共价键越强,熔点越高。 4、金属熔沸点高低的比较: (1)同周期金属单质,从左到右(如Na、Mg、Al)熔沸点升高。
高中化学04晶体结构学生
晶体类型与结构 知识梳理 一、晶体 1.定义: 晶体是指具有规则的几何外形的固体,它具有固定的熔点。 2.类型: 根据化学键的种类不同,我们把晶体分为_________________________ 二、离子晶体 1.定义:由_______形成的晶体是离子晶体,主要包括______________________________ 2.代表物 (1)氯化钠晶体 由图可知,在氯化钠晶体中,每个Na+周围有_____个Cl-,而每个Cl-周围也有____个Na+,它们之间通过离子键的作用结合,并在空间有规律地排列,形成规则的几何形状。 注:NaCl指的是化学式,而不是分子式,其晶体中不存在NaCl分子 (2)CsCl晶体 CsCl晶体是立方体结构,每个Cs+周围有____个Cl-与它距离相等且最近;每个Cl-周围有 ____个Cs+与它距离相等且最近;每个Cl-周围有_____个Cl-与它距离相等且最近。
【思考】构成氯化钠晶体和氯化铯晶体的微粒是什么? 3.离子晶体的构成微粒:____________________ 4.离子晶体的特点 在离子晶体中,由于阴阳离子间存在较强的离子键,所以离子晶体的结构一般比较____,密度____,且具有较_____的熔点、沸点和硬度。 【思考】如何判断某物质属于离子晶体? 三、分子晶体 1.定义 分子晶体的基本结构微粒是__________,是分子间通过___________形成的晶体。主要包括:__________________________________________________________________________________ 2.代表物 (1)干冰 干冰晶体中,二氧化碳分子分布于立方体的每个顶点和每个面心上。与每个二氧化碳分子最相邻的二氧化碳分子共有_____个。 (2)C60(富勒烯):1985年发现,荣获1996年度诺贝尔化学奖 分子中碳原子组成12个五元环和20个六元环,被称为足球烯。
四种晶体比较表
四种晶体比较表 注:离子晶体熔化时需克服离子键,原子晶体熔化时破坏了共价键,分子晶体熔化时只克服分子间作用力,而不破坏化学键。 晶体熔沸点的比较 一、看常态:1、常态:固>液>气。
2、一般情况下,原子晶体>离子晶体(金属晶体)>分子晶体。 3、原子晶体:共价键(取决于原子半径)。 4、离子晶体:离子键(取决于离子半径和离子电荷) 5、金属晶体:金属键(取决于金属原子半径和价电子数) 6、分子晶体:①结构相似,分子量越大,熔沸点越高。 ②分子量相等,正>异>新。③氢键反常 二、看类型 三、分类比较 18.请完成下列各题: (1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有种。 (2)第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为。在GaN晶体中,每个Ga原子与个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为。在四大晶体类型中,GaN属于晶体。 (3)在极性分子NCl3中,N原子的化合物为―3,Cl原子的化合价为+1,请推测NCl3水解的主要产物是(填化学式)。 19.生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。 (1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式。 (2)根据等电子原理,写出CO分子结构式。 (3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。 ①甲醇的沸点比甲醛的高,其主要原因是;甲醛分子 中碳原子轨道的杂化类型为。 ②甲醛分子的空间构型是;1mol甲醛分子中σ键的数 目为。 ③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为。
高中化学晶体结构与性质范文晶体的常识
第三章晶体结构与性质第一节晶体的常识知识归纳 一、晶体与非晶体 1.晶体与非晶体的本质差异: 2.获得晶体的三条途径 (1)______物质凝固; (2)______物质冷却不经液态直接凝固(______); (3)______从溶液中析出。 3.晶体的特点 (1)自范性 ①定义:在适宜的条件下,晶体能够自发地呈现规则的______,这称为晶体的______。非晶体物质没有这个特性。 ②形成条件:晶体______适当。 ③本质原因:晶体中粒子在______里呈现______的______排列。 (2)晶体在不同的方向上表现出不同的物理特质即______。 (3)晶体的______较固定。 (4)区分晶体和非晶体的最可靠的科学方法是对固体进行______实验。 二、晶胞 1.概念 晶胞是晶体中最小的______。 2.结构 晶胞一般都是______,晶体是由无数晶胞“______”而成。 (1)无隙:相邻晶胞之间无任何______。 (2)并置:所有晶胞都是______排列的,取向______。 (3)所有晶胞的______及内部的原子______及几何排列是完全相同的。
【答案】一、1.有周期性没有相对无序 2.(1)熔融态(2)气态凝华(3)溶质 3.(1)多面体外形性质自范性生长的速率三维空间周期性有序 (2)各向异性(3)熔点(4)X-射线衍射 二、1.结构重复单元 2.平行六面体无隙并置(1)间隙(2)平行相同(3)形状种类 知识重点 与晶体有关的计算 晶体结构的计算常常涉及如下数据:晶体密度、N A、M、晶体体积、微粒间距离、微粒半径、夹角等,密度的表达式往往是列等式的依据。解答这类题时,一要掌握晶体“均摊法”的原理,二要有扎实的立体几何知识,三要熟悉常见晶体的结构特征,并能融会贯通,举一反三。 1.“均摊法”原理 晶胞中任意位置上的一个原子如果被n个晶胞所共有,则每个晶胞对这个原子分得的份额就是1 n 。 非平行六面体形晶胞中粒子数目的计算同样可用“均摊法”,其关键仍然是确定一个粒子为几个晶胞所共 有。例如,石墨晶胞每一层内碳原子排成六边形,其顶点(1个碳原子)对六边形的贡献为1 3 ,那么一个六 边形实际有6×1 3 =2个碳原子。又如,在六棱柱晶胞(如下图所示的MgB2晶胞)中,顶点上的原子为6个 晶胞(同层3个,上层或下层3个)共有,面上的原子为2个晶胞共有,因此镁原子个数为12×1 6 +2×
高中化学选修三——晶体结构与性质
晶体结构与性质 一、晶体的常识 1.晶体与非晶体 得到晶体的途径:熔融态物质凝固;凝华;溶质从溶液中析出 特性:①自范性;②各向异性(强度、导热性、光学性质等) ③固定的熔点;④能使X-射线产生衍射(区分晶体和非晶体最可靠的科学方法) 2.晶胞--描述晶体结构的基本单元,即晶体中无限重复的部分 一个晶胞平均占有的原子数=×晶胞顶角上的原子数+×晶胞棱上的原子+×晶胞面上 的粒子数+1×晶胞体心内的原子数 思考:下图依次是金属钠(Na)、金属锌(Zn)、碘(I 2 )、金刚石(C)晶胞的示意图,它们分别平均含几个原子? eg:1.晶体具有各向异性。如蓝晶(Al 2O 3 ·SiO 2 )在不同方向上的硬度不同;又如石墨与 层垂直方向上的电导率和与层平行方向上的电导率之比为1:1000。晶体的各向异性主要表现在() ①硬度②导热性③导电性④光学性质 A.①③ B.②④ C.①②③ D.①②③④ 2.下列关于晶体与非晶体的说法正确的是() A.晶体一定比非晶体的熔点高 B.晶体一定是无色透明的固体 C.非晶体无自范性而且排列无序 D.固体SiO 2 一定是晶体 3.下图是CO 2 分子晶体的晶胞结构示意图,其中有多少个原子? 二、分子晶体与原子晶体 1.分子晶体--分子间以分子间作用力(范德华力、氢键)相结合的晶体 注意:a.构成分子晶体的粒子是分子 b.分子晶体中,分子内的原子间以共价键结合,相邻分子间以分子间作用力结合 ①物理性质 a.较低的熔、沸点 b.较小的硬度 c.一般都是绝缘体,熔融状态也不导电 d.“相似相溶原理”:非极性分子一般能溶于非极性溶剂,极性分子一般能溶于极性溶剂 ②典型的分子晶体 a.非金属氢化物:H 2O、H 2 S、NH 3 、CH 4 、HX等 b.酸:H 2SO 4 、HNO 3 、H 3 PO 4 等 c.部分非金属单质::X 2、O 2 、H 2 、S 8 、P 4 、C 60 d.部分非金属氧化物:CO 2、SO 2 、NO 2 、N 2 O 4 、P 4 O 6 、P 4 O 10 等 f.大多数有机物:乙醇,冰醋酸,蔗糖等 ③结构特征 a.只有范德华力--分子密堆积(每个分子周围有12个紧邻的分子) CO 2 晶体结构图
几种常见晶体结构分析.
几种常见晶体结构分析 河北省宣化县第一中学 栾春武 邮编 075131 栾春武:中学高级教师,张家口市中级职称评委会委员。河北省化学学会会员。市骨干教师、市优秀班主任、模范教师、优秀共产党员、劳动模范、县十佳班主任。 联系电话::: 一、氯化钠、氯化铯晶体——离子晶体 由于离子键无饱和性与方向性,所以离子晶体中无单个分子存在。阴阳离子在晶体中按一定的规则排列,使整个晶体不显电性且能量最低。离子的配位数分析如下: 离子数目的计算:在每一个结构单元(晶胞) 中,处于不同位置的微粒在该单元中所占的份额也有 所不同,一般的规律是:顶点上的微粒属于该单元中 所占的份额为18 ,棱上的微粒属于该单元中所占的份额为14,面上的微粒属于该单元中所占的份额为12 ,中心位置上(嚷里边)的微粒才完全属于该单元,即所占的份额为1。 1.氯化钠晶体中每个Na +周围有6个C l -,每个Cl -周围有6个Na +,与一个Na +距离最近且相等的 Cl -围成的空间构型为正八面体。每个N a +周围与其最近且距离相等的Na + 有12个。见图1。 晶胞中平均Cl -个数:8×18 + 6×12 = 4;晶胞中平均Na +个数:1 + 12×14 = 4 因此NaCl 的一个晶胞中含有4个NaCl (4个Na +和4个Cl -)。 2.氯化铯晶体中每个Cs +周围有8个Cl -,每个Cl -周围有8个Cs +,与 一个Cs +距离最近且相等的Cs +有6个。晶胞中平均Cs +个数:1;晶胞中平 均Cl -个数:8×18 = 1。 因此CsCl 的一个晶胞中含有1个CsCl (1个Cs +和1个Cl -)。 二、金刚石、二氧化硅——原子晶体 1.金刚石是一种正四面体的空间网状结构。每个C 原子以共价键与4 个C 原子紧邻,因而整个晶体中无单个分子存在。由共价键构成的最小 环结构中有6个碳原子,不在同一个平面上,每个C 原子被12个六元环 共用,每C —C 键共6个环,因此六元环中的平均C 原子数为6× 112 = 12 ,平均C —C 键数为6×16 = 1。 C 原子数: C —C 键键数 = 1:2; C 原子数: 六元环数 = 1:2。 2.二氧化硅晶体结构与金刚石相似,C 被Si 代替,C 与C 之间插氧,即为SiO 2晶体,则SiO 2晶体中最小环为12环(6个Si ,6个O ), 最小环的平均Si 原子个数:6×112 = 12;平均O 原子个数:6×16 = 1。 即Si : O = 1 : 2,用SiO 2表示。 在SiO 2晶体中每个Si 原子周围有4个氧原子,同时每个氧原子结合2个硅原子。一个Si 原子可形 图 1 图 2 NaCl 晶体 图3 CsCl 晶体 图4 金刚石晶体
。高中化学晶体的结构与性质知识点及相关例题讲解
高中化学晶体的结构与性质知识点及相关例题 讲解 自然界中的固体可以分为两种存在形式:晶体和非 晶体。晶体是经过结晶过程而形成的具有规则的几何外形的 固体。晶体中原子或分子在空间按一定规律周期性重复的排 列,从而使晶体内部各个部分的宏观性质是相同的,而且具 有固定的熔点和规则的几何外形。 一、晶体 固体可以分为两种存在形式:晶体和非晶体。 晶体的分布非常广泛,自然界的固体物质中,绝大多数 是晶体。气体、液体和非晶体在一定条件下也可转变为晶体。 晶体是经过结晶过程而形成的具有规则的几何外形的 固体。晶体中原子或分子在空间按一定规律周期性重复的排 列,从而使晶体内部各个部分的宏观性质是相同的,而且具 有固定的熔点和规则的几何外形。 二、晶体结构 1.几种晶体的结构、性质比较 2.几种典型的晶体结构: (1)NaCl晶体(如图1):每个Na+周围有6个Cl-,每个Cl-周围有6个Na+,离子个数比为1:1。 (2)CsCl晶体(如图2):每个Cl-周围有8个Cs+,每个Cs+周围有8个Cl-;距离Cs+最近的且距离相等的Cs+
有6个,距离每个Cl-最近的且距离相等的Cl-也有6个,Cs+和Cl-的离子个数比为1:1。 (3)金刚石(如图3):每个碳原子都被相邻的四个碳原子包围,以共价键结合成为正四面体结构并向空间发展, 键角都是109o28',最小的碳环上有六个碳原子。 (4)石墨(如图4、5):层状结构,每一层内,碳原子以正六边形排列成平面的网状结构,每个正六边形平均拥有 两个碳原子。片层间存在范德华力,是混合型晶体。熔点比 金刚石高。 (5)干冰(如图6):分子晶体,每个CO2分子周围紧邻其他12个CO2分子。
四种晶体类型的比较
创作编号: GB8878185555334563BT9125XW 创作者:凤呜大王* 物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr(固)>Br2>HBr(气)。
2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
高中化学-晶体结构【教师版】
比较两种化学键,完成下列表格: 天然的美丽晶体 多数天然珠宝是在特定的地质作用和物理化学条件下,化学元素相互结合的产物。珠宝的特征,从根本上说决定于构成元素本身的性质。组成珠宝的常见元素有30多种,而多数宝石主要由其中8种元素组成,其他元素主要呈微量组分存在。微量成分对珠宝而言十分重要,它们可能在很大程度上决定着珠宝的价值,多数珠宝的颜色成因主要归结于以微量成分存在的过渡金属元素Sr,Ti,V,Cr,Fe,Co,Ni,Cu等。如翡翠、祖母绿等均因为含微量的Cr元素,使宝石呈艳丽的绿色而价值连城。有时微量元素还决定于珠宝的品种。如:刚玉中若含微量Cr元素而显红色,即为红宝石; 若含Fe, Ti等微量元素将显蓝色等,即为蓝宝石 类型成键微粒成键的本质存在的物质表示方法键强弱判断离子键阴、阳离子静电作用离子化合物电子式半径和电荷数 共价键 非极性 键 同种非金属原子 共用电子对 离子化合物 共价单质 共价化合物 电子式、结构式 半径和共用电子对数 离子化合物 共价化合物 极性键 不同种非金属原 子 晶体结构 知识温习 每识每课
一、晶体 1.定义:晶体是指具有规则的几何外形的固体,晶体具有固定的熔点,晶体中的微粒按一定的规则排列。 2.类型:根据化学键的种类不同,我们把晶体分为_______、_______、______和______。 【答案】离子晶体、原子晶体、分子晶体和金属晶体。 二、离子晶体 1.定义:由__________________形成的晶体是离子晶体,主要包括_____________________,如:CaO、KOH、NaCl、Mg(NO3)2、NH4Cl; 2.离子晶体的构成微粒:____________________; 【答案】阴阳离子通过离子键;强碱、金属氧化物及绝大部分的盐;阳离子和阴离子 3.离子晶体的特点: 在离子晶体中,由于阴阳离子间存在较强的离子键,所以离子晶体的结构一般比较________,密度__________,且具有较___________的熔点、沸点和硬度。 离子晶体在水溶液或者熔融状态下均导电;离子晶体中不存在单个分子。 【答案】稳定、较大、高 4.代表物 (1)氯化钠晶体 由图可知,在氯化钠晶体中,每个Na+周围有_____个Cl-,而每个Cl-周围也有____个Na+,它们之间通过离子键的作用结合,并在空间有规律地排列,形成规则的几何形状。 【答案】6、6 注:NaCl指的是化学式,而不是分子式,其晶体中不存在NaCl分子 【思考】构成氯化钠晶体和氯化铯晶体的微粒是什么? 【答案】氯化钠:钠离子和氯离子氯化铯:铯离子和氯离子 新知精讲
晶体类型的判断与比较怎样比较熔点的高低
晶体类型的判断与比较,晶体结构的计算,怎样比较熔点的高低, 8晶体类型的判断与比较 1、判断晶体类型的方法 (1)依据物质的分类判断 金属氧化物(如K2O、Na2O2等),强碱(如NaCl、KOH等)和绝大多数的盐类是离子晶体。大多数非金属单质(除金刚石、石墨、晶体硅、晶体硼外)、气态氢化物、非金属氧化物(除SiO2外)、酸、绝大多数有机物(除有机盐外)是分子晶体。常见的原子晶体单质有金刚石、石墨、晶体硅、晶体硼等;常见的原子晶体化合物有碳化硅、二氧化硅等。金属单质(除汞外)与合金都是金属晶体。 (2)依据物质的性质判断 离子晶体的熔点较高,常在数百至1000余度;原子晶体熔点高,常在100 0度至几千度;分子晶体熔点低,常在数百度以下至很低温度;金属晶体多数熔点高,但也有相当低的。 离子晶体水溶液及熔化时能导电,晶体不导电;原子晶体一般为非导体,但石墨等导电;分子晶体为非导体,而分子晶体中的电解质(主要是酸和非金属氢化物)溶于水,使分子内的化学键断裂形成自由移动的离子也能导电,但熔化不导电,金属晶体是良导体。 2、晶体中的几个不一定 (1)离子晶体除含离子键外不一定不含其他化学键。如氨盐中除含离子键,还含极性键和配位键;Na2O2中除含离子键还含非极性键。
(2)离子晶体不一定肯定含金属阳离子,如NH4Cl中含的阳离子是NH4+(凡是氨盐、肯定同时含离子键、极性键和配位键)。 (3)离子晶体的熔点不一定肯定低于原子晶体,如MgO的熔点高于SiO2。(4)含有阳离子的晶体不一定是离子晶体,如金属晶体中就含有金属阳离子。 (5)金属和非金属形成的晶体不一定都是离子晶体,如AlCl3就是含共价键的分子晶体 (6)具有金属光泽且能导电的单质不一定就是金属,如石墨具有金属光泽且能导电,却是非金属。 3、四类晶体的比较:
