氨基酸测定方法

4.1 光度分析法[5] [6]
β-氨基丙酸和茚三酮溶液在弱酸的条件下可以生成蓝紫色物质[7],其颜色深浅主要与β-氨基丙酸的浓度有关。因此可利用此显色反应采用比色法定量测量β-氨基丙酸。我在实验中发现很多因素如浓度、pH 值、反应温度、以及反应时间等对此显色反应有很大的影响。如忽视这些因素会使实验产生很大的误差。就此显色反应的最佳条件我做了初步的探究。
4.1.1试剂的配制:
缓冲液的配制:配制pH= 6.00的NaAc -HAc 缓冲溶液
β-氨基丙酸标准溶液的配制:
用电子天平准确称取1.020 g β-氨基丙酸(生化纯),溶于250ml pH=6.00缓冲溶液中,得到C = 4.080 g/L 标准溶液。
茚三酮试剂的配制:称取0.5g 茚三酮溶于100ml 蒸馏水中,得到5g/L 的茚三酮水溶液。
4.1.2标准曲线的确定
分别准确移取0.30ml 、0.40ml 、0.50ml 、0.60ml 、0.70ml 、0.80ml 、0.90ml 、1.00ml 标准液于8个比色管中,用pH=6.00的缓冲溶液稀释到5.00ml 再加入1ml 茚三酮水溶液充分摇匀,将其放在沸水浴中加热10min 。冷却到室温,用7230型分光光度计在569nm 下测其吸光度。以吸光度和浓度作一个标准曲线。
4.1.3样品的测定
稀释待测液于0.24mg/ml —0.73mg/ml,调pH 值到6.00,以相同的反应条件,测其吸光值并与上面的标准曲线对照查出稀释液的浓度,再乘以稀释倍数即为β-氨基丙酸的浓度。
4.1.4 标准曲线的测定结果
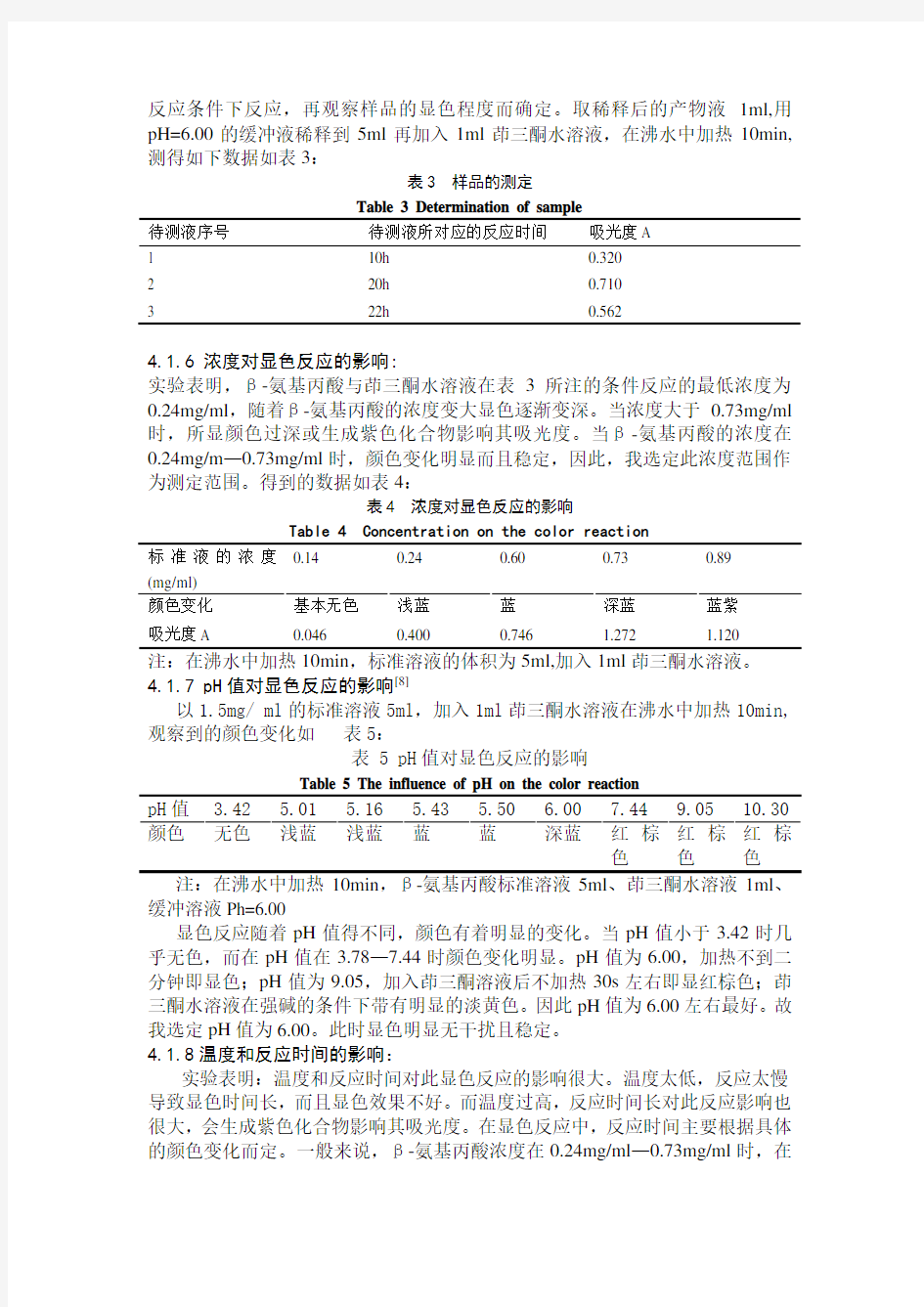
β-氨基丙酸浓度在0.24mg/ml —0.73mg/ml 范围内与茚三酮水溶液反应,颜色表现出由浅蓝到深蓝的递增变化。用茚三酮比色法测得的一组数据得到的标准曲线如图1:
0.20.30.40.50.60.70.80.9 1.0 1.1
0.4
0.6
0.8
1.0
1.2
1.4
吸光度加入标液体积(ml) B
图 1 标准曲线的测定
Fig 1 Determination of the standard curve
注:在沸水中加热10min ,β-氨基丙酸标准溶液5ml 、茚三酮水溶液1ml 、缓冲溶液pH=6.00
4.1.5样品的测定分析
将待测的一批稀释50倍,母液稀释的程度可以根据以与标准溶液在相同的
反应条件下反应,再观察样品的显色程度而确定。取稀释后的产物液1ml,用pH=6.00的缓冲液稀释到5ml再加入1ml茚三酮水溶液,在沸水中加热10min,测得如下数据如表3:
表3 样品的测定
Table 3 Determination of sample
待测液序号待测液所对应的反应时间吸光度A
1 10h 0.320
2 20h 0.710
3 22h 0.562
4.1.6 浓度对显色反应的影响:
实验表明,β-氨基丙酸与茚三酮水溶液在表3所注的条件反应的最低浓度为0.24mg/ml,随着β-氨基丙酸的浓度变大显色逐渐变深。当浓度大于0.73mg/ml 时,所显颜色过深或生成紫色化合物影响其吸光度。当β-氨基丙酸的浓度在0.24mg/m—0.73mg/ml时,颜色变化明显而且稳定,因此,我选定此浓度范围作为测定范围。得到的数据如表4:
表4 浓度对显色反应的影响
Table 4 Concentration on the color reaction
标准液的浓度
(mg/ml)
0.14 0.24 0.60 0.73 0.89
颜色变化基本无色浅蓝蓝深蓝蓝紫
吸光度A 0.046 0.400 0.746 1.272 1.120
注:在沸水中加热10min,标准溶液的体积为5ml,加入1ml茚三酮水溶液。
4.1.7 pH值对显色反应的影响[8]
以1.5mg/ ml的标准溶液5ml,加入1ml茚三酮水溶液在沸水中加热10min,观察到的颜色变化如表5:
表 5 pH值对显色反应的影响
Table 5 The influence of pH on the color reaction
pH值 3.42 5.01 5.16 5.43 5.50 6.00 7.44 9.05 10.30
颜色无色浅蓝浅蓝蓝蓝深蓝红棕
色红棕
色
红棕
色
注:在沸水中加热10min,β-氨基丙酸标准溶液5ml、茚三酮水溶液1ml、缓冲溶液Ph=6.00
显色反应随着pH值得不同,颜色有着明显的变化。当pH值小于3.42时几乎无色,而在pH值在3.78—7.44时颜色变化明显。pH值为6.00,加热不到二分钟即显色;pH值为9.05,加入茚三酮溶液后不加热30s左右即显红棕色;茚三酮水溶液在强碱的条件下带有明显的淡黄色。因此pH值为6.00左右最好。故我选定pH值为6.00。此时显色明显无干扰且稳定。
4.1.8温度和反应时间的影响:
实验表明:温度和反应时间对此显色反应的影响很大。温度太低,反应太慢导致显色时间长,而且显色效果不好。而温度过高,反应时间长对此反应影响也很大,会生成紫色化合物影响其吸光度。在显色反应中,反应时间主要根据具体的颜色变化而定。一般来说,β-氨基丙酸浓度在0.24mg/ml—0.73mg/ml时,在
沸水中加热10min即可,时间太短,反映不完全颜色梯度不明显。时间过长,溶液挥发严重也影响其吸光度。故我把反应时间定在10min左右。
4.1.9其他因素的影响
不同溶剂的茚三酮溶液对显色反应也有一些影响。为了区别它们对显色反应的影响,我做了如下实验:分别称取0.2002g茚三酮三份,分别溶于乙醇、水、丙酮各100ml中,可以观察到:丙酮溶解茚三酮的速度最快,乙醇次之。移取β-氨基丙酸标准溶液(4.080g/l)1ml三份,用pH值为6.00的NaAc-HAc缓冲溶液稀释到5ml再依次加入1ml茚三酮水溶液、乙醇溶液以及丙酮溶液,在沸水中加热。实验表明:在加热2min时,乙醇溶液开始显色;丙酮溶液的显红棕色;水溶液无色。在加热6min时,丙酮溶液的颜色加深;水溶液显浅蓝色;乙醇溶液的所显颜色最深。
乙醇易挥发,在加热的条件下挥发更严重。基于这一点的考虑,我采用茚三酮水溶液。而茚三酮的用量对此显色反应的影响不大,可以选择5ml的被测液与1ml(5g/l)的茚三酮水溶液反应。测定时,最好选择标样与待测液在同一水浴。这样可以减少误差提高测定的准确度。
另外,当被测液中含有其他的氨基酸或是含氨基的化合物也可以与茚三酮发生显色反应,影响测定结果。总之,茚三酮比色法作为一种β-氨基丙酸的定量检测方法具有操作简单、成本低的优点。只要控制好反应条件就能得到较好的测量结果。
三.茚三酮比色法:
1原理:氨基酸在一定pH范围内,能与茚三酮生成兰紫色化合物。可以用比色法定量测定。
2试剂:
(1)磷酸缓冲液(pH.8.04)制备方法如下:
称磷酸二氢钾4.5350g。定容500ml
称NAH2PO4·12H2O 11.9380g分别溶解定容500ml
取磷酸二氢钾10ml与磷酸氢二钠190ml混合即为pH8.04的缓冲液
(2)2%茚三酮溶液:
称茚三酮1g→溶于35ml热水→加入40mg氯化亚锡(SnCl2·H2O)搅拌过滤(作防腐剂)→于冷暗处过夜→定容50ml
①氨基酸标液
称干燥氨基酸(如异亮氨酸)0.2000g→溶解定容100ml→摇匀→吸10ml于另外100ml容量瓶定容100ml,即得200Ug/ml标液
3操作方法:
(1)绘制标准曲线:
取7个25ml容量瓶,吸取标液 0 0.5 1.0 1.5 2.0 2.5 3.0ml于7个25ml容量瓶,加水补充
至容积为4ml,然后加茚三酮和缓冲液各1ml,于水浴加热15分钟,冷却后定容25ml,静置
15分钟,在570nm下测消光值,绘制标准曲线。
(2)样品测定:
取样品5.00~10.0g(液体样5-10ml)→于烧杯中→加50ml水和活性碳约5 g→加热过滤→用
30—40ml热水洗涤活性炭→吸澄清样液1~4ml→加茚三酮和缓冲液各1ml 水浴加热15分钟,
冷却定容,静置15分钟于570nm下测定消光值,按下式计算氨基酸含量。氨基酸含量(毫克/100克)=C/(W×1000)×100
C——从标准曲线上查得得氨基酸的量(Ug)
W——测定得样品溶液相当于样品的量(g)
注意事项:
茚三酮受阳光、温度、湿度、空气等影响易被氧化呈淡红或深红色,使用前要进行纯化,方法如下:
取10g茚三酮容于40ml热水中,加一克活性炭,摇匀静置30分钟,过滤,将滤液放入冰箱中过滤,即出现兰色结晶,过滤,用2ml冷水洗涤结晶,置干燥皿中干燥,装瓶备用。
茚三酮显色法测定氨基酸含量
一、目的
学习茚三酮显色法测定氨基酸含量的方法
二、原理
茚三酮溶液与氨基酸共热,生成氨。氨与茚三酮和还原性茚三酮反应,生成紫色化合物。该化合物颜色的深浅与氨基酸的含量成正比,可通过测定570nm 处的光密度,测定氨基酸的含量。
三、试剂与材料
(1)标准氨基酸溶液:配制成0.3mmol/L 溶液。
(2)pH5.4,2mol/L 醋酸缓冲液:量取86mL 2mol/L 醋酸钠溶液,加入14m L 2mol/L 乙酸混合而成。用pH 检查校正。
(3)茚三酮显色液:称取85mg 茚三酮和15mg 还原茚三酮,用10mL 乙二醇甲醚溶解。
茚三酮若变为微红色,则需按下法重结晶:称取5g 茚三酮溶于15~25mL 热蒸馏水中,加入0.25g 活性炭,轻轻搅拌。加热30min 后趁热过滤,滤液放入冰箱过夜。次日析出黄白色结晶,抽滤,用1mL 冷水洗涤结晶,置干燥器干燥后,装入棕色玻璃瓶保存。
还原型茚三酮按下法制备:称取5g 茚三酮,用125mL 沸蒸馏水溶解,得黄色溶液。将5g 维生素C 用250mL 温蒸馏水溶解,一边搅拌一边将维生素C 溶液滴加到茚三酮溶液中,不断出现沉淀。滴定后继续搅拌15min ,然后在冰箱内冷却到4℃,过滤、沉淀用冷水洗涤3次,置五氧化二磷真空干燥器中干燥保存,备用。
乙二醇甲醚若放置太久,需用下法除去过氧化物:在500mL 乙二醇甲醚中加入5g 硫酸亚铁,振荡1~2h ,过滤除去硫酸亚铁,再经蒸馏,收集沸点为121~125℃的馏分,为无色透明的乙二醇甲醚。
(4)60%乙醇。
(5)样品液:每毫升含0.5~50μg 氨基酸。
(6)分光光度计。
(7)水浴锅。
四、操作步骤
1.标准曲线的制作
分别取0.3mmol/L 的标准氨基酸溶液0,0.2,0.4,0.6,0.8,1.0mL 于试管中,用水补足至1mL 。各加入1mL pH5.4,2mol/L 醋酸缓冲液;再加入1mL 茚三酮显色液,充分混匀后,盖住试管口,在100℃水浴中加热15min ,用自来水冷却。放置5min 后,加入3mL 60%乙醇稀释,充分摇匀,用分光光度计测定O D 570nm 。(脯氨酸和羟脯氨酸与茚三酮反应呈黄色,应测定OD 440nm )。
以OD 570nm 为纵坐标,氨基酸含量为横坐标,绘制标准曲线。
2.氨基酸样品的测定
取样品液1mL ,加入pH5.4,2mol/L 醋酸缓冲液1mL 和茚三酮显色液1mL ,混匀后于100℃沸水浴中加热15min ,自来水冷却。放置5min 后,加3mL 60%乙醇稀释,摇匀后测定OD 570nm (生成的颜色在60min 内稳定)。
将样品测定的OD 570nm 与标准曲线对照,可确定样品中氨基酸含量。
五、 结果计算
氨基酸含量(mmol/L )=
OD 570nm 对应标准曲线查得
值 1 000
石斛中多糖含量的测定
题目石斛中多糖含量的测定 学生姓名高换楼学号1111034082所在学院化学与环境科学学院 专业班级化工1102班 指导教师季晓晖 完成地点陕西理工学院 2015 年 06 月 08 日
石斛中多糖含量的测定 高换楼 (陕西理工学院化学与环境科学学院化工专业1102班,陕西汉中723001) 季晓晖 [摘要] 石斛为我国常用贵重药材,有养阴清热、益胃生津的功效,石斛一直备受国内外研究者的重视。本文利用蒽酮-硫酸法对铁皮石斛多糖的含量进行了测定,并采用正交试验得到最佳实验方案,在石斛粉碎程度为粉末、液料比为50mL/g、提取2次,每次3小时的情况下多糖提取率最高。本文的实验结果为今后铁皮石斛多糖提取的质量评价及其进一步开发和利用提供参考依据。 [关键词] 石斛;多糖;蒽酮-硫酸法;抗氧化性;测定; Determination of Dendrobium polysaccharide content GAO Huanlou (Grade 02, Class 11, Major chemical engineering, School of chemical and environmental science Dept, Shaanxi University of Technology, Hanzhong 72300x, Shaanxi) Tutor: JI Xiaohui Abstract: Dendrobium is in common use in our country precious medicinal herbs, the effect of nourishing yin and clearing heat, nourishing stomach fluid, Dendrobium has attracted a lot of attention of researchers at home and abroad. The anthrone-sulfuric acid method of Dendrobium officinale polysaccharide content were measured, and using the orthogonal test and the optimum solution is obtained. In Dendrobium degree of comminution is in the form of powder, liquid to solid ratio for 50mL/1g, extraction 2 times, every time 3 hours of polysaccharides extraction rate was the highest. The experimental results for the quality evaluation of future Dendrobium officinale polysaccharide extraction and its further development and utilization to provide reference. Key words: Dendrobium; polysaccharide; anthrone-sulfuric acid method; antioxidation; determination;
氨基酸自动分析仪
氨基酸自动分析仪 1.实验目的 ①了解氨基酸自动分析仪的分析原理; ②掌握氨基酸自动分析仪的操作技巧。 2.实验原理 测定原理是利用样品各种氨基酸组分的结构不同、酸碱性、极性及分子大小不同,在阳离子交换柱上将它们分离,采用不同pH值离子浓度的缓冲液将各氨基酸组分依次洗脱下来,再逐个以另一流路的茚酮试剂混合,然后共同流至螺旋反应管中,于一定温度下(通常为115~120℃)进行显色反应,形成在570nm有最大吸收的蓝紫色产物。其中的羟脯氨酸与茚三酮反应生成黄色产物,其最大吸收在440nm。这些有色产物对570nm、440nm光的吸收强度与洗脱出来的各氨基酸的浓度(或含量)之间的关系符合比耳定律,可与标准氨基酸比较作定性和定量测定。 3.实验仪器与耗材 实验仪器: 耗材: 4.实验步骤 ①样品处理: 测定样品中各种游离氨基酸含量,可以除去脂肪杂质后,直接上柱进行分析。 测定蛋白质的氨基酸组成时样品必须经酸水解,使蛋白质完全变成氨基酸后才上柱进行分析。 ②样品分析:经过处理后的样品上柱进行分析。上柱的样品量根据所用自动分析仪的灵 敏度来确定。一般为每种氨基酸0.1μmol 左右(水解样品干重为0.3mg 左右)。测定必须在pH5~5.5、100℃下进行,反应进行时间为10~15min,生成的紫色物质在570nm 波长下进行比色测定。而生成的黄色化合物在440nm 波长下进行比色测定。做一个氨基酸全分析
实验 一游离氨基酸测定
实验一:游离氨基酸测定 实验学时:3学时 实验类型:验证 实验要求:必修 一、实验目的 1、掌握甲醛法测定游离氨基酸的测定原理和方法。 二、实验内容 使用甲醛滴定法测定游离氨基酸 三、实验原理 氨基酸中的NH2基的pK值常在9.0以上,不能和NaOH标准溶液直接滴定,需使这些含氮化合物(包括有机含氮化合物)都转化为氨态氮,然后进行测定。但可以用甲醛法测量。在pH中性和常温条件下,甲醛迅速与氨基酸中的 -氨基相互作用,使滴定终点移至pH值9.0左右,可以用酚酞批示剂,以NaOH标准溶液来滴定NH3+基上的H+,每释放一个氢离子,就相当于有一个氨基氮 R-NH3+→H++R-NH2 R-NH2+2HCHO→R-N(CH2H)2 4 NH4+ + 6 HCHO == (CH2)6N4H+ + 3 H+ + 6 H2O 滴定的结果表示游离a—氨基的含量,其精确度可达理论量的90%。如果样品中只某一种已知的氨基酸,从甲醛法结果可求得该氨基酸的含量。如果样品中是多种氨基酸的混合物(如蛋白水解液),则测定结果不能作为氨基酸的定量依据。一般常用此法测定蛋白质水解程度,随着水解程度的增加滴定值增加,当水解完全后,滴定值即保持恒定。甲醛滴定法采用的甲醛浓度为2.0-3.0mol/L,即滴定后最终浓度为6 %-9 %。 四、实验组织运行要求 集中授课形式 五、实验条件 1.试剂 (1)40%中性甲醛溶液: 在50mL 36 % ~ 37 %甲醛中加入5滴5g/L酚酞乙醇溶液,然后 用0.2mol/L NaOH溶液滴定到微红(使用前需重新中和) (2)酚酞指示剂: 5g/L酚酞的50%乙醇溶液 (3)0.01mol/L氢氧化钠标准溶液 (4)10%(体积分数)乙酸溶液 2.玻璃仪器 ⑴50ml容量瓶 ⑵20ml移液管 ⑶碱式滴定管 ⑷50ml量杯 ⑸250ml三角瓶 六、实验步骤 (1)样品处理称取试样0.2g(准确至1mg),置入研钵中,加5ml 10%乙酸溶液研磨至均匀,用水转移到50mL容量瓶中并定容至刻度,摇匀、过滤(弃去最初部份溶液)。 (2)样品滴定在三角瓶中加入2mL样品滤液,加水4mL,3滴酚酞指示剂,摇匀后用0.01mol/L NaOH标准溶液滴定到微红色。然后加入2mL中性甲醛溶液,摇匀,放置片刻,再用0.01mol/L NaOH标准溶液滴定回到微红色中点,记下甲醛加入后样品消耗NaOH标准溶液的体积。同样,取6mL水按以上操作做空白实验。 七、计算
几种市售枫斗的多糖含量测定
几种市售枫斗的多糖含量测定 .烈斗 浙江省医学科学琏1999年9月(邑弟39期 , 多 .j 几种市售枫斗的多糖含 药帕研究所(3l0013)兰李亚芳 中药枫斗是以石斛属多种植物的茎经过 特殊加工制成的干燥品,亦称耳环石斛.传统 认为质重,嚼之粘牙,无渣者为优,老药工凭 此来判断枫斗的优劣,但无内在的质量评价 标准.近年来,石斛多糖的研究引起人们的重 视,并证明石斛多糖是评价枫斗的重要生理 活性物质之一ll.J.我们于l997年2月~ l999年6月采用苯酚一硫酸比色法,测定r 几种市售枫斗的多糖含量. 一 ,材料与方法 ∈一)材料: 1.样品:铁皮枫斗1(福建),铁皮枫斗2 (福建),枫斗1(云南),枫斗2(云南),小环叉 直条枫斗(云南),野生枫斗(云南),野生紫皮 扭斗(云南),儿洲牌铁皮枫斗(广西): 2仪器:7230型分光光度计(上海分析 仪器厂)
3试剂:苯酚试剂:苯酚(分析纯)l0 加水l50g混匀,溶解即得,置淙色瓶内,冰箱'巾备用;其它试剂(无水乙醇,硫酸等)均为国产分析纯 (二)方法: 多糖的提取与含量测定,参照文献方法i 二,结果 (一)葡萄糖标准液吸光度测定结果:标 准品浓度在495,9.90,1485,1980,2475 297O,3465,396O时,吸光度分别为o069, O135,0203,0287,0366,0428,0500 0.587,以吸光度A为纵坐标,浓度c为横坐标,绘制标准曲线,得回归方程: A=一0010536+0.Ol4923C.r= 25 量测定 z,7/ 丁委静张治国户.f 09994 (二)换算因素 塑重量—— 多糖液葡萄糖浓度(g/m])×多糖稀释因素结果:f为1504. (三)几种市售枫斗多糖含量见表1. 表1几种枫斗的多糖含量 三,讨论 ()结果表明,不同种石斛加工成的枫 斗.多糖含差别很大,已测的几个样品中多糖含最高低相差约4倍
氨基酸含量测定
茚三酮比色测定氨基酸含量 一、实验原理 氨基酸在碱性溶液中能与茚三酮作用,生成蓝紫色或黄色化合物(除脯氨酸外均有此反应),可用吸光光度法测定。生成的蓝紫色或黄色化合物颜色深浅与氨基酸含量成正比,其最大吸收波长分别为570nm或350nm,故据此可以测定样品中氨基酸含量。 二、实验试剂 (1)1.2%茚三酮溶液:称取茚三酮1g于盛有35mL热水的烧杯中使其溶解,加入40mg氯化亚锡(SnCl2?H2O),搅拌过滤(作防腐剂)。滤液置冷暗处过夜,加水至50mL,摇匀备用。 (2)pH 8.04磷酸缓冲液: Ⅰ、准确称取磷酸二氢钾(KH2PO4)4.5350g于烧杯中,用少量蒸馏水溶解后,定量转入500mL容量瓶中,用水稀释至标线,摇匀备用。 Ⅱ、准确称取磷酸氢二钠(Na2HPO4)11.9380g于烧杯中,用少量蒸馏水溶解后,定量转入500mL容量瓶中,用水稀释到标线,摇匀备用。 Ⅲ、取上述配好的磷酸二氢钾溶液10.0mL与190mL磷酸氢二钠溶液混合均匀即为pH8.04的磷酸缓冲溶液。 (3)氨基酸标准溶液:准确称取干燥的氨基酸(如异亮氨酸)0.2000g于烧杯中,先用少量水溶解后,定量转入100mL容量瓶中,用水稀释到标线,摇匀,准确吸取此液10.0mL于100mL容量瓶中,加水到标线,摇匀,此为200μg/mL 氨基酸标准溶液。 三、实验方法及步骤 (1)标准曲线绘制 准确吸取200μg/mL的氨基酸标准溶液0.0、0.5、1.0、1.5、2.0、2.5、3.0mL (相当于0、100、200、300、400、500、600μg 氨基酸),分别置于25mL 容量瓶或比色管中,各加水补充至容积为 4.0mL,然后加入茚三酮溶液(20g/L)和磷酸盐缓冲溶液(pH为8.04)各1mL,混合均匀,于90℃水浴上加热至显色恒定为止(该加热过程至少需要25分钟),取出迅速冷至室温,加水至标线,摇匀。静置15min后,若生成蓝紫色化合物,在570nm波长下,以试剂空白为
齿瓣石斛多糖含量测定比较
齿瓣石斛多糖含量测定比较 石斛是中国名贵中药材,多糖是石斛的主要有效成分之一。本文测定了不同产地,种植方式以及不同部位的齿瓣石斛多糖含量,对齿瓣石斛栽培应用有重要意义。 标签:齿瓣石斛多糖;含量测定;比较 石斛属(Dendrobium)是兰科第二大属,全球约有1500种,主要集中分布在我国华南和西南地区[1]。石斛为我国名贵中药,具有滋阴清热、益胃生津等功效。齿瓣石斛化学成分类型多样,其中糖类也是重要化学成分,广西的加工品一级枫斗含量高达45.89%[2]。本文对不同齿瓣石斛多糖含量进行测定比较。 1仪器和试药 1.1仪器UV-2450紫外分光光度计(日本岛津);电子天平;分析天平(FA200413)。 1.2试药对照品:D-无水葡萄糖(中国食品药品检定研究院,批号:110833-201205)。 1.3试剂双蒸水:自制;无水乙醇,95%乙醇,苯酚。 1.4药材见表1。 2实验方法 2.1紫外可见分光光度法测定石斛多糖含量[3]。 2.1.1对照品溶液的配置取D-无水葡萄糖对照品适量,精密称定,加水制成每1 ml含94.66ug的溶液,即得。 2.1.2供试品溶液的制备取石斛鲜品茎约60 g,精密称定,置于九阳豆浆机中,选择五谷模式榨汁,加水定容至1000ml,混匀,离心(转速为4000转/min)20min,上清液稀释8倍,精密量取2ml置10ml塑料离心管中,精密加入无水乙醇10ml,摇匀,冷藏1 h,离心,弃上清,加80%乙醇洗涤2次,每次8ml,离心,弃上清,沉淀用热水溶解,转移至25ml容量瓶中,放冷,加水至刻度,摇匀,即得。 2.1.3标准曲线的绘制精密量取对照品溶液0、0.1、0.2、0.4、0.6、0.8、1.0ml,分别置10 mL具塞棕色试管中,加水补至1.0 ml,加5%苯酚溶液(临用时配)1.0 ml,摇匀,迅速加入浓硫酸5.0mL,置沸水浴加热20min,取出,立即置冰水浴中冷却5 min后取出,以相应试剂为空白,照紫外-可见分光光度法在488nm
BLAST_核酸氨基酸序列相似性比较
BLAST 核酸/氨基酸序列相似性比较 Blast (Basic Local Alignment Search Tool)是一套在蛋白质数据库或DNA数据库中进行相似性比较的分析工具。BLAST程序能迅速与公开数据库进行相似性序列比较。BLA ST结果中的得分是对一种对相似性的统计说明。 BLAST 采用一种局部的算法获得两个序列中具有相似性的序列。如果您想进一步了解BLAST算法,您可以参考NCBI的BLAST Course ,该页有BLAST算法的介绍。 BLAST的功能 BLAST对一条或多条序列(可以是任何形式的序列)在一个或多个核酸或蛋白序列库中进行比对。BLAST还能发现具有缺口的能比对上的序列。 BLAST是基于Altschul等人在J.Mol.Biol上发表的方法(J.Mol.Biol.215:403-410(19 90)),在序列数据库中对查询序列进行同源性比对工作。从最初的BLAST发展到现在NC BI提供的BLAST2.0,已将有缺口的比对序列也考虑在内了。BLAST可处理任何数量的序列,包括蛋白序列和核算序列;也可选择多个数据库但数据库必须是同一类型的,即要 么都是蛋白数据库要么都是核酸数据库。 所查询的序列和调用的数据库则可以是任何形式的组合,既可以是核酸序列到蛋白库中作查询,也可以是蛋白序列到蛋白库中作查询,反之亦然。 通常根据查询序列的类型(蛋白或核酸)来决定选用何种BLAST。假如是作核酸-核酸查询,有两种BLAST供选择,通常默认为BLASTN。如要用TBLASTX也可,但记住此时不考虑缺口。 BLAST适用于本地查询。可以下载公共数据库,对于该数据库的更新和维护是必不可少的。如果要直接到网上查询也可以(即NetBlast),但记住如果你认为自己的序列很有价值的话,还是谨慎为宜。 如何访问在线的BLAST功能服务? 您只要通过浏览器访问Blast主页(https://www.360docs.net/doc/0d13935.html,/) 。所有的查询和分析都通过浏览器来完成,就象您在您的本地机上一样方便和快捷。 BLAST 采用一种局部的算法获得两个序列中具有相似性的序列。 Blast中常用的程序介绍: 1、BLASTP是蛋白序列到蛋白库中的一种查询。库中存在的每条已知序列将逐一地同每条所查序列作一对一的序列比对。 2、BLASTX是核酸序列到蛋白库中的一种查询。先将核酸序列翻译成蛋白序列(一条核酸序列会被翻译成可能的六条蛋白),再对每一条作一对一的蛋白序列比对。 3、BLASTN是核酸序列到核酸库中的一种查询。库中存在的每条已知序列都将同所查序列作一对一地核酸序列比对。
游离氨基酸
总游离氨基酸测定(完整版) 实验原理:游离氨基酸的游离氨基可与水合茚三酮作用,产生蓝紫色的化合物二酮茚-二酮茚胺,产物的颜色深浅与游离氨基酸含量成正比,用分光光度计在570nm下测其含量。因蛋白质中的游离氨基酸也会产生同样反应,在测定前必须用蛋白质沉淀剂将其除掉. 仪器与用具:100ml容量瓶;漏斗;三角瓶研钵;刻度吸管:0.1ml×1、1ml×2、2ml×2、5ml×1;沸水浴;具塞刻度试管20ml×10;分光光度计. 一、试剂 1.水合茚三铜:称重结晶的茚三铜0.6g,装入烧杯,加入正丙醇15ml,使其溶解加入正丁醇30 ml、乙二醇60 ml、乙酸-乙酸钠缓冲液(pH=5.4)9 ml,混匀,棕色瓶冰箱保存,10天内有效。 2.乙酸-乙酸钠缓冲液(pH5.4):称取化学纯乙酸钠54.4g,加入无氨蒸馏水100 ml,电炉加热至沸,使其体积减半,冷却后加冰乙酸30 ml,加蒸馏水定容至100 ml。 0.2M 醋酸:11.55ml 冰醋酸定容至1000ml。 0.2M 醋酸钠:16.4g 无水醋酸钠或27.2g 醋酸钠.3H2O溶于1000ml水中。 0.2M 醋酸6.8ml 0.2M 醋酸钠43.2ml,混匀,如果有PH计,可以测一下(基本差不多),如果高了点,可以加一点0.2M 醋酸,低了,再加一点醋酸钠,最终浓度为0.2M。如果要别的浓度,可以稀释。 3.氨基酸标准溶液:精确称取80℃烘干至恒重的亮氨酸0.0234g溶于10%异丙醇并定容至50ml。取此液5ml蒸馏水稀释到50ml,即为5μg/ml 氨基酸标液。
氨基酸序列推导
氨基酸序列推导 1.请指出天冬氨酸分别在(1)pH 1.0, (2)pH 3.0 ,(3) pH 6.0 ,(4) pH 11.0 时占优势的净电荷形 式(分别用“+”“-”“0”表示)。 2.将含有Gly, Ala , Glu ,Lys ,Arg , His 的溶液点在滤纸条的中央,用 pH 6的缓冲液浸湿,放入 电场中,请问(1)哪些氨基酸移向正极?(2)哪些氨基酸移向负极?(3)哪些氨基酸停留在原处或接近原处? 3.下述每组混合物分别在正丁醇-醋酸-水系统进行纸层析,指出每组中各组分的相对迁移率(假定水 相的pH 为4.5 ,用“ >”表示):(1).Val和Lys,(2).Phe 和Ser,(3).Ala、Val和 Leu, (4).Tyr、Ala 、Ser和 His 。 4.将含有Asp (pI=2.98),Gly (pI= 5.97),Thr (pI= 6.7),Lys (pI=9.74)的pH为3.0 的柠檬酸溶液, 加到预先用相同缓冲液平衡过的阳离子交换树脂柱上,随后用逐渐增加NaCl浓度的相同缓冲液洗脱,问这四种氨基酸的洗脱顺序? 5.将Lys ,Arg ,Asp ,Glu ,Tyr ,Ala的混合溶液在高pH 时,加到阴离子交换树脂柱上,用连续递减 pH值的溶液洗脱,请预测这些氨基酸的洗脱顺序。 6.已知一个八肽的氨基酸组成为:Asp, Ser ,Gly ,Ala ,Met ,Phe 和Lys2 ,又作了一系列分析结果 如下:(1)FDNB反应后可得到DNP-Ala,(2)胰凝乳蛋白酶水解后,得到一个四肽,其组成为:Asp, Gly, Lys, Met,此四肽的FDNB反应后得到DNP-Gly。(3)胰蛋白酶水解该八肽后得到两个三肽和一个二肽,三肽的组成分别为:Lys , Ala ,Ser和Phe , Lys , Gly。二肽经CNBr处理后产生Asp。请写出该八肽的氨基酸顺序。 7.某肽经CNBr处理得到三个肽段,其顺序分别为:Asn-Trp-Gly-Met; Gly-Ala-Leu; Ala-Arg-Tyr-Asn-Met, 用胰凝乳蛋白酶水解此肽也得到三个片断,其中一个为四肽,用6N的盐酸水解此四肽只得到Asp2和Met,问此肽的氨基酸排列顺序? 8.根据下列数据推导出氨基酸的顺序:(1)完全水解得到Phe, Pro, Glu , Lys2, Met 。(2)用FDNB 处理得到DNP-Phe。(3)CNBr处理得到一个两肽和一个四肽。(4)胰蛋白酶水解得到两个三肽。(5)羧肽酶A或羧肽酶B处理都不能得到阳性结果。 9.一个由Ala, Cys, Lys, Phe和Ser组成的五肽,用TIPC分析,得到PTH-Ser;用胰蛋白酶水解得到 一个N端为Cys的三肽和一个N端为Ser的二肽;用胰凝乳蛋白酶水解上述三肽生成Ala 和一个二肽,写出该五肽的顺序。 10.从以下资料推出五肽的氨基酸序列:(1)含有Phe , Pro , Glu , Lys2(2)Edman 试剂处理得到 PTH-Glu (3)用胰蛋白酶、羧肽酶A和羧肽酶B处理都不能得到阳性结果。 1.(1)pH 1.0, +1;(2)pH 3.0 , 0;(3) pH 6.0, -1 ; (4) pH 11.0,-2 2. Glu 移向正极;Gly, Ala接近原处;Lys ,Arg , His移向负极 3. Val > Lys, (2).Phe > Ser,(3) Leu > Val > Ala,(4).Tyr > Ala > Ser > His 4. Asp、 Gly 、Thr、 Lys 5. Arg ,Lys , Ala ,Tyr , Glu ,Asp , 6. Ala-Ser-Lys-Phe-Gly-Lys- Met-Asp 7. Ala-Arg-Tyr-Asn-Met-Asn-Trp-Gly-Met-Gly-Ala-Leu; 8. 任一答案: Phe-Met-Lys-Glu-Lys-Pro Phe-Met-Lys-Glu-Pro-Lys Phe-Glu-Lys-Met-Pro-Lys Phe-Glu-Lys-Met-Lys-Pro 9. Ser-Lys-Cys-Phe-Ala,
天津第三中心医院全自动氨基酸分析仪项目需求书
天津市第三中心医院全自动氨基酸分析仪项目需求书数量:一台 一、环境条件: 1.电源电压:220V±10%,50Hz。 2.温度:15~30℃。 3.湿度:25~85%。 二、全自动氨基酸分析仪功能要求及配置: (一)功能要求: 1.蛋白水解液及生理体液分析。 2.缓冲液、反应液试剂配方公开,可采用国产试剂。 3.色谱工作站,能够实现仪器的控制、数据采集和处理。能够实现系统的自动清洗,符合GLP/GMP规则,能够进行系统校验性试验、订制客户报告。 (二)配置要求: 1.蛋白水解液的标准分析系统。 2.生理体液分析系统。 3.色谱柱装填工具:1 套。 4.树脂。 5.光源灯:2个。 6.泵密封件:若干。 7.清洗密封件。 8.保护柱芯:若干。 9.电脑系统和打印机。 三、全自动氨基酸分析仪技术要求: (一)系统指标: 1.净分析时间:蛋白水解≤ 50 min; 生理体液90-180 min。 2.保留时间重现性:全部氨基酸平均≤0.5%CV。 3.峰面积重现性:全部氨基酸平均≤1.0%CV。 4.检测限:全部氨基酸平均≤10pmol。
5.分离度:平均≥1.2。 (二)分离柱:可自行填充。 1.柱温范围:室温~99℃。 2.温度稳定性:≤±1℃。 (三)自动进样器:带制冷单元。 1.进样体积:1~500 uL 2.样品位:≥80 (四)检测器: 1.检测波长:570nm,440nm。 2.反应器温度范围:40-140℃。 3.温度稳定性:≤±1℃。 (五)泵系统:具备梯度控制功能。 1.流速稳定性:RSD≤1.0%。 2.最大压力:≥19.6MPa。 3.压力波动≤0.1%。 (六)数据处理工作站: 1.硬件:CPU Pentium IV以上,内存≥1GB,硬盘≥120 GB,DVD刻录光驱,17寸液晶彩显。 2.操作系统:32位操作系统。 四、技术服务:在用户单位现场提供应用技术培训,符合用户指定安装,要求完善的售后服务,以确保临床使用。 五、售后服务:保修期两年,保证开机率95%以上(以365天计算),软件终身免费升级。提供10年以上备件供应。境内具备正规维修机构,出具相关法律文件。境内具备零备件保税库,出具相关法律文件。 六、投标价为免税美元价,按7.7比率折合人民币价格。
氨基酸分析仪检测氨基酸水溶肥中游离氨基酸可行性分析
氨基酸分析仪检测氨基酸水溶肥中游离氨基酸可行性分析【摘要】通过酸水解法测定含氨基酸水溶肥料中17种氨基酸含量,采用sykam全自动氨基酸分析仪,水合茚三酮柱后衍生,结果表明:同一个样品测得的氨基酸峰面积相对标准偏差小,峰面积的回收率在97.8%~101.3%,用此方法测氨基酸具有良好的重复性、准确性。 【关键词】含氨基酸水溶肥;酸水解;氨基酸;柱后衍生 0.前言 我国是一个缺水的农业大国,化肥的使用在农业生产中占重要地位,而传统肥料存在利用率低、养分损失率高而且耗水量大的缺点,水溶肥料由于其迅速溶于水中、养分更易被吸收而且吸收利用率高并可应用于滴灌、喷施、喷灌的节水特点,在我国农业中有广阔的发展前景[1]。氨基酸水溶肥作为水溶肥中的一员,其原理:氨基酸存在肥料中,易于被作物吸收的特点;亦有提高施肥对象抗病性,改善施肥作物品质的功能;补充植物必须的氨基酸,刺激和调节植物快速生长,促使植物生长健壮,促进对营养物质的吸收;增强植物的代谢功能,提高光合作用,促进植物根系发达,加快植物生长繁殖[2]。目前,对于氨基酸的检测大多采用液相色谱、气相色谱-质谱联用、毛细管电泳、凯氏定氮法和光谱法等方法。这些方法或试剂费用昂贵,或分离效率低,或不能同时测多种氨基酸。运用氨基酸分析仪能解决以上问题,并且操作简单方便,重复性好。 1.方法原理
