第十三章有机含氮化合物2
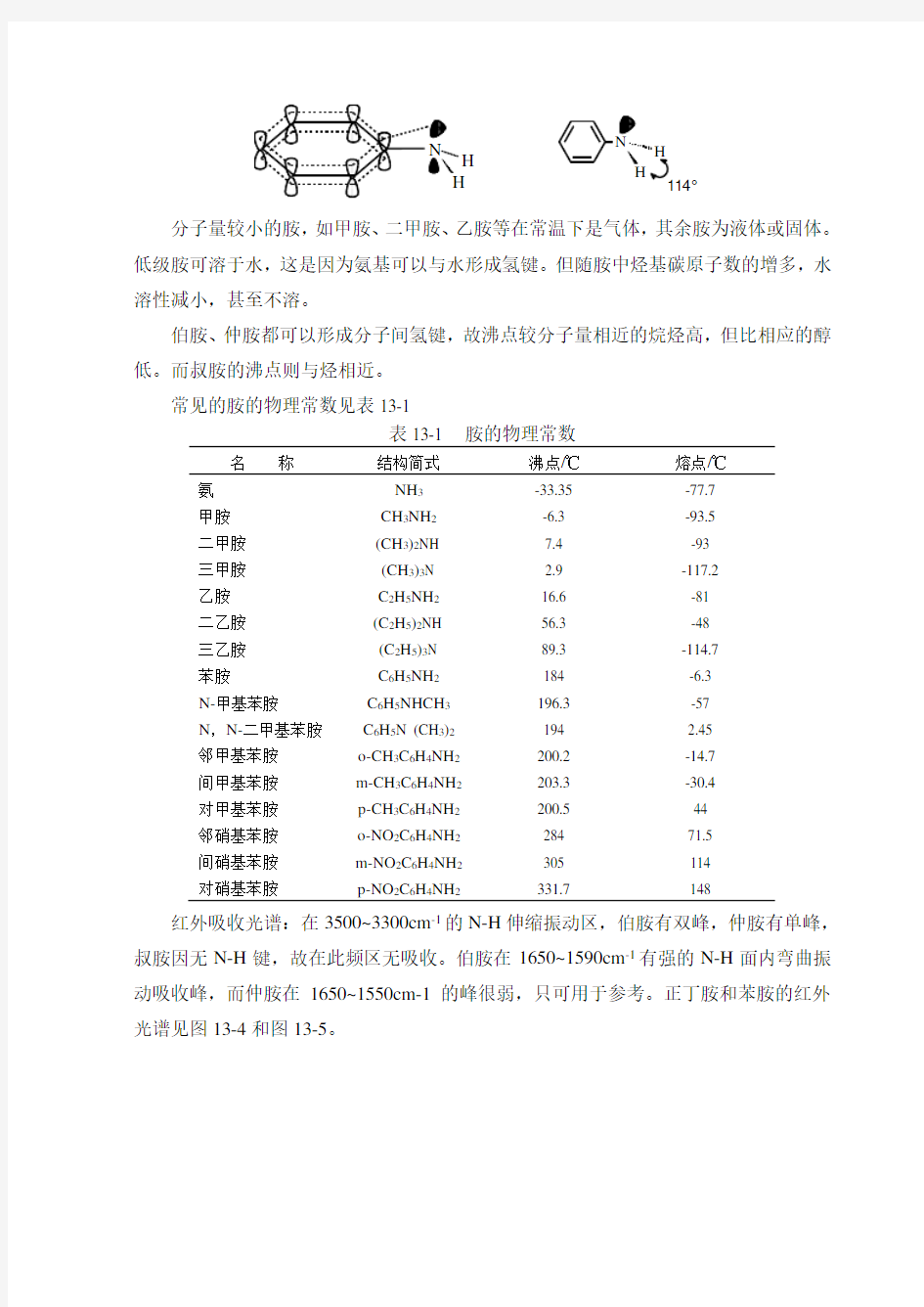
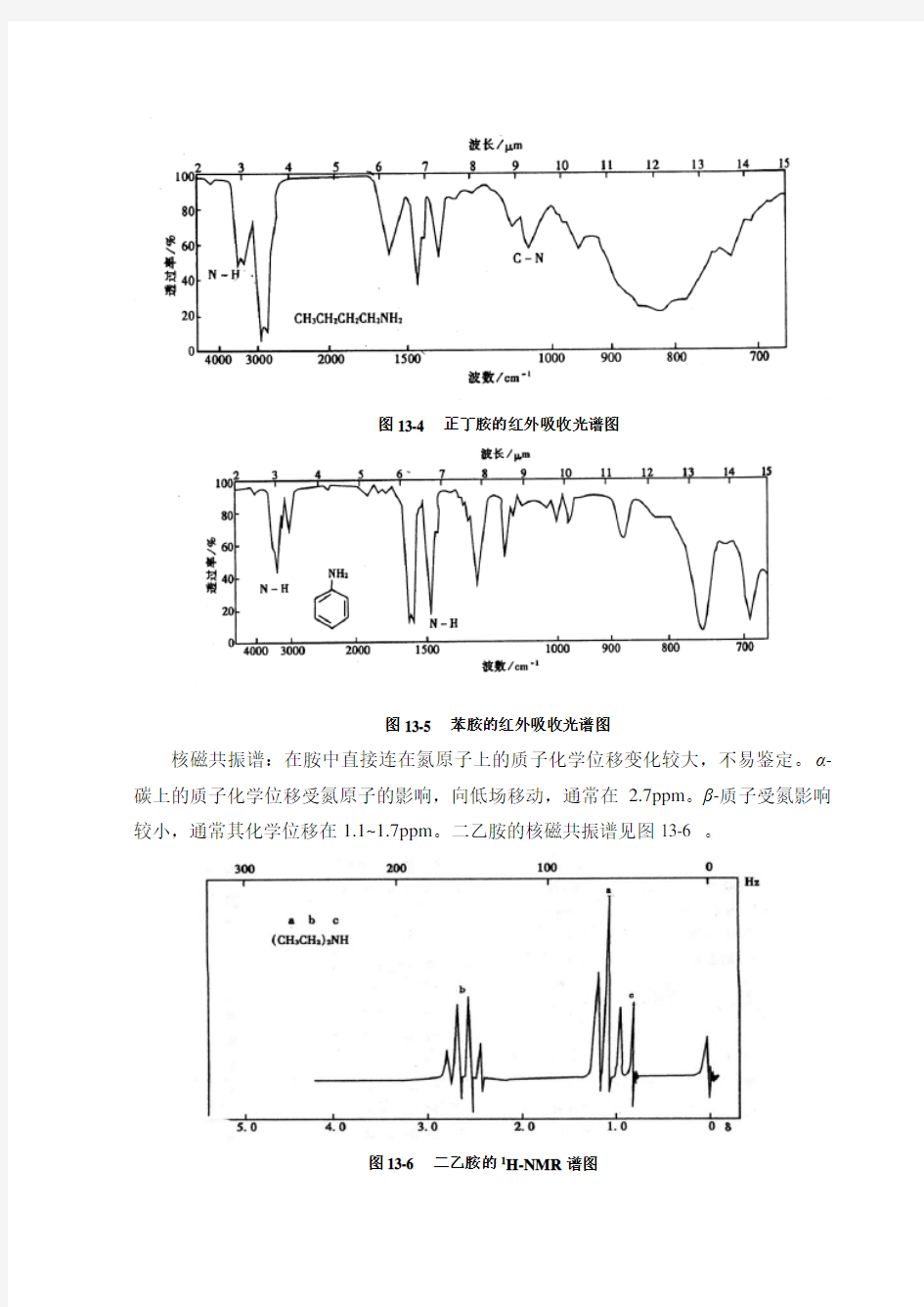
分子量较小的胺,如甲胺、二甲胺、乙胺等在常温下是气体,其余胺为液体或固体。低级胺可溶于水,这是因为氨基可以与水形成氢键。但随胺中烃基碳原子数的增多,水溶性减小,甚至不溶。
伯胺、仲胺都可以形成分子间氢键,故沸点较分子量相近的烷烃高,但比相应的醇低。而叔胺的沸点则与烃相近。
常见的胺的物理常数见表13-1
表13-1 胺的物理常数
名称结构简式沸点/℃熔点/℃
氨NH3-33.35 -77.7
甲胺CH3NH2-6.3 -93.5
二甲胺(CH3)2NH 7.4 -93
三甲胺(CH3)3N 2.9 -117.2
乙胺C2H5NH216.6 -81
二乙胺(C2H5)2NH 56.3 -48
三乙胺(C2H5)3N 89.3 -114.7
苯胺C6H5NH2184 -6.3
N-甲基苯胺C6H5NHCH3196.3 -57
N,N-二甲基苯胺C6H5N (CH3)2194 2.45
邻甲基苯胺o-CH3C6H4NH2200.2 -14.7
间甲基苯胺m-CH3C6H4NH2203.3 -30.4
对甲基苯胺p-CH3C6H4NH2200.5 44
邻硝基苯胺o-NO2C6H4NH2284 71.5
间硝基苯胺m-NO2C6H4NH2305 114
对硝基苯胺p-NO2C6H4NH2331.7 148 红外吸收光谱:在3500~3300cm-1的N-H伸缩振动区,伯胺有双峰,仲胺有单峰,叔胺因无N-H键,故在此频区无吸收。伯胺在1650~1590cm-1有强的N-H面内弯曲振动吸收峰,而仲胺在1650~1550cm-1的峰很弱,只可用于参考。正丁胺和苯胺的红外光谱见图13-4和图13-5。
图13-4 正丁胺的红外吸收光谱图
图13-5 苯胺的红外吸收光谱图
核磁共振谱:在胺中直接连在氮原子上的质子化学位移变化较大,不易鉴定。α-碳上的质子化学位移受氮原子的影响,向低场移动,通常在 2.7ppm。β-质子受氮影响较小,通常其化学位移在1.1~1.7ppm。二乙胺的核磁共振谱见图13-6 。
图13-6 二乙胺的1H-NMR谱图
在各类化合物的物理性质中已分别介绍了它们的红外吸收光谱和核磁共振氢谱中的化学位移,现将这些数据归纳于表13-2和表13-3中。
表13-2各类有机化合物中化学键的红外特征吸收
表13-3 不同类型质子的化学位移(δ)
练习题13.3 下列化合物的红外光谱有何不同?
CH 2NH 2
(A)
(B)CH 3
C
N O
(CH 3)2
练习题13.4 一个烃类,已知不是烯烃就是烷烃,其H’-NMR 谱上有4.8δ,2.7δ,1.9δ,和0.8δ几个吸收,试作出判断。
(三)胺的化学反应
胺中的氮原子是sp3杂化的,其中的一个sp3轨道中具有一未共用电子对,在一定条件下会给出这一对电子,使胺中的氮原子成为碱性中心和亲核中心,胺的主要化学性质都体现在这两个方面。
1.碱性和铵盐的生成 尽管伯、仲、叔胺在结构上有差别,但其共同特征是氮原子上有未共用电子对,因而可以接受质子,呈碱性。多数胺可与强酸形成较稳定的盐,成盐后水溶性增大,这一点可以将胺与其它中性物质分离。
练习题13.5 苯胺进行乙酰化后得到乙酰苯胺,为了将产物与未反应的苯胺分离,
你能设计一个简便的分离方案吗?
胺的碱性,是基于下列平衡
N
+
H
+
K b
K a
N
+
R H
其碱性的大小,既可用p K b 来度量,也可用p K a 来度量。在表13-5中,给出了一些胺的p K a 值。
表13-4一些脂肪胺的碱性
胺 NH 3
p K a 9.24
胺
CH 3CH 2CH 2NH 2
p K a 10.61
CH 3NH 2 10.65 (CH 3CH 2CH 2)2NH 10.91 (CH 3)2NH 10.73 (CH 3CH 2CH 2)3N 10.65 (CH 3)3N 9.78 n-C 4H 9NH 2 10.64 CH 3CH 2NH 2 10.71 iso-C 4H 9-NH 2 10.41 (CH 3CH 2)2NH 11.0 t-C 4H 9NH 2
10.71 (CH 3CH 2)3N
10.75
从表中的数据可以看出,所有的脂肪胺的碱性都比其母体——氨的碱性强,这只能认为是烷基具有给电子的诱导效应,使氮原子上的未共用电子对更易给出。或者说使质子化后的铵离子更趋稳定。但如果仅此一个上述原因,则胺的碱性顺序应为
R 3N > R 2NH > RNH 2 > NH 3
实际上,这样的碱性顺序在气相确实观察到了。但在水溶液中,却观察到仲胺的碱性最强,而伯胺与叔胺碱性都比仲胺弱。这是因为在水溶液中,溶剂化(水合)效应在起作用。当胺与质子结合成盐后,除铵正离子与水的极性相互作用之外,该正离子与水形成氢键的能力对其溶剂化的强弱也起着重要作用。在铵正离子中,氮上的氢原子越多,与水形成氢键的能力就越强,从而导致的稳定化作用就越大。故这种溶剂化作用的能力是:
伯胺>仲胺>叔胺
H OH 2
N
+
R H H
OH 2OH 2
N +
R
H H
OH 2OH 2
R N
+
R R H
OH 2
R
伯胺 仲胺 叔胺
上述这两种影响碱性的因素,仲胺都处于居中的位置,两种因素共同作用的结果是:
仲胺的碱性最强,而伯胺和叔胺次之。至于伯胺与叔胺的碱性孰强孰弱,与其结构密切相关。例如,三甲胺的碱性比甲胺弱,而三乙胺的碱性比乙胺强。这种由于烃基的不同而引起的细微差别用上述两因素仍不能作出说明。
一些取代芳香胺的碱性见表13-5
表13-5取代苯胺的碱性(p K a)
取代基邻间对
H 4.60 4.60 4.60
NH2 4.48 5.00 6.15
CH3O 4.48 4.30 5.30
CH3 4.39 4.96 5.12
OH 4.72 4.17 5.50
Cl 2.70 3.48 4.00
Br 2.48 3.60 3.85
NO2-0.3 2.50 1.20 苯胺的碱性要比氨弱得多,这是因为苯胺中氮上未共用电子对与苯环有共轭作用,分散了氮上的这一对电子,使其碱性大大减弱。在芳胺中,氮上的氢原子若被烷基取代,会使碱性增强。如:
PhNH2PhNHCH3PhN(CH3)2
pK a 4.60 4.85 5.06 很显然,烷基的给电子诱导效应起了重要作用。若氮上的氢原子被芳环取代,则碱性显著降低,这与苯胺碱性较弱的原因是一样的。例如:
PhNH2Ph2NH Ph3N
pK a 4.60 1.0 中性在苯胺中,若苯环上连有取代基,则此取代基团对碱性强弱也会产生影响。这种影响是基团的电子效应和空间效应等综合作用的结果,并且可以大体归纳为:
①绝大多数取代基(在表中除OH),无论是给电子还是吸电子,在邻位时都使碱性减弱。
②给电子基团(如甲基)使碱性增强,而吸电子基团(如硝基)使碱性减弱。并且取代基的这种使碱性增强或减弱的影响在对位比在间位更为明显。如硝基取代的苯胺:
_
_
N
+
O
O
③诱导效应与共轭作用方向不一致时,则要考虑其相对强弱和所在的位置。例如取代基为卤素时,若连在间位,只存在吸电子的诱导效应影响,碱性减弱;连在对位时,其给电子的共轭作用部分抵消了吸电子的诱导效应,碱性仍比苯胺弱,但比其间位异构体强。
练习题13.6 参照取代基对芳环的定位规律,你能否解释对位和间位被甲基取代后的苯胺碱性变化?
2.烃基化
胺类化合物中氮原子上存在一对未共用电子,使其具有亲核性,可以与卤代烷发生亲核取代反应,反应易按S N 2历程进行的。如伯胺与卤代烷反应,得仲铵盐:
NH 2X
R R'
+
-
生成的铵盐经质子转移,可得到仲胺。仲胺的氮上仍有未共用电子对,继续与卤代烷反应,经类似的过程可得叔胺。而叔胺还可再与卤代烷反应得到季铵盐,因此最后得到的是复杂的混合物。
+
NH 2
R R'
+
NH 2R N +
H 3
R +
NH
R R'
NH +
X
R R'
R'X
R'+
NH
R R'
_
NH
+
R R'
R'N
R R
R'
+
NH 3
R NH 2R +
+
N
R R
R'_
+
X R'N +
R R'
R'
R'X
尽管可以通过控制投料比、反应温度、时间等条件使某一胺为主产物,但仍需较繁的后处理。与胺反应时,卤代烷的活性为RI>RBr>RCl 。
练习题13.7 苯胺与氯苄反应基本上只得到一烃基化的产物,
NH 2
+
CH 2Cl
CH 2NH
你能说明可能是什么因素影响的结果吗?
3.酰化和磺酰化 胺中的氮原子作为亲核中心,还可以与酰卤、酸酐甚至酯等发生亲核取代反应而生成酰胺。用酯做酰化剂时反应较慢。芳胺因其碱性弱,亲核性弱,一般需用酰卤或酸酐酰化。例如:
NH 2
+
(CH 3CO)2O
NHCCH 3
O
CH 3CH 2NH 2
+
C OC 2H 5
CH 3O
CH 3C
NHCH 2CH 3
O C 2H 5OH
+
C 2H 5NHCH 3
+
+COCl CON
CH 3
C 2H 5
HCl
用酰卤做酰化剂时,需加入一种碱,以吸收生成的卤化氢,常用的碱是氢氧化钠和吡啶。伯胺分子中虽有两个氢原子,但一般只能引入一个酰基,因为生成酰胺后,氮原子的亲核性大大降低了。正因为如此,可以利用酰化来保护氨基,使其不易被氧化。酰胺可通过酸或碱水解再游离出氨基。
伯胺仲胺能与磺酰氯作用生成磺酰胺
SO 2Cl
CH 3
NH 2
+
SO 2CH 3NH
+
SO 2Cl
CH 3(C 2H 5)2NH SO 2CH 3N(C 2H 5)2
由伯胺生成的磺酰胺,氮原子留下的氢因受磺酰基影响,具有弱酸性,与氢氧化钠作用可形成盐而溶于水;仲胺形成的磺酰胺因氮上无氢原子,不能溶于碱;叔胺则不能被酰化。
SO 2
R
NH
NaOH SO 2
N
R
_
Na +
不溶(白色固体) 溶解
利用这些性质上的不同,可用于三种胺的分离与鉴定,这称为兴斯堡(Hinsberg )反应。
练习题13.8 一不溶于水的液态胺经用苯磺酰氯处理后,加盐酸酸化,没有沉淀出现。你能判断是伯胺、仲胺、还是叔胺吗?
4.与亚硝酸反应 胺类可以与亚硝酸发生反应,但伯、仲、叔胺各有不同的反应结果和现象。脂肪胺与芳香胺的反应也有差异。
芳香伯胺与亚硝酸在低温下反应,生成重氮盐,称为重氮化反应。例如:
NH 2
20-5℃
N
N +
Cl
-
++NaCl H 2O
亚硝酸不稳定,所以用亚硝酸钠加强酸(通常是盐酸或硫酸)代替,反应中亚硝酸钠先与酸反应生成亚硝酸,然后再与胺反应生成重氮盐,这一系列变化如下:
++
NaNO 2 HCl HONO NaCl
+
+
HONO H
+
NO HO
+
NO
H 2O
_
+NH 2
Ar +
NO
N
+
Ar H
H
NO
H
+
H +
N
Ar H
N O
N Ar N
H
+
+N Ar 2
H 2O
_
N
Ar N
+
重氮化反应生成的芳香重氮盐可溶于水。在低温(0~5℃)时较为稳定,加热时水解成酚类。干燥的重氮盐稳定性很差,易爆炸。故制备后直接在水溶液中应用。
芳香重氮盐的用途很广,将在以后介绍。芳香重氮盐与β-萘酚反应,会得到颜色较深的化合物。用于鉴别芳香伯胺。
+
N 2+
Cl
OH
N N
OH
脂肪族伯胺与亚硝酸作用也同样得到重氮盐。但脂肪族重氮盐极不稳定,即使在低温也很快分解,放出氮气,生成相应的碳正离子。这个高度活泼的碳正离子就会与溶液中的任一负离子结合形成取代产物、消除成烯和发生重排反应等,得到各种产物的混合物,因此在制备上很少有实际用途。例如:
+CH 3(CH 2)3NH 2
H 2O, 25℃
NaNO HCl
CH 3(CH 2)3OH H 3CH 2CHCH 3 CH 3(CH 2)3Cl
OH
++
25% 13% 5%
+CH 3CH 2CHCH 3Cl
CH 3CH 2CH CH 2
+
C H 3C
H
C
CH 3
H
+
+
C H 3C
H
C
H
CH 3
+
N 2↑
3% 26% 3% 7%
但这一反应可以定量完成,所以可以根据氮气的生成量来测定伯胺的量。
脂肪族伯胺的一个较有制备价值的反应是扩环反应,可制备五至九元的环酮。例如:
+
CH 2NH 2OH
2
CH 2N 2+
OH
CH 2OH
+
OH
+
O
H
+
练习题13.9 如何由
O
制备 (CH 2NH 2
()2)
O
1OH
?
芳香仲胺和脂肪仲胺与亚硝酸反应的结果基本相同,都是在胺的氮上进行了亚硝化得N-亚硝基化合物。例如:
(C 2H 5)2NH
NaNO H 2SO 4
(C 2H 5)N NO
NHCH 3
HCl
NaNO N NO
CH 3
N-亚硝基仲胺为中性的黄色液体或固体,可用以鉴别仲胺。该亚硝化物经水解或还原得原来的仲胺,可作为胺的精制方法。叔胺因其氮上无氢,不能如仲胺那样形成N-亚硝基化物。
脂肪叔胺只能与亚硝酸形成一个不稳定的盐:
R 3N + HNO 2
[R 3NH]+NO 2ˉ
芳香叔胺因为氨基的强活化作用,芳环上电子云密度较高,易与亲电试剂反应。而O N =+
是个亲电试剂,因此可以在芳环上发生亲电取代,生成对位亚硝基苯胺。如对位已被占
据,则反应在邻位发生:
(CH 3)2N
NaNO HCl
(CH 3)2N
NO
(CH 3)2N CH 3
HCl
NaNO (CH 3)2N
CH 3
ON
这种环上的亚硝基化合物都有明显的颜色,可用以鉴别。如:
(CH 3)2N
N
O
-
+(CH 3)2N
N OH
翠绿色彩 桔黄色
亚硝基化合物是很强的致癌物质。
5.芳环上的取代 芳环上的氨基与羟基一样,对芳环上的亲电取代反应具有较强的致活作用,因此,芳胺的芳环上很易发生亲电取代反应。
(1)卤代反应 苯胺与溴水反应立即生成2,4,6-三溴苯胺:
NH 2
+
Br 2
0℃
H 2O
NH 2
Br
Br
Br
该反应能定量完成,得到不溶于水的白色沉淀,可用于定性与定量分析。
即使苯环上有致钝基团时,仍较容易发生取代反应:
+
Cl 2
N(CH 3)2
COOH
Cl Cl
N(CH 3)2
COOH
H 2O
CH 3COOH
N(CH 3)2
NO 2
N(CH 3)2
Br
NO 2
Br
+
℃℃
氨基被酰化之后,对环的致活作用减弱了,可以得到一卤代产物:
NH 2
NHCCH 3O
NHCCH 3
O Br H 2O,H
+
NH 2
Br
(2)硝化反应 芳伯胺易被氧化。将苯胺直接与硝酸作用可能引起爆炸性氧化分解。所以要先酰化后再硝化:
NHCCH 3
NO 2
O NHCCH 3
O NO 2
NHCCH 3
O
NH 2
20℃
_+
23% 77%
倘若使用硝酸与乙酐作用后生成的硝乙酐(CH 3COONO 2)作酰化剂(详见十四章二)在20℃反应,可使邻位硝化为主产物。
(3)磺化反应 苯胺与浓硫酸作用成盐后在180℃加热脱水,生成不稳定的苯胺磺酸,然后很快重排成对氨基苯磺酸:
_NH 3 HSO 4
180℃
NHSO 3H
NH 3
+
SO 3
-
.
它兼有酸、碱两种官能团,因此以内盐形式存在。内盐是两性离子、熔点高、水溶度小。
对氨基苯磺酰胺是最简单的磺胺类药物,也是其它磺胺药物的母体,其合成过程大致为:
NHCCH 3
O Cl 2NHCCH 3
SO 2Cl O NHCCH 3
SO 2NH 2
O 3
NH 2
SO 2NH 2
℃
+
H 2O,
在氨解时以其它胺类代替NH 3就得到各种磺胺药物。
6.其它反应 芳胺可以与芳香醛缩合生成含C=N 键化合物,称为西佛碱(Schiff ’s base )。这是氮原子为亲核中心对羰基的亲核加成反应。
NH 2
+
CHO
NH
CH
OH 2
_N CH
西佛碱水解又可得原胺和醛,所以可以利用来保护氨基和醛基。
当一个仲胺与一个有α-氢的醛、酮反应时,因加成产物的氮上已无可消除的氢原子,则不能形成西佛碱,而是以另一种方式失水,生成叫做烯胺的产物:
C C H O
+
NHR 2C C H N +
HR 2
O
-C C H NR 2
OH _C
C NR 2
℃℃
在制备烯胺时,加一个强脱水剂,可以使反应进行得很完全。常用的仲胺是一些环
状胺,如六氢吡啶、四氢吡咯、吗啉等。
N O H
N H
N H
吗啉 四氢吡咯 六氢吡啶
O
+
H
N H +
N
+
H 2O
烯胺可以看成是一个“氮烯醇式”。与烯醇负离子类似,有二个可以反应的位置,一是在碳上,另一个是在氮上:
C
C
c
C
N
+
_因此,形成烯胺之后,原羰基的α-碳原子可作为亲核部位,与酰卤或卤烷等发生酰基化或烃基化反应,其反应过程以酰化为例,表示如下:
N
COR
+
2O
COR
+
N H
HCl
反应实例如下:
H 2O
+
N
O
ClCCH 2CH 2COC 2H 5
O
O
3N
O
C CH 2CH 2COOC 2H 5
O
+
O
C CH 2CH 2COOC 2H 5
O
伯胺与氯仿和碱作用可得异腈(又称胩):
NH 2
R
+
CHCl 3
OH -N
R C
_
+
脂肪和芳香伯胺均有此反应。生成的异腈具有特殊臭味,很易察觉,可用于鉴别伯胺。 异腈有毒,可水解破坏之:
+
_
N
R
C
△ H +2NH 2
R
+
HCOOH
练习题13.10 (1) 二甲胺基苯甲醛与磺胺类药物可很灵敏地显示黄色。试写出其 反应产物:
(CH 32
)N CHO +H 2N
SO 2NHR
(2)有一液体,疑为氯仿,试用一简单方法证明之。
(四)胺的制备
1.氨或胺的烃基化 氨与脂肪族的卤烃可以反应生成胺,往往得到的是各种胺的混合物,分离提纯有一定的困难,因而,这一方法的用途有限。
氨与芳卤烃的反应,因卤素原子与芳环的共轭作用,卤素很难被取代,因而需要高温高压的条件才能发生反应。但当卤素的邻、对位有强的吸电子基团(如硝基)存在时,亲核试剂对芳卤烃的亲核取代反应变得容易了。如:
+
CH 3NH 2
Cl
NO 2
EtOH NHCH 3
NO 2
练习题13.11 2,4,6-三硝基甲苯能与苯甲醛发生缩合反应
O N
22
22
2
2
3
CH
CH CH NO NO NO NO CHO
+
O N
指出这是何种类型的反应,并说明2,4,6-三硝基甲苯为什么能发生这个反应。
第12章含氮化合物
第12章 含氮化合物 12-1 命名下列化合物或写出结构式。 (1)2-甲基-3-硝基己烷 (2)N-甲基间甲苯胺 (3)3-甲氨基戊烷 (4)N-乙基苯磺酰胺 (5)氯化三甲基对氯苯铵 (6)氢氧化二甲基二乙基铵 (7)氯化重氮苯 N C O COOC 2H 5 2 CH 3CHCH 2CHCH 2CH 3 NH 2NHCH 3N N H 2NCH 2(CH 2)3CHCH 2NH 2 3 (8) (9) (10)(11) (12) 知识点:含氮化合物的命名。 12-2 比较下列各对化合物的酸性强弱。 CH 2NH 3 (1)(3)(2)NH 3 CH 3NH 3 NH 3 NH 3 3 NH 3 2 A. B. A. B. A. B. (1)B >A ; (2)A >B ; (3)B >A 。 知识点:胺的活性。 12-3 将下列各组化合物按碱性由强至弱的次序排列。 (CH 3)4NOH CH 3CONH 2(1)(2)NH 2 2 A. B. C.D. E. CH 3NH 2 NH 2 SO 2NH 2 (CH 3)3N NH 2 3 NH 2 2 NO 2 (CH 3)2NH A. D. B. E.C. (1)A >C >D >B >E ; (2)E >A >B >C >D 。 知识点:胺的碱性。 12-4 完成下列反应。
(1) HCOOEt NO 2 EtONa CH 3 +NO 2 CH 2CHO (2) NaOCH 3 CH 3OH NO 2 +Cl NO 2 OCH 3 Cl (3) CH 2CH 2NH 2 CH 3COCl (1)LiAlH 4 (2)CH 3OH CH 2CH 2NHCCH 3O CH 2CH 2NHCH 2CH 3 (4) NaNO 2/H 2SO 4 NH 2NO 2 NO 2 室温 N 2HSO 4 2 NO 2 2 2 (5)NaNO 2Ph C CH 2NH 2 OH 3 H 3C C CH 2Ph O (6) N 2 CH 2I +Ag 2O 2CN N CN CH 3 H 3C I N CN CH 3 H 3C OH (7) KOH H 2O,OH, △ NH O O NK O O H 2C PhCH 2NH 2 H N N H (8) H CH 3 H 3C 2N H 3C CH 3 NH 2
最新14-第十四章-含氮有机化合物习题答案(第四版)
第十四章含氮有机化合物(P125-129) 1.给出下列化合物的名称或写出结构式: (1)(2)(3)(4)(5)(6) (7)对硝基氯化苄 (9)(8) (10)苦味酸(11)1,4,6-三硝基萘 2.按其碱性的强弱排列下列各组化合物,并说明理由: (1) NH2NH 2 NH2 O2N H3C (2) 乙酰胺、甲胺和氨 3.比较正丙醇、正丙胺、甲乙胺、三甲胺和正丁烷的沸点高低并说明理由: 4.如何完成下列转变: (1) (2)由到 (3) 由到 (4) 由到
5.完成下列反应,并指出最后产物的构型是(R)或 (S): (1) SOCl 23 2- 6.完成下列反应: (1) N H CH 3 322? 加热 ? ? (1) CH 3I (2)Ag 2O,H 2O (3) 加热 CH 3CH 3 O 2N Fe+HCl ?(CH 3CO)2O ? ? H +,H 2O ? NaNO 2,HCl ?? O 2N CH 3 (2) (3) OCH 3 OCH 3 H 2N (4) (5) 2 (6) CH 3 CH 2CH 2NH 2 (7) NH-COCH 3 Br HNO AcOH ? (8) NO 2F O 2N + N H CH 3O 2 ?
(9) N H + CH 3 H + ? CH 2=CHCOOEt ? H + ? (10) N + 3 CH3 H 3 C - ? 加热 7.指出下列重排反应的产物: (1) (2) (3 (4) (5) (6) ? ? ?
(7) ? ? (8) 8.解释下述实验现象: (1) 对溴甲苯与NaOH在高温下反应,生成几乎等量的对和间甲苯酚。 (2) 2,4-二硝基氯苯可以由氯苯硝化得到,但如果反应产物用NaHCO3水溶液洗 涤除酸则得不到产品。 9.请判断下述霍夫曼重排反应能否实现,为什么? 9. 完成下列反应,并为该反应提供一个合理的反应机理。 (3) 解:
第十三章 含氮有机化合物
第十三章 含氮有机化合物 含氮有机化合物是指含有碳氮键的有机化合物,它们在生物体中起着重要的作用。 第一节 胺 一、胺的分类和命名 胺是氨的烃基衍生物,它可看作是氨分子中的1个氢或几个氢原子被烃基取代后的产物。 (一)胺的分类 1.根据胺分子中氮原子上所连烃基的数目不同,可分为伯胺、仲胺和叔胺。 R —NH 2 R —NH —R ′ R R ′ R ″ 伯胺 肿胺 叔胺 2.根据胺分子中氮原子上所连的烃基种类不同,可分为脂肪胺和芳香胺。 R —NH 2 Ar —NH 2 脂肪胺 芳香胺 氮原子与脂肪烃基直接相连为脂肪胺,与芳环直接相连为芳香胺。 3.根据胺分子中氨基的数目不同,可分为一元胺、二元胺和多元胺。 一元胺:CH 3—CH 2—NH 2 二元胺:H 2N —CH 2—CH 2—NH 2 例如: 脂肪胺 芳香胺 CH 3NH 2 苯胺 甲胺 伯胺: NH 2 NH CH 2 仲胺:二苯胺 甲乙胺 CH 3 CH 3 NH 叔胺:三苯胺 甲乙丙胺 CH 2CH 2CH 2 N CH 3CH 3 CH 3
请注意:伯胺、仲胺、叔胺与伯醇、仲醇、叔醇的区别,胺是根据氮原子上所连烃基数目来分为伯胺、仲胺、叔胺,而醇则是根据羟基所连的烃基来分为伯醇、仲醇、叔醇。例如: C NH 2 CH 3 CH 3 C OH CH 3CH 3 伯胺叔醇 CH 3 CH 3 (二)胺的命名 1.简单的胺以胺为母体,按烃基的名称称为某胺。例如: CH 2 丙胺 CH 2 NH 2 CH 3NH 2 苯胺 甲胺NH 2 CH 3 2.仲胺和叔胺的氮原子上连的烃基相同时,用二或三标明烃基的数目,写在烃基名称前;烃基不同时,从简单到复杂依次写出烃基的名称。例如: (CH 3)2NH (CH 3CH 2)3N (C 6H 5)3N 二甲胺 三乙胺 三苯胺 NH CH 2 甲乙胺CH 3 CH 3 甲乙丙胺 CH 2 CH 2 CH 2 CH 3CH 3 CH 3 3.芳香仲胺和叔胺的氮原子上连有烃基时,以芳香胺为母体,在烃基前标上“N-”,以区别连接在芳环上的烃基。例如: N-甲基苯胺 N ,N-二甲基苯胺 N-甲基-N-乙基苯胺NHCH 3 N (CH 3)2 N CH 3 CH 2CH 3 4.多元胺可参照多元醇命名,二元胺称为某二胺。例如: H 2N —CH 2—CH 2—NH 2 H 2N —CH 2—CH 2—CH 2—CH 2—NH 2 乙二胺 1,4-丁二胺 5.对于结构复杂的胺,则以烃为母体,氨基用为取代基命名。例如:
第十四章 含氮有机化合物练习及答案
第十四章 含氮有机化合物 1. 给出下列化合物名称或写出结构式。 (CH 3)2CH NH 2 (CH 3)2NCH 2CH 3 NH CH 2CH 3 CH 3 NH CH 3 O 2N NC N + NCl - O 2N N N OH OH H 32H 对硝基氯化苄 苦味酸 1,4,6-三硝基萘 答案: 3-氨基戊烷 异丙胺 二甲乙胺 N -乙基苯胺 3-甲基-N -甲基苯胺 2-氰-4-硝基氯化重氮苯 O 2N CH 2CL NO 2 O 2N NO 2 OH NO 2 NO 2 NO 2 2. 按其碱性的强弱排列下列各组化合物,并说明理由。 (1) a b c NH 2 NH 2NH 2 NO 2CH 3 (2) CH 3C O NH 2 CH 3NH 2NH 3 a b c 答案: (1)吸电子基使碱性降低,供电子基使碱性增强,所以有:b > a > c (2)吸电子基使碱性降低,供电子基使碱性增强,所以有:b > c > a 3.比较正丙醇、正丙胺、甲乙胺、三甲胺和正丁烷的沸点高低并说明理由。 答案: 五种化合物中,按形成氢键的可能、能力可推知其沸点从高到低的次序是:
正丙醇 > 正丙胺 > 甲乙胺 > 三甲胺 > 正丁烷 分子间形成分子间氢键沸点高,醇分子中的羟基极性强于胺的官能团,胺三级大于二级又大于一级。 4. 如何完成下列的转变: (1)CH 2 CHCH 2Br CH 2CHCH 2NH 2 (2) NHCH 3 O (3) (CH 3)3C C OH O O C (CH 3)3C CH 2Cl (4) CH 3CH 2CH 2CH 2Br CH 3CH 2CHCH 3 NH 2 答案: (1)CHCH 2Br CH 2 NaCN CH 3CH 2OH CH 2CHCH 2CN LiAlH 4CHCH 2NH 2 CH 2 (2) O NH 3+(H) NH 2 CH 3Br NHCH 3 (3) (4) CH 3CH 2CH 2CH 2Br KOH,CH 3CH 2OH CH 3CH 2CH CH 2 HBr CH 3CH 2CHCH 3 Br 3 CH 3CH 2CHCH 3 NH 2 5. 完成下列各步反应,并指出最后产物的构型是(R )或(S )。 C 6H 5CH 2CHCOOH CH 3 (1)SOCl (2)NH 3 (3)Br 2,OH - C 6H 5CH 2CHNH 2 CH 3 S-(+) (-)
第十三章有机含氮化合物2
分子量较小的胺,如甲胺、二甲胺、乙胺等在常温下是气体,其余胺为液体或固体。低级胺可溶于水,这是因为氨基可以与水形成氢键。但随胺中烃基碳原子数的增多,水溶性减小,甚至不溶。 伯胺、仲胺都可以形成分子间氢键,故沸点较分子量相近的烷烃高,但比相应的醇低。而叔胺的沸点则与烃相近。 常见的胺的物理常数见表13-1 表13-1 胺的物理常数 名称结构简式沸点/℃熔点/℃ 氨NH3-33.35 -77.7 甲胺CH3NH2-6.3 -93.5 二甲胺(CH3)2NH 7.4 -93 三甲胺(CH3)3N 2.9 -117.2 乙胺C2H5NH216.6 -81 二乙胺(C2H5)2NH 56.3 -48 三乙胺(C2H5)3N 89.3 -114.7 苯胺C6H5NH2184 -6.3 N-甲基苯胺C6H5NHCH3196.3 -57 N,N-二甲基苯胺C6H5N (CH3)2194 2.45 邻甲基苯胺o-CH3C6H4NH2200.2 -14.7 间甲基苯胺m-CH3C6H4NH2203.3 -30.4 对甲基苯胺p-CH3C6H4NH2200.5 44 邻硝基苯胺o-NO2C6H4NH2284 71.5 间硝基苯胺m-NO2C6H4NH2305 114 对硝基苯胺p-NO2C6H4NH2331.7 148 红外吸收光谱:在3500~3300cm-1的N-H伸缩振动区,伯胺有双峰,仲胺有单峰,叔胺因无N-H键,故在此频区无吸收。伯胺在1650~1590cm-1有强的N-H面内弯曲振动吸收峰,而仲胺在1650~1550cm-1的峰很弱,只可用于参考。正丁胺和苯胺的红外光谱见图13-4和图13-5。
有机含氮化合物
1 授课内容 Chapter 9 有机含氮化合物 学时数 6 掌握比较含氮化合物碱性强弱的方法、胺与HNO 2的反应、重氮盐的放氮及偶联 反应; 理解杂环的芳香性及反应活性顺序; 了解生物碱的一般性质。 第一节 胺 Amines (胺的碱性、胺与HNO 2的反应); 第二节 重氮和偶氮化合物Diazo and Azo Compounds (放氮和偶联反应); 第三节 酰胺Amides (酸碱性、缩二脲反应) 第四节 含氮杂环化合物Heterocycles (反应活性比较) 第五节 生物碱Alkaloids P250/1, 4, 11, 15 教材:《有机化学》张生勇主编。高等教育出版社。 参考文献: 1.《基础有机化学》邢其毅等编。第二版,高等教育出版社。 2.《Organic Chemistry 》Stephen J. et al. Academic Press 3.《Fundamentals of Organic Chemistry 》(美)John McMurry 著 机械工业出版社 教学目的 (含重点,难点) 主 要 内 容 复习思考题 参 考文献 教 材 教研室意见
2 教 学 内 容 时间 分配 媒体选择 第九章 有机含氮化合物 含氮有机化合物 主要指分子中的氮原子和碳原子直接相连的化合物,也可以看成是烃分子中的一个或几个氢原子被含氮的官能团所取代的衍生物。例如,生物碱、蛋白质、磺胺类药物等。 本章主要讨论胺(amine)、重氮化合物(diazo compound)、偶氮化合物(azo compound)、酰胺(amide)、含氮杂环化合物和生物碱(alkaloid)。 第一节 胺Amines 一、胺的结构、分类和命名Structures, Classification and Nomenclature (一)胺的结构和分类 胺:可看作是氨分子中的氢原子被烃基取代所生成的化合物。 通式:R-NH 2,R 2NH 或R 3N ,其中R 代表烃基,它们分属于伯、仲和叔胺。 官能团: 氨基亚氨基次 氨基-NH 2 NH N R-N-R"R' 叔胺 (3°胺 ) R-NH-R'仲胺 (2°胺 ) R-NH 2伯胺 (1°胺 ) 季铵化合物(quaternary ammonium compound)可看成是铵盐或氢氧化铵(NH 2OH)分子中氮原子上的四个氢原子都被烃基取代生成的化合物,它们分别称为季铵盐和季铵碱。 季铵 盐 季铵 碱 R N X 4+-OH R N 4+- 注:伯、仲、叔胺或季铵化合物分子中的伯、仲、叔的含义与卤代烃或醇中的不同,它是指氮原子上连有一个、两个或是三个烃基,与连接氨基的碳是伯、仲还是叔碳原子没有关系。例如,叔丁醇是叔醇,而叔丁胺却是伯胺。 (二)命名Nomenclature 1. 普通命名法:按照分子中烃基的名称及数目叫做“某胺”,基字一般可以省略。如: CH 3-NH 2NH 2 甲胺 苯胺 CH 3-CH 2-NH 2 乙胺 80min 幻灯
第十四章 含氮有机化合物答案
第十四章含氮有机化合物 1.给出下列化合物名称或写出结构式。 (CH3)2CH NH2(CH3)2NCH2CH3 NH CH2CH3 CH3 NH CH3O2N NC N+NCl- O2N N N OH OH H32 H 对硝基氯化苄苦味酸 1,4,6-三硝基萘 答案: 3-氨基戊烷异丙基胺二甲基乙基胺 N-乙基苯胺N-甲基-3-甲基苯胺氯化-3-氰-5-硝基重氮苯 4-硝基-2,4-二羟基偶氮苯顺-4-甲基-1-环己胺 2.按其碱性的强弱排列下列各组化合物,并说明理由。 (1)
a b c NH 2 NH 2NH 2 NO 2 3 (2) CH 3C O NH 2 CH 3NH 2NH 3 a b c 答案: (1)c > a > b 苯环上存在推电子基团如甲基,可增加N 原子上的电子云密度,使其碱性增强;当苯环上连有拉电子基团如硝基,则降低N 上的电子云密度,使其碱性降低。 (2)b > c > a 在CH 3NH 2中由于—CH3的推电子作用,增强了碱性。在CH 3CONH 2中,由于p -π共轭而降低了N 上的电子云密度,使其碱性减弱。 3.比较正丙醇、正丙胺、甲乙胺、三甲胺和正丁烷的沸点高低并说明理由。 答案: 正丙醇 > 正丙胺 > 甲乙胺 > 三甲胺 > 正丁烷 分子间的氢键导致沸点升高。由于氧的电负性大于氮的电负性,因而正丁醇分子间能形成较强的氢键,沸点较高;正丙胺的氮原子上有两个氢可以形成氢键,甲已胺只有一个,而三甲胺氮原子上没有氢原子,因而不能形成氢键;正丁烷是非极性分子,分子间只存在较弱的色散力,因而沸点最低。 4. 如何完成下列的转变: (1) CH 2 CHCH 2Br CH 2 CHCH 2NH 2
第十五章 有机含氮化合物
有机化学课程教案编写日期:2006 年 11月 9日 章、节(或课题、单元)名称第十五章有机含氮化合物 授课学时 6 目的要求 l、掌握硝基化合物的结构、命名方法、性质、制法及其代表物。 2 能够运用诱导效应、共轭效应解释硝基使苯环上氯原子的亲核取代活性增加和使酚羟基的酸性增强的原因。 3、掌握胺的结构、分类、命名和氮原子的杂化状态;了解胺的物理性质;重点掌握胺的化学性质;掌握通过官能团相互转变制备胺的方法以及伯胺的特殊制法;了解苯胺、二甲胺、乙二胺和已二胺的性质、工业制法和用途。 4、了解季铵盐和季铵碱的性质以及季铵碱的热消除规律(Hofmann规则)。 5、掌握重氮盐的性质以及它们在有机合成上的应用。 6、了解偶氮化合物的结构和颜色的关系,以及染料的显色原理。 重点: 1、胺的碱性及其影响因素。 2、硝基对邻、对位上取代基的影响。 3、胺的制法:硝基物还原、醛酮还原胺化、Hoffmann降级、Gabriel法合成。 4、胺的化性:碱性,烷基化,酰基化,磺酰化,与HNO2作用,氧化,芳环上的取代反应。 5、重氮盐的制备及其在合成上应用。重氮盐的放氮反应、偶联反应。 6、N-H的伸缩振动吸收:3300-3600cm-1,伯胺出双峰,仲胺出单峰,叔胺不出峰。 7、腈和丙烯腈的制法、性质及应用。 难点: 1、胺的酰基化,磺酰化(Hinsber反应),胺与亚硝酸的反应及其应用。 2、重氮盐的制备及其在合成上应用。 教学组织 教学方法:课堂教学采用多媒体教学,以ppt为主。习题课采用黑板教学
与学生讨论相结合的方式。 作业:P526一(1~6)、三(2、6)、四(1、3)、五、六(1、3)、七、八、十、十一(2选做、3、7除外)、十六、十七、十八 参考书目文献: 1、张黯主编,有机化学教程下册,北京:高等教育出版社,1990.580~602 2、邢其毅等著,基础有机化学(第二版) 下册,北京:高等教育出版社,1994. 635~668,720~756 3、徐寿昌编,有机化学(第二版) ,北京:高等教育出版社,1993,360~399 5、袁履冰主编,有机化学,北京:高等教育出版社,1999, 339~367 授课小结 授课情况正常。
第十三章含氮化合物(6学时)
第十三章含氮化合物(6学时) 目标要求 1.掌握硝基化合物的性质 2.了解硝基化合物的制备 3.掌握季铵盐的性质及霍夫曼规则 4.了解胺的制法 5.掌握重氮化合物和偶氮化合物的结构 6.掌握重氮盐的取代反应和偶联反应及其在有机合成上的应用 7.掌握各类分子重排机理 教学重点: 硝基化合物、胺类化合物、重氮化合物,分子偶联反应、分子重排机理 教学难点: 硝基化合物、胺类化合物、重氮化合物,分子重排机理 主要内容 1.硝基化合物的性质及制备 2.胺的分类、结构和重要的化学性质 3.季铵盐的性质及霍夫曼规则 4.胺的制法 5.重氮化合物和偶氮化合物的结构 6.重氮盐的取代反应和偶联反应及其在有机合成上的应用 7.各类分子重排机理 胺可以看作是氨中的氢被烃基取代的衍生物。胺类和它们的衍生物是十分重要的化合物,其与生命活动有密切的关系。 第一节胺的分类和命名 一、胺的分类 1、根据胺分子中氮上连接的烃基不同,分为脂肪胺与芳香胺。 2、根据胺分子中与氮相连的烃基的数目,可分为一级、二级或三级胺。 3、根据胺分子中所含氨基的数目,可以有一元、二元或多元胺。 胺盐或氢氧化胺中的四个氢被烃基取代而生成的化合物称为季铵盐或碱。 NH2 CH3NH2 甲胺苯胺CH2CH2 NH2 NH2 乙二胺 [R4N]+ X-[R4N]+OH- 季胺盐季胺碱 二、胺的命名 1、简单的胺的命名可以用它们所含的烃基命名。 2、比较复杂的胺的是以烃基作为母体,氨基作为取代基来命名。 3、胺盐可看作是铵的衍生物。
(CH 3)2CHCH CH 3 2 CH 3CH 2CH CHCH 3 2H 5)2 CH 32-氨-3-甲基丁烷 2-(N,N-二乙氨基)-3-甲基戊烷 第二节 胺的物理性质 氨和胺分子具有四面体棱锥形结构。状态:甲胺、二甲胺、三甲胺是气体。低级胺是液体。 高级胺是固体。有氨的刺激性气味及腥臭味。芳胺的毒性很大。伯、仲胺能形成分子间氢键,也能与水形成氢键。 一、 溶解性 低级易溶于水,随烃基的增大,水溶解度降低。 二、 熔沸点 沸点:比相应的醇、酸低,并且伯胺 > 仲胺 > 叔胺;芳胺是高沸点液体或低熔点固体。 三、 光谱性质 (1)、红外光谱: N-H 键:在3500~3600cm-1有伸缩吸收峰。叔胺没有N-H 键,所以在该区域没有吸收峰。 C-N 键:1350~1000 cm-1有伸缩吸收峰。 (2)、核磁共振谱 : 胺的核磁共振特征类似于醇和醚。 氨基质子: δ 0.6~5.0,可变,不易鉴定。 α-碳上质子:δ 2.7~3.1 β-碳上质子:δ 1.1~1.7 第三节 胺的反应 一、 碱性 ?路易斯酸碱的定义:碱是电子对的给予体,酸是电子对的接受体。 N 原子有未共用的电子对,能接受质子,胺是路易斯碱,是亲核试剂。胺是弱碱,所以胺盐遇强碱则释放出游离胺,可分离提纯胺。 RNH 2+RNH 3Cl - H 2O NaCl +NaOH RNH 2++ 1、 胺的碱性: (1)Kb 值越大,或pKb 越小,碱性越强。 (2)从电子效应考虑,烷基愈多碱性愈强。 (3)从溶剂化考虑,烷基愈多碱性愈弱。 (4)还有立体效应的影响。 2、碱性秩序: (1) 脂肪胺 气态: Me 3N > Me 2NH > MeNH 2 > NH 3 水溶液中:Me 2NH > MeNH 2 > Me 3N > NH 3 (2)芳胺 < NH 3 < 脂肪胺 (3)芳胺:
第十四章 含氮有机化合物 习题
第十四章 含氮有机化合物 1、给出下列化合物名称或写出结构式。 三氨基戊烷 异丙基胺 NHCH 2CH 3 N-乙基苯胺 CH 3NHCH 3 N-甲基-3-甲基苯胺 NC N NCl O 2N 氯化-3-氰基-5-硝基重氮苯 O 2N N N HO OH 4`-硝基-2,4-二羟基偶氮苯 2H 3顺-4-甲基-1-环己烷 对硝基氯化苄 O 2N CH 2Cl 苦味酸 O 2N O 2N HO NO 2 1,4,6-三硝基萘 O 2N NO 2 NO 2 2、按其碱性的强弱排列下列各组化合物,并说明理由。
(1) NH2 NO2 NH2NH2 CH3 解: NH2 NO2 NH2 NH2 CH3 >> 因为甲基是供电子基,使氮上的电子云密度能增加,故胺的碱性增大,而硝基是吸电子基,使氮上的孤对电子密度减少,故碱性减小。 (2) CH3CONH2CH3NH2NH3 解: CH3CONH2 CH3NH2NH3 >> 在甲胺中,由于甲基供电子效应,使氮的电子云密度增大,碱性增强。在酰胺 中,由于氮上的孤对电子与羰基共轭,使氮上的电子云密度减小,从而碱性减弱。 3、比较正丙醇、正丙胺、甲乙胺、三甲胺和正丁烷的沸高低并说明理由。 解:正丙醇>正丙胺>甲乙胺>三甲胺>正丁烷 分子间的氢键导致沸点升高。由于氧的电负性大于氮的电负性,因而正丙醇分子间能形成较强的氢键,沸点最高;正丙胺的氮原子上有两个氢可以形成氢键,甲乙胺只有1个,而三甲胺氮原子上没有氢原子,因而不能形成氢键;正丁烷是非极性分子,分子间只存在较弱的色散力,因而沸点最低。 4、如何完成下列的转变: (1) CH2=CHCH2Br CH2=CHCH2CH2NH2 解:CH2=CHCH2Br CH2=CHCH2CH2NH2 4 CH2=CHCH2CN (2) 3 O 解:O 32 NCH3NHCH 3 2 (3) (CH3)3CCOOH(CH3)3COCH2Cl
基础有机化学第12章 有机含氮化合物习题答案
第十三章 有机含氮化合物习题答案 1. 命名下列化合物或写出构造式 (1)(2) (3) NHCH 3 CH 3 (CH 3)2CHNH 2 NHCH 2CH 3 (4)对硝基苄胺 (5)2,4,7-三硝基萘酚 (8) β-苯基丙胺 解: (1) 异丙基胺 (2) N-乙基苯胺 (3)N-甲基间甲苯胺 CH 2NH 2O 2N OH NO 2 NO 2 O 2N CHCH 2NH 2CH 3 (6) (5) (4) 2. 用化学方法鉴别下列各组化合物:乙醇、乙醛、乙酸、乙胺 乙醇乙醛乙酸 乙胺 NaHCO 3 气泡 乙酸 无气泡 银氨溶液 银镜 乙醛 无银镜乙醇 乙胺 乙醇 乙醛乙胺 NaNO 2乙胺 无气体 HCl 气体 乙醇 3. 按碱性强弱次序排列下列各组化合物 (1) A. 苯胺 B. 对甲基苯胺 C. 对甲氧基苯胺 D. 对硝基苯胺 (2) A. 苄胺 B. 间氯苄胺 C. 间甲苄胺 D. N 甲基苄胺 (1) C>B>A>D (2) D>C>A>B 4. 完成反应式。 (1) CH 3 (CH 3CO)2O CH 3 NO 2混酸 ,60℃ Fe +HCl CH 3NH 2 CH 3 NHCOCH 3 HNO 3 + H 2SO 4 CH 3 NHCOCH 3 NO 2 OH -/H 2O CH 3 NH 2 NO 2 CH 3 N 2+Cl -NO 2 CH 3 NO 2 NaNO 2/HCl 0-5℃ H 3PO 2 (2)CH 3CH 2CN (1)OH -/H 2O (2)H + CH 3CH 2COOH SOCl 2 CH 3CH 2COCl CH 3CH 2CO-NH(CH 2CH 2CH 3)2LiAlH 4(CH 3CH 2CH 2)2NH CH 3CH 2CH 2NH(CH 2CH 2CH 3)2 O 2N Cl Cl CH 3ONa/CH 3OH (3)O 2N Cl OCH 3 5. 完成下列转变
第十四章含氮有机化合物
·168· 第十四章 含氮有机化合物 学习要求 1.掌握芳香族硝基化合物的制法,性质。理解硝基对苯环邻对位取代基(X 、OH )性质的影响。 2.掌握胺的分类、命名和制法。 3.熟练掌握胺的性质及胺的碱性强弱次序,理解影响胺的碱性强弱的因素。 4.掌握区别伯、仲、叔胺的方法及氨基保护在有机合成中的应用。 5.掌握重氮盐的反应和偶联反应在有机合成中的应用。 6.了解季铵盐、季铵碱的性质和应用,初步了解偶氮染料。 7.学习、掌握重要的分子重排反应。 分子中含有C-N 键的有机化合物称为含氮有机化合物。含氮有机化合物种类很多,本章简单讨论硝基化合物,重点讨论胺、重氮盐和分子重排反应。 §14-1 硝基化合物 硝基化合物一般写为R-NO 2 ,Ar-NO 2 ,不能写成R-ONO (R-ONO 表示硝酸酯)。 一、分类、命名、结构 1. 分类 (略) 2. 命名 (与卤代烃相次似) 3. 硝基的结构 一般表示为 (由一个N=O 和一个N →O 配位键组成) 物理测试表明,两个N —O 键键长相等,这说明硝基为一P-π共轭体系(N 原子是以sp 2 杂化成键的,其结构表示如下: 二、硝基化合物的制备 见P 430。 1. 卤代烃与亚硝酸盐反应。 2. 芳烃的硝化。 三、硝基化合物的性质 1.物理性质 (略) 2.脂肪族硝基化合物的化学性质 (1)还原 硝基化合物可在酸性还原系统中(Fe 、Zn 、 Sn 和盐酸)或催化氢化为胺。 (2)酸性 硝基为强吸电子基,能活泼α- H ,所以有α- H 的硝基化合物能产生假酸式-酸式互变异构,从而具有一定的酸性。 例如硝基甲烷、硝基乙烷、硝基丙烷的pKa 值分别为:10.2、8.5、7.8 。 N O R
大学有机化学总结之含氮化合物
第十四章 含氮有机化合物 学习要求 1.掌握芳香族硝基化合物的制法,性质。理解硝基对苯环邻对位取代基(X 、OH ) 性质的影响。 2.掌握胺的分类、命名和制法。 3.熟练掌握胺的性质及胺的碱性强弱次序,理解影响胺的碱性强弱的因素。 4.掌握区别伯、仲、叔胺的方法及氨基保护在有机合成中的应用。 5.掌握重氮盐的反应和偶联反应在有机合成中的应用。 6.了解季铵盐、季铵碱的性质和应用,初步了解偶氮染料。 7.学习、掌握重要的分子重排反应。 分子中含有C-N 键的有机化合物称为含氮有机化合物。含氮有机化合物种类很多, 本章简单讨论硝基化合物,重点讨论胺、重氮盐和分子重排反应。 §14.1 硝基化合物 硝基化合物一般写为R-NO 2 ,Ar-NO 2 ,不能写成R-ONO (R-ONO 表示硝酸酯)。 14.1.1 分类、命名、结构 1.分类 (略) 2.命名 (与卤代烃相次似) 3.硝基的结构 一般表示为N=O 和一个N →O 配位键组成)物理测试表明,两个 N —O 键键长相等,这说明硝基为一P-π共轭体系(N 原子是以sp 2杂化成键的,其结构表 示如下: N O R
14.1.2 硝基化合物的制备 见P 430。 1.卤代烃与亚硝酸盐反应。 2.芳烃的硝化。 14.1.3 硝基化合物的性质 1.物理性质 (略) 2.脂肪族硝基化合物的化学性质 (1)还原 硝基化合物可在酸性还原系统中(Fe 、Zn 、Sn 和盐酸)或催化氢化为 胺。 (2)酸性 硝基为强吸电子基,能活泼α- H ,所以有α- H 的硝基化合物能产生假酸式-酸式互 变异构,从而具有一定的酸性。例如硝基甲烷、硝基乙烷、硝基丙烷的pKa 值分别为: 10.2、8.5、7.8 。 (3)与羰基化合物缩合 有α- H 的硝基化合物在碱性条件下能与某些羰基化合物起缩合反应。 R CH 2N O O R CH N OH O NaOH R CH N O O Na 假酸式 酸式(主)(较少) R CH 2NO 2R'C O H (R'' ) +OH R'C OH H (R'' ) C NO 2 R'H R'C H (R'' ) C NO 2 R'
第十四章 含氮有机化合物剖析
第十四章含氮有机化合物 第一节硝基化合物 一、硝基化合物的命名与结构 分子中含有硝基(-NO2)的化合物称为硝基化合物。RNO2或ArNO2。它的命名类似卤代烃.根据硝基化合物具有较高的偶极矩,键长测定两个氧原子和氮原子之间的距离相等,从价键理论观点看,氮原子的sp2杂化轨道形成三个共平面的σ键,未参加杂化的一对电子的p轨道与每个氧原子的p轨道形成共轭体系,因此,硝基化合物的分子结构可以表示如下: 共振结构式: 氮带一个正电荷,每个氧各带?负电荷,这与硝基化合物高的偶极矩相联系。根据R的不同,偶极矩在3.5D 和4.0D之间,由于硝基化合物的偶极特征,结果比相同分子量的酮沸点高(挥发慢)。如硝基甲烷(MW61)沸点101℃,丙酮(MW58)沸点56℃。意外地,在水中溶解度低,在水中硝基甲烷的饱和溶液,以重量计少于10%,而丙酮完全溶于水。 二硝基化合物的制备 1.烷烃的硝化:烷烃可与硝酸进行气相或液相硝化,生成硝基烷烃。其中以气相硝化更具有工业生产价值.烷烃的硝化是以游离基历程进行的: 烷烃的碳骼对硝化速度具有一定的影响,活性次序为:叔C-H > 仲C-H > 伯C-H 。在高温气相硝化,产物为混合物。 2.亚硝酸盐的烃化 ①与卤代烃:
两者的比例与卤代烃的结构有关,生成硝基烷烃比例为:伯卤代烃〉仲卤代烃〉叔卤代烃;卤代烃中卤素被取代的难易是:I>Br>Cl>F i 卤代烃与亚硝酸银的反应: ii 卤代烷与亚硝酸锂(钠、钾)反应 实际上硝基化合物和亚硝酸酯两者同时生成,在DMF和DMSO中,硝基化合物为主要产物。所以,这个反应是制备脂肪和脂环族硝基化合物的简单有效方法。这个反应能进行的关键是亚硝酸碱金属盐和卤代烷都有一定量溶解在溶剂中,常用溶剂为DMF、DMSO。 ②与α-氯代羧酸: 3.芳烃的硝化:
第十二章有机含氮化合物
第十二章有机含氮化合物 【教学重点】 胺类化合物的化学性质、重氮和偶氮化合物。 【教学难点】 季铵碱的热分解。 【教学基本内容】 硝基化合物的结构;硝基化合物的化学性质(α-氢的活泼性、还原反应、硝基对苯环的影响)。 胺的结构;胺的制备方法(氨或胺的烃基化、腈和酰胺的还原、醛和酮的氨化还原、酰胺的降解、硝基化合物的还原、Gabriel合成法);胺的化学性质——碱性及影响碱性强度的因素、烃基化、酰基化、磺酰化、与亚硝酸反应、芳环上的取代反应。 季铵盐和季铵碱、季铵碱的热分解。 重氮盐的制备方法及重氮盐的结构;重氮盐的化学性质(放氮反应、保留氮的反应)及在合成上的应用。 Ⅰ目的要求 前面我们已经讨论了烃、卤代烃和烃的含氧衍生物,本章对含氮有机化合物加以讨论。 从广义上讲,分子中含有氮元素的有机化合物统称为含氮有机化合物。常见的含氮有机化合物有如下几种类型:硝酸酯(-ONO2)、亚硝酸酯(-ONO)、酰胺、肼、腙、肟(以上几类以在前面有关章节中加以介绍);硝基(-NO2)、亚硝基(-NO)、胺(-NH2、-NHR、- ⊕ NR2)、腈(-C≡N)、异腈(-N≡C)、异氰酸酯(-N=C=O)、重氮化合物(-N≡N-Y)偶氮化合物(-N=N-)。这些都是着重讨论的化合物。生命的基础物质—氨基酸和蛋白质,甚至连含氮的杂环化合物也认为是属于含氮化合物的范围,由于它们在天然化合物中占有重要地位,另有专章讨论。 通常所说的含氮化合物是指含有碳氮键的化合物。它们可以看作是烃分子中氮原子被含氮官能团取代的产物。含氮有机物比含氧化合物的种类还要多。本章重点介绍硝基化合物、胺、重氮和偶氮化合物。 本章学习的具体要求: 1、了解硝基化合物的主要性质; 2、掌握胺的分类、结构及其性质; 3、在掌握重氮化,偶合等重要反应的基础上,熟悉它们在有机合成上的重要应用。 4、掌握季铵盐在相转移催化反应中的应用,以及季铵碱受热反应的规律。 5、了解腈、异氰酸酯。 在含氮化合物的学习中,特别要注意含氮官能团的特征及其变化,因为氮原子在化合物中的价态是有变化的。这是含氧化合物所没有的现象。
生物化学习题集:第八章 含氮化合物代谢
第八章含氮化合物代谢 一、知识要点 蛋白质和核酸是生物体中有重要功能的含氮有机化合物,它们共同决定和参与多种多样的生命活动。在自然界的氮素循环中,大气是氮的主要储库,微生物通过固氮酶的作用将大气中的分子态氮转化成氨,硝酸还原酶和亚硝酸还原酶也可以将硝态氮还原为氨,在生物体中氨通过同化作用和转氨基作用等方式转化成有机氮,进而参与蛋白质和核酸的合成。 (一)蛋白质和氨基酸的酶促降解 在蛋白质分解过程中,蛋白质被蛋白酶和肽酶降解成氨基酸。氨基酸用于合成新的蛋白质或转变成其它含氮化合物(如卟啉、激素等),也有部分氨基酸通过脱氨和脱羧作用产生其它活性物质或为机体提供能量,脱下的氨可被重新利用或经尿素循环转变成尿素排出体外。 (二)氨基酸的生物合成 转氨基作用是氨基酸合成的主要方式。转氨酶以磷酸吡哆醛为辅酶,谷氨酸是主要的氨基供体,氨基酸的碳架主要来自糖代谢的中间物。不同的氨基酸生物合成途径各不相同,但它们都有一个共同的特征,就是所有氨基酸都不是以CO2和NH3为起始原料从头合成的,而是起始于三羧酸循环、糖酵解途径和磷酸戊糖途径的中间物。不同生物合成氨基酸的能力不同,植物和大部分微生物能合成全部20种氨基酸,而人和其它哺乳动物及昆虫等只能合成部分氨基酸,机体不能合成的氨基酸称为必须氨基酸,人有八种必需氨基酸,它们是:Lys、Trp、Phe、V al、Thr、Leu、Ile和Met。 (三)核酸的酶促降解 核酸通过核酸酶降解成核苷酸,核苷酸在核苷酸酶的作用下可进一步降解为碱基、戊糖和磷酸。戊糖参与糖代谢,嘌呤碱经脱氨、氧化生成尿酸,尿酸是人类和灵长类动物嘌呤代谢的终产物。其它哺乳动物可将尿酸进一步氧化生成尿囊酸。植物体内嘌呤代谢途径与动物相似,但产生的尿囊酸不是被排出体外,而是经运输并贮藏起来,被重新利用。 嘧啶的降解过程比较复杂。胞嘧啶脱氨后转变成尿嘧啶,尿嘧啶和胸腺嘧啶经还原、水解、脱氨、脱羧分别产生β-丙氨酸和β-氨基异丁酸,两者经脱氨后转变成相应的酮酸,进入TCA循环进行分解和转化。β-丙氨酸还参与辅酶A的合成。 (四)核苷酸的生物合成 生物能利用一些简单的前体物质从头合成嘌呤核苷酸和嘧啶核苷酸。嘌呤核苷酸的合成起始于5-磷酸核糖经磷酸化产生的5-磷酸核糖焦磷酸(PRPP)。合成原料是二氧化碳、甲酸盐、甘氨酸、天冬氨酸和谷氨酰氨。首先合成次黄嘌呤核苷酸,再转变成腺嘌呤核苷酸和鸟嘌呤核苷酸。嘧啶核苷酸的合成原料是二氧化碳、氨、天冬氨酸和PRPP,首先合成尿苷酸,再转变成UDP、UTP和CTP。 在二磷酸核苷水平上,核糖核苷二磷酸(NDP)可转变成相应的脱氧核糖核苷二磷酸。催化此反应的酶为核糖核苷酸还原酶系,此酶由核苷二磷
第十三章含氮有机化合物
第十三章含氮有机化合物 【教学目的】 1、掌握一般胺和酰胺的命名,胺的碱性与酰胺的水解, 2、了解重要的杂环母核 【教学重点】 胺和酰胺的命名,胺的碱性与酰胺的水解 【教学难点】 酰胺的水解 【教学方法】 讲解,练习 【教学内容】 含氮有机化合物通常是指氮原子和碳原子直接相连而构成的有机化合物。主要有胺、酰胺、偶氮化合物、生物碱、含氮杂环化合物、氨基酸、硝基和亚硝基化合物等。 第一节胺 一、胺的结构和分类 (一)胺的结构 胺(amine)是氨(NH3)分子中的氢原子被烃基取代的产物。胺的结构与氨相似,氮原子为不等性sp3杂化,胺分子中的氮原子与碳的四面体结构相类似,但不是正四面体。 (二)胺的分类 胺分子中的氮原子上连有1个、2个和3个烃基的胺分别称为伯胺(1°胺)、仲胺(2°胺)和叔胺(3°胺)。 NH3 RNH2 R2NH R3N 氨伯胺(1°) 仲胺(2°) 叔胺(3°) 胺分子中的氮原子与脂肪烃基相连的为脂肪胺(aliphatic amine),与芳环直接相连的为芳香胺(aromatic amine)。例如: 脂肪胺:CH3NH2CH2NH CH3 CH2CH3 CH2CH3 N CH3 芳香胺:H2N NH2NH N(CH3)2 H3C 伯胺仲胺叔胺 氨基 (一NH2)、亚氨基(NH )和次氨基( N ),分别是伯、仲、叔胺的官能团。 胺的伯、仲、叔胺的分类与醇的伯、仲、叔醇的分类有差异。叔胺指氮原子上连有3个烃基,而叔醇是指羟基与叔碳原子相连。例如:
C CH 3 CH 3 CH 3 NH 2 C CH 3 CH 3CH 3 OH 伯胺 叔醇 相应于氢氧化铵和铵盐的四烃基取代物,分别称为季铵碱和季铵盐 R 4N + OH - R 4N +X - 季铵碱 季铵盐 二、胺的命名 简单胺的命名以胺为母体,例如: CH 3NH 2 (CH 3CH 2)2NH N CH(CH 3)2 CH 3 CH 2CH 3 CH 3CH 2CHCH 2CHCH 3 2 2 甲胺 二乙胺 甲乙异丙胺 2,4-己二胺 NH 2 NH NH 2 O 2N NH 2 苯胺 二苯胺 对-硝基苯胺 β-萘胺 若芳香胺的氮原子上连有脂肪烃基,命名时常以芳香胺为母体,在脂肪烃基名称前标上“N ”,例如: NHCH 3 N(CH 3)2 N CH 2CH 3 CH 3 CH 2CH 2CH 3 N-甲基苯胺 N ,N-二甲基苯胺 N-甲基-N-乙基丙胺 结构复杂的胺可以烃或其他官能团为母体,氨基做取代基来命名。例如: CH NH 2 CH 3 CH 2 CH CH 3 CH 3 (CH 3)2N CHO CH 3CHCH 2CH 2CHCH 3 NHCH 3 2NH 2 2-甲基-4-氨基戊烷 4-二甲氨基苯甲醛 2-氨甲基-5-甲氨基己烷 季铵盐、季铵碱的命名类似无机铵类化合物。例如: NH 4C1 (C 2H 5)4N + Br - HOCH 2CH 2N + (CH 3)3OH - 氯化铵 溴化四乙铵 氢氧化羟乙基三甲基铵(胆碱) 命名胺类化合物时应注意“氨”、“胺”、“铵”字的用法。表示基团时用“氨”,如氨基、亚氨基、甲氨基(CH 3NH-)、氨甲基(H 2NCH 2-)等;表示氨的烃类衍生物时用“胺”;表示季铵类化物或胺的盐时用“铵”。 三、胺的性质
物理化学第12章 含氮化合物
第十二章 含氮化合物 12.1 写出分子式为C 4H 11N 的胺的各种异构体,命名,并指出个属哪级胺。 答案: CH 3CH 2CH 2CH 2NH 2 CH 3CHCH 2NH 2 CH 3CH 3CH 2CHNH 2 CH 3 正丁胺(伯胺或一级胺)仲丁胺(伯胺或一级胺) 异丁胺(伯胺或一级胺) CH 3CH 2CH 2NHCH 3 CH 2CNH 2 CH 3 CH 3CH 3CH 2N(CH 3)2 二甲乙胺(叔胺或三级胺) 甲丙胺(仲胺或二级胺)叔丁胺(伯胺或一级胺) 12.2 命名下列化合物或写出结构式 a.CH 3CH 2NO 2 b.NO H 3C c. NHC 2H 5 d.H 3C N 2+Br - e. Br NHCOCH 3 f. CH 3CH 2CH 2CN g.NHNH 2 O 2N h.H 2NCH 2(CH 2)4CH 2NH 2 i. NH O O j.(CH 3CH 2)2N -NO k. C 6H 5CH 2N CH 3 CH 3 C 12H 25 + Br - l.胆碱 m. 多巴胺 n. 乙酰胆碱 o.肾上腺素 p.异丁胺 q.胍 r.CH 3CH 2N(CH 3)2 答案: a. 硝基乙烷 b. p —亚硝基甲苯 c. N -乙基苯胺 d. 对甲苯重氮氢溴酸盐或溴化重氮对甲苯 e. 邻溴乙酰苯胺 f. 丁腈 g. 对硝基苯肼 h. 1,6-己二胺 i. 丁二酰亚胺 j. N-亚硝基二乙胺 k. 溴化十二烷基苄基二甲铵
[(CH 3)3N +CH 2CH 2OH]OH - m.HO l.-CH 2CH 2NH 2 HO - n.[(CH 3)3N +CH 2CH 2OCOCH 3]OH - o.HO HO CH(OH)CH 2NHCH 3 p.(CH 3)2CHCH 2NH 2 r.N,N -二甲基乙胺 q.H 2N-C-NH 2 NH 12.3 下列哪个化合物存在对映异构体? a. CH 3NHCH 2CH 2Cl b. (CH 3)2N +(CH 2CH 2Cl)2Cl - c. N CH 3 d. CH 2CHCH 3 NH 2 答案: a, d 存在。但a 的对映异构体在通常条件下很容易相互转化。 12.4 写出下列体系中可能存在的氢键: a. 二甲胺的水溶液 b. 纯的二甲胺 答案: O H H O H N H 3C H 3C H O N H 3C H 3C H H 3C H 3C H 3 H 3 Ⅰ Ⅱ Ⅲ a.中有 Ⅲ Ⅱ Ⅰ Ⅰ三种氢键 b. 中只有一种氢键 H H 12.5 如何解释下列事实? a. 苄胺(C 6H 5CH 2NH 2)的碱性与烷基胺基本相同,而与芳胺不同。 b. 下列化合物的pK a 为 O 2N NH 2 NH 2 H 3C NH 2 pK b =13.0 pK b =9.37 pK b =8.70 答案: a. 因为在苄胺中,N未与苯环直接相连,其孤对电子不能与苯环共轭,所以碱性与烷基 胺基本相似。
