乙醇-丙醇气液平衡数据相图
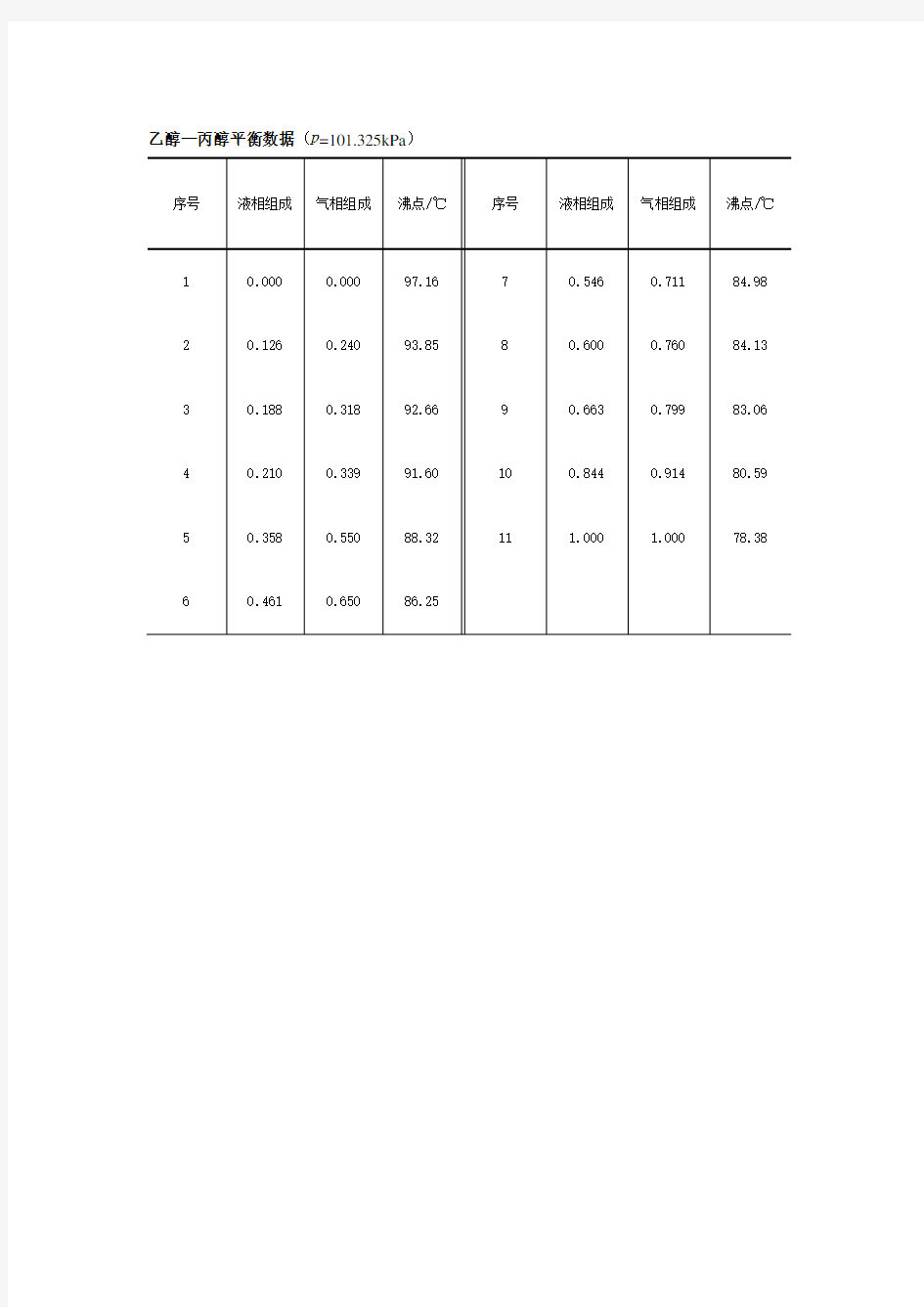
乙醇—丙醇平衡数据(p=101.325kPa)
二元液系气液平衡相图
实验二二元液系气液平衡相图 一、实验目的 1、了解环己烷—乙醇系的沸点—组成图 2、由图上得出其最低恒沸温度及最低恒沸组成(含乙醇%) 3、学会使用数字阿贝折射仪 4、学会使用WTS—05数字交流调压器 二、原理 一个完全互溶双液体系的沸点—组成图,表明在气液二相平衡时沸点和二相成分间的关系,它对了解这一体系对行为及分馏过程都有很大的实用价值。 在恒压下完全互溶双液系的沸点与组分关系有下列三种情况:1、溶液沸点介于二纯组分之间;2、溶液有最高恒沸点;3、溶液有最低恒沸点。 图1表示有最低恒沸点,本次实验图形也像如此的样子,A′LB′代表液相线的交点表示在该温度时互成平衡的二相的成份。 绘制沸点—成份图的简单原理如下:当总成份为X的溶液开始蒸馏时,体系的温度沿虚线上升,开始沸腾时成份为Y的气相生成。若气相量很少,x、y二点即代表互成平衡时液气二相成份。继续蒸馏,气相量逐渐增多,沸点沿虚线继续上升,气液二相成份分别在气相和液相线上沿箭头指示方向变化。当二相成份达到某一对数值x′和y′,维持二相的量不变,则体系气液二相又在此成份达到平衡,而二相的物质数量按杠杆原理分配。 本实验利用回流的方法保持气液二相相对量一定,则体系温度恒定。待二相平衡后,取出二相的样品,用阿贝折光仪测定其折射率。得出该温度下气液二相平衡成份的坐标点,改变体系的总成份,再用上法找出一对坐标点,这样测得若干坐标点后,分别按气相点和液相点连成气相线和液相线,即得T—X平衡图。 三、步骤 1、安装接通仪器,打开冷凝水; 2、加入环己烷20ml,蒸馏至沸腾,待小兜有液体后回流三次,温度平衡2—3分钟基本不变,记下温度,关闭调压器; 3、A组加入乙醇0.5ml,用上法测定温度,然后关闭调压器,取出气相,液相的样品,测其折射率,以后分别加入1.0,2.0,4.0,8.0,12.0ml乙醇;
分离乙醇正丙醇混合液的精馏塔设计课程设计共46页word资料
TOC \o "1-3" \h \u 一设计任务书.. PAGEREF _Toc7399 2 二塔板的工艺设计 (5) (一)设计方案的确定 (5) (二)精馏塔的物料衡算 (5) 1.原料液及塔顶、塔釜产品的摩尔分数 (5) 2. 物料衡算 (6) (三)物性参数的计算 (6) 1.操作温度的确定 (7) 2. 密度的计算 (7) 3.混合液体表面张力的计算 (11) 4.混合物的粘度 (12) 5.相对挥发度 (13) (四)理论板数及实际塔板数的计算 (14) 1.理论板数的确定 (14) 2.实际塔板数确定 (18) (五)热量衡算 (18) 1.加热介质的选择 (18)
2. 冷却剂的选择: (19) 3.比热容及汽化潜热的计算 (19) (六)塔径的初步设计 (23) 1.汽液相体积流量的计算 (23) 2.塔径的计算与选择 (23) (七)溢流装置 (25) 1.堰长 (25) 2.弓形降液管的宽度和横截面积 (25) 3.降液管底隙高度 (26) 4.塔板分布 (26) 5. 浮阀数目与排列 (26) (八)汽相通过浮阀塔板的压降 (29) 1.精馏段 (29) 2.提馏段 (30) (九)淹塔 (30) 1.精馏段 (30) 2.提馏段 (31) (十)雾沫夹带 (31)
(十一)塔板负荷性能图 (32) 1.雾沫夹带线 (32) 2.液泛线 (34) 3.液相负荷上限线 (35) 4.漏液线 (35) 5.液相负荷下限线 (35) 三、塔总体高度计算 (38) 1.塔顶封头 (39) 2.塔顶空间 (39) 3.塔底空间 (39) 5.进料板处板间距 (40) 6.裙座 (40) 四、塔的接管 (40) 1.进料管 (40) 2.回流管 (41) 3.塔底出料管 (41) 4.塔顶蒸汽出料管 (41) 5.塔底蒸汽管 (42)
双液系气液平衡相图的绘制(华南师范大学物化实验)
双液系气-液平衡相图的绘制 一、实验目的 (1)用回流冷凝法测定沸点时气相与液相的组成,绘制双液系相图。找出恒沸点混合物的组成及恒沸点的温度。 (2)掌握测定双组分液体的沸点及正常沸点的测定方法。 (3)了解阿贝折射计的构造原理,熟悉掌握阿贝折射计的使用方法。 二、实验原理 2.1液体的沸点 液体的沸点是液体饱和蒸汽压和外压相等时的温度,在外压一定时,纯液体的沸点有一个确定值。 2.2双液系的沸点 双液系的沸点不仅与外压有关,而且还与两种液体的相对含量有关。理想的二组分体系在全部浓度范围内符合拉乌尔定律。结构相似、性质相近的组分间可以形成近似的理想体系,这样可以形成简单的T-x (y )图。大多数情况下,曲线将出现或正或负的偏差。当这一偏差足够大时,在T-x (y )曲线上将出现极大点(负偏差)或极小点(正偏差)。这种最高和最低沸点称为恒沸点,所对应的溶液称为恒沸混合物。 恒定压力下,真实的完全互溶双液系的气-液平衡相图(T -x ),根据体系对拉乌尔定律的偏差情况,可分为3类: (1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(a)所示。 (2)最大负偏差:存在一个最小蒸汽压值,比两个纯液体的蒸汽压都小,混合物存在着最高沸点,如盐酸—水体系,如图1(b)所示。 (3)最大正偏差:存在一个最大蒸汽压值,比两个纯液体的蒸汽压都大,混合物存在着最低沸点,如水-乙醇体系,如图1(c))所示。 图1. 二组分真实液态混合物气—液平衡相图(T-x 图) 考虑综合因素,实验选择具有最低恒沸点的乙醇-乙酸乙酯双液系。根据相平衡原理,对二组分体系,当压力恒定时,在气液平衡两相区,体系的自由度为1。若温度一定时,则气液亮相的组成也随之而定。当溶液组成一定时,根据杠 t A t A t A t B t B t B t / o C t / o t / o x B x B x B A B A A B B (a) (b) (c)x ' x '
二元液系相图(实验数据分析)
实验名称:二元液系相图 学院:XXXXXXXXXX 班级:XXXXXXXXX 姓名(学号):XXX(XXXXXXXX) 指导教师:XXX 实验时间:XXXXXXXXXXXXXX
二元液系相图 一、实验目的 1.测定环己烷-乙醇系统的沸点组成图(T-X图)。 2.掌握阿贝(Abbe)折光仪的使用方法。 二、实验原理 两种液态物质以任何比例混合都形成均相溶液的系统称这完全 互中溶双液系。在恒定压力下溶液沸点与平衡的气液相组成的关系,可用沸点-组成图(t-x图)表示。 完全互溶双液系的沸点-组成图可分为两三种: 一种为最简单的情况,溶液沸点介于两个纯组分沸点之间,如图6-1所示。纵坐标表示温度,横坐标表示组分B的摩尔分数(x B,y B)。下面一条曲线表示气液平衡时温度(即溶液沸点)与液想组成的关系,称液相线(T-x线)。上面的线表示平衡温度与气相组成的关系,称气相线(T-y线)。若总组成为Z B的系统在压力p及温度t时达到气液两相平衡,其液相组成为x B气相组成为y B(见图6-1)。 另两种类型为具有恒沸点的完全互溶双液系统气液平衡相图,如图6-2所示。其中(a)为具有低恒沸点相图,(b)为具有高恒沸点相图。这两类相图中气相线与液相线在某处相切。相切点对应的温度称为恒沸温度,对应组成的混合物称恒沸混合物。恒沸混合物在恒沸点达气液平衡,平衡的气、液组成相同。同一双液系在不同压力下,恒沸点及恒沸混合物是不同的。
本实验绘制环己烷-乙醇二元液系的T-X图。其方法为将不同组成的溶液于蒸馏仪中进行蒸馏,沸腾平衡后记下温度,依次吸取少量的蒸馏液和蒸出液。分别用阿贝折光计测定其折射率,然后由环己烷-乙醇的折射率-组成标准曲线或其数据表确定相应组成,从而绘制环己烷-乙醇二元液系相图。 三、仪器和试剂 沸点测定仪;取样管;阿贝折光仪。 环己烷(分析纯);无水乙醇(分析纯);环己烷摩尔分数分别为0.2、0.4、0.6、0.8的乙醇溶液。 四、实验步骤 1.纯液体折光率的测定 分别测定乙醇和环己烷的折光率。 2.标准曲线的绘制 测定环己烷摩尔分数分别为0.2、0.4、0.6、0.8的乙醇溶液的折光率,绘制标准曲线。 3.测定沸点-组成数据 1)安装沸点测定仪。 2)溶液配制。 粗略配制环己烷质量百分数分别为0.05、0.1、0.2、0.45、0.55、0.6、0.7、0.8、0.9等组成的环己烷-乙醇溶液约50ml。
二组分系统气液平衡相图的绘制(含数据)
二组分系统气液平衡相图的绘制 一实验目的 1.确定不同组成的环己烷——乙醇溶液的沸点及气、液两相的平衡浓度,由此绘制其沸点组成图。 2.掌握阿贝折射仪的原理及使用方法。 二实验原理 本实验用回流冷凝法测定不同浓度的环己烷——乙醇溶液的沸点和气、液两相的组成,从而绘制T----x图。 下图为环己烷——乙醇的沸点组成图的大致形状,ADC和BEC为气相线,AD′C和BE′C 为液相线。体系总组成为x的溶液开始沸腾时,气象组成为y ,继续蒸馏,气相量增加,液相量减少(总量不变),溶液温度上升,回流作用,控制了两相的量一定,沸点一定。此时,气相组成为y′,与其平衡的液相组成为x′,体系的平衡沸点为t沸,此时气液两相服从杠杆原理。 当压力一定时,对两相共存区进行相律分析:独立组分K=2,相数P=2,则自由度f=K-P+1=2-2+1=1 即有,体系温度一定,则气液两相成分确定。总量一定时,亮相的量也一定。在一实验装置中,控制气液两相的相对量一定,使体系温度一定, 则气液组成一定。 用精密温度计可以测出平衡温度,取出气液两相样品 测定其折射率可以求出其组成。折射率和组成有一一对应 关系,可以通过测定仪系列已知组成的样品折射率,绘出 工作曲线。测出样品就可以从工作曲线上找到未知样品的 组成。 三仪器与药品 仪器:阿贝折射仪、超级恒温槽、蒸馏瓶、调压 变压器、1/10℃刻度温度计、25ml移液管一支、5ml、 10ml移液管各两支、锥形瓶四个、滴管若干支 药品:环己烷、乙醇、丙酮 四实验步骤 1.工作曲线的测定 把超级恒温槽调至25℃,连接好恒温槽与阿贝折 射仪,使恒温水流经折射仪。 准确配制下列溶液,测定纯环己烷,乙醇和下列 溶液的折射率,并测定溶液温度。 环己烷 1 2 3 4ml 乙醇 4 3 2 1ml 2.测定环己烷的沸点 按图装好仪器,调压变压器调至最小,将25ml苯加入蒸馏瓶,打开冷凝水,接通电源,
乙醇和正丙醇物系分离系统的设计
北京理工大学珠海学院 课程设计任务书 2011 ~2012学年第一学期 学生姓名:谢威宁专业班级:09化工1班 指导教师:李青云工作部门:化工与材料学院 一、课程设计题目乙醇和正丙醇物系分离系统的设计 二、课程设计内容(含技术指标) 1.设计条件 生产能力:25000吨/年(每年按300天生产日计算) 原料状态:苯含量40%(wt%);温度:25℃;压力:100kPa;泡点进料; 分离要求:塔顶馏出液中苯含量99%(wt%);塔釜苯含量2%(wt%)操作压力:100kPa 其它条件:塔板类型:浮阀塔板;塔顶采用全凝器;R=1.9R m 2.具体设计内容和要求 (1)设计工艺方案的选定 (2)精馏塔的工艺计算 (3)塔板和塔体的设计 (4)水力学验算 (5)塔顶全凝器的设计选型 (6)塔釜再沸器的设计选型 (7)进料泵的选取 (8)绘制流程图 (9)编写设计说明书 (10)答辩
三、进度安排 时间设计安排 10.26—10.28 设计动员,下达任务书,查阅资料,拟定设计方案,方案论证,物性数据计算 10.28—11.11 工艺计算(物料衡算、确定回流比、计算理论板层数、实际板层数、实际进料板位置) 11.11—11.18 塔结构设计(物性数据的计算、塔径计算、塔结构尺寸的计算、水力学性能校验、负荷性能图及塔高的计算) 11.18—11.25 热量衡算;附属设备的选型和计算 11.25-12.02 绘制带控制点的工艺流程图(CAD图) 12.02—12.09 绘制带控制点的工艺流程图,(借图板和丁字尺,手工绘制图)12.09—12.16 编写设计说明书,答辩要求 2012.01.03 将说明书及图纸装订并提交 2012.1.4—1.5 答辩 四、基本要求 序号设计内容要求 1 设计工艺方案的选定精馏方式及设备选型等方案的选定和论证(包括 考虑经济性;工艺要求等)绘制简单流程图 2 精馏塔的工艺计算物料衡算,热量衡算,回流比、全塔效率、实际 塔板数、实际进料位置等的确定 3 塔板和塔体的设计设计塔高、塔径、溢流装置及塔板布置等 4 水力学验算绘制塔板负荷性能图 5 塔顶全凝器的设计选型计算冷凝器的传热面积和冷却介质的用量 6 塔釜再沸器的设计选型计算再沸器的传热面积和加热介质的用量 7 进料泵的选取选取进料泵的型号 8 绘图绘制带控制点的流程图(CAD和手工绘制) 9 编写设计说明书目录,设计任务书,设计计算结果,流程图,参 考资料等 10 答辩每班数不少于20人答辩 教研室主任签名: 2011年10 月14 日
【清华】实验2_双液系的气液平衡相图_2006011835
`` 实验2 双液系的气液平衡相图 唐盛昌2006011835 分6 同组实验者:徐培 实验日期:2008-10-9,提交报告日期:2008-10-23 带实验助教:尚培华 1 引言(简明的实验目的/原理) 实验目的: 1.用沸点仪测定在常压下环已烷—乙醇的气液平衡相图。 2.掌握阿贝折射仪的使用方法。 实验原理: 将两种挥发性液体混合,若该二组分的蒸气压不同,则溶液的组成与其平衡气相的组成不同。在压力保持一定,二组分系统气液达到平衡时,表示液态混合物的沸点与平衡时组成关系的相图,称为沸点和组成(T-x)图。沸点和组成(T-x)的关系有下列三种:(1)理想液体混合物或接近理想液体混合物的双液系,其液体混合物的沸点介于两纯物质沸点之间见图5—1(a);(2)各组分蒸气压对拉乌尔定律产生很大的负偏差,其溶液有最高恒沸点见图5—1(b);(3)各组分蒸气压对拉乌尔定律产生很大的正偏差,其溶液有最低恒沸点见图5—1(c)。第(2)、(3)两类溶液在最高或最低恒沸点时的气液两相组成相同,加热蒸发的结果只使气相总量增加,气液相组成及溶液沸点保持不变,这时的温度称恒沸点,相应的组成称恒沸组成。第一类混合物可用一般精馏法分离出这两种纯物质,第(2)、(3)类混合物用一般精馏方法只能分离出一种纯物质和另一种恒沸混合物。 图1 沸点组成图 为了测定二元液系的T-x图,需在气液达到平衡后,同时测定溶液的沸点、气相和液相组成。 本实验是测定具有最低恒沸点的环己烷—乙醇双液系的T-x图。方法是用沸点仪(图2)直接测定一系列不同组成之溶液的气液平衡温度(即沸点),并收集少量馏出液(即气相冷凝液)及吸取少量溶液(即液相),分别用阿贝折射仅测定其折射率。为了求出相应的组成,必须先测定已知组成的溶液的折射率,
二组分真实液态混合物的气—液平衡相图的绘制
实验四二组分真实液态混合物的气—液平衡相图的绘制 一、实验目的 1.掌握二组分真实液态混合物的沸点、气液组成的测定方法。 2.掌握阿贝折光仪的使用。 3.绘制环已烷—乙醇体系的沸点—组成图,确定其恒沸点及恒沸组成。 二、实验原理 在恒定压力下,二组分达到气液平衡时,表示溶液的沸点与组成的相图称为沸点—组成图,即t x —图可分为三类: —图。二组分真实液态混合物的t x (1)溶液的沸点介于两纯组分沸点之间(图4—10(a))。 (2)各组分对拉乌尔定律发生最大正偏差,其溶液有最低恒沸点(图4—10(b))。 (3) 各组分对拉乌尔定律发生最大负偏差,其溶液有最高恒沸点(图4—10(c))。 对(2)、(3)类系统在最低或最高沸点处的气液两相组成相同,加热蒸发的结果只能使气相总量增加,气液两相组成及溶液沸点保持不变,这是的温度称为恒 沸点,相应的组成称为恒沸组成。 为了测定t x —图,需在气—液两相达到平衡后,同时测 定气相组成、液相组成和溶液的沸点。本实验采用折光率法 测定系统的组成。即需测定已配置好的不同组成的溶液的折 光率,然后绘制折光率与组成的标准曲线,即本实验的工作 曲线。实验采用简单蒸馏瓶,用电热丝直接放入溶液中加热 (如图4—11),以减少过热和暴沸现象。气相分析是取冷凝 器下端小玻璃球中的冷凝液,液相分析是取蒸馏瓶内的液体。 分析仪器采用阿贝折光仪。 三、仪器和药品 蒸馏瓶一个;温度计一支(50℃~100℃,0.01精度);阿 贝折光仪一台;长、短滴管各一支;20ml量筒一个;1ml刻 度滴管一支。 环已烷;无水乙醇;20%、40%、60%、80%环已烷—乙 醇混合液;脱脂棉。 四、实验步骤
双液系气液平衡相图的绘制
实验三双液系气液平衡相图的绘制姓名:学号: 班级:实验日期:2015年9月21日 提交报告日期:2015年9月28日 1、实验目的 1.了解沸点仪的原理和使用方法。 2.在大气压力下用沸点仪测绘环己烷-乙醇双液系的气相平衡相图。 3.掌握阿贝折射仪的使用方法。 2、实验原理 双液系是指两种液态物质混合而成的物系。双液系可以分为完全互溶双液系、部分互溶双液系和完全不溶双液系。 将两种挥发性液体混合,若该二组分的蒸气压不同,则溶液的组成与其平衡气相的组成不同。在压力保持一定,二组分系统气液达到平衡时,表示液态混合物的沸点与平衡时组成关系的平衡状态图,简称相图。沸点和组成的关系有下列三种:(1)理想液体混合物或接近理想液体混合物的双液系,其液体混合物的沸点介于两纯物质沸点之间;(2)各组分蒸气压对拉乌尔定律产生很大的负偏差,其溶液有最高恒沸点见;(3)各组分蒸气压对拉乌尔定律产生很大的正偏差,其溶液有最低恒沸点。第(2)、(3)两类溶液在最高或最低恒沸点时的气液两相组成相同,加热蒸发的结果只使气相总量增加,气液相组成及溶液沸点保持不变,这时的温度称恒沸点,相应的组成称恒沸组成。第一类混合物可用一般精馏法分离出这两种纯物质,第(2)、(3)类混合物用一般精馏方法只能分离出一种纯物质和另一种恒沸混合物。 为了测定二元液系的相图,需在气液达到平衡后,同时测定溶液的沸点、气相和液相组成。 本实验是测定具有最低恒沸点的环己烷—乙醇双液系的相图。方法是用沸点仪直接测定一系列不同组成之溶液的气液平衡温度(即沸点),并收集少量馏出液(即气相冷凝液)及吸取少量溶液(即液相),分别用阿
编号123456 7 8 贝折射仅测定其折射率。为了求出相应的组成,必须先测定已知组成的溶液的折射率,作出折射率对组成的工作曲线,在此曲线上即可查得对应于样品折射率的组成。 3、实验仪器和试剂 1.仪器 沸点仪1个、加热电源(0.5kW)1台、阿贝折射仪1台、长颈胶头滴管2支、镜头纸、 超级恒温槽、50~10℃温度计1支。 2.药品 乙醇、环己烷、丙酮。 4、实验操作步骤及方法要点 1.启动超级恒温槽的加热和搅拌系统,把超级恒温槽的控制温度调至27℃。 2.测定标准溶液的折射率 用与超级恒温槽相连接的已经恒温的阿贝折射仪测定标准溶液的折射率,作折射率对组成的工作曲线。 3.溶液沸点及气液平衡组成的测定。 往沸点仪中加入20mL乙醇,通冷却水,打开电源并调电压至12V,加热溶液至沸腾。待其温度计上所指示的温度保持恒定后,读下该温度值,同时停止加热,并立即在小泡中取气相冷凝液,迅速测定其折射率,并用另一滴管取少量液相测定其折射率。 接下来,往沸点仪中分别加入1mL、2mL、2mL、2mL、5mL环己烷,并按前述方法测定气液平衡温度和气液两相的折光率。结束后,将沸点仪中溶液倒入回收瓶并用电吹风把沸点仪烘干。 往沸点仪中加入20mL环己烷,经行实验。在之后往沸点仪中分别加入的是1mL、2mL、2mL、2mL、5mL乙醇。 注意:每次测量折射率后,要将折射仪的棱镜打开晾干,以备下次测定用。 5、实验数据 1)原始实验测量数据 大气压力:97.13kPa 室温:25.5℃ 以下数据测定过程中阿贝折射仪(恒温槽)温度为27.0℃。
二组分气液平衡相图的绘制讲义
双液系气-液平衡相图的绘制 一、实验目的、要求 1. 测定常压下环己烷-乙醇二元系统的汽液平衡数据,绘制101325Pa下的沸点-组成的相图。 2. 掌握阿贝折射仪的原理和使用方法。 二、实验原理 液体混合物中各组分在同一温度下具有不同的挥发能力。因而,经过汽液见相变达到平衡后,各组分在汽、液两相中的浓度是不相同的。根据这个特点,使二元混合物在精馏塔中进行反复蒸馏,就可分离得到各纯组分。为了得到预期的分离效果,设计精馏装置必须掌握精确的汽液平衡数据,也就是平衡时的汽、液两相的组成与温度、压力见的依赖关系。大量工业上重要的系统的平衡数据,很难由理论计算,必须由实验直接测定,即在恒压(或恒温)下测定平衡的蒸汽与液体的各组分。其中,恒压数据应用更广,测定方法也较简便。 本实验测定的恒压下环己烷-乙醇二元汽液平衡相图。图中横坐标表示二元系的组成(以B的摩尔分数表示),纵坐标为温度。用不同组成的溶液进行测定,可得一系列数据,据此画出一张由液相线与汽相线组成的完整相图。 下图为环己烷——乙醇的沸点组成图的大致形状,ADC和BEC为气相线,AD′C和BE′C 为液相线。体系总组成为x的溶液开始沸腾时,气象组成为y ,继续蒸馏,气相量增加,液相量减少(总量不变),溶液温度上升,回流作用,控制了两相的量一定,沸点一定。此时,气相组成为y′,与其平衡的液相组成为x′,体系的平衡沸点为t沸,此时气液两相服从杠杆原理。 当压力一定时,对两相共存区进行相律分析:独立组分C=2,相数P=2,则自由度F=C-P+1=2-2+1=1 即有,体系温度一定,则气液两相成分确定。总量一定时,两相的量也一定。在一实验装置中,控制气液两相的相对量一定,使体系温度一定, 则气液组成一定。用精密温度计可以测出平衡温度,取出 气液两相样品测定其折射率可以求出其组成。折射率和组 成有一一对应关系,可以通过测定仪系列已知组成的样品 折射率,绘出工作曲线。测出样品就可以从工作曲线上找 到未知样品的组成。 三、使用仪器、材料 沸点仪1套,阿贝折射仪,移液管,环己烷,无水乙醇 四、实验步骤 1、测定折射率与组成的关系,绘制工作曲线 将9支小试管编号,依次移入0.1 ml, 0.2 ml, …, 0.9 ml的环己烷,然后依次移入0.9 ml, 0.8 ml,…, 0.1 ml的无水乙醇,配成9份已知浓度的溶液,用阿贝折射仪测定每份溶液的折射率及纯环己烷和纯无水乙醇的折射率,以折射率对浓度作图。 2、测定环己烷-乙醇体系的沸点与组成的关系 (1) 右半部沸点-组成关系的测定取20 ml无水乙醇加入沸点仪中,然后依次加入环己烷0.5, 1.0, 1.5, 2.0, 4.0, 14.0 ml,测定溶液沸点,及气、液组分折射率n。完成后,将溶液倒入回收瓶。 (2) 左半部沸点-组成关系的测定取25 ml环己烷加入沸点仪中,然后依次加入
双液系的气液平衡相图
双液系的气-液平衡相图 1. 简述由实验绘制环己烷-乙醇气-液平衡T-x相图的基本原理。 答:通过测定不同沸点下组分的气、液相的折射率,在标准的工作曲线上找出该折射率对应的浓度,结合其沸点画出平衡相图。 2. 在双液系的气-液平衡相图实验中,作环己烷-乙醇的标准折光率-组成曲线的目的是什么? 答:作标准曲线的目的是通过测气、液相相得折射率从而在标准工作曲线上找出对应的浓度。 3. 用精馏的方法是否可把乙醇和环己烷混合液完全分离,为什么? 答:不能完全分离。因为环己烷-乙醇二组分具有最低恒沸点。 4. 测定纯环己烷和纯乙醇的沸点时,沸点仪中有水或其它物质行吗? 答:有水和其他物质都是不行的。因为有水和其他物质会使所测沸点改变。 5. 为什么工业上常生产95%酒精?只用精馏含水酒精的方法是否可能获得无水酒精? 答:因为水-乙醇二组分具有最低恒沸点,所以工业上常生产95%的酒精。用精馏的方法无法获得无水酒精,只能获得95%的酒精。 6. 在双液系的气-液平衡相图实验中,如何判断气-液相达平衡状态?
答:观察贝克曼温度计的读数,如果读数稳定3-5分钟,说明已达平衡状态。 7. 在双液系的气-液平衡相图实验中,每次加入沸点仪中的环己烷或乙醇是否应按记录表所规定的体积精确计量?为什么? 答:不需要按记录表的加。因为组分的浓度不是按所加物质的量计算得来的,而是通过测折射率间接得到的。 8. 在双液系的气-液平衡相图实验中,在测定沸点时,溶液出现分馏现象,将使绘出的相图图形发生什么变化? 答:出现馏分将使测得的沸点偏高,使相图向上移动。 9. 在双液系的气-液平衡相图实验中,蒸馏器中收集气相冷凝的小球大小对结果有何影响? 答:小球太小难以收集气相,小球太大,小球内的组分更新太慢,产生馏分,导致实验误差。 10. 在双液系的气-液平衡相图实验中,通过测定什么参数来测定双液系气-液平衡时气相和液相的组成? 答:通过测定组分的折射率来测定双液系气-液平衡时气相和液相的组成。 11. 在双液系的气-液平衡相图中,如何通过测定溶液的折光率来求得溶液的组成? 答:通过测得的折射率在标准曲线上找出对应的浓度,根据气、液相平衡浓度与测得的沸点作出平衡相图。
双液系的气—液平衡相图
双液系的气—液平衡相图 一、实验目的 1.绘制在Pθ环已烷—乙醇的气液平衡相图,了解相图和相律基本概念; 2.掌握测定双组分液体的沸点及正常沸点的方法; 3.掌握用折光率确定二元液体的组成方法。 二、实验原理 液体的沸点是指液体的蒸气压和外压相等时的温度,在一定的外压下,纯液体的沸点有确定值。但双液系的沸点不仅与外压有关,而且还与两种液体的相对含量有关。根据相律: 自由度=组分数-相数+2 因此,一个气—液共存的二组分体系,其自由度为2。只要任意再确定一个变量,整个体系的存在状态就可以用二维图形来描述。 两种挥发性液体混合,若该二组分的蒸气压不同,则溶液的组成与其平衡气相的组成不同。在压力保持一定,二组分系统气液达到平衡时,表示液态混合物的沸点与平衡时组成关系的相图,称为沸点和组成(T-x)图。沸点和组成(T-x)的关系有下列三种: (1)理想液体混合物或接近理想液体混合物的双液系,其液体混合物的沸点介于两纯物质沸点之间见图1(a); (2)各组分蒸气压对拉乌尔定律产生很大的负偏差,其溶液有最高恒沸点见图1(b); (3)各组分蒸气压对拉乌尔定律产生很大的正偏差,其溶液有最低恒沸点见图1(c)。 第(2)、(3)两类溶液在最高或最低恒沸点时的气液两相组成相同,加热蒸发的结果只使气相总量增加,气液相组成及溶液沸点保持不变,这时的温度称恒沸点,相应的组成称恒沸组成。
图1. 沸点和组成(T-x)图 本实验是测定具有最低恒沸点的环己烷—乙醇双液系的T-x图。方法是用沸点仪(如图2所示)直接测定一系列不同组成之溶液的气液平衡温度(即沸点),并收集少量馏出液(即气相冷凝液)及吸取少量溶液(即液相),分别用阿贝折光仪测定其折光率。根据已知组成的溶液折光率,作出一定温度下(25℃)该溶液的折光率—组成工作曲线,然后根据测得的样品溶液的气液两相的折光率,在此曲线上即可按描法得到待测未知样品溶液的组成。 图2. 沸点测定仪示意图 三、仪器与药品 沸点测定仪1只丙酮(分析纯) 水银温度计(50~100℃,分度值0.1℃)1支超级恒温水浴1台玻璃温度计(0~100℃,分度值1℃)1支称量瓶(高型)10只
二元液系相图实验报告
二元液系相图 一、实验目的 二、1、用沸点仪测定在常压下环己烷-乙醇的气液平衡相图。 三、2、了解沸点的测定方法。 四、3、掌握阿贝折射仪的测量原理及使用方法。 五、二、实验原理 六、1、液体的沸点是指液体的饱和蒸汽压和外压相等时的温度。在一定外压下,纯液体的沸点有确定的值。但对于完全互溶的双液系,沸点不仅与外压有关,而且还与双液系的组成有关。 七、 八、2、用阿贝折射仪测定气液组成的折光率,来获得气液组成。 三、实验装置
四、仪器及试剂 仪器:EF-03沸点测量仪、阿贝折射仪、沸点仪、取样管 试剂:无水乙醇、环己烷 五、实验步骤 1、安装好干燥的沸点仪。 2、加入纯乙醇30ml左右,盖好瓶塞,使电热丝浸入液体中,温度传感器与液面接触。
3、开冷凝水,将稳流电源调至(1.8-2.0A),接通电热丝,加热至沸腾,待数字温度计上读数恒定后,读下该温度值。 4、关闭电源,停止加热,将干燥的取样管自冷凝管上端插入冷凝液收集小槽中,取气相冷凝液样,迅速用阿贝折射仪测其折光率。 5、用干燥的小滴管取液相液样,用阿贝折射仪测其折光率。 6、分别在沸点仪中加入混合液,1、2、3、4、5、6重复上述操作。 7、根据环己烷-乙醇标准溶液的折射率,将上述数据转换成环己烷的摩尔分数,绘制相图。 8、实验完毕后,关闭冷凝水,关闭电源,整理实验台。 六、阿贝折光仪的使用 1、用擦镜纸将镜面擦干,取样管垂直向下将样品滴加在镜面上,注意不要有气泡,然后将上棱镜合上,关上旋钮。 2、打开遮光板,合上反射镜。 3、轻轻旋转目镜,使视野最清晰。 4、旋转刻度调节手轮(下手轮),使目镜中出现明暗面(中间有色散面),图a。
双液系的气液平衡相图(物理化学实验)
双液系的气液平衡相图 实验者:林澄昱生04 2010030007 同组者:张弯弯 实验日期:2012-03-10 提交日期:2012-03-16 实验指导:刘晓惠 1引言 两种蒸气压不同的挥发性液体在混合之后,其溶液组成与与其平衡气相的组成不同。 在恒外压下,二组分系统达到气液平衡时,表示液态混合物的沸点与平衡时气液两相组成关系的相图,称为沸点和组成(T-x)图。大致分为三大类,包括: (1)理想液体混合物或接近理想液体混合物的双液系,其混合物沸点介于两纯物质沸点之间。见图1(a); (2)各组分蒸气压对拉乌尔定律产生很大的负偏差,有最高恒沸点。见图1(b); (3)各组分蒸汽压对拉乌尔定律产生很大的正偏差,有最低恒沸点。见图2(c)1。 图1 三类沸点组成(T-x)图 本实验为了绘制常压下环己烷-乙醇的气液平衡相图,先利用阿贝折射仪测定一系列已知组成混合溶液及纯液体的折射率,绘制标准曲线,再通过沸点仪测定一系列混合溶液的沸点,收集少量气相冷凝液以及溶液,测定其各自折射率,反查标准曲线得到气液两相的组成,绘得双液系的气液平衡相图。 2实验操作 2.1实验药品、仪器及测试装置示意图 2.1.1实验药品 环己烷,无水乙醇; 2.1.2实验仪器 沸点仪,调压器,温度传感器,锥形瓶,分析天平(AR2140),阿贝折射 仪(型号不明,为靠近恒温箱的一台),恒温箱,胶头滴管,10ml吸量管, 洗耳球; 2.1.3装置示意图
1. 冷却水入口 2. 气相冷凝液贮存小泡 3. 温度传感器 4. 喷嘴 5. 电热丝 6. 调压器2 图2 沸点仪 2.2实验条件 恒温槽温度:26 ℃ 室温:未测 气压:未测 2.3实验操作步骤及方法要点 2.3.1标准曲线的测定及绘制 2.3.1.1标准溶液的配制 取5个干燥、洁净的锥形瓶,编号为1~5,分别称量空瓶质量并记录;依照表1分别量取并加入相应体积的环己烷和无水乙醇,每加 入一种溶液以后称量其质量并记录;得到5份已知组分的标准溶液。 表1 标准溶液的配制方案 通过称量得到的质量,可以计算得到每锥形瓶中液体含有的环己烷质量分数,通过测定其折射率,可以确定特定环己烷质量分数与折 射率的关系;同时,直接量取纯的无水乙醇和环己烷,测定其折射率, 可以绘制在环己烷质量分数在0~1之间的无水乙醇混合溶液与折射率 的关系曲线。 2.3.1.2标准溶液折射率测定 (1)将阿贝折射仪与恒温箱相连,调节反光镜使目镜视野明亮,此 时仪器可以用来测量; (2)用胶头滴管加入待测溶液,在右目镜视野中观察,用右侧旋钮 调节色散程度,使明暗分界线清晰,再用左侧旋钮调节,使明 暗交界线处于叉丝中心。注意接下来实验过程中保证左侧旋钮
课程设计:分离乙醇和正丙醇(详细版)
一、课程设计题目乙醇和正丙醇物系分离系统的设计 二、课程设计内容(含技术指标) 1.设计条件 生产能力:25000吨/年(每年按300天生产日计算) 原料状态:乙醇含量35%(wt%);温度:25℃;压力:100kPa;泡点进料; 分离要求:塔顶馏出液中乙醇含量99%(wt%);塔釜乙醇含量2%(wt%)操作压力:100kPa 其它条件:塔板类型:浮阀塔板;塔顶采用全凝器;R=1.5R m 2.具体设计内容和要求 (1)设计工艺方案的选定 (2)精馏塔的工艺计算 (3)塔板和塔体的设计 (4)水力学验算 (5)塔顶全凝器的设计选型 (6)塔釜再沸器的设计选型 (7)进料泵的选取 (8)绘制流程图 (9)编写设计说明书 (10)答辩 三、进度安排
四、基本要求 教研室主任签名: 年月日 摘要 精馏是分离液体混合物最常用的一种单元操作,在化工,炼油,石油化工等领域中被广泛应用。精馏是使易挥发组分进入气相,难挥发组分进入液相,从而使液体混合物分离。本次设计任务为处理25000吨/年的乙醇和正丙醇混合物。 浮阀塔是在泡罩塔的基础上发展起来的,它主要的改进是取消了升气管和泡罩,在塔板开孔上设有浮动的浮阀,浮阀可根据气体流量上下浮动,自行调节,使气缝速度稳定在某一数值。这一改进使浮阀塔在操作弹性、塔板效率、压降、生产能力以及设备造价等方面比泡罩塔优越。但在处理粘稠度大的物料方面,又不及泡罩塔可靠。浮阀塔广泛用于精馏、吸收以及脱吸等传质过程中。本设计通过物料衡算,热量衡算,工艺计算,结构设计和校核等一系列工作来设计一个具有可行性的合理的浮阀塔。 关键词浮阀塔乙醇正丙醇回流比
完全互溶双液系气液均衡相图的绘制
四川理工学院实验报告 系:材化系 课程名称:简明物理化学实验 日期:2011年4月18日 姓名 学号 实验室 528 专业 材料科学与工程 班号 2009级2班 老师鉴定 实验名称 完全互溶双液系气液平衡相图的绘制 成绩评定 一、实验目的 (1)测定常压下环已烷—乙醇二元系统的气液平衡数据,绘制沸点—组成相图;(2)掌握双组分沸点的测定方法,通过实验进一步理解分馏原理;(3)掌握阿贝折射仪的使用方法。二、实验原理 两种液体物质混合而成的两组分体系称为双液系。根据两组分间溶解度的不同,可分为完全互溶、部分互溶和完全不互溶3种情况。两种挥发性液体混合形成完全互溶体系时,如果该两组分的蒸气压不同,则混合物的组成与平衡时气相的组成不同。当压力保持一定,混合物沸点与两组分的相对含量有关。 恒定压力下,真实的完全互溶双液系的气—液平衡相图(图),根据体系对拉乌x T 尔定律的偏差情况,可分为3类: (1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯—苯体系 ,如图2.7(a ) 所示。 (2)最大负偏差:存在一个最小蒸气压值,比两个纯液体的蒸气压都小,混合物存在着最高沸点,如盐酸—水体系,如图2.7(b )所示。 (3)最大正偏差:存在一个最大蒸气压值,比两个纯液体的蒸气压都大,混合物存在着最低沸点,如正丙醇—水体系,如图2.7(c )所示。 B B B B (a) (b) (c) 图2.7 二组分真实液态混合物气—液平衡相图(T-x 图) 后两种情况为具有恒沸点的双液系相图。它们在最低或最高恒沸点时的气相和液相组成相同,因而不能像第一类那样通过反复蒸馏的方法而使双液系的两个组分相互分离,而只能采取精馏等方法分离出一种纯物质和另一种恒沸混合物。 为了绘制双液系的T-x 相图,需测定几组原始组成不同的双液系在气—液两相平衡后的沸点和液相、气相的平衡组成。 本实验以环已烷—乙醇为体系,该体系属于上述第3种类型。在沸点仪(如图2.8所示)中蒸馏不同组成的混合物,测定其沸点及相应的气、液二相的组成,即可作出T-x 相图。本实验中气液两相的组成均采用折光率法测定。 折光率是物质的一个特征数值,它与物质的浓度及温度有关,因此在测量物质的折光率
乙醇正丙醇分离设计
化工原理课程设计任务书 1.设计题目: 常压连续筛板式精馏塔分离乙醇—正丙醇二元物系的设计。 2.原始数据及条件: 进料:乙醇含量0.5(摩尔分数,下同),其余为正丙醇,F=3400Kg/h,塔顶进入全凝器,塔板压降0.7Kpa。 分离要求:塔顶乙醇含量0.90;回收率为0.95;全塔效率0.55。 操作条件:塔顶压强1.03atm(绝压);泡点进料; R/Rmin=1.6 。 3.设计任务: (1)完成该精馏塔的各工艺设计,包括设备设计及辅助设备选型。(2)画出带控制点的工艺流程图、塔板版面布置图、精馏塔设计条件图。 (3)写出该精馏塔的设计说明书,包括设计结果汇总和设计评价。
摘要 在本次任务中,根据化工原理课程设计的要求设计的是乙醇----丙醇连续浮阀精馏塔,除了要计算其工艺流程、物料衡算、热量衡算、筛板塔的设计计算,以外,并对精馏塔的主要工艺流程进行比较详细的设计,并画出了精馏塔的工艺流程图和设备条件图。 本次设计选取回流比R=1.8Rmin=1.6×1.34=2.144应用图解法计算理论版数,求得理论塔板NT为12块(包括塔釜再沸器),第6块为进料板。设计中采用的精馏装置有精馏塔 ,冷凝器等设备,采用间接蒸汽加热,物料在塔内进行精馏分离,余热由塔顶产品冷凝器中的冷却介质带走,完成传热传质. 塔的附属设备中,所有管线均采用无缝钢管。预热器采用管壳式换热器。用99.97℃塔釜液加热。料液走壳程,釜液走管程。本设计采用了筛板塔对乙醇-丙醇进行分离提纯,塔板为碳钢材料,通过板压降、漏液、液泛、液沫夹带的流体力学验算,均在安全操作范围内。 关键字:乙醇-丙醇筛板塔物料衡算
双液系气液平衡相图的绘制实验报告
双液系沸点-组成图测绘实验报告 实验时间:2015年4月15日 学号:1120132970 一、目的要求 1 ?测定相应组成时的沸点并制作常压下环已烷一无水乙醇双液系的平衡相图。 2 ?从沸点组成图了解分馏原理。 3.了解沸点的测定技术,掌握两组分液体沸点的测定方法。 4 ?掌握折光率与组成的关系及阿贝折光仪的测量原理和使用方法。 二.实验原理 1、由液态物质混合而成的二组分系统称为双液系统。若两液体能以任意比例互 溶,称其为完全互溶双液系,若两液体只能部分互溶,称其为部分互溶双液系。 一个完全互溶的二元体系,两个纯液体组分在所有组成范围内完全互溶。在 定压下,完全互溶的二元体系的沸点一组成图可分为三类,如图C7.1所示。 a. 溶液的沸点介于两纯组分沸点之间,如苯一甲苯体系; b. 溶液有最低恒沸点,如环己烷-乙醇体系; c. 溶液有最高恒沸点,如丙酮一氯仿体系。 Xi JF4 Xi jn B A B X x B 下面以a为例,简单说明绘制沸点-组成图的原理。加热总组成为x1的溶液, 体系的温度上升,达液相线上1点时溶液开始沸腾,组成为x2的气相开始生成,但气相量很少,趋于0,x1、x2二点代表达到平衡时液、气两相组成。继续加热, 气相量逐渐增多,沸点继续上升,气、液二相组成分别在气相线和液相线上变化,当达某温度(如2点)并维持温度不变时,则x3、x4为该温度下液、气两相组成,气相、液相的量之比按杠杆规则确定。从相律 f = c - p +2 可知:当外压恒定时,在气、液两相共存区域自由度等于1;当温度一定时,则气、液两相的组成也就确定,总组成一定,由杠杆
规则可知两相的量之比也已确定。因此,在一定的实验装置中,全回流的加热溶液,在总组成、总量不变时,当气相的量与液相的量之比也不变时(达气-液平衡),则体系的温度也就恒定。分别取出气、液两相的样品,分析其组成,得到该温度下气、液两相平衡时各相的组成。改变溶液总组成,得到另一温度下气、液两相平衡时各相的组成。测得溶液若干总组成下的气液平衡温度及气、液相组成,分别将气相点用线连接即为气相线,将液相点用线连接即为液相线,得到沸点-组成图。 气相、液相的成份分析采用折光率法:折光率是物质的一个特征数值,它与物质的浓度及温度有关,因此在测量物质的折光率时要求温度恒定。溶液的浓度不同、组成不同,折光率也不同。因此可先配制一系列已知组成的溶液,绘出折光率-组成(n-x)的等温线,方法是在定温下测定已知各种组成(x )的折光率(n),绘出n-x等温线。对于未知组成的样品,取出各相样品后,迅速测出该温度下的折光率(n),便可以从n-x线查出其相应组成。 2、阿贝折光仪的原理 它的主要部分为两块直角棱镜PI,PII,棱镜PI的粗糙表面与PII的光学平面镜AD之间约有0.1到0.15mm的空隙,用于装待测液体并使在PI、PII间铺成一簿层。光线从反射镜射入棱镜PI后,由于面是粗糙的毛玻璃而发生漫射,从各种角度透过缝隙的被测液体;进入棱镜PII中,由前所知,从各个方向进入棱镜PII的光线均产生折射,而其折射角都落在临界角rc之内(因为棱镜的折 射率大于液体的折射率,因此人射角从到的全部光线都能通过棱镜而发生折 射)。具有临界角rc的光线穿出棱镜PII后射于目镜上,此时若将目镜的十字线调节到适当位置,则会见到目镜上半明半暗。 从几何光学原理可以证明,缝隙中液体的折射率n液与rc间的关系为:n 液=sinB ,B对一定的棱镜为一常数,n棱镜在定温下也是个定值。所以液体的折射率n液是角rc的函数。由rc可计算液体折射率。折光仪上已经把读数rc 换算成n液的值,可直接读出n液的值。 3、阿贝折光仪使用方法
双液体系气液平衡相图的绘制及思考题样本
双液体系气—液平衡相图的绘制 一、 实验目的 1. 绘制环己烷—异丙醇双液体系的沸点组成图, 确定其恒沸组成和恒沸温度。 2. 掌握回流冷凝管法测定溶液沸点的方法。 3.掌握阿贝折射仪的使用方法。 二、 实验原理 两种液体物质混合而成的两组分体系称为双液系。根据两组分间溶解度的不 同, 可分为完全互溶、 部分互溶和完全不互溶三种情况。两种挥发性液体混合形成完全互溶体系时, 如果该两组分的蒸气压不同, 则混合物的组成与平衡时气相的组成不同。当压力保持一定, 混合物沸点与两组分的相对含量有关。 恒定压力下, 真实的完全互溶双液系的气-液平衡相图( T -x ) , 根据体系对拉乌尔定律的偏差情况, 可分为3类: ( 1) 一般偏差: 混合物的沸点介于两种纯组分之间, 如甲苯-苯体系, 如图 (a)所示。 ( 2) 最大负偏差: 存在一个最小蒸汽压值, 比两个纯液体的蒸汽压都小, 混合物存在着最高沸点, 如盐酸—水体系, 如图 (b)所示。 ( 3) 最大正偏差: 存在一个最大蒸汽压值, 比两个纯液体的蒸汽压都大, 混合 物存在着最低沸点如图 (c)) 所示。 t A t A t A t B t B t B t / o C t / o t / o x B x B x B A B A A B B (a) (b) (c) x ' x '
上图为二组分真实液态混合物气—液平衡相图( T-x图) 后两种情况为具有恒沸点的双液系相图。它们在最低或最高恒沸点时的气相和液相组成相同, 因而不能象第一类那样经过重复蒸馏的方法而使双液系的两个组分相互分离, 而只能采取精馏等方法分离出一种纯物质和另一种恒沸混合物。 为了测定双液系的T-x相图, 需在气-液平衡后, 同时测定双液系的沸点和液相、气相的平衡组成。 本实验以环己烷-异丙醇为体系, 该体系属于上述第三种类型, 在沸点仪中蒸馏不同组成的混合物, 测定其沸点及相应的气、液二相的组成, 即可作出T -x相图。 本实验中两相的成分分析均采用折光率法测定。 三、仪器与试剂 1、仪器: 沸点仪1台; 调压变压器1台; 阿贝折射仪1台; 温度计(0-100℃) 1支; 长滴管1个; 短滴管2支; 2、试剂: 环己烷(分析纯); 异丙醇(分析纯) 异丙醇—环己烷标准溶液(异丙醇分别为0.20, 0.40, 0.50, 0.60, 0.80, 0.90) 四、主要实验步骤 1. 测定环己烷、异丙醇及标准溶液的折射率 调节阿贝折射仪, 用一支干燥的短滴管吸取环己烷数滴, 注入折射仪的加液孔内, 测定其折射率n, 读数两次, 取其平均值。然后打开棱镜组, 待环己烷挥发后, 再用擦镜纸轻轻吸去残留在镜面上的液体, 合上棱镜组。
