木质纤维检测方法

木质纤维质量要求及检测方法
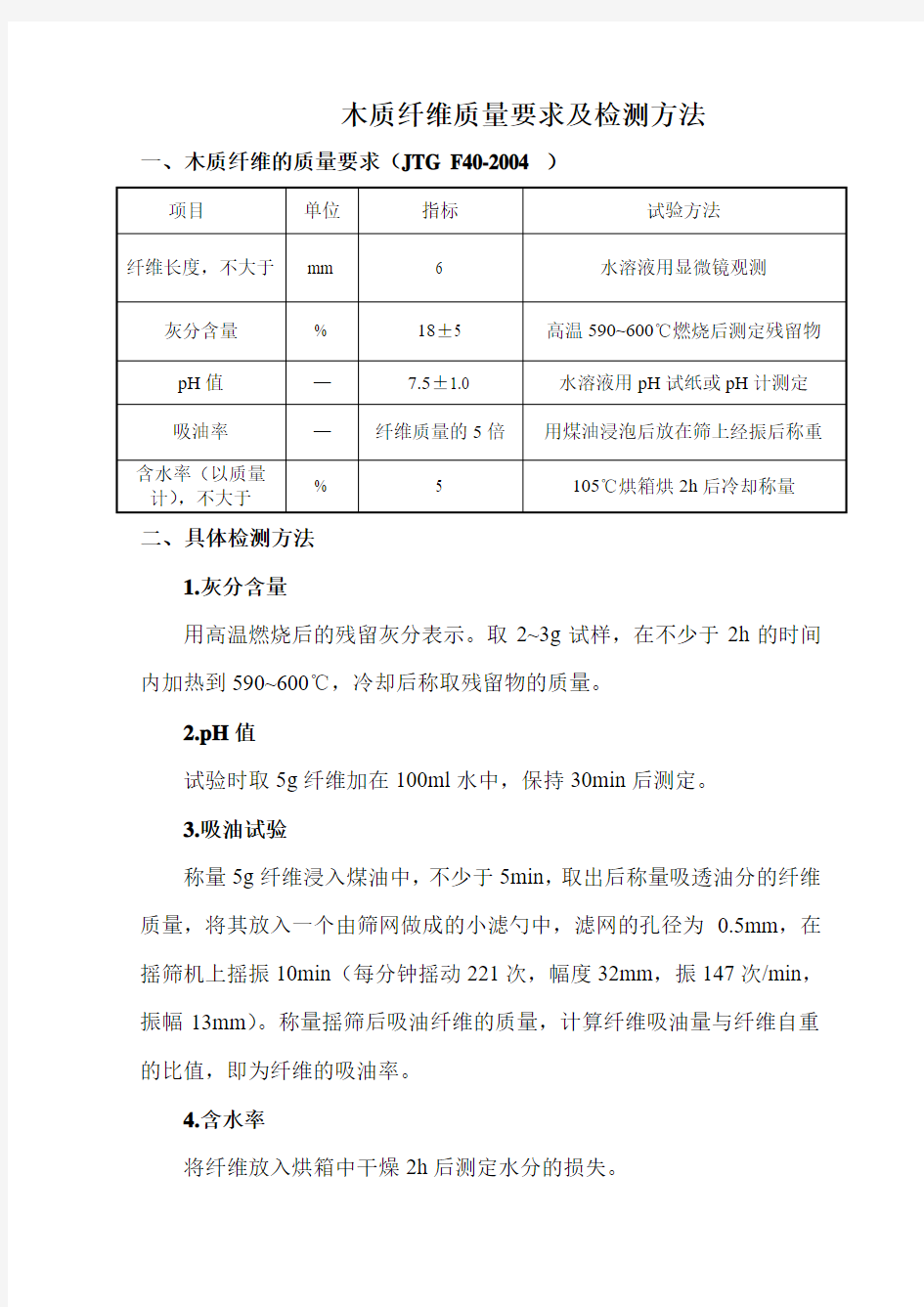
一、木质纤维的质量要求(JTG F40-2004 )
项目单位指标试验方法
纤维长度,不大于mm 6 水溶液用显微镜观测灰分含量% 18±5 高温590~600℃燃烧后测定残留物pH值—7.5±1.0 水溶液用pH试纸或pH计测定吸油率—纤维质量的5倍用煤油浸泡后放在筛上经振后称重
含水率(以质量
% 5 105℃烘箱烘2h后冷却称量计),不大于
二、具体检测方法
1.灰分含量
用高温燃烧后的残留灰分表示。取2~3g试样,在不少于2h的时间内加热到590~600℃,冷却后称取残留物的质量。
2.pH值
试验时取5g纤维加在100ml水中,保持30min后测定。
3.吸油试验
称量5g纤维浸入煤油中,不少于5min,取出后称量吸透油分的纤维质量,将其放入一个由筛网做成的小滤勺中,滤网的孔径为0.5mm,在摇筛机上摇振10min(每分钟摇动221次,幅度32mm,振147次/min,振幅13mm)。称量摇筛后吸油纤维的质量,计算纤维吸油量与纤维自重的比值,即为纤维的吸油率。
4.含水率
将纤维放入烘箱中干燥2h后测定水分的损失。
5.相对密度
木质纤维由于材质较轻,且纤维内部吸收一部分水,溶解某些物质,所以测定相对密度时需要通过另一种已知相对密度液体转换。具体方法是称取适量的纤维放入一个经过标定的测定相对密度的瓶中,向瓶中注入一种密度小于这种纤维且不使纤维发生溶解的液体,为防止瓶中出现气泡,可以事先用该液体浸泡纤维,必要时可采取捣实或离心的方式除去气泡,将液体注满。
相对密度=(m瓶+纤维-m瓶)/(m注满瓶的水-(m瓶+纤维+液体-m瓶+纤维)/液体相对密度)。
纤维素的测定方法
纤维素的测定方法-CAL-FENGHAI.-(YICAI)-Company One1
植物的主要化学成分是纤维素、半纤维素和木质素这三部分。它们是构成植物细胞壁的主要组分。其中,纤维素组成微细纤维,构成纤维细胞壁的网状骨架,而半纤维素和木质素是填充在纤维和微细纤维之间的“粘合剂”和“填充剂”。 1. 纤维素 生物制粉末在加热的情况下用醋酸和硝酸的混合液处理,在这种情况下,细胞间的物质被溶解,纤维素也分解成单个的纤维,木质素、半纤维素和其它的物质也被除去。淀粉、多缩戊糖和其它物质受到了水解。用水洗涤除去杂质以后,纤维素在硫酸存在下被重铬酸钾氧化成二氧化碳和水。 C6H10O5 + 4K2Cr2O7 + 16H2SO4 = 6CO2 + 4Cr2(SO4)3 + 4K2SO4 + 21H2O 过剩的重铬酸钾用硫酸亚铁铵溶液滴定,再用硫酸亚铁铵滴定同量的但是未与纤维素反应的重铬酸钾,根据差值可以求得纤维素的含量。 2. 半纤维素 用沸腾的80%硝酸钙溶液使淀粉溶解,同时将干扰测定半纤维素的溶于水的其它碳水化合物除掉。将沉淀用蒸馏水冲洗以后,用较高浓度的盐酸,大大缩短半纤维素的水解时间,水解得到的糖溶液,稀释到一定体积,用氢氧化钠溶液中和,其中的总糖量用铜碘法测定。 铜碘法原理:半纤维素水解后生成的糖在碱性环境和加热的情况下将二价铜还原成一价铜,一价铜以Cu2O的形式沉淀出来。用碘量法测定Cu2O的量,从而计算出半纤维素的含量。 测定还原性糖的铜碱试剂中含有KIO3和KI,它们在酸性条件下会发生反应,也不会干扰糖和铜离子的反应。加入酸以后,会发生反应释放出碘: KIO3 + 5KI +3H2SO4 = 3I2 + 3K2SO4 +3H2O 加入草酸以后,碘与氧化亚铜发生反应: Cu2O + I2 + H2C2O4 = CuC2O4 + CuI2 + H2O 过剩的碘用Na2S2O3溶液滴定:2Na2S2O3 + I2 = Na2S4O6 + 2NaI 3. 木质素 用1%的醋酸处理以分离出糖、有机酸和其它可溶性化合物。然后用丙酮处理,分离出叶绿素、拟脂、脂肪和其它脂溶性化合物。将沉淀用蒸馏水洗涤以后,在硫酸存在下,用重铬酸钾氧化水解产物中的木质素: C11H12O4 + 8K2Cr2O7 + 32H2SO4 = 11CO2 + 8K2SO4 + 8Cr2(SO4)3 + 32H2O 过量的重铬酸钾用硫酸亚铁铵溶液滴定。方法和测定纤维素相同。 实验所需试剂和仪器 1. 实验试剂 硫酸亚铁铵分析纯,重铬酸钾分析纯,硫代硫酸钠分析纯, 硝酸钙分析纯,硫酸铜分析纯,可溶性淀粉分析纯, 碘酸钾分析纯,草酸分析纯,酒石酸分析纯, 氯化钡分析纯,邻菲啰啉分析纯,浓硫酸分析纯, 盐酸分析纯,冰醋酸分析纯,硝酸分析纯。 2. 实验仪器 50mL酸式滴定管,50mL碱式滴定管,10mL离心试管若干,不同型号烧杯若干, 真空塞,250mL锥形瓶若干,电炉,离心沉淀器。 五实验步骤 (一)纤维素含量的测定
土壤纤维素酶测定方法
纤维素酶 一、试剂: 1)醋酸缓冲液(pH 5.5):164.08 g无水醋酸钠(C2H3O2Na)溶于700 ml去离子水,用醋酸(C2H4O2)调节pH至5.5,用去离子水稀释至1 L。 2)CMC溶液(0.7%,w:v):7 g羧甲基纤维素钠盐溶于1 L醋酸缓冲液,45℃下搅拌2 h,此溶液在4℃下可存放7天。 3)还原糖试剂: 试剂A:16 g无水碳酸钠(Na2CO3)和0.9 g氰化钾(KCN)溶于去离子水并稀释至1 L。试剂B:0.5 g六氰铁钾(K4Fe(CN)6)溶于去离子水并稀释至1 L,贮于棕色瓶中。 试剂C:1.5 g 硫酸铁铵(NH4SO4Fe2(SO4)2·H2O)、1 g十二烷基硫酸钠(C12H25O4SNa)和4.2 ml浓硫酸溶于50℃去离子水,冷却后稀释至1 L。 4)水合葡萄糖溶液:28 mg水合葡萄糖溶于少量去离子水中,并定容至1 L。 二、仪器设备 恒温培养箱,水浴锅,分光光度计,搅拌器,三角瓶 三、操作步骤 取10.00 g(耕地)或5.00 g(林地)新鲜土壤(<2 mm)于100 ml三角瓶中,加15 ml 醋酸缓冲液和15 ml CMC溶液,盖上塞子,于50℃下培养24 h,过滤。同时做空白对照,但在培养结束时才加入15 ml CMC溶液,并迅速过滤。 取2.00 ml滤液于50 ml容量瓶中,并用去离子水定容至刻度。吸取2.00 ml稀释液于20 ml试管中,加2.00 ml还原糖试剂A和2.00 ml还原糖试剂B,盖紧混匀,在100℃水浴中加热15 min 后,立即至于20℃水中冷却5 min。加10.00 ml还原糖试剂C,混匀,20℃下静置显色60 min,于690 nm波长处比色测定(要求在30 min内完成)。 标准曲线:吸取0,0.1,0.2,0.3,0.4,0.5,0.6,0.7,0.8,0.9,1.0 ml水合葡萄糖溶液,用去离子水稀释至2 ml,同上加入还原糖试剂A、B、C后,比色测定还原糖含量。c) 空白: 无土空白:不加土样,其余操作与样品试验相同,整个试验设置一个,重复一次。 无基质空白:以等体积水代替基质,每个土样设置一个。 四、结果计算 土壤纤维素酶活性(μg·g-1·(24 h)-1)=(C*V*f)/ dwt 式中C为样品的葡萄糖含量(μg·ml-1);V为土壤溶液体积(30 ml);f为稀释倍数(25);
范式法测定纤维素
原理 采用范氏(Van Soest)的洗涤纤维分析法测定中性洗涤纤维(NDF)和酸性洗涤纤维(ADF)原理: 植物性饲料经中性洗涤剂煮沸处理,不溶解的残渣为中性洗涤纤维,主要为细胞壁成分,其中包括半纤维素、纤维素、木质素和硅酸盐。植物性饲料经酸性洗涤剂处理,剩余的残渣为酸性洗涤纤维,其中包括纤维素、木质素和硅酸盐。酸性洗涤纤维经72%硫酸处理后的残渣为木质素和硅酸盐,从酸性洗涤纤维值中减去72%硫酸处理后的残渣为饲料的纤维素含量。将72%硫酸处理后的残渣灰化,在 灰化过程中逸出的部分为酸性洗涤木质素(ADL)的含量。 试剂的配制 中性洗涤剂(3%十二烷基硫酸钠):准确称取18.6g乙二胺四乙酸二钠(EDTA,C10H14O8Na2?2H2O,分析纯)和6.8g硼酸钠(Na2B4O7?10H2O,分析纯)放入烧杯中,加入少量蒸馏水,加热溶解后, 再加入30g十二烷基硫酸钠(C12H25NaO4S,分析纯)和 10ml乙二醇乙醚(C4H10O2,分析纯);再称取4.56 g无水磷酸氢二钠(Na2HPO4,分析纯)置于另一烧杯中,加入少量蒸馏水微微加热溶解后,倒入前一个烧杯中,在容量瓶中稀释至1000ml,其中pH 值约为6.9~7.1(pH值一般勿需调整); 1N 硫酸:量取约27.87 ml浓硫酸(分析纯,比重1.84,98%),徐徐加入已装有500ml蒸馏水的烧杯中,冷却后注入1000ml容量瓶定容,标定;酸性洗涤剂(2%十六烷三甲基溴化铵):称取20g十六烷三甲基溴化铵(CTAB,分析纯)溶于1000ml1N硫酸,必要时过滤; 中性洗涤纤维测定 准确称取1.0000g样品(通过40目筛)置于直筒烧杯中,加入100ml中性洗涤剂和数滴十氢化萘及0.5g无水亚硫酸钠。将烧杯套上冷凝装置于电炉上,在5~10min内煮沸,并持续保持微沸60min。煮沸完毕后,取下直筒烧杯,将烧杯中溶液倒入安装在抽滤瓶上的已知重量的玻璃坩埚中进行过滤,将烧杯中的残渣全部移入,并用沸水冲洗玻璃坩埚与残渣,直洗至滤液呈中性为止。用20ml丙酮冲洗二次,抽滤。将玻璃坩埚置于105℃烘箱中烘2h后,在干燥器中冷却30 min称重,直称至恒重。 酸性洗涤纤维测定 准确称取1.0000g样品(通过40目筛)置于直筒烧杯中,加入100 ml酸性洗涤剂和数滴十氢化萘及0.5g无水亚硫酸钠。将烧杯套上冷凝装置于电炉上,在5~10min内煮沸,并持续保持微沸60min。趁热用已知重量的玻璃坩埚抽滤,并用沸水反复冲洗玻璃坩埚及残渣至滤液呈中性为止。用少量丙酮冲洗残渣至抽下的丙酮液呈无色为止,并抽净丙酮。将玻璃坩埚置于105℃烘箱中烘2h后,在干燥器中冷却30 min称重,直称至恒重。 酸性洗涤木质素和酸不溶灰分(AIA)测定将酸性洗涤纤维加入72%硫酸,在20℃消化 3h后过滤,并冲洗至中性。消化过程中溶解部分为纤维素,不溶解的残渣为酸性洗涤木质素和酸不溶灰分,将残渣烘干并灼烧灰化后即可得出酸性洗涤木质素和酸不溶灰分的含量。 结果计算 中性洗涤纤维含量的计算:NDF(%)=(W1-W2)/ W×100 式中: W1—玻璃坩埚和NDF重(gW2—玻璃坩埚重(g) W—试样重(g) 酸性洗涤纤维含量的计算:ADF(%)=(G1-G2)/G×100 式中: G1—玻璃坩埚和ADF重(g) G2—玻璃坩埚重(g) W—试样重(g) 半纤维素含量的计算:半纤维素(%)=NDF(%)-ADF(%) 纤维素含量的计算:纤维素=ADF(%)-经72%硫酸处理后的残渣(%)
纤维蛋白原降解产物FDP液体双试剂使用说明书
纤维蛋白及纤维蛋白原分解产 物测定试剂 Reagent for P-FDP Test 版本号:YS2012-A01 编制日期:2012年1月 【预期用途】 本试剂用于体外定量检测人血浆中的纤维蛋白及纤维蛋白原分解产物(FDP:Fibrin and Fibrinogen Degradation Products)的含量。FDP是纤溶酶分解纤维蛋白及纤维蛋白原的多种产物的总称,因为纤溶系统的亢进而增加,从而引起纤溶系统的异常,特别是在播散性血管内凝血(DIC:Disseminated Intravacular Coagulation Syndrome)诊断,病程观察中,成为重要检查项目之一。随着凝固纤溶系统与肾病的关联被关注,可检测作为肾小球局部的凝固纤溶动态指标的尿中FDP。现在应用于肾炎,接受肾脏移植的患者,膀胱肿瘤,妊娠中毒症的诊断,病程观察,还用于对肾小球体内,下部尿路,流血中等反映凝固纤溶动态的检查。 【测定原理】 本品以乳胶凝集法为原理。样本中的FDP,可与附着在乳胶颗粒上的抗体产生抗原抗体的凝集反应,凝集反应产生的浊度的变化可通过测定特定波长的吸光度值,即可算出样本中FDP的含量。 【试剂成份】 组成规格比例主要组份 FDP试剂1:1 缓冲液、抗人FDP单克隆抗体胶乳颗粒 FDP校准品1ml(冻干) FDP、稳定剂,定值见瓶签 FDP质控品0.5ml(冻干) FDP、稳定剂,定值见瓶签 【试剂制备】 液体双试剂,可直接使用。 【稳定性和贮存】 本试剂在2~8℃避光条件下贮存(勿冷冻)可稳定至失效期;若试剂空白>1.5则视为失效。 【标本收集和处理】 新鲜血液9份体积与1份体积的0.11mol/L柠檬酸钠混合后,离心(3,000rpm,10~30分钟)后得到的上清可作为血浆样本使用。样本要采血后直接离心,当天进行检测。如当天不能检测的情况下,冷藏(2~10℃)可保存1天,冷冻(-80℃)可保存1个月。但是,解冻后的样本只限1次使用,不能反复冻溶。【操作参数】 【测定步骤】 空白管(B)校准管(S)样品管(U)蒸馏水(μL) 4 ― ― 校准液(μL)― 4 ― 样品(μL)― ― 4 试剂1(μL)100 100 100 混匀,37℃孵育3~5分钟 试剂2(μL)100 100 100 混匀,37℃孵育20秒后读取第一点吸光度,5分钟后读取第二点吸光度。将第二点吸光度减去第一点吸光度,读取各管的吸光度变化ΔA。【结果计算】 样本中FDP浓度(μg/mL)=×C S 式中:ΔA U样品管的吸光度变化 ΔA S校准管的吸光度变化 ΔA B空白管的吸光度变化 C S校准液中FDP的浓度 根据多点校准品浓度和对应吸光度变化值ΔA,采用多点非线性校准模式确定工作曲线,样本吸光度变化在工作曲线上相对应的浓度值即为测定浓度。 【校准】 请使用“yesen” FDP校准液。 【质量控制】 为确保测试质量,请使用“yesen”或其他商品化的定值控制血清与被测样本同时测试。控制血清给定的值必须经本方法确认。控制血清的使用可以检查仪器及试剂的性能。可能影响测试结果的因素包括仪器性能、温度控制、器皿的清洁和加样器的准确性。 【注意事项】 1.本试剂仅用于科研、实验、技术支持,不直接用于临床诊断; 2.请避免接触皮肤、眼睛及粘膜,一旦接触,应即用水冲洗污染部位; 3.试剂体积和样本体积可因仪器要求不同,按比例增减,计算公式不变; 4.不同方法学试剂的质控结果之间会存在差异,使用时请确保质控选择与试剂的方法学保持一致; 5.不同批号的试剂不建议混用,如混用应重新校准。 6.试剂中含有动物源性物质“抗体”,来源于非疫区,并经检验检疫,不排除含有其他未知的传染性物质存在,因此在使用时应按传染性物质对待。 7.当样本中FDP的浓度超过100μg/mL时,应将样本稀释后再测,测得的结果乘以稀释倍数。 【参考值(参考范围)】 <5μg/mL,建议各实验室应建立自己的参考范围。可取本区域内健康体检者样品进行测定,得FDP均值和标准差s, 以±1.96s即95%置信区间为参考范围。 【性能数据】 下面结果是用本试剂在全自动生化分析仪上测试获得的。 1.试剂空白吸光度≤1.5(570nm,37℃)。 2.分析灵敏度:当样品中FDP浓度为20μg/mL时,其吸光度A≥0.010。 3.测量精密度:重复性CV批内%≤8%、CV批间%≤15%; 4.准确性:相对偏差不超过±15%; 5.线性范围:2.5μg/mL~100μg/mL (r>0.99); 6.抗干扰性:当样品中TBIL≤342μmol/L、TG≤20mmol/L、TC≤20mmol/L、Hb≤ 5.0g/L时对测定结果无显著影响; 7.方法比对:用本试剂与进口相同方法的试剂分别测定100例样本中FDP含量,结果y=0.982x+0.052r=0.999。 【产品特点】 1.消浊配方设计,保证很好的抗干扰性。 2.采用高品质的单克隆抗体,与其它蛋白不发生交叉反应。 3.测定灵敏度高,特异性好; 4.配套校准品,保证结果的准确性。 方法:终点法反应时间:10分钟 主波长:570nm 副波长:无 样品量:4μL 试剂量:100μL/100μL 反应方向:正向定标方式:多点非线性元升生物科技(上海)有限公司 电话:(021)67827182 传真:(021)67827181 http//https://www.360docs.net/doc/484780005.html, E-mail:yesenbio@https://www.360docs.net/doc/484780005.html, 技术支持与用户服务 E-mail:yesen2011@https://www.360docs.net/doc/484780005.html, yesen1998@https://www.360docs.net/doc/484780005.html, (中国) E-mail:yesen2013@https://www.360docs.net/doc/484780005.html, yesen2014@https://www.360docs.net/doc/484780005.html, (境外) 地址:上海市松江工业区泖亭路188弄财富兴园-国际企业公园5号103-3 ΔA U-ΔA B ΔA S-ΔA B x x
纤维素的测定方法
实验原理 植物的主要化学成分是纤维素、半纤维素和木质素这三部分。它们是构成植物细胞壁的主要组分。其中,纤维素组成微细纤维,构成纤维细胞壁的网状骨架,而半纤维素和木质素是填充在纤维和微细纤维之间的“粘合剂”和“填充剂”。 1. 纤维素 生物制粉末在加热的情况下用醋酸和硝酸的混合液处理,在这种情况下,细胞间的物质被溶解,纤维素也分解成单个的纤维,木质素、半纤维素和其它的物质也被除去。淀粉、多缩戊糖和其它物质受到了水解。用水洗涤除去杂质以后,纤维素在硫酸存在下被重铬酸钾氧化成二氧化碳和水。 C6H10O5 + 4K2Cr2O7 + 16H2SO4 = 6CO2 + 4Cr2(SO4)3 + 4K2SO4 + 21H2O 过剩的重铬酸钾用硫酸亚铁铵溶液滴定,再用硫酸亚铁铵滴定同量的但是未与纤维 素反应的重铬酸钾,根据差值可以求得纤维素的含量。 2. 半纤维素 用沸腾的80%硝酸钙溶液使淀粉溶解,同时将干扰测定半纤维素的溶于水的其它碳水化合物除掉。将沉淀用蒸馏水冲洗以后,用较高浓度的盐酸,大大缩短半纤维素的水解时间,水解得到的糖溶液,稀释到一定体积,用氢氧化钠溶液中和,其中的总糖量用铜碘法测定。 铜碘法原理:半纤维素水解后生成的糖在碱性环境和加热的情况下将二价铜还原成一价铜,一价铜以Cu2O的形式沉淀出来。用碘量法测定Cu2O的量,从而计算出半纤维素的含量。 测定还原性糖的铜碱试剂中含有KIO3和KI,它们在酸性条件下会发生反应,也不会干扰糖和铜离子的反应。加入酸以后,会发生反应释放出碘: KIO3+ 5KI +3H2SO4= 3I2+ 3K2SO4+3H2O 加入草酸以后,碘与氧化亚铜发生反应: Cu2O + I2+ H2C2O4= CuC2O4+ CuI2+ H2O 过剩的碘用Na2S2O3溶液滴定:2Na2S2O3 + I2 = Na2S4O6 + 2NaI 3. 木质素 用1%的醋酸处理以分离出糖、有机酸和其它可溶性化合物。然后用丙酮处理,分离出叶绿素、拟脂、脂肪和其它脂溶性化合物。将沉淀用蒸馏水洗涤以后,在硫酸存在下,用重铬酸钾氧化水解产物中的木质素: C11H12O4 + 8K2Cr2O7 + 32H2SO4 = 11CO2 + 8K2SO4 + 8Cr2(SO4)3 + 32H2O
测定纤维素酶活实验方法总结及优化方案
DNS法测定酶活实验方法总结及优化方案 目前纤维素酶没有统一的测定方法,诸多因素影响纤维素酶酶活测定大小的比较。选择适宜的酶活测定条件,提高测定结果的准确性,可根据有关资料中采用的测定条件,以及通过控制变量法对酶活力测定中的主要影响因素进行研究。 目前实验室采用测酶活方法: 1、葡萄糖标准曲线制作: 530nm比色。 2、酶活测定方法:
考虑到酶液中培养基成分会对吸光值造成一定的影响,所以空白管0还是采用先将酶高温灭活的方法,后面保持实验条件一致,显色时间与标准曲线的显色时间保持一致。 单位酶活的计算:T n k OD ml U 1000 1 )/(???=酶活力 n :稀释倍数; K :曲线斜率; T :反应时间,min ; 1000:mg 换算成ug. 以下是近期所做的实验结果: 葡萄糖标准曲线 两种产纤维素酶细菌不同测试结果
测定结果 实验结论:从以上几种对酶液的处理方法来看,183的酶活要比R2高,两种菌都是以胞外酶为主。目前尚没找到有关于加缓冲溶液并且超声破碎的文献,所得测量结果与前面三种方法均不符,这一步需另外探索。 根据《纤维素酶活力测定条件研究》(夏服宝等,《饲料工业》2005年第26卷第16期)和《影响纤维素酶活力测定的几个因素》(刘妙莲等,中国食品发酵工业研究所)这两篇文献,实验室可先从底物浓度、温度、DNS用量、显色时间以及对菌体的超声破碎时间这几方面进行探索,进而优化实验方法。 刚果红染色法:常用的刚果红染色法有两种, 一种是先培养微生物,再加入刚果红进行颜色反应,另一种是在倒平板 时就加入刚果红。方法一在长出茵落的培养基上,覆盖质量浓度为1 mg /mI。的CR溶液,10~15 min后,倒去CR溶液,加入物质的量浓度为l mol/I。的NaCI溶液,15 min后倒掉NaCl溶液,此时,产生纤维素酶的 茵落周围将会出现透明圈。 方法二配制质量浓度为10 mg/mI。的CR溶液,灭菌后,按照每200 mI。培养基加入1 mI。的比例加入CR溶液,混匀后倒平板。等培养基上长 出茵落后,产生纤维素酶的菌落周围将会出现明显的透明圈。 两种刚果红染色法的比较刚果红在筛选纤维素分解菌上的应用已经 有超过20年的历史,课本中给出了两种方法。 方法一是传统的方法,缺点是操作繁琐,加入刚果红溶液会使菌落之间 发生混杂;其优点是这样显示出的颜色反应基本上是纤维素分解菌的作用。 方法二的优点是操作简便,不存在菌落混杂问题,缺点是由于在纤维素 粉和琼脂、土豆汁中都含有淀粉类物质,可以使能够产生淀粉酶的微生物出
化学纤维质量指标及其检测方法
化学纤维质量指标及其检测方法 一:纤维长度 1.名义长度:切断长度:棉型纤维(30—40mm);毛型纤维(70—150mm);中长纤维(51—65mm)。 超长纤维:长度超过一定界限的短纤维 倍长纤维:长度超过名义长度2倍及以上 2.长度偏差率:长度偏差率=,反映短纤维长度均匀性 二:细度(线密度、纤度) 1.定义:纤维粗细程度 2.表示法: (1)公制支数Nm:1克重的纤维所具有的长度米数;Nm↑→纤维越细 (2)旦Dn:9000米长的纤维所具有的重量克数;Dn↑→纤维越粗 (3)特Tex:1000米长的纤维所具有的重量克数;Dn↑→纤维越粗 三:吸湿性: 1.定义:标准温湿度(20℃、65%相对湿度)下,纤维吸收或放出气态水的能力; 2.表示法:回潮率、含湿率 3.纤维吸湿原因: (1)纤维大分子结构(亲水基团) (2)纤维结晶度 (3)纤维表面吸湿 4.大小:羊毛>粘胶>麻、蚕丝>棉>醋酯>维纶、锦纶>腈纶>涤纶>氯纶、丙纶5.增加吸湿方法: (1)化学改性:大分子上引入亲水基 (2)物理改性:纤维中造成有规律的毛细孔 (3)表面处理: 四:密度: 1.大小:氨纶>粘胶>麻>涤纶、蚕丝>棉、羊毛>维纶>腈纶>锦纶>丙纶 五:热收缩: 1.定义:受热条件下,纤维形态尺寸的收缩,温度降低后不可逆 2.表示法:沸水收缩率、热空气收缩率、过热蒸汽收缩率 六:拉伸性能: 1.断裂强度cN/tex: (1)绝对强度:N或cN;纤维断裂时承受的最大负荷
(2)强度极限:cN/cm2 (3)相对强度:cN/tex; 麻、锦纶、丙纶>涤纶>维纶>腈纶、棉、蚕丝>粘胶>羊毛、氨纶 (4)湿强度:润湿下的强度;回潮率↑→湿强<干强(合成纤维与再生纤维的区别) (5)影响:断裂强度↑→断头↓→绕辊↓ 2.断裂伸长%:应力 (1)定义:拉伸至断裂时试样产生的伸长P (2)表示法:绝对伸长、相对伸长(绝对伸长/试样长度) (3)影响:断裂伸长↑→手感柔软↑、毛丝↓、断头↓→应变% →织物变形↑→→→→→→→→→→10—30%为佳 3.初始模量cN/tex: (1)定义:试样在小负荷(1%伸长)下变形的难易(材料刚性)——应力应变曲线初始一段直线的斜率 (2)影响:纤维柔性↓、结晶度↑、取向度↑→初始模量↑→刚性↑→织物变形↓、织物挺括、不易起皱 (3)大小:涤纶>腈纶、维纶、粘胶>丙纶>锦纶 4.断裂功、断裂比功、功系数: (1)定义:材料拉伸至断裂时外力所做的功(负荷伸长曲线下的面积) (2)断裂比功:单位长度或单位线密度的试样断裂时外力所做的功(应力应变曲线下的面积) (3)功系数:负荷伸长曲线下的面积与断裂伸长和断裂强度乘积之比 (4)表征:三者↑→纤维耐冲击↑、耐磨↑、韧性↑ 5.屈服点、屈服应力、屈服应变: (1)屈服点:拉伸曲线中起始一段直线向延伸区过渡的转折点P (2)影响:屈服点以前:纤维形变(弹性形变——可恢复); 屈服点以后:纤维形变(塑性形变——永久性变); 屈服点高→难产生塑性形变→织物尺寸稳定性 6.回弹性: (1)定义:材料在外力作用(拉伸或压缩)产生形变;外力去除后,恢复原状的能力 (2)表示法:一次负荷回弹性质(回弹率、弹性功);多次负荷回弹性质 (3)影响:回弹性↑→织物抗皱、挺括 氨纶>锦纶>涤纶>腈纶>粘胶 七:耐疲劳性: 1.定义:纤维耐多次变形性(应力循环次数) 2.影响:纤维弹性↑→应力循环次数↑→耐疲劳性↑(锦纶)
冻干人纤维蛋白原说明书
冻干人纤维蛋白原说明书 【批准文号】 国药准字S1******* 【中文名称】 冻干人纤维蛋白原 【产品英文名称】 Human Fibrinogen, Freeze Dried 【生产企业】 上海生物制品研究所 【功效主治】 1.先天性纤维蛋白原减少或缺乏症。 2.获得性纤维蛋白原减少症:严重肝 脏损伤;肝硬化;弥散性血管内凝血;产后大出血和因大手术、外伤或内出血等引起的纤维蛋白原缺乏而造成的凝血障碍。 【化学成分】 主要组成成分:人纤维蛋白原。 【药理作用】 在凝血过程中,纤维蛋白原经凝血酶酶解变成纤维蛋白,在纤维蛋白稳定因子(FXIII)作用下,形成坚实纤维蛋白,发挥有效的止血作用。 【药物相互作用】 不可与其他药物同时合用。 【不良反应】 一般无不良反应,仅少数过敏体质患者会出现过敏反应,严重反应者应采取应急处理措施。 【禁忌症】 在严格控制适应症的情况下,无已知禁忌症。 【产品规格】 0.5g 【用法用量】 用法:使用前先将本品及灭菌注射用水预温至30~37℃,然后按瓶签标示量注入预温的灭菌注射用水,置30~37℃水浴中,轻轻摇动使制品全部溶解(切忌剧烈振摇以免蛋白变性)。用带有滤网装置的输液器进行静
脉滴注。滴注速度一般以每分钟60滴左右为宜。 用量:应根据病情及临床检验结果决定,一般首次给1~2g,如需要可 遵照医嘱继续给药。 【贮藏方法】 应严格保存于10℃以下避光干燥处。效期:在瓶签标明的有效期内使用。【注意事项】 1 本品专供静脉输注。 2 本品溶解后为澄清略带乳光的溶液,允许有少量细小的蛋白颗粒存在, 为此用于输注的输血器应带有滤网装置,但如发现有大量或大块不溶物 时,不可使用。 3 在寒冷季节溶解本品或制品刚从冷处取出温度较低的情况下,应特别注 意先使制品和溶解液的温度升高到30~37℃,然后进行溶解。温度过低 往往会造成溶解困难并导致蛋白变性。 4 本品一旦溶解应尽快使用。 招商代理信息 药店名称药店地址药店联系方式更新时间 冻干人纤维蛋白原网友点评 查看更多评论
范氏洗涤剂法-木质纤维素测定标准方法
原理: 采用范氏(Van Soest)的洗涤纤维分析法测定中性洗涤纤维(NDF)和酸性洗涤纤维(ADF)原理: 植物性饲料经中性洗涤剂煮沸处理,不溶解的残渣为中性洗涤纤维,主要为细胞壁成分,其中包括半纤维素、纤维素、木质素和硅酸盐。植物性饲料经酸性洗涤剂处理,剩余的残渣为酸性洗涤纤维,其中包括纤维素、木质素和硅酸盐。酸性洗涤纤维经72%硫酸处理后的残渣为木质素和硅酸盐,从酸性洗涤纤维值中减去72%硫酸处理后的残渣为饲料的纤维素含量。将72%硫酸处理后的残渣灰化,在灰化过程中逸出的部分为酸性洗涤木质素(ADL)的含量。 溶剂配制: 中性洗涤剂(3%十二烷基硫酸钠):准确称取18.6g乙二胺四乙酸二钠(EDTA,C10H14O8Na2?2H2O,分析纯)和6.8g硼酸钠(Na2B4O7?10H2O,分析纯)放入烧杯中,加入少量蒸馏水,加热溶解后,再加入30g十二烷基硫酸钠(C12H25NaO4S,分析纯)和10ml乙二醇乙醚(C4H10O2,分析纯);再称取4.56 g无水磷酸氢二钠(Na2HPO4,分析纯)置于另一烧杯中,加入少量蒸馏水微微加热溶解后,倒入前一个烧杯中,在容量瓶中稀释至1000ml,其中pH 值约为6.9~7.1(pH值一般勿需调整);1N硫酸:量取约27.87 ml浓硫酸(分析纯,比重1.84,98%),徐徐加入已装有500ml 蒸馏水的烧杯中,冷却后注入1000ml容量瓶定容,标定;酸性洗涤剂(2%十六烷三甲基溴化铵):称取20g十六烷三甲基溴化铵(CTAB,分析纯)溶于1000ml1N硫酸,必要时过滤; 操作步骤: 准确称取1.0000g样品(通过40目筛)置于直筒烧杯中,加入100 ml 酸性洗涤剂和数滴十氢化萘及0.5g无水亚硫酸钠。将烧杯套上冷凝装置于电炉上,在5~10min内煮沸,并持续保持微沸60min。趁热用已知重量的玻璃坩埚抽滤,并用沸水反复冲洗玻璃坩埚及残渣至滤液呈中性为止。用少量丙酮冲洗残渣至抽下的丙酮液呈无色为止,并抽净丙酮。将玻璃坩埚置于105℃烘箱中烘2h后,在干燥器中冷却30 min称重,直称至恒重。 酸性洗涤木质素和酸不溶灰分(AIA)测定将酸性洗涤纤维加入72%硫酸,在20℃消化3h后过滤,并冲洗至中性。消化过程中溶解部分为纤维素,不溶解的残渣为酸性洗涤木质素和酸不溶灰分,将残渣烘干并灼烧灰化后即可得出酸性洗涤木质素和酸不溶灰分的含量。 结果计算: 中性洗涤纤维含量的计算:NDF(%)=(W1-W2)/ W×100 式中: W1—玻璃坩埚和NDF重(g)W2—玻璃坩埚重(g)W—试样重(g)酸性洗涤纤维含量的计算:ADF(%)=(G1-G2)/G×100 式中: G1—玻璃坩埚和ADF重(g)G2—玻璃坩埚重(g)W—试样重(g)
土壤纤维素酶活性测定(3,5- 二硝基水杨酸比色法)
土壤纤维素酶活性测定(3,5-二硝基水杨酸比色法) 一、原理 纤维素是植物残体进入土壤的碳水化合物的重要组分之一。在纤维素酶作用下,它的最初水解产物是纤维二糖,在纤二糖酶作用下,纤维二糖分解成葡萄糖。所以,纤维素酶是碳素循环中的一个重要的酶。纤维素酶解所生成的还原糖与?3,5-二硝基水杨酸反应而生成橙色的3-氨基-5-硝基水杨酸。颜色深度与还原糖量相关,因而可 用测定还原糖量来表示蔗糖酶的活性。 二、试剂 1)甲苯 2)1%羧甲基纤维素溶液:1g羧甲基纤维素钠,用50%的乙醇溶至100ml。 3)pH5.5醋酸盐缓冲液: 0.2mol/L醋酸溶液11.55ml95%冰醋酸溶至1L; 0.2mol/L醋酸钠溶液16.4gC2H3O2Na或27.22gC2H3O2Na.3H2O溶至1L; 取11ml0.2mol/L醋酸溶液和88ml0.2mol/L醋酸钠溶液混匀即成PH5.5醋酸盐缓冲液。4)3,5-二硝基水杨酸溶液:称1.25g二硝基水杨酸,溶于50ml2mol/LNaOH和125ml 水中,再加75g酒石酸钾钠,用水稀释至250ml(保存期不过7天)。 5)葡萄糖标准液(1mg/mL) 预先将分析纯葡萄糖置80℃烘箱内约12小时。准确称取50mg葡萄糖于烧杯中,用蒸馏水溶解后,移至50mL容量瓶中,定容,摇匀(冰箱中4℃保存期约一星期)。 若该溶液发生混浊和出现絮状物现象,则应弃之,重新配制。 三、操作步骤 葡萄糖标准曲线:分别吸1mg/mL的标准葡糖糖溶液0、0.1、0.2、0.4、0.6、0.8mL 于试管中,再补加蒸馏水至1mL,加DNS溶液3ml混匀,于沸腾水浴中加热5min,
常用纤维的检验方法
常用纖維的檢驗方法1、利用手觸摸質感的辨別 2、利用燃燒來鑑別
成分布料之中英對照
基本的天然纖維: 棉---cotton 羊毛---wool 蠶絲---silk 麻--- leaf fiber 較長見的人造纖維: 聚酯纖維,學名: PET fiber (polyester fiber),俗名:特多龍(Tetoron,日本商標名) 聚醯胺纖維,學名: PA fiber(polyamide fiber),俗名:尼龍(Nylon,美國商標名) 聚丙烯腈,學名: PAN fiber(polyacrylonitrile fiber),俗名:開司米龍(Cashmilon,日本商標名) 聚乙烯醇纖維,學名: PVA fiber (polyvinyl alcohol fiber),俗名:維尼龍(Vinylon,日本商標名) 聚丙烯纖維,學名: PP fiber (polypropylene fiber)
聚氯乙烯纖維,學名: PVC fiber (polyvinyl chloride fiber) 聚乙烯纖維,學名: PE fiber (polyethylene fiber) 聚氨基甲酸酯纖維,學名: PU fiber (polyurethane fiber),俗名: 萊卡(Lycra,美國杜邦商標名); Spandex(美國商標名) 粘膠纖維---viscose fiber, viscose rayon 醋酸纖維---acetate fiber 三醋酸纖維---triacetate fiber PBT, PTT, PLA等許多的新興纖維材料: 尼龍nylon 彈性纖維lycra 聚酯纖維polyester-----以上都是人造纖維man-made fiber 鏍瑩rayon-----天然纖維加工而成
人纤维蛋白原
人纤维蛋白原 【药品名称】 通用名称:人纤维蛋白原 英文名称:Human Fibrinogen 【成份】 主要组成成分:人纤维蛋白原。 【适应症】 1.先天性纤维蛋白原减少或缺乏症。 2.获得性纤维蛋白原减少症:严重肝脏损伤;肝硬化;弥散性血管内凝血;产后大出血和因大手术、外伤或内出血等引起的纤维蛋白原缺乏而造成的凝血障碍。 【用法用量】 用法:使用前先将本品及灭菌注射用水预温至30~37℃,然后按瓶签标示量注入预温的灭菌注射用水,置30~37℃水浴中,轻轻摇动使制品全部溶解(切忌剧烈振摇以免蛋白变性)。用带有滤网装置的输液器进行静脉滴注。滴注速度一般以每分钟60滴左右为宜。用量:应根据病情及临床检验结果决定,一般首次给1~2g,如需要可遵照医嘱继续给药。 【不良反应】 一般无不良反应,仅少数过敏体质患者会出现过敏反应,严重反应者应采取应急处理措施。【禁忌】 在严格控制适应症的情况下,无已知禁忌症。 【注意事项】 1本品专供静脉输注。2本品溶解后为澄清略带乳光的溶液,允许有少量细小的蛋白颗粒存在,为此用于输注的输血器应带有滤网装置,但如发现有大量或大块不溶物时,不可使用。
3在寒冷季节溶解本品或制品刚从冷处取出温度较低的情况下,应特别注意先使制品和溶解液的温度升高到30~37℃,然后进行溶解。温度过低往往会造成溶解困难并导致蛋白变性。4本品一旦溶解应尽快使用。 【特殊人群用药】 儿童注意事项: 尚无研究资料 妊娠与哺乳期注意事项: 对孕妇及哺乳期妇女用药应慎用,只有经过利弊权衡后认为患者确有必要使用时方可使用,并在医师指导和严密观察下使用。 老人注意事项: 尚无研究资料 【药物相互作用】 不可与其他药物同时合用。 【药理作用】 在凝血过程中,纤维蛋白原经凝血酶酶解变成纤维蛋白,在纤维蛋白稳定因子(FXIII)作用下,形成坚实纤维蛋白,发挥有效的止血作用。 【贮藏】 应严格保存于10℃以下避光干燥处。效期:在瓶签标明的有效期内使用。 【有效期】 24个月 【批准文号】 国药准字S2*******
木质纤维素预处理技术
木质纤维素预处理技术 单独某一种预处理方法并非对任何原料都有较好的效果。目前的木质纤维素预处理方法有很多种,可分为物理法、化学法、物理化学法、分步组合法和生物法几大类。 1物理方法 物理方法预处理主要是增大比表面积、孔径,降低纤维素的结晶度和聚合度。常用的物理方法包括机械粉碎、机械挤出、高能辐射等[1]。 1.1机械粉碎 机械粉碎即将物料切碎、碾磨处理成10~30mm或0.2~2mm的颗粒,比表面积增高,结晶度、聚合度降低,可及度增加,有利于提高基质浓度和酶解效率,但不能去除木质素及半纤维素。 粉碎分为干粉碎、湿粉碎,包括球磨、盘磨、辊磨、锤磨、胶体磨、机械挤出等,胶体磨适用湿物料,而球磨对干、湿物料都适合。 由于粒径与能耗相关,经济性不高,效果单一,故粉碎常与其他方法相互补充[2]。研究表明,甘蔗渣、麦秆经球磨与盘磨粉碎后酶解率及乙醇得率均显著提高;经宽角X射线衍射分析,球磨主要通过降低结晶度改善酶解,而盘磨则主要依靠去纤维化。机械挤出是一种应用前景良好的预处理新技术,处理效果受到设备尺寸及参数的影响。物料通过挤出器时在热、混合和剪切作用下引起物理、化学性质的改变,依靠螺旋挤出转速及温度打破木质纤维结构,引发去纤维化、纤维化效应,缩短纤维长度,改善了酶对底物的可及性[1]。 1.2高能辐射 高能辐射是用高能射线如电子射线、γ射线对原料进行预处理,可使纤维素聚合度下降,降解为小纤维片段、寡葡聚糖甚至纤维二糖,使结构松散,打破纤维素晶体结构,增加反应活性。 采用γ射线辐照处理秸秆,可使纤维素酶解转化率提高至88.7%。KIM等[3]证明电子束照射确实能增加纤维素的酶解率:稻秆用80kGy、0.12mA、1MeV的电子束照射后酶解葡萄糖得率达52.1%,比直接酶解的22.6%增加近30%。 2化学方法 2.1酸预处理 酸法是研究得最早、最深入的化学预处理方法,分为低温浓酸法和高温稀酸法。低温浓酸(如72%H2SO4、41%HCl、100%TFA)处理效果通常优于高温稀酸,能溶解大部分纤维素和半纤维素,但是其毒性、腐蚀性及危害大,需要特殊的防腐反应器,酸回收难度较大,后期中和需消耗大量的碱,因此应用受到限制[2]。稀酸法是目前较常用而成熟的方法之一,生物质在较高温度(如140~190℃)和低浓度酸(如0.1%~1%硫酸)作用下,可实现较高的反应速率,半纤维素组分几乎100%除去,纤维素的平均聚合度下降,反应能力增大,酶水解率显著提高,但去除木质素不很有效。稀酸法因其效果好、污染少成为研究的热点并获得了较大进展,如美国国家可再生能源实验室(NREL)开发了比较成熟的稀硫酸预处理—酶解发酵工艺并建成了中试装置。稀酸法最大的缺点是产生副产物如甲酸、乙酸、糠醛、羟甲基糠醛、糖醛酸、己糖酸等,即影响酶解又抑制微生物生长和发酵。稀酸法可在较高温度(180℃)处理较短时间(5min)也可在较低温度(120℃)处理较长时间(30~90min),温度和酸浓度越剧烈预处理效果越好,但抑制产物会增加。 CHEN等[4]提出“半纤维素/纤维素分离-分步发酵”(XCFSF)工艺路线,玉米芯经稀硫酸预处理后木糖得率为78.4%,纤维素回收率为96.81%,水解木糖和纤维素残渣酶解后的糖液发酵乙醇,酶解残渣同步糖化发酵(SSF),最终将70.4%的半纤维素和89.77%的纤维素转化为乙醇。酸可以用硫酸、硝酸、盐酸、磷酸、碳酸等无机酸,也可用乙酸、丙酸、草酸等有机酸。将蔗渣在高于160℃条件下经稀磷酸预处理,可有效水解半纤维素为单糖,且副反应少[5]。用80%乙酸、0.92%硝酸在120℃处理麦秆20min,81%的半纤维素和92%的木质素被水解或
纤维素酶的检测方法
纤维素CMC酶、FPA酶和半纤维素酶测定 1.纤维素CMC酶 1.0标题 用3.5一二硝基水杨酸法测定纤维素CMC酶活性单位。 2.0范围 生产分析和质量控制部门适用。 3.0原理 纤维素CMC酶(EC3.2.1.4)水解羧基纤维素分子中β-1.4葡萄糖苷键,释放出的还原糖(以葡萄糖计)与3.5二硝基水杨酸(DNS)反应,产生颜色变化,这种颜色变化与释放还原糖(以葡萄糖计)的量成正比关系,即与酶样品中的酶活性成正比。通过在550nm的光吸收值查对标准曲线(以葡萄糖为标准物)可以确定还原糖产生的量,从而确定出酶的活力单位。 4.0试剂 4.1无水醋酸钠(分析纯) 4.2冰醋酸(分析纯) 4.3 3.5-二硝基水杨酸 4.4无水葡萄糖 4.5四水酒石酸钾钠(分析纯) 4.6氢氧化钠(分析纯) 4.7重蒸苯酚(分析纯) 4.8无水亚硫酸钠(分析纯) 4.9叠氮化钠(分析纯) 4.10羧甲基纤维素钠 5.0仪器 5.1水浴锅(恒温)50±1℃ 5.2电热干燥箱80±1℃ 5.3 722型分光光度机计 5.4分析天平感量0.1㎎ 5.5一级玻璃制品 5.6电冰箱 6.0试剂的准备 6.1乙酸-乙酸钠缓冲溶液(PH=4.8) 溶液A:量取冰醋酸6ml,定容至1000ml,制成0.1M醋酸钠溶液。 溶液B:称取8.2g醋酸钠,溶解后容至1000ml,制成0.1M醋酸钠溶液。 以A:B=4:6的比例混合,低温冷藏备用。 6.2 DNS试剂: 溶液A:称分析纯NaOH 104g溶于1300ml水中,加入30g分析纯3.5一二硝基水杨酸。 溶液B:称分析纯酒石酸钾钠910g,溶于2500ml热水中,再称取25g重蒸苯酚和25g无水亚硫酸钠加入酒石酸钾钠溶液。 将A、B溶液混合,定容至5000ml,贮存于棕色瓶中,暗处放置一星期后可使用。 6.3 CMC溶液:用羧甲基纤维素钠(CMC)以PH4.8醋酸缓冲液配成1%的溶液。 7.0标准曲线制作: 7.1无水葡萄糖80℃烘干至恒重。 7.2准确称取1.000g溶于1000ml水中,加10mg叠氮化钠防腐,4℃冷藏备用。 7.3标准葡萄糖曲线制作
纤维素酶活力测定方法_张瑞萍
测试与标准 纤维素酶活力测定方法 张瑞萍 南通工学院(226007) 摘 要 用DN S 为显色剂,分别以滤纸和CM C 为底物,以滤纸糖酶活性(FP A )和羧甲基纤维素酶活性(CM C a se )表征纤维素酶活力。确定酶活测定用波长为530nm,参比溶液应为失活酶、底物和DN S 等共热的反应物;比较了两种底物的酶活力测定方法。结果表明,CM C a se 比FP A 高,说明酶对水溶性底物有较高的活力,也表明吸附对酶的活性部位与纤维素分子链段的结合及催化均有很大影响;对于不同牌号的纤维素酶,织物的酶减量率与CM C 酶活力关系密切。 叙 词: 测试 纤维素酶 活度中图分类号: TS197 纤维素酶是多组分复合物,各组分的底物专一性不同。纤维素酶作用的底物比较复杂,反应产物不同,致使纤维素酶活力测定方法很多,各国的方法亦不统一。我们选择滤纸、CM C 为底物,原理系利用纤维素酶催化水解纤维素,产生纤维多糖、二糖及葡萄糖等还原糖,与显色剂反应,求出还原糖的浓度,间接求出酶的活力。由不同底物测得的酶活力分别称作FPA (滤纸糖酶活力)和CM C ase (羧甲基纤维素酶酶活力)。本文分析确定酶活力测定的主要条件,比较两种底物的酶活力测定方法的结果,探讨纤维素酶活力与织物减量率的关系,为酶在生产中的利用提供依据。 1 实验方法 1.1 化学药品、材料 纤维素酶(工业品),DNS 试剂(自配),冰醋酸,醋酸钠,葡萄糖(均为分析纯),滤纸(定性),羧甲基纤维素酶CM C (试剂级),纯棉针织物半制品(南通针织厂)。 1.2 FPA 滤纸酶活力和CMC 酶活力的测定 取适当稀释的酶液,分别以滤纸或1%的CM C 溶液为底物,于50℃恒温水解反应1h ;然后加入显色剂DNS,沸水浴中煮沸5min;再加入蒸馏水,于530nm 测定吸光度OD 值。 酶活可定义为:每毫升酶液1min 产生1mg 葡萄糖为一个单位( )。 1.3 针织物酶减量率的测定 将酶处理前后的试样在烘箱中105℃烘至恒重。减量率= 处理前织物干重-处理后织物干重 处理前织物干重 ×100% 2 结果与讨论 2.1 显色剂的选择 选用DNS ,在碱性条件下与还原糖反应,生成有色化合物,用分光光度计比色,确定低分子糖含量。 碱性条件下DNS 与还原糖共热反应如下: O 2N OH O 2N CO OH +还原糖 H 2N OH CO OH O 2N DN S(黄色) 3-氨基-5-硝基水杨酸(棕红色) 生成的棕红色氨基化合物系比色法测定基础。2.2 最大吸收波长的确定 选取490~580nm 波长对显色液进行比色。由图1可知,不同浓度的葡萄糖溶液在490~500nm 处有最大吸收,DNS 在此波长下也有较明显的吸收。为了排除DNS 的干扰,选择在波长 530nm 处进行测定,此波长下的葡萄糖吸收虽有所降低,然而符合“吸收最大、干扰最小”的原则。 图1 D NS 与葡萄糖的吸收曲线 2.3 底物及酶本身含糖量的影响 在实验过程中发现,底物特别是滤纸,也含有一定的还原糖,在碱性的DNS 试剂中也会发色。而且,试验所用的纤维素酶是一种工业级的复合酶,品种不同,其本身含糖量也不同。为了排除这类还原糖的干扰,参比溶液取失活后的酶、底物、DNS 等共热的反应物。2.4 葡萄糖标准曲线 用不同浓度的葡萄糖溶液作为标准溶液,与DNS 共热反应显色后,测出其吸光度OD 值(见图2)。标准曲线的线性相关系数R 2为0.9991(见图2),线性相当好,可以用于酶活力的测定。 38 印 染(2002No .8) www .cdfn .com .cn
