气相色谱方法验证报告

气相色谱方法验证报告
本文通过一系列的验证分析,利用数理统计方法,计算得到了GB/T5750.8-2006方法的三氯甲烷、四氯化碳最低检出限和定量检出限、标准曲线相关系数、精密度和加标回收率。
一、方法原理
样品液经前处理后上Clarus680分析测试。绘制标准曲线,对待测液进行定性定量分析,测试浓度。
二、仪器设备与化学试剂
1. 气相色谱仪;
2. 电子捕获检测器
3. 高纯氮气(99.999%);
4. 纯水:色谱检验无待测组分;
5. 标准物质:10.0mg/L(三氯甲烷);1.0mg/L(四氯化碳)
三、简要操作步骤
1.标准曲线绘制
取上述2种标准物质用纯水配成1ug/L、2ug/L、5ug/L、10ug/L、20ug/L(三氯甲烷);
0.1ug/L、0.2ug/L、0.5ug/L、1.0ug/L、2.0ug/L(四氯化碳)混合标准工作液系列,绘制标准曲线。
2. 测定
方法检出限用空白加标0.2ug/L(三氯甲烷)、0.1ug/L(四氯化碳)混合标准工作液测试;精密度用空白加标5ug/L(三氯甲烷)、0.5ug/L(四氯化碳)混合标准工作液测试,线性范围用1ug/L、2ug/L、5ug/L、10ug/L、20ug/L(三氯甲烷);0.1ug/L、0.2ug/L、0.5ug/L、1.0ug/L、2.0ug/L(四氯化碳)混合标准工作液测试;空白加标回收率分别在限量附近、限量以上2个水平测试。
四、分析方法验证程序
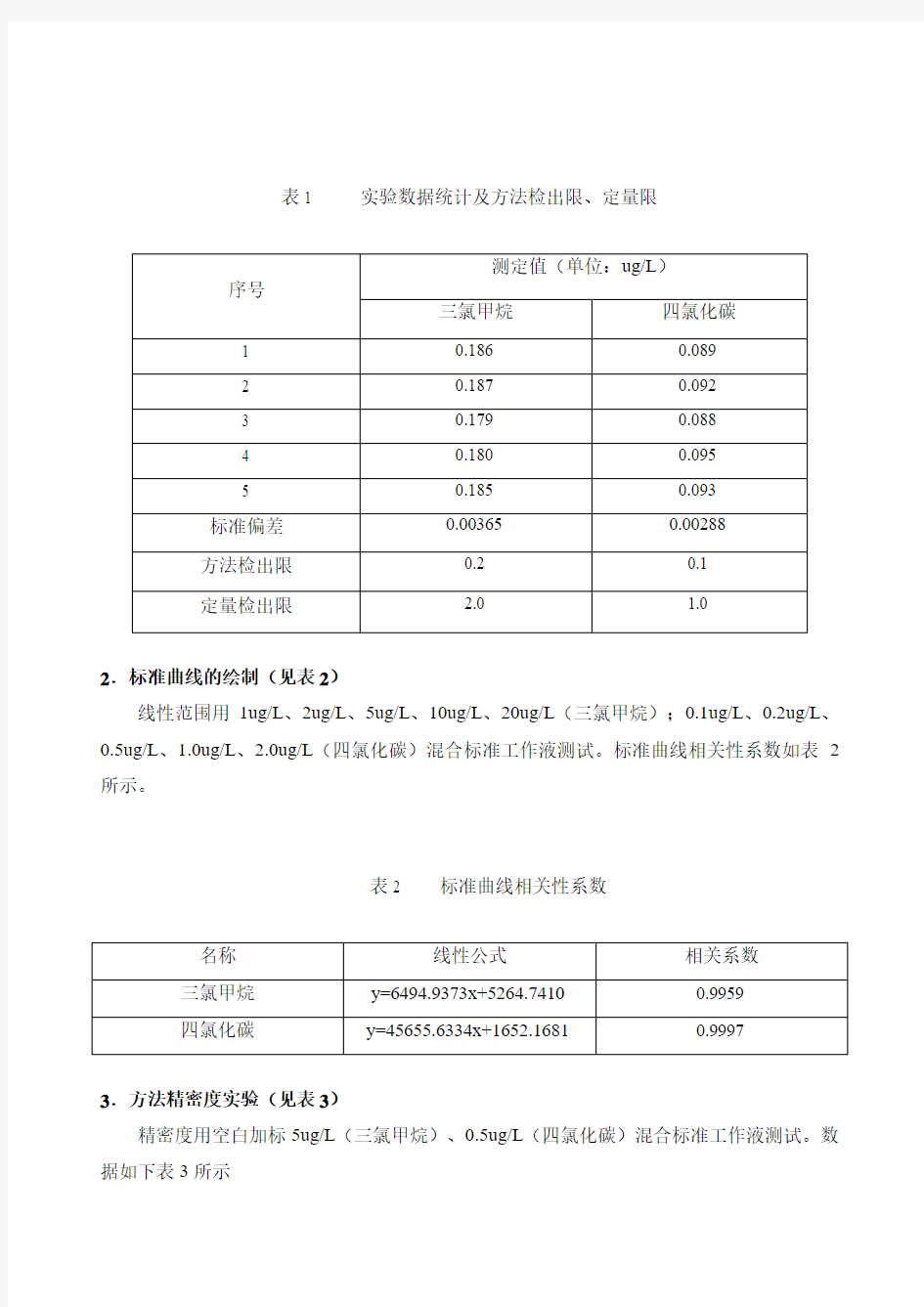
1.方法检出限和定量限:因标准方法给出的检出限为0.2ug/L(三氯甲烷)、0.1ug/L(四氯化碳),故以检出限浓度配成实际样品进样,结果见表1。以检出限10倍为定量限配制实际样品进样结果见表1
表1 实验数据统计及方法检出限、定量限
2.标准曲线的绘制(见表2)
线性范围用1ug/L、2ug/L、5ug/L、10ug/L、20ug/L(三氯甲烷);0.1ug/L、0.2ug/L、0.5ug/L、1.0ug/L、2.0ug/L(四氯化碳)混合标准工作液测试。标准曲线相关性系数如表2所示。
表2 标准曲线相关性系数
3.方法精密度实验(见表3)
精密度用空白加标5ug/L(三氯甲烷)、0.5ug/L(四氯化碳)混合标准工作液测试。数据如下表3所示
表3 精密度实验
4.准确度实验
以前项精密度实验测定数据最大值为基础,做准确度分析。
表4 准确度实验
5.空白加标回收实验(见表5)
在限量附近和限量以上两个水平做2个加标回收率实验,数据如下表5所示。
表5 加标回收率
五、评价与验证结论
1.评价
1.1 方法检出限和定量限评价
本方法三氯甲烷的检出限为0.2ug/L,定量限为2.0ug/L;四氯化碳的检出限为0.1ug/L,定量限为1.0ug/L;
参考GB/T 5750.5-2006《生活饮用水标准检验方法无机非金属指标》本方法测定的检测限符合该要求。
1.2 标准曲线评价
本方法三氯甲烷的标准曲线相关系数为0.9959,四氯化碳的标准曲线相关系数为0.9997,参考GB/T27404-2008《实验室质量控制规范食品理化检测》对标准曲线的要求,本方法标准曲线相关系数均大于0.99,符合该要求。
1.3 精密度评价
本方法三氯甲烷的变异系数为 3.94%,四氯化碳的变异系数为 3.34%。参考GB/T27404-2008《实验室质量控制规范食品理化检测》对精密度的要求,本方法的精密度均小于5.3%,符合该要求。
1.4 准确度评价
本方法三氯甲烷的偏差为6.6%,四氯化碳的偏差为4.0%,参考GB/T27404-2008《实验室质量控制规范食品理化检测》对准确度的要求,本方法的偏差均小于15%,符合该要求。
1.5 加标回收率评价
参考GB/T27404-2008《实验室质量控制规范食品理化检测》对回收率的要求,本方法的加标回收率均在90%-110%之间,符合该要求。
2.结论
通过对上述各项指标的验证,表明该项目可在本实验室开展。
气相色谱法实验报告记录
气相色谱法实验报告记录
————————————————————————————————作者:————————————————————————————————日期:
实验五—气相色谱法实验 姓名:张瑞芳 学号:2013E8003561147 班级:化院413班 培养单位:上海高等研究院 指导教师:李向军 组别:2013年12月30日第二组
气相色谱法实验 一、实验目的 1.了解气相色谱仪的各部件的功能。 2.加深理解气相色谱的原理和应用。 3.掌握气相色谱分析的一般实验方法。 4.学会使用FID气相色谱对未知物进行分析。 二、实验原理 1.气相色谱法基本原理 气相色谱的流动向为惰性气体,气-固色谱法中以表面积大且具有一定活性的吸附剂作为固定相。当多组分的混合样品进入色谱柱后,由于吸附剂对每个组分的吸附力不同,经过一定时间后,各组分在色谱柱中的运行速度也就不同。吸附力弱的组分容易被解吸下来,最先离开色谱柱进入检测器,而吸附力最强的组分最不容易被解吸下来,因此最后离开色谱柱。如此,各组分得以在色谱柱中彼此分离,顺序进入检测器中被检测、记录下来。气相色谱仪器框图如图1所示: 图1.气相色谱仪器框图 仪器均由以下五个系统组成:气路、进样、分离、温度控制、检测和记录系统。 2.气相色谱法定性和定量分析原理 在这种吸附色谱中常用流出曲线来描述样品中各组分的浓度。也就是说,让
分离后的各组分谱带的浓度变化输入换能装置中,转变成电信号的变化。然后将电信号的变化输入记录器记录下来,便得到如图2的曲线。它表示组分进入检测器后,检测器所给出的信号随时间变化的规律。它是柱内组分分离结果的反映,是研究色谱分离过程机理的依据,也是定性和定量的依据。 图2.典型的色谱流动曲线 3.FID的原理 本次试验所用的为氢火焰离子化检测器(FID),它是以氢气和空气燃烧的火焰作为能源,利用含碳有机物在火焰中燃烧产生离子,在外加的电场作用下,使离子形成离子流,根据离子流产生的电信号强度,检测被色谱柱分离出的组分。 三.实验试剂和仪器 (1)试剂:甲醇、异丙醇、异丁醇 (2)仪器:气相色谱仪带氢火焰离子化检测器(GC-2014气相色谱仪); 氢-空发生器(SPH-300氢气发生器)、氮气钢瓶; 色谱柱; 微量注射器。 四.实验步骤 1.打开稳定电源。 2.打开N2钢瓶(减压阀),以N2为载气,开始通气,检漏;调整柱前压约为 0.12MPa。
气相色谱中的内标法与外标法
气相色谱中的内标法与外标法 内标法与外标法 一、内标法 什么叫内标法?怎样选择内标物? 内标法是一种间接或相对的校准方法。在分析测定样品中某组分含量时,加入一种内标物质以校谁和消除出于操作条件的波动而对分析结果产生 的影响,以提高分析结果的准确度。 内标法在气相色谱定量分析中是一种重要的技术。使用内标法时,在样品中加入一定量的标准物质,它可被色谱拄所分离,又不受试样中其它组分峰的干扰,只要测定内标物和待测组分的峰面积与相对响应值,即可求出待测组分在样品中的百分含量。采用内标法定量时,内标物的选择是一项十分重要的工作。理想地说,内标物应当是一个能得到纯样的己知化合物,这样它能以准确、已知的量加到样品中去,它应当和被分析的样品组分有基本相同或尽可能一致的物理化学性质(如化学结构、极性、挥发度及在 溶剂中的溶解度等)、色谱行为和响应特征,最好是被分析物质的一个同 系物。当然,在色谱分析条什下,内标物必须能与样品中各组分充分分离。 需要指出的是,在少数情况下,分析人员可能比较关心化台物在一个复杂过程中所得到的回收率,此时,他可以使用一种在这种过程中很容易被完全回收的化台物作内标,来测定感兴趣化合物的百分回收率,而不必遵循以上所说的选择原则。
在使用内标法定量时,有哪些因素会影响内标和被测组分的峰高或峰面积的比值? 影响内标和被测组分峰高或峰面积比值的因素主要有化学方面的、色谱方面的和仪器方面的三类。 由化学方面的原因产生的面积比的变化常常在分析重复样品时出现。 化学方面的因素包括: 1、内标物在样品里混合不好; 2、内标物和样品组分之间发生反应, 3、内标物纯度可变等。 对于一个比较成熟的方法来说,色谱方面的问题发生的可能性更大一些,色谱上常见的一些问题(如渗漏)对绝对面积的影响比较大,对面积比的影响则要小一些,但如果绝对面积的变化已大到足以使面积比发生显著变化的程度,那么一定有某个重要的色谱问题存在,比如进样量改变太大,样品组分浓度和内标浓度之间有很大的差别,检测器非线性等。进样量应足够小并保持不变,这样才不致于造成检测器和积分装置饱和。如果认为方法比较可靠,而色谱固看来也是正常的话,应着重检查积分装置和设置、斜率和峰宽定位。对积分装置发生怀疑的最有力的证据是:面积比可变,而峰高比保持相对恒定, 在制作内标标准曲线时应注意什么? 在用内标法做色话定量分析时,先配制一定重量比的被测组分和内标样品
生物样品定量分析方法验证指导原则
9012 生物样品定量分析方法验证指导原则
1. 范围
准确测定生物基质(如全血、血清、血浆、尿)中的药物浓度,对于药物和 制剂研发非常重要。这些数据可被用于支持药品的安全性和有效性,或根据毒动 学、药动学和生物等效性试验的结果做出关键性决定。因此,必须完整地验证和 记录应用的生物分析方法,以获得可靠的结果。
本指导原则提供生物分析方法验证的要求,也涉及非临床或临床试验样品实 际分析的基本要求,以及何时可以使用部分验证或交叉验证,来替代完整验证。
生物样品定量分析方法验证和试验样品分析应符合本指导原则的技术要求。 应该在相应的生物样品分析中遵守 GLP 原则或 GCP 原则。
2. 生物分析方法验证
2.1 分析方法的完整验证
分析方法验证的主要目的是,证明特定方法对于测定在某种生物基质中分析 物浓度的可靠性。此外,方法验证应采用与试验样品相同的抗凝剂。一般应对每 个物种和每种基质进行完整验证。当难于获得相同的基质时,可以采用适当基质 替代,但要说明理由。
一个生物分析方法的主要特征包括:选择性、定量下限、响应函数和校正范 围(标准曲线性能)、准确度、精密度、基质效应、分析物在生物基质以及溶液 中储存和处理全过程中的稳定性。
有时可能需要测定多个分析物。这可能涉及两种不同的药物,也可能涉及一 个母体药物及其代谢物,或一个药物的对映体或异构体。在这些情况下,验证和 分析的原则适用于所有涉及的分析物。
对照标准物质 在方法验证中,含有分析物对照标准物质的溶液将被加入到空白生物基质 中。此外,色谱方法通常使用适当的内标。 应该从可追溯的来源获得对照标准物质。应该科学论证对照标准物质的适用 性。分析证书应该确认对照标准物质的纯度,并提供储存条件、失效日期和批号。 对于内标,只要能证明其适用性即可,例如显示该物质本身或其相关的任何杂质 不产生干扰。 当在生物分析方法中使用质谱检测时,推荐尽可能使用稳定同位素标记的内 标。它们必须具有足够高的同位素纯度,并且不发生同位素交换反应,以避免结 果的偏差。
1
气相色谱实验报告word精品
气相色谱实验报告 一、实验目的 1、了解气相色谱仪的基本结构及掌握分离分析的基本原理; 2、了解顶空气相色谱法; 3、了解影响分离效果的因素; 4、掌握定性、定量分析与测定的方法。 二、实验原理气相色谱分离是利用上试样中各组分在色谱柱中的气相和固定相间的分配系数不同,当气 化后的试样被载气带入色谱柱进行时,组分就在其中的两相中进行反复多次的分配,由于固定相各个组分的吸附或溶解能力不同,因此各组分在色谱柱中的运行速度就不同。经过 一定的柱长后,使彼此分离,顺序离开色谱柱进入检测器。检测器将各组分的浓度或质量的变化转换成一定的电信号,经过放大后在记录仪上记录下来,即可得到各组分的色谱峰。根据保留时间和峰高或峰面积,便可进行定性和定量的分析。 (1)顶空色谱法及其原理介绍顶空气相色谱是指对液体或固体中的挥发性成分进行气相色谱分析的一种间接测定法,它是在热力学平衡的蒸气相与被分析样品同时存在于一个密闭系统中进行的。这一方法从气相色谱仪角度讲,是一种进样系统,即“顶空进样系统” 。其原理如下: 一个容积为V、装有体积为V o浓度为0)的液体样品的密封容器,在一定温度下达到平衡时,气相体积为Vg,液相体积为Vs,气相样品浓度为Cg,液相中样品浓度为Cs,贝平衡常数K=Cs/Cg 相比3 =Vg/Vs V=Vs+Vg=V o+Vg 又因为是密封容器,所以 C o V o=CoVs=CsVs+CgVg= KCgVs + CgVg C o=KCg+CgVg/Vs=KCg+ 3 Cg=Cg()K+ 3 Cg=C0/(K+ 3 = K'(C 可见, 在平衡状态下, 气相组成与样品原组成为正比关系, 根据这一关系我们可以进行定性和定量分析。(2)顶空色谱法的优点 顶空色谱进样器可与国内外各种气相色谱仪相连接, 它是将液体或固体样品中的挥发性组分直接导入气相色谱仪进行分离和检测的理想进样装置。 它采用气体进样,可专一性收集样品中的易挥发性成分,与液-液萃取和固相萃取相比 既可避免在除去溶剂时引起挥发物的损失, 又可降低共提物引起的噪音, 具有更高灵敏度和分析速度,对分析人员和环境危害小,操作简便,是一种符合“绿色分析化学”要求的分析手段。固相萃取和液相萃取时不可避免地带入共萃取物干扰分析。顶空分析可看成是气相萃
气相色谱仪验证方案
编号:STP-YZ-HY-015-00 检测仪器验证方案 GC-14C气相色谱仪
目录1概述 2验证目的 3验证依据及验证范围 4参与验证的相关部门及其职责 5验证工作小组 6验证内容 6.1安装确认 6.1.1文件资料 6.1.2售后服务 6.1.3消耗性备品备件 6.1.4安装检查 6.2运行确认 6.2.1灵敏度及稳定性测试 6.2.1.1稳定性 6.2.1.2灵敏度 6.3性能确认 6.3.1系统适用性试验: 6.3.2定量重复性试验 7验证结果综合评价: 8偏差说明及措施: 9验证小组人员签字/日期: 10偏差处理及验证总结报 11再验证要求:
1概述 GC-14C 型气相色谱仪为日本岛津分析仪器有限公司生产,是由单片机控制的有较高性价比的气相色谱仪,采用氢焰离子化检测器,可以进行恒温及程序升温操作,适用于本公司所有产品的定量和定性分析。 2验证目的 为了确保使用该仪器检测数据真实可靠,也为了确认该仪器的各项指标能达到该仪器所设计的性能指标,对该仪器进行验证。 3验证依据及适用范围 参照国家技术监督局《实验室气相色谱仪检定规程》及《中国药典》2005版二部附录V E气相色谱法起草本验证方案。本验证方案适用于实验室GC-14C 型气相色谱仪的验证。 4参与验证的相关部门及其职责 4.1验证小组 4.1.1负责验证方案的审批; 4.1.2负责验证数据及结果的审核; 4.1.3负责验证报告的审核; 4.1.4负责验证周期的确认; 4.1.5负责发放验证证书; 4.2工程部 4.2.1负责设备的安装、调试,并做好相应的记录; 4.2.2负责拟定验证周期; 4.2.3负责收集预、安装确认的试验记录; 4.3质量管理部 4.3.1负责对验证参数要求进行确认; 4.3.2负责根据检验结果出具检验报告单; 4.3.3负责仪器、仪表的校验; 4.3.4负责起草设备操作、清洁和维护保养等方面的标准操作规程; 4.3.5负责设备日常的维护保养工作; 4.3.6负责建立设备档案。
药物非临床药代动力学研究技术指导原则
附件5 药物非临床药代动力学研究技术指导原则 一、概述 非临床药代动力学研究是通过体外和动物体内的研究方法,揭示药物在体内的动态变化规律,获得药物的基本药代动力学参数,阐明药物的吸收、分布、代谢和排泄(Absorption, Distribution, Metabolism, Excretion, 简称ADME)的过程和特征。 非临床药代动力学研究在新药研究开发的评价过程中起着重要 作用。在药物制剂学研究中,非临床药代动力学研究结果是评价药物制剂特性和质量的重要依据。在药效学和毒理学评价中,药代动力学特征可进一步深入阐明药物作用机制,同时也是药效和毒理研究动物选择的依据之一;药物或活性代谢产物浓度数据及其相关药代动力学参数是产生、决定或阐明药效或毒性大小的基础,可提供药物对靶器官效应(药效或毒性)的依据。在临床试验中,非临床药代动力学研究结果能为设计和优化临床试验给药方案提供有关参考信息。 本指导原则是供中药、天然药物和化学药物新药的非临床药代动力学研究的参考。研究者可根据不同药物的特点,参考本指导原则,科学合理地进行试验设计,并对试验结果进行综合评价。 本指导原则的主要内容包括进行药物非临床药代动力学研究的 基本原则、试验设计的总体要求、生物样品的测定方法、研究项目(血
药浓度-时间曲线、吸收、分布、排泄、血浆蛋白结合、生物转化、对药物代谢酶活性及转运体的影响)、数据处理与分析、结果与评价等,并对研究中其他一些需要关注的问题进行了分析。附录中描述了生物样品分析和放射性同位素标记技术的相关方法和要求,供研究者参考。 二、基本原则 进行非临床药代动力学研究,要遵循以下基本原则: (一)试验目的明确; (二)试验设计合理; (三)分析方法可靠; (四)所得参数全面,满足评价要求; (五)对试验结果进行综合分析与评价; (六)具体问题具体分析。 三、试验设计 (一)总体要求 1. 受试物 中药、天然药物:受试物应采用能充分代表临床试验拟用样品和/或上市样品质量和安全性的样品。应采用工艺路线及关键工艺参数确定后的工艺制备,一般应为中试或中试以上规模的样品,否则应有充分的理由。应注明受试物的名称、来源、批号、含量(或规格)、保存条件、有效期及配制方法等,并提供质量检验报告。由于中药的特殊性,建议现用现配,否则应提供数据支持配制后受试物的质量稳定性及均匀性。当给药时间较
气相色谱法实验报告
气相色谱定性和定量分析实验报告 班级 姓名 学号: 成绩: 一、实验目的 1.熟悉气相色谱仪的工作原理及操作流程; 2.能够根据保留值对物质进行定性分析; 3.能够对物质进行定量分析 二、实验原理 气相色谱法是一种用以分离、分析多组分混合物极有效的分析方法。它是基于被测组分在两相间的分配系数不同,从而达到相互分离的目的。在混合物分离以后,利用已知物保留值对各色谱峰进行定性是色谱法中最常用的一种定性方法。它的依据是在相同的色谱条件下,同一物质具有相同的保留值,利用已知物的保留时间与未知组分的保留时间进行对照时,若两者的保留时间相同,则认为是相同的化合物。 气相色谱法分离分析醇系物的基本原理是基于醇系物中各组分在气相和固相两相间分配系数的不同。当试样流经色谱柱时被相互分离,被分离组分依次通过检测器时,浓度(或质量)信号被转换为电信号输出到记录仪,获得醇系物的色谱流出曲线(如图1),完全分离时,可依据流出曲线上各组分对应的色谱峰面积进行定量。 色谱分析的定性方法有多种,当色谱条件固定且完全分离时,采用将未知物的保留值与已知纯试剂(标样)的保留值相对照的方法定性较为简单,两者相同或相近即为同一物质。 实际测定可采用相对保留值is r 代替保留值进行定性分析。 M Rs M Ri Rs Ri is t t t t t t r --=='' 式中:t ’Ri ——被测组分的调整保留时间 t ’Rs ——标准物质的调整保留时间 t Ri ——被测组分保留时间 t Rs ——标准物质的保留时间(热导池检测器的标准物质一般指定为:苯) t M ——死时间 常用的色谱定量方法有归一化法、外标法、内标法。 归一化法是将样品中的所有色谱峰的面积之和除某个色谱峰的面积,即得色谱峰相应组分在混合物中的含量。
9012生物样品定量分析方法验证指导原则
中国药典2015年版 9012生物样品定置分析方法验证 指导原则 一、范围 准确测定生物基质(如全血、血清、血浆、尿)中的药物浓度,对于药物和制剂研发非常重要。这些数据可被用于支持药品的安全性和有效性,或根据毒动学、药动学和生物等效性试验的结果做出关键性决定。因此,必须完整地验证和记录应用的生物分析方法,以获得可靠的结果。 本指导原则提供生物分析方法验证的要求,也涉及非临床或临床试验样品实际分析的基本要求,以及何时可以使用部分验证或交叉验证,来替代完整验证。本指导原则二和三主要针对色谱分析方法,四针对配体结合分析方法。 生物样品定量分析方法验证和试验样品分析应符合本指导原则的技术要求。应该在相应的生物样品分析中遵守 G L P原则或GC P原则。 二、生物分析方法验证 (一)分析方法的完整验证 分析方法验证的主要目的是,证明特定方法对于测定在某种生物基质中分析物浓度的可靠性。此外,方法验证应采用与试验样品相同的抗凝剂。一般应对每个新分析方法和新分析物进行完整验证。当难于获得相同的基质时,可以采用适当基质替代,但要说明理由。 一个生物分析方法的主要特征包括:选择性、定量下限、响应函数和校正范围(标准曲线性能)、准确度、精密度、基质效应、分析物在生物基质以及溶液中储存和处理全过程中的稳定性。 有时可能需要测定多个分析物。这可能涉及两种不同的药物,也可能涉及一个母体药物及其代谢物,或一个药物的对映体或异构体。在这些情况下,验证和分析的原则适用于所有涉及的分析物。 对照标准物质 在方法验证中,含有分析物对照标准物质的溶液将被加人到空白生物基质中。此外,色谱方法通常使用适当的内标。 应该从可追溯的来源获得对照标准物质。应该科学论证对照标准物质的适用性。分析证书应该确认对照标准物质的纯度,并提供储存条件、失效日期和批号。对于内标,只要能证明其适用性即可,例如显示该物质本身或其相关的任何杂质不产生干扰。 当在生物分析方法中使用质谱检测时,推荐尽可能使用稳定同位素标记的内标。它们必须具有足够高的同位素纯度,并且不发生同位素交换反应,以避免结果的偏差。 1.选择性 该分析方法应该能够区分目标分析物和内标与基质的内源性组分或样品中其他组分。应该使用至少6个受试者的适宜的空白基质来证明选择性(动物空白基质可以不同批次混 9012生物样品定量分析方法验证指导原则 合),它们被分别分析并评价干扰。当干扰组分的响应低于分析物定量下限响应的20%,并低于内标响应的5%时,通常即可以接受0 应该考察药物代谢物、经样品预处理生成的分解产物以及可能的同服药物引起干扰的程度。在适当情况下,也应该评价代谢物在分析过程中回复转化为母体分析物的可能性。 2.残留 应该在方法建立中考察残留并使之最小。残留可能不影响准确度和精密度。应通过在注射高浓度样品或校正标样后,注射空白样品来估计残留。高浓度样品之后在空白样品中的残留应不超过定量下限的20%,并且不超过内标的5%。如果残留不可避免,应考虑特殊措施,在方法验证时检验并在试验样品分析时应用这些措施,以确保不影响准确度和精密度。这可能包括在高浓度样品后注射空白样品,然后分析下一个试验样品。 3.定量下限 定量下限是能够被可靠定量的样品中分析物的最低浓度,具有可接受的准确度和精密度。定量下限是标准曲线的最低点,应适用于预期的浓度和试验目的。 4.标准曲线 应该在指定的浓度范围内评价仪器对分析物的响应,获得标准曲线。通过加人已知浓度的分析物(和内标)到空白基质中,制备各浓度的校正标样,其基质应该与目标试验样品基质相同。方法验证中研究的每种分析物和每一分析批,都应该有一条标准曲线。 在进行分析方法验证之前,最好应该了解预期的浓度范围。标准曲线范围应该尽量覆盖预期浓度范围,由定量下限和定量上限(校正标样的最髙浓度)来决定。该范围应该足够描述分析物的药动学。 应该使用至少6个校正浓度水平,不包括空白样品(不含分析物和内标的处理过的基质样品)和零浓度样品(含内标的处理过的基质〉。每个校正标样可以被多次处理和分析。 应该使用简单且足够描述仪器对分析物浓度响应的关系式。空白和零浓度样品结果不应参与计算标准曲线参数。 应该提交标准曲线参数,测定校正标样后回算得出的浓度应一并提交。在方法验证中,至少应该评价3条标准曲线。 校正标样回算的浓度一般应该在标示值的:t l5%以内,定量下限处应该在±20%内。至少75%校正标样,含最少6个有效浓度,应满足上述标准。如果某个校正标样结果不符合这些标准,应该拒绝这一标样,不含这一标样的标准曲线应被重新评价,包括回归分析^ 最好使用新鲜配制的样品建立标准曲线,但如果有稳定性数据支持,也可以使用预先配制并储存的校正标样。 5.准确度 分析方法的准确度描述该方法测得值与分析物标示浓度的接近程度,表示为:(测得值/真实值)x l00?^应采用加人已知 ? 363
醇类气相色谱法方法确认报告
GBZ/T 160.48-2007 工作场所空气有毒物质测定 醇类化合物--方法确认报告 一、线性 1 目的 确认GBZ/T 160.48-2007用气相色谱法对甲醇、异丙醇、正丁醇检测的线性范围。 2 过程 2.1 2.2 检验其标准曲线的相关系数(R)达到最低要求:R>0.999。 3 Results(结果)
4 结论 最终确认正己烷的线性范围达到R >0.999。 二、方法检出限MDL 1 目的 确认GBZ/T 160.48-2007方法中用气相色谱法测定甲醇、异丙醇、正丁醇的方法检出限。 2 Procedure(过程) 2.1 将样品空白打入气相色谱中并读取噪声读数。 2.2 计算检出限MDL (等于3倍噪声(单位时间)相对应的浓度)。 3 结果 4 结论 最终确认甲醇、异丙醇、正丁醇的方法检出限为0.54ug/mL 、0.51ug/mL 、0.38ug/mL 。 三、精密度 1 目的 确认GBZ/T 160.48-2007方法检测的精密度。 2 过程
2.1 在不同3天内各取7份空白活性炭管(不含待分析物的空白样品)到解吸瓶中。 2.2 2.3 按照GBZ/T 160.48-2007解吸样品。 2.4 用气相色谱仪分析样品中的甲醇、异丙醇、正丁醇浓度。 2.5 计算精密度(即相对标准偏差),相对标准偏差不大于10%。 3 结果
4 结论 最终确认高、中、低浓度的RSD均小于10%。 四、准确度 1 目的 确认GBZT 160.48-2007方法的准确度。 2 过程 2.1 在不同3天内各取7份空白活性炭管(不含待分析物的空白样品)到解吸瓶中。 2.2 往样品中加入标准溶液中间浓度甲醇:500mg/L,异丙醇:10000mg/L,正丁醇2000 mg/L。 2.3 按照GBZ/T 160.48-2007解吸样品。 2.4 用气相色谱仪分析样品中的甲醇、异丙醇、正丁醇浓度。 2.4 回收率在90%到110%之间。 3 结果 加标回收实验(引用精密度中间浓度测试数据),其结果如下: 4 结论 最终确认准确度符合要求。
测量系统分析报告(MSA)方法
测量系统分析(MSA)方法 测量系统分析(MSA)方法**** 1.目的 对测量系统变差进行分析评估,以确定测量系统是否满足规定的要求,确保测量数据的质量。 2.范围 适用于本公司用以证实产品符合规定要求的所有测量系统分析管理。 3.职责 3.1质管部负责测量系统分析的归口管理; 3.2公司计量室负责每年对公司在用测量系统进行一次全面的分析; 3.3各分公司(分厂)质检科负责新产品开发时测量系统分析的具体实施。 4.术语解释 4.1测量系统(Measurement system):用来对被测特性赋值的操作、程序、量具、设备以及操作人员的集合,用来获得测量结果的整个过程。 4.2偏倚(Bias):指测量结果的观测平均值与基准值的差值。 4.3稳定性(Stability):指测量系统在某持续时间内测量同一基准或零件的单一特性时获 得的测量平均值总变差,即偏倚随时间的增量。 4.4重复性:重复性(Repeatability)是指由同一位检验员,采用同一量具,多次测量同一产品的同一质量特性时获得的测量值的变差。 4.5再现性: 再现性(Reproductivity) 是指由不同检验员用同一量具,多次测量同一产品的同一质量特性时获得的测量平均值的变差。 4.6分辨率(Resolution):测量系统检出并如实指示被测特性中极小变化的能力。 4.7可视分辨率(Apparent Resolution):测量仪器的最小增量的大小,如卡尺的可视分辨率为0.02mm。 4.8有效分辨率(Effective Resolution):考虑整个测量系统变差时的数据等级大小。用测量系统变差的置信区间长度将制造过程变差(6δ)(或公差)划分的等级数量来表示。关于 有效分辨率,在99%置信水平时其标准估计值为1.41PV/GR&R。 4.9分辨力(Discrimination):对于单个读数系统,它是可视和有效分辨率中较差的。 4.10盲测:指在实际测量环境中,检验员事先不知正在对该测量系统进行分析,也不知道所
抗药抗体免疫原性分析方法学验证指导原则(中文版)
抗药抗体免疫原性分析方法学验证指导原则 摘要: 几乎所有的生物制药产品都会引起一定的抗药抗体(anti-drug antibody,ADA)反应,抗药抗体反应可能会降低药物疗效或导致严重的不良反应。在人体内,抗药抗体通常不会引起明显的临床反应。但是对于某些治疗性蛋白质,抗药抗体反应能引起各种临床的不良反应,包括温和事件及严重不良事件。临床前研究表明,抗药抗体能对药物暴露、药物毒性作用、药物代谢动力学、药物效应动力学等造成影响。因此治疗性蛋白质的免疫原性引起了临床医生、药企及监管机构的注意。为了评估生物药物分子的免疫原性,以及将实验结果与临床事件联系起来,在临床前研究和临床研究中,很有必要开发可靠的能够有效评估抗药抗体反应的实验方法。这里方法学验证显得尤为重要,并且方法学验证是药物上市申请必不可少的。现行的监管文件对于免疫分析方法的验证的指导相当有限,特别是缺乏有关免疫原性分析方法的验证的指导。因此,本文对抗药抗体免疫分析方法的验证提供科学的建议。在现有的关于生物分析的规范性文件的基础上加入独特的性能验证。笔者建议采用实验和统计学的方法进行免疫分析的方法学验证。这些建议被视为最佳的例子,旨在促进整个医药行业形成一个更加统一的抗体检测方法。 1.简介: 生物制药产品包括氨基酸聚合物、碳水化合物或核酸,一般通过人细胞系、哺乳动物细胞或细菌进行表达,比常规的小分子药物更大(一般大于1~3KD)。由于以上特性,生物制药产品引起免疫反应的潜力更大。生物制药的免疫原性与产品的内在因素(种属特异性表位、外源性、糖基化程度、聚合或变性程度、杂质和制剂)、外在因素(给药途径、慢性或急性给药、药代动力学及内源性当量)、患者因素(自身免疫性疾病、免疫抑制、和替代疗法)相关。 抗药抗体反应可能会导致严重的临床症状,包括过敏、自身免疫和不同的药代动力学特征(例如,药物中和、生物分布异常和药物清除率增强等均可能会使
PE气相色谱仪验证方案要点
PE Clarus680型气相色谱仪确认方案 2013年11月
目录 1 方案审批................................................................ 11.1 确认方案起草.......................................................... 11. 2 确认方案审核.......................................................... 1 1.3 确认方案批准.......................................................... 1 2 确认时间进度计划........................................................ 2 3 概述.................................................................... 2 3.1 设备基本情况.......................................................... 2 4 确认目的................................................................ 2 5 确认标准和依据.......................................................... 2 6 确认实施人员及有关部门职责.............................................. 2 7 确认内容、认可标准及检查方法............................................ 37.1 设计确认.............................................................. 37.2 安装确认.............................................................. 47.3 运行确认.............................................................. 4 7.4 性能确认.............................................................. 5 8 再确认.................................................................. 6 9 文件要求................................................................ 6 10 附录................................................................... 6 11 记录................................................................... 6
钯元素测定分析方法验证报告
Palladium Analytical Method Validation Report 钯元素测定分析法验证报告Effective Day 生效日期:
TABLE OF CONTENTS 目录 1PURPOSE 目的 (3) 2SCOPE 围 (3) 3RESPONSIBILITIES^ (3) 4ABBREVIATIONS 缩略语 (3) 5REGULATIONS AND GUIDELINES 法规和指南 (4) 6REFERENCE DOCUMENTS 参考文件 (4) 7CONFIRMATION PREREQUISITES先决条件确认 (4) 8CONFIRM THE TEST RESULT确认检测结果汇总 (5) 9DEVIATION HANDING 偏差处理总结 (8) 10SUMMARY AND CONCLUSION 总结与结论 (8) 11ADVICE (IF ANY) 建议(如有) (8) 12ATTACHMENT LIST附件清单 (8)
1Purpose 目的 本验证报告的目的是通过记录在案的测试,证明原子吸收分光光度法适用于 原料药(API)中钯元素残留进行定量分析。证明此法适用于盐酸伐昔洛韦钯元素含量检测;6.00ppm 的限度本法可以检出。 2Scope 围 本验证报告适用于盐酸伐昔洛韦中钯元素测定分析法的验证。 3Responsibilities 职责 3.1验证委员会负责验证文件的审批。负责验证的协调工作,以保证本确认文件规定项目的 顺利实施。负责验证数据及结果的审核。 3.2质量管理部负责审核验证文件、及数据的最后确认。负责各种取样验证工作。 负责拟订验证文件。负责验证文件相关确认活动的实施。 3.3生产部负责建立设备档案。负责仪器、仪表的校正。 4Abbreviations 缩略语下面表格中规定了本案中使用的缩略语: 5Regulations and Guidelines 法规和指南 为编写本案,参考了以下法规和指南。 5.1法规 食品药品监督管理总局(CFDA ),中国,药品生产质量管理规(2010 年修订),
气相色谱验证性实验
实验二 甲醇、异丙醇与正丁醇的气相色谱分析 一、实验目的 1. 了解气相色谱仪的基本结构和工作原理. 2. 学习归一化法定量的基本原理和方法. 3. 掌握气相色谱操作的基本要求. 二、实验原理 1. 纯物质保留时间定性分析 利用同一种物质在相同的色谱条件下应具有相同的保留时间的特点,采用纯物质定性法,对混合物中的甲醇、异丙醇与正丁醇进行定性,以确定混合物样品中甲醇、异丙醇与正丁醇的存在与否,并得出它们相应的出峰顺序。 2. 面积归一化法定量分析 应用归一化法进行色谱定量分析,要求试样中各组分都必须全部流出并得到完全分离,根据色谱图中各色谱峰的数据,可按下式计算各组分的含量: 100%1?∑==n i fiAi fiAi ci 本实验以峰面积A i 为测定参数,假定fi 恒等于1,利用FL9500色谱工作站对进样后所得到的各色谱峰进行直接定量,并打印出样品组分的色谱分析结果报告单。 三、仪器与试剂 1. 福立气相色谱仪 2. 微量注射器 0.5 uL 3. 高纯氮、高纯氢、低噪声空气净化源 4. 甲醇(AR );异丙醇(AR );正丁醇(AR ); 甲醇、异丙醇与正丁醇的混合液
四、色谱条件 1. 固定液:聚甲基硅烷(非极性);色谱柱:毛细管0.32×30 mm/m 2. 柱温:80 ℃;气化室温度:150 ℃;检测器温度:150 ℃ 3. 载气:氮气;检测器:氢火焰离子化检测器(FID) 4. 进样量:0.1 uL 五、实验步骤 1 . 开N2钢瓶:⑴逆时针转动减压阀手柄至放松位置,此时减压阀处于关闭状态. ⑵逆时针打开钢瓶上的总阀门,并记录瓶中余气压力. ⑶顺时针旋紧减压阀,直至分压值达所需压力0.5 Mpa. 2. 接通电源,开净化器,三个全打开. 3. 开色谱仪上的两电源,并调毛细管柱前压(主机顶上表压力)0.06 Mpa. 4. 设置参数,选择优化条件:1.柱温(柱箱键). 2. 汽化室(辅助I). 3. FID(检测器). 4. 其它参数(参数键,通过上行和下行调出极性,量程等参数). 5. 待所设参数达到设置条件时(显示键查看),开H2钢瓶. H2钢瓶的开法:⑴.逆时针转动减压阀手柄至放松位置. ⑵.逆时针打开钢瓶上的总阀门. ⑶.逆时针打开减压阀左边的小通道(使用阀). ⑷. 顺时针旋紧减压阀直至分压值达所需压力0.2 Mpa. 6. 调色谱仪主板上H2表Ⅱ的压力为0.1 Mpa. 7. 开低噪声空气净化源,调色谱仪主板上空气压力为0.03 Mpa. 8. 点火,若点火困难,可先调高氢气至0.15 Mpa,点火后调回至0.1 Mpa. 9. 打开电脑,点桌面上的FL9500色谱工作站图标进入系统,点通道1或2,在菜单样品设置中点新建,输入样品名及各种信息.点下一步,点下一步选择定量方法等,点下一步,点下一步,点下一步,点完成,填入仪器条件,点确定. 10. 待基线平直后,即可进样,进样后按工作站的通道A或B上的按时器或在工作界面上 点击开始按钮即进行进样分析。(注意:进样前一定要将微量注射器用相应试剂清洗干净,清洗干净的微量注射器应该专用,不能与准备进样别的试剂的微量注射器混用). 11. 采样结束后点停止,若想处理色谱图点进样后处理,点转入再处理,打印结果,待所有 样品采样结束后,关色谱程序窗,关电脑.
分析方法验证报告2.2
分析方法验证报告 2019QQHJKX01 分析方法:《水质石油类的测定紫外分光光度法(试行)》(HJ970-2018) 验证人员: 验证时间:2019年01月23日—25日 乌拉特前旗环境保护监测站
1参加人员情况 2仪器、标准物质情况 3 工作曲线的测定 3.1 工作曲线的测定条件 分析日期:2019年01月23日 温度:20℃湿度:18% 测定波长:225nm 3.2 工作曲线的测定
3.2 标准曲线的绘制 4 方法检出限的测定 依据《环境监测分析方法标准制修订技术导则》(HJ168-2010)附录A 方法特性指标确定方法。 方法检出限的一般确定方法: 按照样品分析的全部步骤,重复n(≥7)次空白试验,将各测定结果换算为样品中的浓度,计算n次平行测定的标准偏差,按公式A-1计算,方法检出限按公式A-2计算。
标准偏差S= (A-1) 式中:n —— 样品的平行测定次数 X i —— 单次测定值 X —— 测定平均值 MDL=t (n-1,0.99)×S (A-2) 式中:MDL —— 方法检出限 n —— 样品的平行测定次数 t —— 自由度为n -1 ,置信度为99%时的t 分布 S —— n 次平行测定的标准偏差 ( ) 1 1 2 - ? ? ? ? ? - ∑ = n X x n i i
5 精密度、准确度测试 分别对标准浓度为0.4mg/L、0.8mg/L、1.0mg/L和有证标准物质BW022四个浓度进行6次测定,测定结果见表5-1。
6 评价与验证结论 6.1 评价 根据《水质石油油类的测定紫外分光光度法(试行)》(HJ970-2018)对本实验的检出限、精密度、准确度进行相关评价。 6.1.1 空白值最低检出限评价 根据《水质石油油类的测定紫外分光光度法(试行)》(HJ970-2018)中的检出限为0.01 mg/L,本实验石油类的检出限为0.004mg/L,符合标准方法要求。 6.1.2 精密度评价 本次实验分别对油浓度为0.4 mg/L、0.8 mg/L、1.0 mg/L和有证标准物质BW022进行测试,相对标准偏差分别为4.6%、2.9%、4.7%、5.0%,符合标准方法要求。 6.1.3 准确度评价 根据方法条件,本次实验测定的加标回收率为96%-104%,平均值为99.75%,对标准浓度为0.4 mg/L、0.8 mg/L、1.0 mg/L和有证标准物质BW022的测定,相对误差分别为 2.5%、-1.2%、0.0%、5.0%,其结果均在标准范围内。 6.2 结论 通过对上述指标的验证,证明本站具备按照《水质石油油类的测定紫外分光光度法(试行)》(HJ970-2018)进行监测的能力,该项目可在本监测站正常开展。 分析者:复核者:审核者: 报告编写时间:2019年01月26日
气相色谱法挥发性有机物测定实验报告
GC-MS测定挥发性有机物实验报告 专业:环境工程学号:1233351 姓名:刘鹏一、实验方法 进样器参数设定如下: 用预溶剂冲洗次数: 3 用溶剂冲洗次数: 3 用样品冲洗次数: 2 柱塞速度: 高粘度补偿时间: 0.2 sec 柱塞进样速度: 高进样器进样速度: 高注射模式: 一般抽吸次数: 5 进样口停留时间: 0.3 sec 尾部空气间隙: 否活塞吹扫速度: 高清洗体积: 8uL 注射器吸入位置: 1.0 mm 注射器注射位置: 0.0 mm 使用3个溶剂瓶: 1个瓶 [GC-2010] 柱箱温度:30.0℃进样温度:250.00℃进样模式:分流 流量控制模式:线速度压力:45.6 kPa 总流量:14.0 mL/min 柱流量:1.00 mL/min 线速度:35.9 cm/sec 吹扫流量:3.0 mL/min 分流比:10.0 高压进样模式:关载气节省器:关分流阻尼固定:关 柱温箱: 是SPL1: 是MS: 是 < 检测器(FTD)检查完毕> < 基线移动检查完毕> < 进样流量检查完毕> SPL1 载气: 是SPL1 吹扫: 是 < APC流量检查完毕> < 检测器APC流量检查完毕> 外部等待:否平衡时间: 2.0 min [GC 程序] [GCMS-QP2010 SE] 微扫描半峰宽:0.00 amu 离子源温度:200.00 ℃接口温度:250.00 ℃ 溶剂延迟时间:2.50 min 检测器增益方式:相对检测器增益:0.83 kv +0.00 kV
M 0 0 0 二、标准物质色谱图 三、实验结果 ①实验数据 浓度(ppm)保留时间(min)峰面积20 Chloroform 2.812 57512 Methane, tetrachloro- (CAS) Carbon tetrachloride 3.383 49049 Methane, bromodichloro- 4.068 66435 Methane, dibromochloro- 5.687 75262 Methane, tribromo- (ISTD)7.409 138822 40 Chloroform 2.811 129095 Methane, tetrachloro- (CAS) Carbon tetrachloride 3.376 111609 Methane, bromodichloro- 4.071 129212 Methane, dibromochloro- 5.694 182065 Methane, tribromo- (ISTD)7.414 162528 60 Chloroform 2.812 189860 Methane, tetrachloro- (CAS) Carbon tetrachloride 3.373 151922 Methane, bromodichloro- 4.075 193871 Methane, dibromochloro- 5.702 254807 Methane, tribromo- (ISTD)7.419 155012 80 Chloroform 2.806 235776 Methane,tetrachloro-(CAS)Carbon tetrachloride 3.366 178609 Methane, bromodichloro- 4.072 244831 Methane, dibromochloro- 5.706 334295 Methane, tribromo- (ISTD)7.421 151093 100 Chloroform 2.812 350007 Methane, tetrachloro- (CAS) Carbon tetrachloride 3.367 265810 Methane, bromodichloro- 4.08 354933 Methane, dibromochloro- 5.712 440660
气相色谱验证报告
目录 1.确认目的 (2) 2.确认范围 (2) 3.方案说明 (2) 4.验证职责 (2) 5.仪器概述 (2) 6.确认步骤 (2) 7.偏差处理 (7) 8.风险评估 (7) 9.确认总结 (7) 10.再验证周期 (8) 11.验证证书 (9)
一、确认目的 此验证是为确认气相色谱仪的运行和各种性能指标是否满足规定要求。 二、确认范围 证明并保证本仪器确认后,经本仪器检验的数据真实可靠。 三、方案说明 1.尽可能详细地填写本方案中的所有表格。用墨水笔填写。完成表格的人员应签上姓名和日期。如果 由一个以上的人填写,那么每一个人都应签上姓名和日期。 2.方案执行时可能会发现偏差。一旦这种情况发生,应将一份“异常情况报告”送交验证领导小组进 行处理。 3.验证小组最终做出验证报告,该报告由公司验证负责人批准。 四、验证职责 1.验证领导小组 负责验证工作的组织和协调。负责验证数据及结果的审批。负责验证报告的审批。 2. 质量部 负责验证的检验工作。负责保管验证文件。 五、设备概述 1、设备概述:本仪器由安捷伦科技有限公司生产,主要用于实验的检测,存放于气液相室。该仪器更快的柱箱降温速率和更强的反吹功能,使您的分析时间更短,样品的分析成本更低。第五代电子气路控制 (EPC)和数字电路为压力设定和保留时间锁定 (RTL)的精度(0.001psi)设置了新的标准,使安捷伦GC7820A具有前所未有的可靠性。 2、设备名称:气相色谱仪 3、设备型号:GC7820A 4、制造商:安捷伦仪器有限公司 六、确认步骤 1、人员培训确认 进行测试的人员必须接受足够的培训并将培训计划和考核结果存档(培训是现行GMP所要求的),熟悉检验仪器的操作原则,理解人员安全要求,全面理解仪器及检验的标准操作规程。 确认: A.已建立适当的培训计划。 是:否: B.操作人员已接受正常的指导。
