南开大学 无机化学(专业代码:070301 授予理学硕士学位)
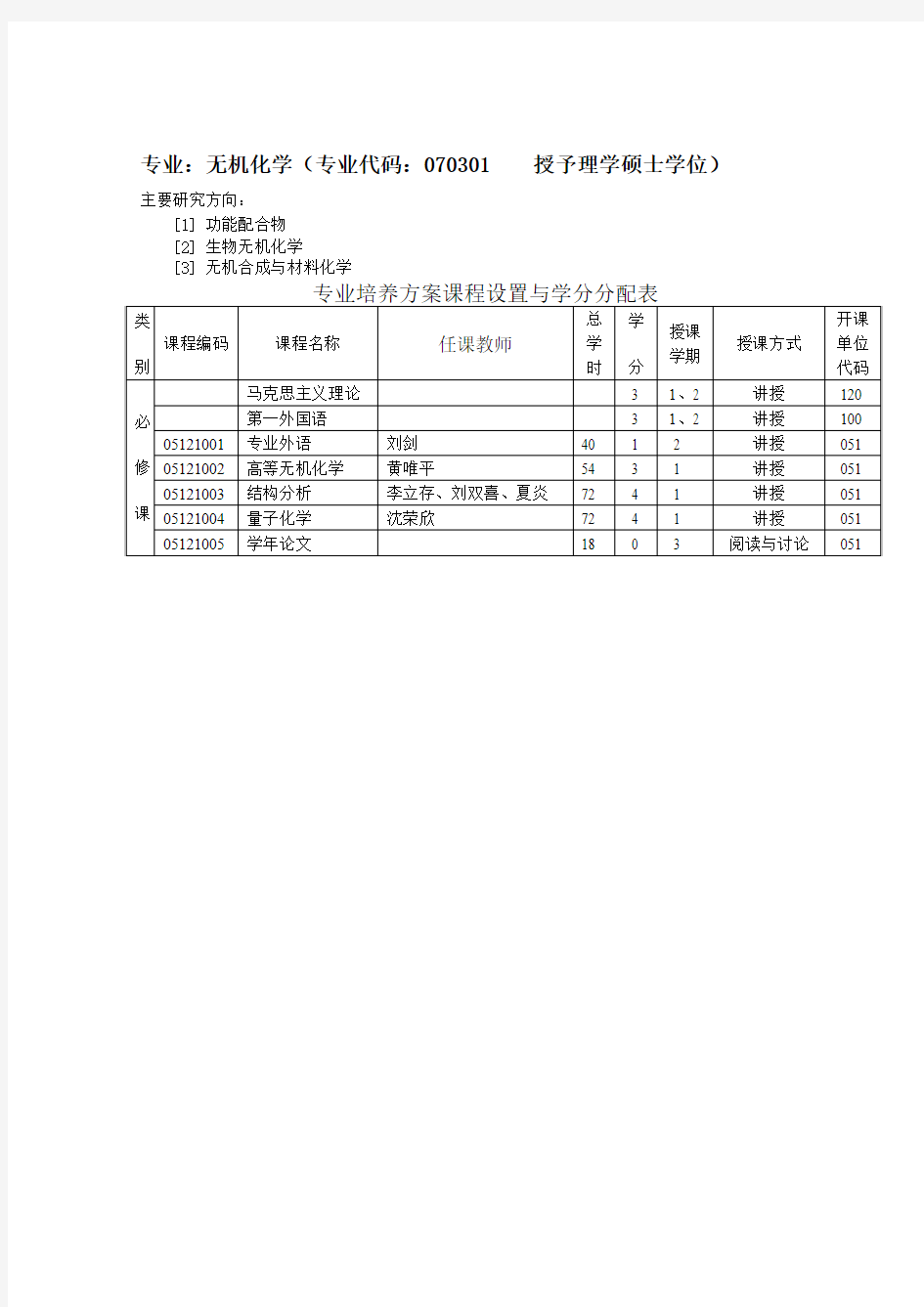

专业:无机化学(专业代码:070301 授予理学硕士学位)
主要研究方向:
[1]功能配合物
[2]生物无机化学
[3]无机合成与材料化学
专业:分析化学(专业代码:070302 授予理学硕士学位)
主要研究方向:
[1]光谱/质谱及联用技术
[2]电分析化学
[3]分离科学
[4]化学信息学
[5]生命分析化学
[6]环境分析化学
[7]药物分析化学
[8]食品安全分析化学
专业培养方案课程设置与学分分配表
专业:有机化学(专业代码:070303 授予理学硕士学位)
主要研究方向:
1.有机合成化学
2.金属有机化学
3.物理有机化学
4.有机分析化学
5.天然产物有机化学
6.杂原子有机化学
7.化学生物学
专业培养方案课程设置与学分分配表
专业:化学生物学(专业代码:070320 授予理学硕士学位)
主要研究方向:
化学生物学
专业培养方案课程设置与学分分配表
专业:物理化学(专业代码:070304 授予理学硕士学位)
主要研究方向:
[1]功能配位物理化学
[2]超分子化学
[3]化学反应动力学
[4]计算化学
[5]分子模拟
[6]非均相催化
[7]环境友好催化
[8]分子筛与纳米催化
[9]有机-无机复合材料和手性催化
[10]纳米催化
专业:高分子化学与物理(专业代码:070305 授予理学硕士学位)
主要研究方向:
1.高分子合成化学
2.高分子物理
3.生物医用高分子材料
4.功能高分子材料
5.高分子-无机纳米杂化材料
6.聚合物波谱学
专业:精细化学品化学(专业代码:070321 授予理学硕士学位)主要研究方向:
精细化学品化学
专业培养方案课程设置与学分分配表
专业:材料物理与化学(专业代码:080501 授予工学硕士学位)
主要研究方向:
[1]催化材料
[2]能源材料
[3]纳米材料
[4]有机-无机复合材料
专业培养方案课程设置与学分分配表
专业:材料学(专业代码:080502 授予工学硕士学位)
主要研究方向:
01纳米功能材料
02材料设计与合成
03新型碳材料
04新能源材料
05化学电源
06能源催化材料
专业培养方案课程设置与学分分配表
专业:应用化学(专业代码:081704 授予工学硕士学位)
主要研究方向:
[1]计算机应用化学
[2]有机结构与性能分析
[3]现代仪器分离与分析
专业培养方案课程设置与学分分配表
专业:农药学(专业代码:090403 授予理学硕士学位)
研究方向:
1绿色新农药的设计、合成和生物活性研究;
2农药分析
专业:植物病理学(专业代码:090401 授予理学硕士学位)
专业培养方案课程设置与学分分配表
专业:农药学(专业代码:090403 授予理学硕士学位)
研究方向:农药生物学
专业:植物病理学(专业代码:090401 授予理学硕士学位)
专业培养方案课程设置与学分分配表
化学学院(051)
专业:无机化学(专业代码:070301 授予理学博士学位)
专业:分析化学(专业代码:070302 授予理学博士学位)
专业:物理化学(专业代码:070304 授予理学博士学位)
专业:高分子化学与物理专业(专业代码:070305授予理学博士学位)专业培养方案课程设置与学分分配表(三年制博士)
专业:有机化学(专业代码:070303 授予理学博士学位)
专业:化学生物学(专业代码:070320 授予理学博士学位)
专业:精细化学品化学(专业代码:070321 授予理学博士学位)专业:农药学(专业代码:090403 授予理学博士学位)
专业培养方案课程设置与学分分配表
化学学院(051)
专业:材料物理与化学(专业代码:080501 授予工学博士学位)专业:材料学(专业代码:080502 授予工学博士学位)专业培养方案课程设置与学分分配表
2014年南开大学751世界历史(日本研究院)考研真题(回忆版)及详解(圣才出品)
2014年南开大学751世界历史(日本研究院)考研真题(回忆版)及详解 一、名词解释 1.高句丽 答:高句丽是公元前1世纪至公元7世纪在我国东北地区和朝鲜半岛存在的一个民族政权。大多数的史籍认为高句丽建于公元前37年或1世纪中期,“高句丽”作为一个地理名词出现在《汉书》中的年份是公元前113年。朝鲜前三国时代,高句丽扩张到汉江流域;公元224年,高句丽都城被曹魏摧毁,高句丽王逃往沃沮;在朝鲜三国时代,高句丽与新罗、百济处于军事对峙状态;公元5世纪末,高句丽好太王统治时,高句丽进入鼎盛时期。后因内部纠纷逐渐衰落,但在与隋唐的战争中不落下风,最终在唐与新罗联合攻击下于公元7世纪中期覆亡。 2.武士团 答:武士团是日本平安时代地方豪族和名主在同族内以血缘关系结成的团体。地方豪族是土地所有者,名主拥有政治实力,他们为了对抗国司,维护自身利益,将团体武装化,于平安中期后初步形成武士团。 3.朱熹 答:朱熹(1130年~1200年)是中国南宋时著名的理学家、思想家、哲学家、诗人,字元晦,又字中晦,谥文,世称朱文公。他是儒学集大成者,著有《四书章句集注》、《楚辞集注》等,后人辑有《朱子大全》、《朱子集语象》等,其中《四书章句集注》成为钦定的教科书和科举考试的标准。他提倡义理之学,总结了宋代理学思想,成为宋代理学之大成,而
其本身则与孔子并提;他提出“理气论”认为万物各有其理,理是事物的规律和伦理道德的基本准则。他与同时代心学大师陆九渊在信州(今江西上饶)鹅湖举行辩论会,史称“鹅湖之会”。“存天理,灭人欲”就是朱熹理学思想的重要观点。日本江户时代,朱子学也受到尊崇,成为幕藩体制的官学。 4.卡尔·马克思 答:卡尔·马克思(1818年5月5日~1883年3月14日)是德国哲学家,马克思主义创始人,世界无产阶级和劳动人民的伟大导师。他结合德国古典哲学、英国政治政治经济学、英法空想社会主义创立马克思主义。这个宏大的理论体系由历史唯物主义、唯物辩证法、科学社会主义构成。他的著作包括《德意志意识形态》、《神圣家族》、《共产党宣言》、《资本论》等。他领导了第一国际,为国际工人运动做出了巨大的贡献。1999年,他被英国广播公司评为“千年第一思想家”。 5.万国公法 答:《万国公法》,又称《国际法原理》,是美国外交官、国际法学者惠顿撰写的国际法著作,1836年出版。全书分四卷,分别释公法之义、论诸国自然之权、论诸国平时往来之权、交战条规。美国传教士丁韪良在1863年将此书翻译成中文,次年京师崇实管刊印,定名《万国公法》。后此书流传到日本,对明治维新时国家体制设计有重大影响。 6.波茨坦公告 答:波茨坦公告,全称《中美英三国促令日本投降之波茨坦公告》,是1945年7月17日~8月2日,美、苏、英三国首脑在柏林附近的波茨坦举行会议的会后成果,考虑到苏联
湖南理工学院无机化学课件之复习题第二章化学反应一般原理3
化学平衡该章总题数:66 1. (本题难度系数15)已知某反应的Δr>0,则该反应的平衡常数值() A >0 B <0 C >1 D <1 2. (本题难度系数15) 500 K时,反应 SO2(g) + O2(g) SO3(g) 的Kp = 50,在同温下,反应2SO3(g) 2SO2(g) + O2(g) 的K p 必等于() A 100 B 2 × 10-2 C 2500 D 4 × 10-4 3. (本题难度系数15)某温度时,化学反应A +B A2B的平衡常数K = 1 ×104,那在同温度下,反应A2B 2A +B的平衡常数为() A 1 × 104 B 1 × 100 C 1 × 10-4 D 1 × 10-8 4. (本题难度系数15)在一定条件下,一个反应达到平衡的标志是() A 各反应物和生成物的浓度相等 B 各物质浓度不随时间改变而改变 C Δr=0 D 正逆反应速率常数相等 5. (本题难度系数30)在523 K时,PCl5(g) PCl3(g) + Cl2(g) = 1.85,则反应的Δr(KJ · mol-1)为() A 2.67 B -2.67 C 26.38 D -2670 6. (本题难度系数30) 已知在20℃, H2O(l) H2O(g) ,Δγ = 9.2KJ · mol-1H2O(l)的饱和蒸气压为2.33 kPa,则( ) A Δr>0, H2O(g)将全部变为液态 B 20℃,H2O(l)和H2O(g)不能达到平衡 C 20℃时,p H2O = 2.33 kPa,体系的Δγ=0 D 水蒸气压为100 kPa时,平衡向形成H2O(g)的方向移动 7. (本题难度系数15)某一气相反应A=B,同一温度下=,则该反应的平衡常数是() A 0 B 大于1 C 小于1 D 1 8. (本题难度系数30)硫酸铜有多种不同水合物,它们脱水反应的K p分别
南开大学无机化学专业考研真题
天津考研网(https://www.360docs.net/doc/f14585059.html,) 南开大学无机化学专业考研真题 南开大学无机化学专业考研复习都是有依据可循的,考研学子关注事项流程为:考研报录比-大纲-参考书-资料-真题-复习经验-辅导-复试-导师,缺一不可。 南开大学无机化学专业主要考的是无机化学和综合化学这两门专业课,在我看来想要考好专业课一定需要做到两点首要条件,其一一定要使用一套比较好的参考资料,其二一定要做历年的真题资料,这两点都能做到的同学我相信考试的成功率一定会大上很多。 现在已经即将步入9月,给我们复习的时间已经不是那么多了,相信现在的同学们已经都度过了看参考书学知识点的阶段了,那么现在的主要任务就是考试做真题资料来巩固自己的所学,并且检查自己是否那里复习的不到位,及时发现到底有没有把所有的知识点全部学到,当然现在同学们最关心的相信也是真题方面,但是奈何找不到真的历年真题,毕竟现在市面上假资料泛滥,同学们很容易步入他们的陷阱而买到了假资料,不仅耽误了复习的时间而且还严重影响了心情。不过天津考研网主编的《南开大学无机化学专业(无机化学+综合化学)考研红宝书》你大可不必担心,资料保证全面,而且真题是2005-2016年全部的历年真题,都是根据理解研究生的回忆所模拟出来的真实考研试卷,无论是题型还是出题结构都和考研试卷一样,能够让同学们了解考研是怎样一回事,做真题试卷可以让我们了解其结构框架,整理答题思路,在规定的时间内了解我们能够做完,这都十分的重要,所以复习过程中真题资料是必不可少的。 最后呢我也希望所有报考南开大学无机化学专业的同学都能够百折不挠,攻克所有难关达到成功的彼岸,在研究生生活中再创辉煌。
关于日语专业考研院校分析一览表
综合类大学 1.南开大学 在综合大学中,提到日语,就不能不提南开大学。作为综合性重点大学南开,日语专业的办学水平是全国一流的。在日本语能力测试的辅导用书中,我们看到最多的都是南开大学出版社的书籍,他们所编纂的辅导用书质量高,重点突出。”南开大学日本语言文学系拥有教师15人,其中教授3人,副教授10人。其研究生培养方向主要分为:日本语学方向、日本文学方向、何日本文化方向。具体来说,日本语学主要涉及日语词汇学、日中语言文化比较研究等领域;日本文学主要研究日本古典文学、日中文学比较等;日本文化方面主要进行日本文化研究、日中文化比较研究等领域的探讨。 南开大学还另设有日本研究院。本院属于国家重点学科,博士学位授予单位。是对日本进行综合性研究的实体学术机构。现有教授7人,且均为博士生导师,副教授10人。主要研究方向为:日本政治史(博士学位授予权)、日本经济史(博士学位授予权)、日本近代外交史(中日关系史,博士学位授予权)、日本社会史(家族制度史,博士学位授予权)、日本文化史(洋学史)、日本经济(硕士、博士授予权)、日本政治。 招生方向:南开大学日本研究院:世界史日本史方向、国际政治日本政治方向、世界经济日本经济方向; 外国语学院:日本语学、日本文学、日本文化专业。 2.吉林大学 吉林大学日语研究生招生分为两个机构接收:专业日语和公共日语。也就是说,专业日语由外国语学院日语系招生;公共日语由公共外语学院招生;但两大专业的毕业生都属于语言及应用语言学的硕士研究生。吉大日语的毕业生去向广泛,现主要集中在大企业或者ZF外交部门,以及高校科研机构和出版社等岗位。 研究方向:日本语学、日本文学、日本文化。 3.武汉大学 武汉大学为近代中国第一批国立大学。其外国语学院日文系现有教师15人,教授2人,副教授5人。在武大日文系学习,要求我们同时具备日语语言、文学、历史、政治、经济、外交、社会文化等多方面的基本理论和基础知识。拥有一定的科学研究能力,但是由于武汉大学学科相对综合,因此报考武大日文系的竞争不是很激烈,适合成绩中上的考生为之努力。研究方向:日本语言学方向、日本文学方向、翻译学方向。 师范类大学 1. 东北师范大学 东北师范大学外国语学院日语系实力雄厚,连续在2002~2004年日语专业排名中位居全国第一,为东北地区为数不多的日语语言文学硕士、博士学位授予点。日语语言文学专业拥有一批优秀的教育骨干,现有教授5名,副教授3名。研究生教育期间,注重培养学生动手查阅资料、分析利用资料的能力,并在研究生课堂开展讨论,提高学生的科研能力。值得一提的是,东北师范大学日本研究所,是我国成立最早的专门研究日本的综合科研机构之一。拥有世界经济、国际政治、世界史、日语语言文学四个专业的硕士学位授予权,其中日语语言文学专业有博士学位授予权。此外,主办的《日本学论谈》在国内日语界颇具影响。毕业生多就职于国家科研单位、大学、国家外事机构、外贸机构等,师大日语系的就业率每年都居学校整体就业率的前列。 外国语学院:日语语言文学;日语教学论; 日本研究所:世界经济,包括日本经济政策论和日本企业制度及经营学;国际政治,包括近现代日本政治与外交;日语语言文学,包括日本近代文学、日本社会文化;世界史,包括日本近现代史、中日关系史、日本思想史。
大学无机化学第二版河北师范大学课后习题答案
第1章 物质的聚集态习题答案 1-1 实验室内某氦气钢瓶,内压为18 MPa ,放出部分氦气后,钢瓶减重500 kg ,瓶内氦气的压强为9.5 MPa 。假定放出气体前后钢瓶的温度不变,钢瓶原储有氦气为多少(物质的量)? 解:V 与T 一定时,n 与p 成正比, 即: mol .0026 410500MPa )5.918(MPa 183?=-总n 解得 mol 10645.25?=总n 1-2 273K和101 kPa 的1.00 dm 3干燥空气缓慢通过液态的二甲醚(CH 3OCH 3)。假定(1)通过二甲醚后的空气被二甲醚饱和且液态二甲醚损失0.0335g ;(2)被二甲醚饱和的空气的总压强仍为101kPa 。计算二甲醚在273K时的饱和蒸汽压。 解:由理想气体状态方程得: 空气的物质的量:m ol 0445.0K 273K m ol dm 8.314kPa 1.00dm kPa 1011133 =?????==--空RT pV n 二甲醚的物质的量:mol 10283.7mol g 0.46g 02335.041--二甲醚?=?==M m n 二甲醚的摩尔分数:0161.00445 .010283.710283.744=+??=+=--二甲醚空二甲醚二甲醚n n n x 二甲醚的饱和蒸汽压: 1.626kPa kPa 1010161.0=?=?=p x p 二甲醚二甲醚 1-3 在273.15 K 和1.01325×105 Pa 压力下,测得某气体的密度为1.340 g ·dm -3,在一实验中测得这种气体的组成是C 79.8%和H 20.2%。求此化合物的分子式。 解 =30.02(g·mol -1) 每分子含碳原子:30.02×0.798/12.01=1.9953≈2 每分子含氢原子:30.02×0.202/1.008=6.016≈6 即分子式为:C 2H 6 1-4 在293 K 和9.33×104 Pa 条件下,在烧瓶中称量某物质的蒸气得到下列数据,烧瓶
南开大学物理化学专业考研大纲和复习经验
南开大学物理化学专业考研大纲和复习经验 南开大学物理化学专业考研复习都是有依据可循的,考研学子关注事项流程为:考研报录比-大纲信息-参考书-资料-真题-复习经验-辅导-复试-导师。缺一不可,考研大纲会在九十月份发布,研友们不要着急,一定要耐心等待,可以参照去年的大纲先复习着,首先呢,南开大学物理化学专业下包含综合化学与物理化学(含结构化学),二者择其一。我个人的复习经验可以简单说一说,首先刚开始的时候,关注了一些考研公众号,在贴吧寻找经验,看到很多学长像我现在一样,分享着自己的考研经验,但是我很不擅长总结这种东西,一个理科生,原谅我吧。我会把该说的都说到。先列出大纲吧,再说一下我如何利用复习资料的,还有复习进度。 下面是南开大学物理化学专业综合化学考试大纲 一、考试目的 综合化学考试是为我校招收化学类、植物保护类专业的硕士研究生而设置的入学考试科目。 二、考试的性质与范围 本考试是测试考生化学水平的尺度参照性水平考试,考试范围包括本大纲规定的内容。 三、考试基本要求 要求考生比较系统地掌握在大学阶段在化学方面的基础理论,基本知识和基本技能,能综合运用所学知识分析问题、解决问题以及考查考生知识面的广度。 四、考试形式 本考试采取客观试题与主观试题相结合,单项技能测试与综合技能测试相结合的方法,强调考生运用化学基本原理解决问题的能力。 考试时间为180分钟,答题方式为闭卷考试(可以使用数学计算器)。 试卷满分150分,分四部分,其中无机化学40分,分析化学30分,有机化学40分,物理化学40分。 五、考试内容 本科目各部分考试内容,请对应参照科目无机化学、分析化学(不含仪器分析内容)、有机化学(化学学院)、物理化学(不含结构化学内容)的考试大纲。 下面是南开大学物理化学专业物理化学(含结构化学)考试大纲 一、考试目的本考试是化学学院全日制物理化学专业硕士学位研究生的入学资格考试之专业基础课。 二、考试的性质与范围本考试是测试考生物理化学(包括结构化学)水平的尺度参照性水平考试。考试范围包括本大纲规定的物理化学和结构化学内容。 三、考试基本要求 1.要求考生具备物理化学和结构化学相应的背景知识。 2.掌握物理化学和结构化学的基本原理,并能应用这些原理和思想方法处理、解决化学中的实际问题。 四、考试形式本考试采取客观试题与主观试题相结合,单项技能测试与综合技能测试相结合的方法,强调考生运用物理化学、结构化学基本原理解决问题的能力。试卷满分为150分,考试时间为180分钟。 五、考试内容本考试包括两个部分:物理化学(占70%)、结构化学(占30%)。
南开大学E类课分类
南开大学公共选修课分类目录 一、自然科学与技术 序号开课学院任课教师课程名称 1 数学科学学院顾沛等数学文化(国家级精品课)* 2 信息技术科学学院张伟刚等科研方法论(国家级精品课)* 3 信息技术科学学院张伟刚科学素养与科研方法 4 环境科学与工程学院冯剑丰等海洋与人类文明* 5 化学学院杨光明等化学与社会* 6 化学学院杨光明等化学与社会概要 7 物理科学学院宋锋等物理与社会发展* 8 生命科学学院张金红等基础生命科学导论* 9 医学院李玉皓等医学与人类健康* 10 化学学院邱晓航化学史话* 11 环境科学与工程学院吴婧环境保护概论* 12 数学科学学院向兵并行计算程序设计 13 数学科学学院胡刚数学建模 14 化学学院乔园园化学软件应用 15 化学学院乔园园化学的多元应用 16 化学学院陈志来计算机安全技术 17 化学学院张更辉新兴技术的风险评估与伦理学 18 化学学院刘冲网站开发技术 19 化学学院王维软物质导论 20 化学学院邱晓航生活中的化学实践 21 环境科学与工程学院王南林邵超 峰 可持续发展与环境伦理 22 环境科学与工程学院卜欣欣环境科学信息检索与利用 23 环境科学与工程学院肖羽堂环境安全
24 环境科学与工程学院刘春光环境与健康 25 医学院倪虹急救与灾难应变 26 医学院倪虹日常急救技术 27 医学院张京玲疾病与用药 28 医学院张京玲关注体质养生 29 医学院刘文人体部分器官结构与保护 30 医学院沈啸洪重要疾病的病因与预防 31 校医院严铁毅心身保健 32 生命科学学院魏东盛微生物与人类 33 生命科学学院张金红等基础生命科学导论实验 34 生命科学学院古松自然地理学 35 生命科学学院古松全球变化生态学 36 信息技术科学学院敖建平奇妙的材料世界 37 信息技术科学学院张毅电子材料导论 38 退休赵守珍飞速崛起的薄膜产业 39 退休霍玉华神奇的超导世界概论 40 物理科学学院赵春红物理演示实验 41 物理科学学院张天浩前进中的物理学与人类文明 42 药学院李弟灶新药设计原理与方法 43 药学院李弟灶活性多肽与药物开发 44 药学院金金中药方剂学 45 药学院李汀百年诺贝尔 46 药学院郭宇药物发现简史 47 信息化建设与管理办公室林初建网络技术 48 退休赵晓俊现代农业生物技术概论 49 退休苏宜天文学概论(理科生选)
大学无机化学第二章试题及答案解析
第二章 化学热力学基础 本章总目标: 1:掌握四个重要的热力学函数及相关的计算。 2:会用盖斯定律进行计算。 3:理解化学反应等温式的含义,初步学会用吉布斯自由能变化去判断化学反应的方向。 各小节目标: 第一节:热力学第一定律 了解与化学热力学有关的十个基本概念(敞开体系、封闭体系、孤立体系、环境、状态、状态函数、过程、途径、体积功、热力学能),掌握热力学第一定律的内容(△U=Q-W )和计算。 第二节:热化学 1:掌握化学反应热的相关概念: ○ 1反应热——指恒压或恒容而且体系只做体积功不做其它功的条件下,当一个化学反应发生后,若使产物的温度回到反应物的起始温度,这时体系放出或吸收的热量称为反应热。()。 ○ 2标准生成热——某温度下,由处于标准状态的各元素的指定单质生成标准状态的1mol 某纯物质的热效应。符号f m H θ?,单位:1J mol -?或1kJ mol -?)。 ○ 3燃烧热——在100kPa 的压强下1mol 物质完全燃烧时的热效应。符号:c m H θ?;单位:1kJ mol -?。 2:掌握恒容反应热△U=Q v -W;恒压反应热Q p =△H 恒容反应热和恒压反应热的关系:p V Q Q nRT =+?
3:掌握盖斯定律内容及应用 ○1内容:一个化学反应若能分解成几步来完成,总反应的热效应等于各步反应的热效应之和。 ○ 2学会书写热化学方程式并从键能估算反应热。 第三节:化学反应的方向 1:了解化学热力学中的四个状态函数——热力学能、焓、熵、吉布斯自由能。 2:重点掌握吉——赫公式r m r m r m G H T S θθθ ?=?-?的意义及计算。 3;建立混乱度、标准摩尔反应焓、标准摩尔反应自由能和标准熵以及标准摩尔反应熵的概念,并学会对化学反应的方向和限度做初步的讨论会运用吉布斯自由能判断反应的自发性。 Ⅱ 习题 一 选择题 1.如果反应的H 为正值,要它成为自发过程必须满足的条件是( ) A.S 为正值,高温 B.S 为正值,低温 C.S 为负值,高温 D.S 为负值,低温 2.已知某反应为升温时 rG 0值减小,则下列情况与其相符的是( ) A. rS 0<0 B. rS 0>0 C. rH 0>0 D.rH 0<0 3.该死定律认为化学反应的热效应与途径无关。这是因为反应处在( )(《无
简明无机化学第二版答案
简明无机化学第二版答案 【篇一:《无机化学》习题解析和答案】 》北京师范大学、华中师范大学、南京师范大学无机化学教研室编,高等教育出版社,2002年8月第4版。 2、参考书 《无机化学》北京师范大学、华中师范大学、南京师范大学无机化 学教研室编,高等教育出版社,1992年5月第3版。 《无机化学》邵学俊等编,武汉大学出版社,2003年4月第2版。 《无机化学》武汉大学、吉林大学等校编,高等教育出版社,1994 年4月第3版。《无机化学例题与习题》徐家宁等编,高等教育出 版社,2000年7月第1版。《无机化学习题精解》竺际舜主编, 科学出版社,2001年9月第1版 《无机化学》电子教案 绪论(2学时) 第一章原子结构和元素周期系(8学时) 第二章分子结构(8学时) 第三章晶体结构(4学时) 第四章配合物(4学时) 第五章化学热力学基础(8学时) 第六章化学平衡常数(4学时) 第七章化学动力学基础(6学时) 第八章水溶液(4学时)
第九章酸碱平衡(6学时) 第十章沉淀溶解平衡(4学时) 第十一章电化学基础(8学时) 第十二章配位平衡(4学时) 第十三章氢和稀有气体(2学时) 第十四章卤素(6学时) 第十五章氧族元素(5学时) 第十六章氮、磷、砷(5学时) 第十七章碳、硅、硼(6学时) 第十八章非金属元素小结(4学时) 第十九章金属通论(2学时) 第二十章 s区元素(4学时) 第二十一章 p区金属(4学时) 第二十二章 ds区元素(6学时) 第二十三章 d区元素(一)第四周期d区元素(6学时) 第二十四章 d区元素(二)第五、六周期d区金属(4学时) 第二十五章核化学(2学时) 1 .化学的研究对象 什么是化学? ● 化学是研究物质的组成、结构、性质与变化的一门自然科学。(太宽泛) ● 化学研究的是化学物质 (chemicals) 。
无机化学(周祖新)习题解答第二章
无机化学(周祖新)习题解答第二章 https://www.360docs.net/doc/f14585059.html,work Information Technology Company.2020YEAR
第二章化学热力学初步 思考题 1.状态函数的性质之一是:状态函数的变化值与体系的始态与终态 有关;与过程无关。在U、H、S、G、T、p、V、Q、W中,属于状态函数的是U、S、G、T、p、V。在上述状态函数中,属于广度性质的是U、H、S、G、V,属于强度性质的是T、p。 2.下列说法是否正确: ⑴状态函数都具有加和性。 ⑵系统的状态发生改变时,状态函数均发生了变化。 ⑶用盖斯定律计算反应热效应时,其热效应与过程无关。这表明任何情况下,化学反应的热效应只与反应的起止状态有关,而与反应途径无关。 ⑷因为物质的绝对熵随温度的升高而增大,故温度升高可使各种化学反应的△S大大增加。 ⑸△H,△S受温度影响很小,所以△G受温度的影响不大。 2.⑴错误。强度状态函数如T、p就不具有加和性。 ⑵错误。系统的状态发生改变时,肯定有状态函数发生了变化,但并非所有状态函数均发生变化。如等温过程中温度,热力学能未发生变化。 ⑶错误。盖斯定律中所说的热效应,是等容热效应ΔU或等压热效应ΔH。前者就是热力学能变,后者是焓变,这两个都是热力学函数变,都是在过程确定下的热效应。 ⑷错误。物质的绝对熵确实随温度的升高而增大,但反应物与产物的绝对熵均增加。化学反应△S的变化要看两者增加的多少程度。一般在无相变的情况,变化同样的温度,产物与反应物的熵变值相近。故在同温下,可认为△S不受温度影响。 ⑸错误。从公式△G=△H-T△S可见,△G受温度影响很大。 3.标准状况与标准态有何不同? 3.标准状态是指0℃,1atm。标准态是指压力为100kPa,温度不规定,但建议温度为25℃。
大学无机化学第二版-河北师范大学-课后习题答案
第1章 物质得聚集态习题答案 1—1 实验室内某氦气钢瓶,内压为18 MPa,放出部分氦气后,钢瓶减重500 kg,瓶内氦气得压强为9、5 MPa 。假定放出气体前后钢瓶得温度不变,钢瓶原储有氦气为多少(物质得量)? 解:V 与T 一定时,n 与p成正比, 即: 解得 1-2 273K与101 k Pa得1、00 dm 3干燥空气缓慢通过液态得二甲醚(CH 3OCH 3)。假定(1)通过二甲醚后得空气被二甲醚饱与且液态二甲醚损失0、0335g;(2)被二甲醚饱与得空气得总压强仍为101kPa.计算二甲醚在273K 时得饱与蒸汽压。 解:由理想气体状态方程得: 空气得物质得量:m ol 0445.0K 273K m ol dm 8.314kPa 1.00dm kPa 1011133 =?????==--空RT pV n 二甲醚得物质得量: 二甲醚得摩尔分数: 二甲醚得饱与蒸汽压: 1—3 在273、15 K 与1、01325×105 Pa 压力下,测得某气体得密度为1、340 g ·dm -3,在一实验中测得这种气体得组成就是C 79、8%与H 20、2%.求此化合物得分子式。 解:因为 所以=30、02(g·mol -1) 每分子含碳原子:30、02×0、798/12、01=1、9953≈2 每分子含氢原子:30、02×0、202/1、008=6、016≈6 即分子式为:C 2H 6 1-4 在293 K与9、33×104 Pa 条件下,在烧瓶中称量某物质得蒸气得到下列数据,烧瓶容积为2、93×10—4 m 3,烧瓶与空气得总质量为48、3690 g ,烧瓶与该物质蒸气质量为48、5378 g ,且已知空气得平均相对分子质量为29.计算此物质得相对分子质量. 解:设该物质得相对分子质量为M i ,则 9、33×104×2、93×10-4=(48、5378—48、3690)×8、314×293/(M i -29)
湖南理工学院无机化学课件之复习题第二章--化学反应的一般原理1
湖南理工学院无机化学课件之复习题第二章--化学反应的一般原理1
第二章化学反应的一般原理 习题1 化学热力学基础部分1 1.应用公式θm r G?(T)=θm r H ?(T)-Tθm r S?(T),计算下列反应的θm rH?(298.15K)值,并判断反应在298.15K及标准态下能否自发向右进行。 8Al(s)+3Fe3O4(s)→4A12O3(s)+9Fe(s) 2.通过计算说明下列反应: 2CuO(s)→Cu2O(s)+21O2(g) (1)在常温(298.15K)、标准态下能否自发进行? (2)在700K时、标准态下能否自发进行? 3.写出下列反应的平衡常数K c、K p、Kθ的表达式: (1)CH4(g)+H2O(g)?CO(g)+3H2(g) (2)NH3?21N2(g)+23H2(g) (3)CaCO3(s)?CaO(s)+CO2(g) (4)A12O3(s)+3H2(g)?2Al(s)+3H2O(g) 4.298.15K时,下列反应:
2H 2O 2(l) ? 2H 2O(l)+O 2(g) 的 θ m r H ?=-196.10kJ·mol -1 ,θm r S ?=125.76kJ·ml -1 ·K -1 。 试分别计算该反应在298.15K 和373.15K 的K θ 值。 5.试判断下列反应: N 2(g)+3H 2(g)→2NH 3(g) (1)在298.15K 、标准态下能否自发进行。 (2)计算298.15K 时该反应的K θ 值。 6. 在294.8K 时反应:NH 4HS(s)?NH 3(g)+H 2S(g) K θ =0.070,求: (1)平衡时该气体混合物的总压。 (2)在同样的实验中,NH 3的最初分压为25.3kPa 时,H 2S 的平衡分压为多少? 7. 将NO 和O 2注入一保持在673K 的固定容器中,在反应发生以前,它们的分压分别为:p(NO)=101kPa ,p(O 2)=286kPa 。当反应:2NO(g)+O 2(g)?2NO 2(g)达平衡时,p(NO 2)=79.2kPa 。计算该反应的K θ 和 θ m r G ?值。
考研无机化学专业就业方向及前景分析
考研有机化学专业就业方向及前景分析 一、专业介绍 1、学科简介 有机化学是一级学科化学下设的二级学科以天然有机产物和生物活性分子、金属与元素有机化合物为主要研究对象,从研究有机合成化学和物理有机化学着手,发展有机化学的反应、合成、方法和理论。 2、培养目标 依据研究生教育要"面向现代化、面向世界、面向未来"的要求,培养德、智、体全面发展的现代化建设所需要的有机化学专业的专门人才。 (1)硕士研究生应具有坚定正确的政治方向,热爱祖国,遵纪守法,具有严谨的科学态度,良好的素质。 (2)有机化学专业硕士研究生要掌握有机合成化学、金属有机化学、有机分析化学等方面的基础理论和系统的专门知识,了解本研究方向的国内外发展动态。 (3)较熟练地掌握一门外国语。能熟练地查阅本专业的外文文献,具有较强的外文写作能力。 (4)掌握本学科的现代实验技能,能独立的从事科学技术研究,具有新技术、新方法、新产品开发研究能力,毕业后能胜任高等院校、科研院所、企业和其他单位的教学、科研、技术管理工作。 3、专业方向 01物理有机化学 02有机合成化 03元素有机化学 04药物合成化 05有机大分子化学 06配位化学 4、考试科目 ①101思想政治理论 ②201英语一 ③721物理化学(含结构化学) ④837有机化学或838有机化学和分析化学(注:各个学校专业方向、考试科目,以上以复旦大学为例) 二、推荐院校 兰州大学、南开大学、北京大学、浙江大学、清华大学、四川大学、中国科学技术大学、武汉大学、山东大学、南京大学、吉林大学、华中师范大学、复旦大学、中山大学、厦门大学、苏州大学、徐州师范大学、湖南师范大学、云南大学、郑州大学、华东理工大学相近专业 与有机化学相近的一级学科下的其他专业有: 有机化学、分析化学、有机化学、物理化学、高分子化学和物理、材料物理与化学。 培养目标 依据研究生教育要"面向现代化、面向世界、面向未来"的要求,培养德、智、体全面发展的现代化建设所需要的有机化学专业的专门人才。
中外高校校名、国内研究所(中文全称和英文缩写对照)
精品文档 中文全称英文缩写 浙江大学ZHEJIANG UNIV 中国科学院CHINESE ACAD SCI 清华大学TSINGHUA UNIV 东南大学SOUTHEAST UNIV 大连理工大学DALIAN UNIV TECHNOL 南京大学NANJING UNIV 四川大学SICHUAN UNIV 上海交通大学SHANGHAI JIAO TONG UNIV 中山大学SUN YAT SEN UNIV 华中科技大学HUAZHONG UNIV SCI TECHNOL 北京大学PEKING UNIV 山东大学SHANDONG UNIV 复旦大学FUDAN UNIV 南开大学NANKAI UNIV 北京邮电大学BEIJING UNIV POSTS TELECOMMUN 中国科学技术大学UNIV SCI TECHNOL CHINA 吉林大学JILIN UNIV 西安交通大学XI AN JIAO TONG UNIV 哈尔滨工业大学HARBIN INST TECHNOL 天津大学TIANJIN UNIV 兰州大学LANZHOU UNIV 华南理工大学S CHINA UNIV TECHNOL 武汉大学WUHAN UNIV 湖南大学HUNAN UNIV 华南师范大学S CHINA NORMAL UNIV 北京航天航空大学BEIJING UNIV AERONAUT ASTRONAUT 东北大学NORTHEASTERN UNIV 电子科技大学UNIV ELECT SCI TECHNOL CHINA 华东科技大学 E CHINA UNIV SCI TECHNOL 中南大学CENT S UNIV 西安电子科技大学XIDIAN UNIV 同济大学TONGJI UNIV 厦门大学XIAMEN UNIV 北京交通大学BEIJING JIAOTONG UNIV 东吴大学SOOCHOW UNIV 安徽大学ANHUI UNIV 北京理工大学BEIJING INST TECHNOL 香港城市大学CITY UNIV HONG KONG 湘潭大学XIANGTAN UNIV 北京师范大学BEIJING NORMAL UNIV 华东师范大学 E CHINA NORMAL UNIV 南京理工大学NANJING UNIV SCI TECHNOL 东北师范大学NE NORMAL UNIV
大学无机化学第二章试题及答案
第二章 化学热力学基础 本章总目标: 1:掌握四个重要的热力学函数及相关的计算。 2:会用盖斯定律进行计算。 3:理解化学反应等温式的含义,初步学会用吉布斯自由能变化去判断化学反应的方向。 各小节目标: 第一节:热力学第一定律 了解与化学热力学有关的十个基本概念(敞开体系、封闭体系、孤立体系、环境、状态、状态函数、过程、途径、体积功、热力学能),掌握热力学第一定律的内容(△U=Q-W)与计算。 第二节:热化学 1:掌握化学反应热的相关概念: ○ 1反应热——指恒压或恒容而且体系只做体积功不做其它功的条件下,当一个化学反应发生后,若使产物的温度回到反应物的起始温度,这时体系放出或吸收的热量称为反应热。()。 ○ 2标准生成热——某温度下,由处于标准状态的各元素的指定单质生成标准状态的1mol 某纯物质的热效应。符号f m H θ?,单位:1J mol -?或1kJ mol -?)。 ○3燃烧热——在100kPa 的压强下1mol 物质完全燃烧时的热效应。符号:c m H θ?;单位:1kJ mol -?。 2:掌握恒容反应热△U=Q v -W;恒压反应热Q p =△H 恒容反应热与恒压反应热的关系:p V Q Q nRT =+? 3:掌握盖斯定律内容及应用 ○ 1内容:一个化学反应若能分解成几步来完成,总反应的热效应等于各步反应的热效应之与。 ○ 2学会书写热化学方程式并从键能估算反应热。
第三节:化学反应的方向 1:了解化学热力学中的四个状态函数——热力学能、焓、熵、吉布斯自由能。 2:重点掌握吉——赫公式r m r m r m G H T S θθθ?=?-?的意义及计算。 3;建立混乱度、标准摩尔反应焓、标准摩尔反应自由能与标准熵以及标准摩尔反应熵的概念,并学会对化学反应的方向与限度做初步的讨论会运用吉布斯自由能判断反应的自发性。 Ⅱ 习题 一 选择题 1、如果反应的H 为正值,要它成为自发过程必须满足的条件就是( ) A 、S 为正值,高温 B 、S 为正值,低温 C 、S 为负值,高温 D 、S 为负值,低温 2、已知某反应为升温时rG 0值减小,则下列情况与其相符的就是( ) A 、rS 0<0 B 、rS 0>0 C 、rH 0>0 D 、rH 0<0 3、该死定律认为化学反应的热效应与途径无关。这就是因为反应处在( )(《无机化学例题与习题》吉大版) A 、可逆条件下进行 B 、 恒压无非体积功件下进行 C 、 恒容无非体积功件下进行 D 、以上B,C 都正确 4、在298K 时反应 H 2(g)+1/2O 2(g)=H 2O(g)的Qp 与Qv 之差(KJ/mol)就是( ) A 、-3、7 B 、3、7 C 、1、2 D 、-1、2 5、冰的熔化热为330、5KJ/mol,00C 时将1、00g 水凝结为同温度的冰,其S 为 ( )(《无机化学例题与习题》吉大版) A 、-330、5Jmol -1K -1 B 、-1、21Jmol -1K -1 C 、0 D 、+1、21Jmol -1K -1 6、下列变化为绝热过程的就是( )(《无机化学例题与习题》吉大版) A 、体系温度不变 B 、体系不从环境吸收热量 C 、体系与环境无热量交换 D 、体系的内能保持不变 7、某反应在298K 时的Kc 1=5,398K 时Kc 2=11,则反应的rH 0值为( ) A 〈0 B 、 〉0 C 、于0 D 、不一定 8、 298K 时 的rG 0=-10KJ/mol 、已知:298K 时A,B,C,D 皆为气体,当由等物质的量的A 与B 开始反应时,则达到平衡时混合物中( ) A 、C 与D B 、 A 与B C 、 A 与B 、C 及 D 都有,A 与B 的量大于C 与D 的量 D 、 A 与B 、C 及D 都有,但C 与D 的量大于A 与B 的量 9、热化学方程式:Zn(S)+1/2O 2(g)=ZnO(s) rH 10=-348、3KJ/mol 2Hg(1)+O 2(g)=2HgO(s) rH 20=-181、6KJ/mol 则反应:Zn(s)+HgO(s)=ZnO(s)+Hg(l)的rH 0( ) A 、166、7KJ/mol B 、-257、5KJ/mol C 、–439、1KJ/mol D 、 -529、9KJ/mol
南开大学化学学院2012年硕士研究生招生书目
南开大学化学学院2012年硕士研究生招生书目院系所名称:化学学院电话:23505121 综合化学 《无机化学》吉林大学、武汉大学、南开大学合编高等教育出版社2004年第一版《定量化学分析》许晓文等南开大学出版社96年8月 《有机化学》王积涛等南开大学出版社2003年第二版 《近代物理化学》(上、下)朱志昂主编科学出版社2004年9月 无机化学 《无机化学》吉林大学、武汉大学、南开大学合编高等教育出版社2004年第一版《近代化学导论》申泮文等高等教育出版社2002、1 《Inorganic Chemistry》 Catherine E. Houssecroft & Alan G. Sharpe Ashford Colour Press Ltd Gosport,2001 分析化学 《定量化学分析》许晓文等南开大学出版社96年8月 《仪器分析教程》北京大学化学系北京大学出版社1997年5月 有机化学 《有机化学》王积涛等南开大学出版社2003年第二版 《有机化学习题解》张宝申、庞美丽南开大学出版社2004年1月 《有机化学辅导》张宝申、庞美丽南开大学出版社2004年7月 物理化学 《物理化学》(上、下)傅献彩等高教出版社第4版.第5版 《近代物理化学》(上、下) 朱志昂主编科学出版社2004年9月 《物理化学学习指导》朱志昂、阮文娟主编科学出版社2006年6月 《结构化学基础》周公度、段连运编北京大学出版社2002年7月第三版 高分子化学与物理 《高分子物理》何曼君等复旦大学出版社2003年第十次印刷 《近代高分子科学》张邦华、朱常英、郭天瑛主编化学工业出版社2006年第1版《高分子化学教程》王槐三主编科学出版社2006年1月第5次印刷 有机化学与农药化学 《有机化学》王积涛等南开大学出版社2003年第二版 《农药化学》唐除痴等南开大学出版社1998年第一版
无机化学二版电子教案(第二版)02习题库
学习指南 重点:1、影响化学反应速率的因素及其应用2、化学平衡常数3、化学平衡的移动 难点:1、活化能理论2、影响化学平衡移动的因素及其化学平衡移动的应用 原理知识:1、速率方程2、有效碰撞理论3、化学平衡4、化学平衡的移动 习题: 1.下列说法错误的是( ) A. 一步完成的反应是基元反应。 B. 由一个基元反应构成的化学反应称简单反应。 C. 由两个或两个以上基元反应构成的化学反应称复杂反应。 D. 基元反应都是零级反应。 2.若有一基元反应,X+2Y=Z,其速率常数为k,各物质在某瞬间的浓度: C=2mol·L-1 C=3mol·L-1 C=2mol·L-1 ,则v为( ) A. 12k B. 18k C. 20k D. 6k 3.103BA01 有基元反应,A+B=C,下列叙述正确的是( ) A. 此反应为一级反应 B. 两种反应物中,无论哪一种的浓度增加一倍,都将使反应速度增加一倍 C. 两种反应物的浓度同时减半,则反应速度也将减半 D.两种反应物的浓度同时增大一倍,则反应速度增大两倍, 4.103BB05 298K时,反应aW+bY=dZ的实验数据如下: 5.初始浓度(mol·L-1 ) 初速度(mol·L-1·S-1 ) C C 1.0 1.0 2.4×10 2.0 1.0 2.4×10 1.0 2.0 4.8×10 1.0 4.0 9.6×10 此反应对W,Y的反应级数分别为( ) A. a B. b C. 0 D. 1 E. 2 6.103BA06 已知2A+2B=C,当A的浓度增大一倍,其反应速度为原来的2倍,当B 的浓度增大一倍,其反应速度为原来的4倍,总反应为( )级反应. A. 1 B. 2 C. 3 D. 0 7.氨在金属钨表面分解,当氨的浓度增大一倍,其反应速度没有变化,则 该反应属( )级反应, A. 0 B. 1 C. 2 D. 无法判断 8.已知:2NO+2H 2=N 2 +2H 2 O,当反应容器体积增大一倍,其反应速度为原来的 1/8,则该反应为( )级反应. A. 1 B. 2 C. 3 D. 0 9.下列叙述正确的是( ) A. 反应的活化能越小,单位时间内有效碰撞越多。 B. 反应的活化能越大,单位时间内有效碰撞越多。 C. 反应的活化能越小,单位时间内有效碰撞越少。
无机化学课程自评报告
《无机化学》课程自评报告 1.教研室概况 1.1师资队伍 教研室目前在编教师2人,其中教授1人,讲师1人2。35岁以下青年教师1人,主讲教师具有硕士以上学位或讲师以上职称,在职博士1人。 1.2承担教学任务 本课程组近三年承担的教学任务: 2004级12个班的无机化学、2005级7个班的无机化学、2006级7个班的无机化学理论教学和52个实验教学班的实验教学及2003级8个班、2004级8个班、2005级5个班的普通化学理论和42个实验教学班实验课教学。虽然承担的教学任务较重还是保质保量的完成了教学任务。 2.师资队伍建设 高水平的师资队伍是保证课程改革与建设,提高教学质量的关键。多年来教研室一直重视师资队伍的建设,目前形成了一支学术水平较高、有崇高的师德和敬业精神的师资队伍。 2.1师资结构 高级职称教师比例:课程组具有高级职称的教师1人,占课程组人数的50%。 2.2教书育人 教师的师德和教风,不仅直接关系到教学质量的高低,还对学生的世界观、价值观、人生观的形成有着直接的影响,因此,教研室高度重视学风的建设。老教师身体力行,以严谨的科学态度和高度的责任心,以“传、帮、带”的形式传给青年教师,使教研室保持了科学、严谨、认真、负责的优良传统。近几年由于
扩招,工作量不断增大,不管承担多大的教学任务,教师以高度的责任心,做到作业全批全改。教师还利用课余时间和学生谈心,密切了师生关系,受到学生的好评。杨云老师获得2004学年度天津商学院优秀教师。 2.3学术水平和教学水平 2.3.1师资培养 建设一支结构合理、相对稳定、热爱教学、勇于创新的教师队伍是实现教学目标的根本保证。无机化学课程组现有教授1人,省部及有突出贡献的专家1人,享受国务院特殊津贴专家1人,讲师1人。 教研室非常重视师资队伍建设,在教学任务繁重的情况下,采取多种方式制定了提高教师素质的计划,现有1人在职攻读博士学位,准备07-08年底,再送一名教师攻读博士,争取到08年,实现课程组教师队伍都具有硕士以上学历。 随着招生规模的扩大和选修课的增加,计划近5年引进博士生1—2名;5年内晋升1副教授,使课程组教师在学历层次,年龄结构、职称比例,学缘关系更趋合理,教学和科研水平有较大幅度提高。 2.3.2学术水平 近三年教研室的全体教师积极参加科学研究和教学研究工作,共承担校级课题两项,发表教改论文1篇,学术论文10余篇,其中SCI收录3篇。马书林老师获得2004年度天津商学院科研贡献奖。杨云老师获得天津商业大学2006年度科研贡献奖。 2.3.3教学水平 高级职称教师全部为本科生授课,授课率达100%。所有主讲教师都具有硕士学位或讲师以上职称。能系统开出两门课的比率100%。 2006年教学论文《如何做好普通高校工科无机化学教学之我见》发表于天津商学院高教研究。 3.深化教学改革,提高教学质量 3.1建立无机化学教学课程体系 我们根据多年的教学经验及工科院校人才培养的要求,通过近两年大纲的修改,制订出符合学校办学方针相一致的《无机化学》课程教学大纲,优化与重组
