黄酮类化合物

天然黄酮类化合物分离纯化及鉴定研究概况
摘 要 黄酮类化合物是一类在植物中分布广泛、具有多种生物活性的多酚类化合物。在人类的营养、健康和疾病防治有着广阔的应用前景。本文介绍了天然黄酮类化合物的结构特点、提取分离、纯化及鉴定研究方法,综述了部分国内外近年来分离纯化鉴定黄酮类化合物的文献报道,并对其研究和应用前景进行展望。
关键词 黄酮类化合物 分离纯化 鉴定 研究方法 研究概况
黄酮类化合物又称黄碱素或黄酮体,是一类存在于植物中的天然产物,在自然界中广泛分布,属于植物次级代谢产物,在植物的叶子和果实中少部分以游离形式存在,大部分与蔗糖合成苷类,以配基的形式存在。到目前为止,已经发现5000多种植物中含有黄酮类化合物,黄酮类化合物主要存在于芸香科、唇形科、豆科、伞形科、银杏科与菊科等植物中。许多研究已表明黄酮类化合物具有显著的生理药理活性,除具有抗菌、消炎、抗突变、降压、清热解毒、镇静、利尿等作用外,在抗氧化、抗癌、防癌、抑制脂肪酶等方面也有显著效果。它是大多数氧自由基的清除剂,对冠心病、心绞痛等疾病的治疗效果显著[1]。黄酮类化合物安全、无毒,即是药品又是食品,在医药、食品加工等方面已被广泛应用。此外,黄酮类化合物还具有保鲜和护肤美容等作用。因此,黄酮类化合物的功用引起了人们的广泛重视,对该类化合物的研究已成为国内外研究的热门课题。
1 黄酮类化合物的结构和种类
黄酮类化合物,又名生物类黄酮化合物,是色原酮或色原烷的衍生物。黄酮类化合物以前主要是指基本母核结构为2- 苯基色原酮类化合物,目前则泛指 2 个具有酚羟基的苯环(A 和 B ) 通过中央三碳链相互连结而成的一系列化合物。它们一般是由二个苯环(A -环与B -环)通过中央三碳链(C -链)相互连接而成,即具有C6-C3-C6基本骨架。黄酮类化合物的基本结构见图1。 O
O O O A C 23456
7
8B 1'
2'3'4'5'6'O 原酮C 6C 3C 612-苯基色原酮
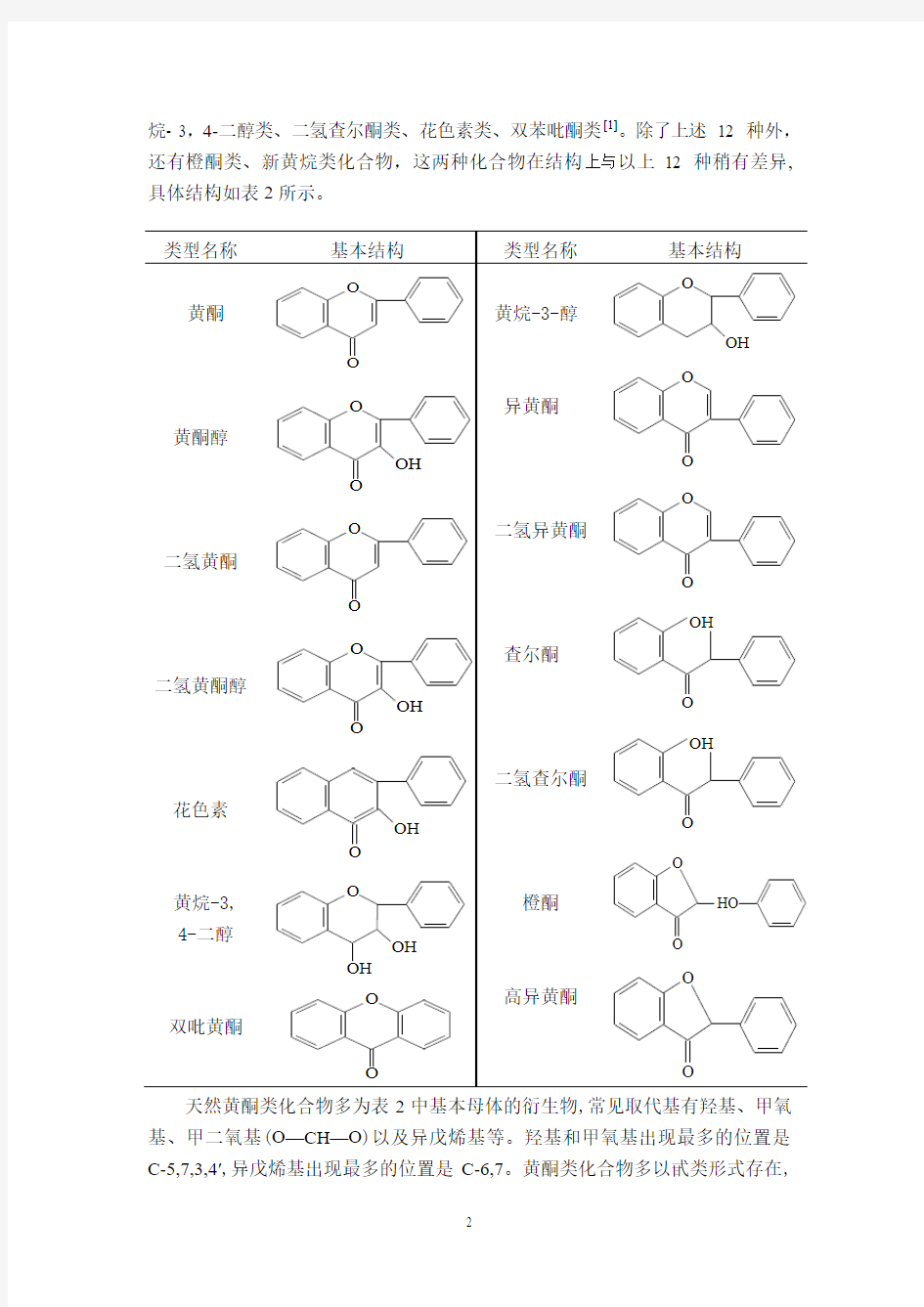
根据三碳链氧化程度、B 环 (苯基) 联结位置(2 位或 3 位) 以及三碳链是否呈环状等特点,可将黄酮类化合物大致分为:黄酮类、黄酮醇类、二氢黄酮类、二氢黄酮醇类、异黄酮类、二氢异黄酮类、黄烷- 3-醇、查尔酮类 、黄图1 黄酮类化合物的基本结构
烷- 3,4-二醇类、二氢查尔酮类、花色素类、双苯吡酮类[1]。除了上述 12 种外,还有橙酮类、新黄烷类化合物,这两种化合物在结构上与以上12 种稍有差异,具体结构如表2所示。
天然黄酮类化合物多为表2中基本母体的衍生物,常见取代基有羟基、甲氧基、甲二氧基(O —CH —O )以及异戊烯基等。羟基和甲氧基出现最多的位置是C-5,7,3,4′,异戊烯基出现最多的位置是C-6,7。黄酮类化合物多以甙类形式存在, 类型名称
基本结构 类型名称 基本结构
黄酮
黄酮醇
二氢黄酮
二氢黄酮醇
花色素
黄烷-3,
4-二醇
双吡黄酮
O O O O OH O O O O OH O OH O OH OH O O 黄烷-3-醇 异黄酮 二氢异黄酮 查尔酮 二氢查尔酮 橙酮 高异黄酮 O OH O O O O O OH O OH O O HO O O
并且由于糖的种类、数量、联接位置及连接方式的不同,可以组成各种各样的黄酮甙类。组成黄酮甙类的糖类主要有D-葡萄糖、D-半乳糖、L-鼠李糖、L-阿拉伯糖、D-木糖、D-葡萄糖醛酸等,或由这些糖组成的双糖或三糖。糖的连接位置与甙元的结构类型有关,如单糖链氧甙的连接位置经常是C-3,7,3′,4′位;二糖链氧甙的连接位置常见的是C-3,7、C-3,4、或C-7,4′位。花色素甙糖多连在C-3或形成3,5-二葡萄糖甙。在碳甙中,糖多连接在C-6或C-8位上。
在植物体中,黄酮类化合物因其所在组织不同,其存在状态也不尽相同[2]。在木质部中,多以苷元形式存在,而在花、叶、果实等器官中,多以糖苷形式存在。此外,也有一些特殊类型黄酮类物质,如生物碱型黄酮等。
2 黄酮类化合物的研究方法
2.1黄酮类化合物的提取方法
2.1.1有机溶剂提取法
这是目前国内外使用最广泛的方法。利用黄酮类化合物与混入的杂质极性不同,选用不同的溶剂可提取出黄酮类化合物。常用的有机溶剂有甲醇、乙醇、乙酸乙酯、乙醚、丙酮等。由于甲醇、丙酮等毒性较大,因此有机溶剂提取法中最常采用乙醇作为萃取剂[3]。本法主要用于提取脂溶性基团占优势的黄酮类化合物,对设备要求简单,产品得率高,但成本较高,杂质含量也较高。可用加热回流或冷浸法提取,然后,可得其粗提物。
2.1.2 超临界流体萃取法
超临界流体萃取分离过程是利用超临界流体的溶解能力与其密度的关系,即利用压力和温度对超临界流体溶解能力的影响而进行的。当气体处于超临界状态时,其性质介于液体和气体之间的单一相态,具有和液体相近的密度,粘度虽高于气体但明显低于液体,扩散系数为液体的10~100倍,因此对物料有较好的渗透性和较强的溶解能力,能够将物料中某些成分提取出来。该技术的主要特点是提取量高、产品不含有害物质、无污染[4]。但是由于超临界提取所需设备价格昂贵、生产成本高,且提取物中烷基酚含量较高,目前仍不能进行规模化生产。
2.1.3超声提取法
超声波法的原理是利用超声波产生的强烈振动、高的加速度、强烈的空化效应、搅拌作用等加速药物有效成分进入溶剂,从而提高提取率,缩短提取时间,并且免去高温对提取成分的影响。超声波对媒质主要产生独特的机械振动作用和空化作用。该法具有设备简单、操作方便、能耗低、提取时间短、产率高、溶解能力强、不破坏有效成分和无需加热等优点。
2.1.4 半仿生提取方法
半仿生提取法,是将整体药物研究法与分子药物研究法相结合,是从生物药
剂角度,模仿药物在肠胃转运过程所经历的环境,采用选定pH 的酸性水和碱性水依次连续提取,从而得到含黄酮成分高的混合物[5]。此方法生产周期短,可提取和保留更多的有效成分。
2.1.5双水相提取
双水相萃取法属于液—液萃取。由于此技术具有对生物产品稳定性好、易放大等优点,在生物大分子如蛋白质、核酸和细胞器等产品中得到广泛应用。双水相体系具有分相快,使用温度低,易操作等特点,且所用的PEG 及盐类对人体及环境无毒害,提取率高,为黄酮化合物富集分离的一种有效方法。
2.2黄酮类化合物的纯化分离方法
2.2.1柱色谱法
分离黄酮类化合物常用的吸附剂或载体有硅胶、聚酰胺、葡聚糖凝胶、大孔吸附树脂及纤维素粉等。此外,也有用氧化铝、氧化镁和硅藻土等作为吸附剂或载体的。
2.2.2制备薄层色谱法
利用薄层色谱法快速、简便、高灵敏度、高分辨效率等特点分离制备纯物质的方法称为制备薄层色谱法,常用硅胶做吸附剂。薄层制备色谱法属于固—液吸附色谱,兼备了柱色谱和纸色谱的优点,是快速分离和定性分析少量物质的一种很重要的分离方法。
2.2.3高效液相色谱法(HPLC 法)
高效液相色谱法又称“高压液相色谱”法,该法具有分离效率高、分析速度快、检测灵敏度高等特点,以液体为流动相,采用高压输液系统,将具有不同极性的单一溶剂或不同比例的混合溶剂、缓冲液等流动相泵入装有固定相的色谱柱,在柱内各成分被分离后,进入检测器进行连续检测,从而还实现对样品的分析。
2.2.4 大孔吸附树脂法
大孔吸附树脂是一种新型高效的分离纯化材料,是一类不含离子基团的网状结构高分子聚合物吸附剂,广泛用于物质的分离纯化,具有吸附快,吸附容量大,洗脱率高,树脂再生简单,吸附选择性好、解吸条件温和、使用周期长、易于构成闭路循环及节省费用等优点,适合于工业化生产[5]。
2.2.5梯度 pH 值萃取法
梯度 pH 值萃取法适合于对酸性强弱不同的游离黄酮类化合物的分离。根据黄酮类化合物酚羟基数目及位置的不同,其酸性也不同的性质,可以将混合物溶于有机溶剂 (如乙醚) 后,依次用质量分数为 5%的3C a O H N (萃取出7,4-二羟基黄酮),5%的3
2CO Na (萃取出7- 羟基黄酮或4- 羟基黄酮),0.2%NaOH
(萃取出一般酚羟基黄酮)及4%的NaOH水溶液(萃取出5-羟基黄酮分步萃取,从而达到分离的目的。
2.3黄酮类化合物的鉴定方法
2.3.1化学元素分析法
用化学方法是将复杂的分子降解为几个稳定的碎片,碎片一般能通过一些官能团的显色反应、理化常数的测定、元素的分析等方法可合成证明的简单化合物,然后按降解反应的原理推导出原化合物可能的结构。这种方法耗时,操作繁琐,需要大量的分析样品,对于特别复杂的化合物很难得出其准确的结构。因此,随着科学技术的发展,化学法测定黄酮类化合物的结构已基本上让位于各种光谱和波谱的综合分析。
2.3.2 波谱技术
波谱技术主要包括紫外—可见光谱(UV—VIS)、红外光谱(IR)、质谱(MS)、核磁共振氢谱(1HNMR)、核磁共振碳谱(13CNMR)、二维核磁共振谱(2D—NMR)等方法[7]。这些方法成功地解决了含糖数目较多的黄酮苷中苷键的构型,以及糖与糖之间的连接顺序和连接位置等一系列结构确定中的棘手问题。结合单晶X—射线衍射法可以获取化合物分子中各原子的坐标,得到了化合物中各原子空间的结合位置,为确定分子结构提供了直观可靠的立体图形。2.3.2.1红外光谱(IR)法
被测物质的分子在红外线照射下,只吸收与其分子振动、转动频率相一致的红外光谱。对红外光谱进行剖析,可对物质进行定性分析。化合物分子中存在着许多原子团,各原子团被激发后,都会产生特征振动,其振动频率也必然反映在红外吸收光谱上。据此可鉴定化合物中各种原子团,也可进行定量分析。
物质的红外光谱具有特征性,不同的物质其红外光谱不同,故可用来进行物质的定性、结构分析及定量分析等,应用比紫外吸收光谱广泛。
2.3.2.2紫外光谱(UV)检测法
紫外光谱(UV)检测法是一种利用某些物质的分子吸收波长 200~800 nm光谱区的辐射来进行分析测定的方法,研究化合物结构的主要作用是推测官能团结构中的共轭体系中取代基的位置和数目等主要是确定有机物中是否存在双键或共轭体系,其本质是电子在二轨道上的跃迁,对应的能量在紫外光谱上的位置。
2.3.2.3质谱 (MS) 法
质谱分析是一种测量离子荷质比(电荷—质量比)的分析方法,其基本原理是使试样中各组分在离子源中发生电离,生成不同荷质比的带正电荷的离子,经加速电场的作用,形成离子束,进入质量分析器。在质量分析器中,再利用电场和磁场使发生相反的速度色散,将它们分别聚焦而得到质谱图,从而确定其质量。
质谱法主要应用于鉴定复杂分子并确定元素的同位素质量及分布。
2.3.2.4 核磁共振谱(1HNMR ,13CNMR )法
核磁共振波谱法是研究原子核在磁场中吸收射频辐射能量进而发生能级跃迁现象的一种波谱法。通常专指气原子的核磁共振波谱(质子核磁共振谱)的研究。同一核素的原子核在不同化学环境下能产生位置、强度、宽度等各异的谱线,为研究复杂的分子结构提供重要的信息。由核磁共振提供的信息,可以分析各种有机和无机物的分子结构。
3近年来国内外黄酮类化合物分离纯化鉴定研究进展
由于天然植物中所含黄酮类化合物种类众多,成分复杂,含量较低,并具有多种多样的生物活性,因此从天然植物中分离纯化黄酮类化合物极具重要性和挑战性。随着色谱分离技术和光谱鉴定技术的发展,更为快速准确的实验方法和实验手段被应用于天然黄酮类化的的提取、分离、纯化、分析、鉴定,致力于该领域的国内外研究者们也不断取得新的研究成果,1950年发现的黄酮类化合物仅有104种,到目前为止已达到8000余种,研究发展非常迅速。以下从国内和国外两个分别阐述些近年来的一些最新研究成果。
3.1 国内研究进展
王克勤[8]等将芹菜叶经乙醇回流提取后,采用大孔树脂(XDA-1)、聚酰胺树脂和葡聚糖凝胶(Sephadex LH-20)色谱柱分离纯化得到黄酮化合物单体[8]。经NMR H 1-,NMR C 13-,HMBC ,MS ,UV 等方法鉴定,3 个芹菜黄酮单体化 合物分别为芹菜素(5,7,4′-Trihydroxyflavone )、芹菜苷Apigenin-7-(2-O-apiosylgl- Ucoside)、柯伊利素7-O-葡萄糖-2-O-芹糖苷(Chrysoeiol7-O-glucose-2-O-apiosylgl- ucoside) 。在分离得到的3个黄酮单体中芹菜素为水解产物,分离得到的另2个黄酮苷均为双糖苷。
邹文韬[9]等利用微波辅助提取法从杭白菊中提取黄酮类化合物,经石油醚、水饱和正丁醇萃取后,用大孔吸附树脂柱层析、聚酰胺柱层析初步分离,再用半制备型高效液相色谱分离制备单体化合物。分离得到3个单体化合物经鉴定分别为木犀草素7-O-β-D-葡萄糖苷(Luteolin 7-O-β-D-glucoside)、芹菜素7-O-β-D-葡萄糖苷(Apigenin 7-O-β-D-glucoside)、香叶木素7-O-β-D-葡萄糖苷(Diosmetin 7-O-β-D-glucoside)。
杨洁等[10]以湖北大宗油菜蜂花粉为材料,对其中微量特征成分黄酮类化合物进行鉴定。采用超声波辅助技术提取,运用二次回归正交旋转组合实验优化提取工艺,通过响应面分析和岭嵴寻优分析,确定黄酮类化合物的最佳提取条件。采用 HPLC-DAD 以及 HPLC-MS 对酸解后的提取液进行分析,结果表明:超声波辅助技术提取油菜蜂花粉中黄酮类化合物的最佳条件为体积分数 76% 乙
醇、料液比 1:30、超声波时间33min ,超声波温度为51℃。蜂花粉中总黄酮含量的理论得率为2.12%,实际得率为1.89%,实测得率达到理论预测值的89.15%。HPLC-DAD 以及HPLC-MS 分析结果证实油菜蜂花粉中可能含有 9 种黄酮苷元。其中可以推定的黄酮类物质是槲皮素、山奈酚、异鼠李素和柚皮素。另外 5 种黄酮苷元(2种黄酮醇3种黄酮)的准确结构信息,还需要进一步分析和鉴定
杜琪珍等[11]利用高速逆流色谱、制备型液相色谱等技术对常春油麻藤花中的黄酮类化合物进行分离纯化和结构鉴定,并采用 DPPH 法测定其抗氧化活性。分离得到8个化合物单体分别鉴定为矢车菊3-O-6"-O-α-鼠李糖-β-D-葡萄糖苷 (cyanidin3-O-6"-O-α -rhamnopyranosyl-β-D-glucopyranoside,I)、矢车菊3-O-β-D-葡萄糖苷(cyanidin 3-O-β-D- glucopyranoside,II)、槲皮素-3-O-β-D- 葡萄糖苷(quercetin-3-O-β-D-glucopyranoside,III)、二氢槲皮素(dihydroquercetin,IV)、山奈酚(kaempferol,V)、异夏佛塔苷(6-C-β-L-arabinopyranosyl-8-C-β-D-glucopyrano- sylapigeni,VI)、山奈酚-3-O-α -L-鼠李糖基-(1-6)-β-D-半乳糖苷 (kaempferol-3-O-α -L-rhamnopyranosyl-(1-6)-β-D- galactopyranoside ,VII)和山奈酚-3-O-α -L-鼠李糖 基-(1-4)-β-D-葡萄糖苷(kaempferol-3-O-α-L-rhamnopyranosyl-(1-4)-β-D-glucopyra- noside),VIII)。其中黄酮 I ~V 为主要的抗氧化物质,其抗氧化活性存在剂量效应关系,黄酮 VI ~VIII 抗氧化活性较低。
邹耀洪,顾小燕用反相高效液相色谱法,以SpharisorbODS 柱为固定相,甲醇-四氢吠喃一水一甲酸为流动相,并应用二极管阵列检测技术,分析了天精中的黄酮类化合物[12]。经UV 、IR 、HNMR 1、CNMR 13、MS 等波谱分析,5种黄酮类化合物分别鉴定为5,7,3'-三羟基-6,4',5'-三甲氧基黄酮(1),金合欢素(2),金合欢素-7-O-α-L-鼠李糖基(l→6)-β-D-葡萄糖武(3),木樨草素(4),槲皮素-3-0-α-L-鼠李糖基(l→6)-β-D-葡萄糖武(5),其中(l)为新化合物。
李万华等[13]研究中药材皂角刺中黄酮类化合物化学成分。采用溶剂萃取、反复柱层析方法,分离纯化皂角刺中黄酮类化合物,通过NMR,MS 等波谱技术确定其化学结构,并进行细胞模型的体外活性筛选。从皂角刺中分离得两种黄酮类化合物,结构鉴定为(+)trans-2R, 3R-3′,4′, 5, 7-tetrahydroxyflavanonol(1)和8-C-glucopyranosyl-3, 4′, 7-trihydroxyflavone(2),化合物2显示出明显的组织蛋白酶B 抑制活性(CAT-B 模型)。该两种化合物均为首次从皂角刺中分离得到的单体黄酮类化合物,且发现化合物2具有组织蛋白酶B 抑制活性。
任顺成等[14]从玉米须中提取、分离黄酮类成分。通过溶剂法提取醇溶性成分,柱层析法得到6种黄酮类化合物。其中,化合物Ⅴ和化合物Ⅵ经鉴定分别为7, 4′-二羟基-5-甲氧基黄酮-2″-O-α-L-鼠李糖基-6-C-岩藻糖苷和6, 4′-二羟基-3′, 5′-二甲氧基黄酮-7-O-葡萄糖苷。
张沐新等[15]将玉米( Zea mays L) 苞叶粉碎后,用乙醇提取法得乙醇粗提物。将粗提物用水溶解后,上AB-8大孔树脂柱,依次用蒸馏水、体积分数不同的乙醇梯度洗脱,再将洗脱物用硅胶柱色谱分离,得组分Ⅰ,Ⅱ,Ⅲ和Ⅳ。组分Ⅰ,Ⅱ和Ⅲ经反复重结晶分别得到化合物 1,2和 3 ; 组分Ⅳ 经葡聚糖凝胶柱色谱分离,并用甲醇洗脱得化合物4。它们分别为苜蓿素( 1) 、苜蓿素-5-O-β-D-吡喃葡萄糖苷( 2) 、苜蓿素-7-O-β-D-吡喃葡萄糖苷( 3) 和苜蓿素-7-O-[β-D-呋喃芹糖基-( 1→2) ]β-D-吡喃葡萄糖苷( 4) 。其中,化合物4 为新化合物,化合物 1 ~ 3 为首次从该植物中分离得到。
吕应年等[16]将半边旗干燥的全草经粉碎后,以80%乙醇回流萃取得浸膏,浸膏再用石油醚、氯仿和乙酸乙酯依次抽提,将乙酸乙酯抽提物减压蒸干得到半边旗黄酮样品。样品经薄板层析、化学显色反应及紫外光谱分析,初步鉴定了其中的黄酮物质成分;样品经液相色谱-质谱联用分析,进一步确证了半边旗黄酮中含有芹菜素、木犀草素和木犀草素葡萄糖苷。样品用2322I O S Na ,滴定试验考察发现其具有良好的抗氧化活性。
3.2 国外研究进展
Saeed Ahmad [17]等从骆驼刺中分离出了一个新的黄酮类化合物,异鼠李糖-3-O-[α-1-吡喃鼠李糖基-(1→ 3)]-β-d-吡喃葡萄糖苷(isorhamnetin-3-O-[-α-l-rhamnopyranosyl-(1 → 3)]-β-d-glucopyranoside )(1),及两个已知的黄酮类化合物3'-O-甲基(3'-O-methylorobol )(2)和槲皮素3-O-β-D-吡喃葡萄糖苷(quercetin 3-O-β-d-glucopyranoside )(3)。采用一维和二维磁共振光谱,质谱法,并参考文献的数据进行比较,测得其结构。
Abulimiti Yili 等[18]经Sephadex LH-20柱初步清理,采用高速逆流色谱法从粗蜡菊样本中成功分离出三个黄酮类化合物。结构分别鉴定为柚皮素-7-O-β-d-葡萄糖苷(Naringenin-7-O-β-d-glycoside )(2.3毫克),异槲皮苷(isoquercitrin )(3.5毫克),紫云英苷(astragalin)(6.7毫克),纯度为96.05%,93.63%,95.23%。 Y . Hugh Guan, Ian A. Sutherland 等[19]采用高速逆流色谱系统,以氯仿-甲醇-水(9.5:10:5)两相体系从木蝴蝶叶中分离出多种黄酮类化合物,并鉴定为有黄苓素(baicalein ),黄苓素-7-O-葡萄糖甙(baicalein-7-O-glucoside ),黄苓素-7-O-葡萄糖苷(baicalein-7-O-diglucoside ),白杨素-7-O-葡萄糖醛酸苷(chrysin-7-O-glucuronide ),黄苓素-7-O-葡萄糖醛酸(baicalein-7-O-glucuronide ),其中黄苓素-7-O-葡萄糖醛酸苷和黄苓素-7-O-葡萄糖醛酸是首次从该植物中提取出的。本研究还提取出了一个新的白杨-葡萄糖苷提取物。结果表明,高速逆流色谱分离是一个强大的工具,可以促进植物成分的确定和量化。
Haji Akber Aisa 等[20]采用AB-8大孔吸附树脂,高速逆流色谱法(HSCCC )
成功从金银花棉蚜中分离出四种黄酮类化合物。高速逆流色谱法用氯仿-甲醇-异丙醇-水(5:5:1:3,V/V)组成的两相溶剂系统,固定相的水溶液中加入0.4%的磷酸。四种黄酮类化合物分别鉴定为槲皮素(yielded quercetin)(5.6毫克),槲皮素-3'-O-D-葡萄糖苷(quercetin-3'-O-D-glucoside)(7.2毫克),槲皮素-3-O-β-D-葡萄糖苷(quercetin-3-O-β-D-glucoside)(16毫克),槲皮素-7-O-β-D-葡萄糖苷(quercetin-7-O-β-D-glucoside)(8.3毫克)。
4 前景展望
近年来,高新技术的应用如热反应技术、生物技术、微胶囊包埋技术、干燥技术、膜分离技术、超临界萃取技术、超微粉碎技术、电磁技术以及多种技术的组合,为黄酮类化合物的提取、分离、纯化、分析、鉴定等提供了更为快速准确的实验方法和新的手段思路。随着分离提取技术的发展,发现了大量新黄酮类化合物,也掀起了研究热潮,开发了数种含有该物质成分的产品。在医药方面,根据其在心血管系统、内分泌系统、抗肿瘤方面的药理作用,很多以黄酮类成分为主的制剂已经上市。黄酮类化合物来自于天然植物,在食品中也有广阔的应用前景。黄酮类化合物是一类优良的抗氧化剂资源,在食品中,除了应用于功能性食品添加剂,如天然甜味剂、天然抗氧化剂、天然色素等;还应用于功能食品,如生物类黄酮口香糖、银杏叶袋泡茶等防衰、抗癌和提高免疫力食品近年来,除了从药材中提取分离黄酮类化合物不断被报道外,一些农作物如柑橘、大豆、山楂等的黄酮类化合物的分离鉴定也日益受到关注。虽然从各种植物中分离和提取了大量的新黄酮类化合物,掀起了黄酮类化合物的研究热潮,但对其吸收、代谢机制、活性机理,具有生理功能的活性基团、稳定性等方面仍缺乏全面的认识。因此,应加强此方面的工作,以较先进的检测分析手段对其功能成分进行定性及定量分析,确定这些功能成分的提取工艺,并通过相应的动物及人体试验,验证这些功能成分的保健作用,并揭示其量效关系,为黄酮类化合物的进一步开发利用
奠定坚实的基础。
总之,黄酮类化合物作为一类生物活性很强的化合物,具有众多优点,其在医药、食品等领域中具有广阔的应用前景。
参考文献:
[1] 董彩军,李锋.黄酮类化合物的研究进展[J].农产品加工·学刊,2010,2(2): 65-69.
[2] 宋秋华,张磊,梁飞,姚小丽.黄酮类化合物提取和纯化工艺研究进展[J].山西化工,2007,27
(4):24-27.
[3] 王长远,吴洪奎,于长青,马万龙.黄酮类化合物研究进展[J].黑龙江八一农垦大学学报,19
(2):75-78.
[4] 张胜,赵玲玲.黄酮类化合物的提取纯化研究进展[J].温州大学学报,2007,28(5) :25-29.
[5] 赖毅勤,周宏兵.近年来黄酮类化合物提取和分离方法研究进展[J].食品与药品,2007,9(4):
54-58.
[6] 李凤林,李青旺,高大威,冯彩宁,郜俊杰.天然黄酮类化合物分离纯化研究进展[J].开发与
研究,2008,25(5):20-24.
[7] 张赟彬,李彩侠,吴亚卿.黄酮类化合物的研究进展[J].食品与机械,2005,21(5):69-73.
[8] 王克勤,罗军武,刘仲华,陈亮,陈静萍.芹菜叶中黄酮类化合物的提取分离与鉴定[J].食品
与机械,2009,25(6):66-70.
[9] 邹文韬,张因皎,俞菊红,房晓敏,周志明,许传莲.杭白菊中黄酮类化合物的分离与鉴定[J].
浙江理工大学学报,2012,27(1):140-144.
[10] 杨洁,陈纯,邢建军,刘睿.油菜蜂花粉中黄酮类化合物的提取与鉴定[J].食品科学,2010,31
(22):273-278.
[11] 杜琪珍,赵永春,李博.常春油麻藤花黄酮类化合物结构鉴定及抗氧化活性分析[J].食品
科学,2011,32(23):111-115.
[12] 邹耀洪,顾小燕.天精中黄酮类化合物的结构鉴定[J].常熟高专学报,2000,14(2):49-54.
[13] 李万华,李琴,王小刚,赵文明.皂角刺中黄酮类化学成分的分离鉴定[J].西北大学报,2005,
35(6):763-770.
[14] 任顺成,丁霄霖.玉米须黄酮类成分的提取分离与结构鉴定(Ⅱ)[J].河南工业大学学
报,2007,28(4):34-40.
[15] 张沐新,刘银燕,孙薇,杨晓虹,王广树.玉米苞叶中新黄酮类化合物的分离和鉴定[J].高等
学校化学学报,2011,32(11):2554-2557.
[16] 吕应年,蒋桂香,吴科锋,邓亦峰,梁念慈.半边旗中黄酮成分的分离鉴定与抗氧化活性研究
[J].化学世界,2007,205(4):24 -220.
[17] Naheed Riaz,Muhammad Saleem,Abdul Jabbar,Mohammad Ashraf,etal.Antioxidant flavonoi-
ds from Alhagimaurorum[J]. Journal of Asian Natural Products Research, 2010,12(2):138- 143.
[18] Abulimiti Yili,Gulnar Sabir,Haji Akber Aisa,etal.Separation and Purification of Three Flavon-
Oids from Helichrysum arenarium (L.) Monech by HSCCC[J].Chromatographia,2009,69(9): 963-967.
[19] Y. Hugh Guan, Ian A. Sutherland,etal.Separation of Flavonoids from the Leaves of Oroxylum
indicum by HSCCC [J]. Chromatographia,2008,68(11):885-892.
[20] Haji Akber Aisa,Yoichiro Ito,etal.Preparative Isolation and Purification of Four Flavonoids
from Flos Gossypii by High-Speed Countercurrent Chromatography[J].Journal of Liquid Chromatography & Related Technologies,2008,31(10):1523-1531.
The natural flavonoids Purification and
identification of profile
Chemistry and Environment Science College,Inner Mongolia Normal
Abstract: Flavonoids are a class of widely distributed in plants, with a variety of biologically active polyphenolic compounds. Has broad application prospects in human nutrition, health and disease prevention. This article describes the structural characteristics of natural flavonoids, extraction and separation, purification and identification methods, some of the domestic and foreign Separation, Purification and Identification of flavonoids in recent years reported in the literature, and its research and application prospects.
Keywords:flavonoid; Separation and purification; Identification Research Methods; Research Profile
黄酮类化合物——第二次作业
一、填空题 3.中药红花在开花初期,由于主要含有无色的新红花苷及微量红花苷,故花冠呈淡黄色;开花中期主要含的是黄色的红花苷,故花冠显深黄色;开花后期则氧化变成红色的醌式红花苷,故花冠呈红色。 4.黄酮类化合物呈酸性,是由于其多数带有_酚羟基__;黄酮类成分也具有微弱的碱性,是由于其结构中_7-吡喃环上的1位氧原子的存在。 7.不同类型黄酮苷元中水溶性最大的是花色素类,原因是以离子形式存在,具有盐的通性;二氢黄酮的水溶性比黄酮大,原因是系非平面性分子,故分子与分子间排列不紧密,分子间引力降低,有利于水分子进入。 8.黄酮类化合物结构中大多具有酚羟基,故显一定的酸性,不同羟基取代的黄酮其酸性由强至弱的顺序为7,4’-二羟基、7或4'-羟基、一般酚羟基、5-羟基。 9.黄酮类化合物γ-吡喃酮环上的1位氧因有未共享电子对,故表现出微弱的碱性,可与强无机酸生成样盐。 10.锆盐-枸橼酸反应常用于区别3-羟基和5-羟基黄酮,加入2%二氯氧锆甲醇溶液,两者均可生成黄色锆络合物,再加入2%枸橼酸甲醇溶液后,如果黄色不减褪,示有3-羟基黄酮;如果黄色减褪,示有5-羟基黄酮。 11.黄酮类化合物常用的提取方法有水提法、溶剂萃取法、碱提取酸沉淀法等。 12.聚酰胺柱色谱分离黄酮苷和苷元,当用含水溶剂(如乙醇-水)洗脱时,黄酮苷先被洗脱;当用有机溶剂(如氯仿-甲醇)洗脱时,苷元先被洗脱。
.二.单选题: 1.黄酮类化合物的基本碳架是( E ) A .C 6-C 6-C 3 B . C 6-C 6-C 6 C .C 6-C 3-L 6 D .C 6-C 3 E .C 3-C 6-C 3 2.与2ˊ-羟基查耳酮互为异构体的是( A ) A .二氢黄酮 B .花色素 C .黄酮醇 D .黄酮 E .异黄酮 3.水溶性最大的黄酮类化合物是(C ) A .黄酮 B .黄酮醇 C .二氢黄酮 D .查耳酮 E .异黄酮 4.酸性最强的黄酮类化合物是( E ) A .5-羟基黄酮 B .4’-羟基黄酮 C .3-羟基黄酮 D .3’-羟基黄酮 E .4’-羟基二氢黄酮 5.黄酮类化合物色谱检识常用的显色剂是(A ) A .盐酸-镁粉试剂 B .FeCl 3试剂 C .Gibb’s 试剂 D .2%NaBH 4甲醇溶液 E .l %AlCl 3甲醇溶液 6.在碱液中能很快产生红或紫红色的黄酮类化合物是( B ) A .二氢黄酮 B .查耳酮 C .黄酮醇 D .黄酮 E .异黄酮 7.将总黄酮溶于乙醚,用 5%NaHCO 3萃取可得到( E ) A .5,7-二羟基黄酮 B .5-羟基黄酮 C .3’,4’-二羟基黄酮 D .5,8-二羟基黄酮 E .7,4’-二羟基黄酮 8.下列化合物进行聚酰胺柱色谱分离,以浓度从低到高的乙醇洗脱,最先被洗脱的是( D ) A .2’,4’-二羟基黄酮 B .4’-OH 黄酮醇 C .3’,4’-二羟基黄酮 D .4’-羟基异黄酮 E .4’-羟基二氢黄酮醇 8.盐酸-镁粉反应鉴别黄酮类化合物,下列哪项错误( D ) A .多数查耳酮显橙红色 B .多数黄酮苷显橙红-紫红色 C .多数二氢黄酮显橙红-紫红色 D .多数异黄酮不显红色 9.用于鉴别二氢黄酮类化合物的试剂是(A ) A .ZrOCl 2 B .NaBH 4 C .HCl-Mg 粉 D .SrCl 2 10.下列化合物按结构应属于( D ) A. 黄酮类 B. 异黄酮类 C. 查耳酮类 D. 二氢黄酮类 O O OH CH 3 HO H 3C
药物综述-黄酮类化合物
药物综述——黄酮类化合物 关键词:黄酮类;来源;发展史;药理作用;不足之处 摘要:黄酮类化合物分布广泛,具有多种生物活性,但目前,黄酮类药物仍有些不足之处。 正文: 1.发展史:黄酮类化合物的发现历史十分悠久。早在二十世30年代初,欧洲一 位药物化学家在研究柠檬皮的乙醇提取物时无意中得到一种白色结晶,将其命名为“维生素P”。动物试验证实:维生素P的抗坏血作用胜过维生素C10倍。2年后,这位科学家进一步发现:维生素 P实际上是一种由黄酮组成的混合物而非单一物质,故后来有人形象化地将维生素P更名为柠檬素。黄酮类化合物作为保健产品首次引起国际医药界的注意是在二十世纪八十年代末。法国一家保健食品厂商率先推出具有市场引导作用的黄酮类保健新品“碧萝芷”。它是从法国地中海沿岸地区生长的一种主要树种“滨海松”树皮中提取的一种黄酮混合物。由于碧萝芷能预防和治疗西方国家极为常见的冠心病与心肌梗塞等心血管疾病,故上市后销售情况极为红火。在上市10年以后,临床医学研究人员不断发现碧萝芷有不少令人感兴趣的新用途,其中包括抗哮喘、防止长期抽烟引起的脑动脉硬化与脑血栓形成以及降血压作用等。据科学家研究,法国生产的碧萝芷含有极其复杂的黄酮成分,其中包括:儿茶素、表倍儿茶素、紫杉素、原花青素及其单体、2倍体、3倍体与多倍体混合物。正是这些复杂的黄酮构成碧萝芷多样化药理作用的基础。 2.来源:天然黄酮类化合物是植物体多酚类的内信号分子及中间体或代谢物, 包括黄酮、异黄酮、黄酮醇、异黄酮醇、黄烷酮、异黄烷酮、查耳酮等,最集中分布于被子植物中。如黄酮类以唇形科、爵麻科、苦苣苔科、玄参科、菊科等植物中存在较多;黄酮醇类较广泛分布于双子叶植物;二氢黄酮类特别在蔷薇科、芸香科、豆科、杜鹃花科、菊科、姜科中分布较多;二氢黄酮醇类较普遍地存在于豆科植物中;异黄酮类以豆科蝶形花亚科和鸢尾科。 植物中存在较多。在裸子植物中也有存在,如双黄酮类多存在松柏纲、银杏纲和凤尾纲等植物中。黄酮类化合物具有能够改变机体对变能反应原、病毒及致癌物反应的能力,并保护机体组织不受氧化性侵袭的伤害,因此具有"天然生物反应调节剂"的美称。黄酮类化合物一般存在于蔬菜和水果的可食性果肉中。当把它们从中分离出来后,其味道有些发苦,如桔子、柠檬、葡萄和柚等这些柑桔类植物是黄酮类化合物特别丰富的来源。许多植物如樱桃、葡萄、蔷薇果、青椒、花茎甘蓝、洋葱和番茄等,以及许多草药如越桔、银杏、乳蓟等都含有高质量的黄酮类化合物。此外,多种植物的叶、干和根部也发现了一些黄酮类化合物,如山茶花报春黄甙(干燥后用来生产绿茶和黑茶)的叶子,松树皮和成熟和葡萄籽是各种黄酮类化合物的最好来源。 3.药理活性: a.心血管系统活性。不少治疗冠心病有效的中成药均含黄酮类化合物。研究发现黄酮类化合物不仅有明显的扩冠作用,对缺血性脑损伤有保护作用,对心肌缺血性损伤有保护作用,对心肌缺氧性损伤有明显保护作用,还有有抗心率失常作用。
黄酮类化合物
黄酮测定的研究进展 简要:黄酮类化合物(Flavonoids),又称生物黄酮(Bioflavon-oids)或植物黄酮,是植物在长期自然选择过程中产生的一些次级代谢产物,黄酮类化合物有着广泛的生物活性和多种药理活性,比如抗氧化、抗炎、抗诱变、抗肿瘤形成与生长等,特别是近年来关于黄酮在心血管、脑血管、肿瘤等方面的研究已经比较深入,此外黄酮类物质还有低毒性的特点,因此长期以来一直是天然药物和功能性食品研究开发的热点[1]。 关键词:黄铜,含量,测定方法,研究进展 前言:黄酮类物质是植物光合作用产生的一种天然有机物。植物界中分布广泛,主要分布于芸香料、唇形科、豆科、伞形科、银杏科、菊科等。根据化学方法定义黄酮类物质为含一个共同的苯基苯并二氢吡喃环结构,有一个或多个羟基取代基,包括其衍生物。在食物中,黄酮类物质一般以酯类、醚类或配糖类衍生物及混合物的形式存在,共有5000 多种化合物。对于哺乳动物,只能通过饮食获取黄酮物质,这些食物包括水果、蔬菜、谷物、坚果、茶及红酒。在日常膳食中,黄酮类物质通常表现为具有抗氧化性的羟基衍生物形态,显示出多种生物活性,对于一些疾病,例如癌症和心血管疾病,胃和十二指肠的病理性失调,以及病毒和细菌感染的预防和治疗。此外,类黄酮还被发现有广泛的药物特性,包括抗氧化性、抗过敏、抗病毒及预防糖尿病,对肝和胃的保护,抗病原体及抗瘤活性。除在医药工业上已广泛应用其生理活性外,目前也将黄酮类物质作为功能食品的添加剂[2] 。 (一)测定黄铜的几种方法 1 紫外分光光度法 紫外分光光度法具有重复性好、准确、简便、易掌握、不需要复杂的仪器设备, 加之所需试剂便宜易得, 因此该方法应用于测定植物中黄酮含量最为广泛[ 3]。 1.1 直接测定法 大多数黄酮类化合物分子中存在桂皮酰基和苯甲酰基组成的交叉共轭体系, 其MeOH 谱200 nm~400 nm的区域内存在两个主要的紫外吸收带, 峰带I(300 nm~400nm)和峰带Ⅱ( 220 nm~280 nm)[ 4]。 1.2 比色法 向供试样品中加入显色剂后测定吸光度以测定其含量, 这种方法称为比色法。黄酮类化合物分子中若具有3- 羟基、5- 羟基或邻二酚羟基, 易于与金属盐类如铝盐、锆盐、锶盐、镁盐等反应, 生成有色金属络合物。常用于黄酮类化合物含量测定的金属盐试剂有Al(NO3)3、A1Cl3等,这些络合物作用在光
黄酮类化合物试题
中药化学试题库 第六章黄酮类化合物 一、选择题 (一)A型题(每题有5个备选答案,备选答案中只有1个最佳答案) 1.黄酮类化合物的基本碳架是() A.C6-C6-C3 B.C6-C6-C6 C.C6-C3-C6 D.C6-C3 E.C3-C6-C3 正确答案:C 2.与2’-羟基查耳酮互为异构体的是()A.二氢黄酮B.花色素 C.黄酮醇D.黄酮 E.异黄酮 正确答案:A 3.水溶性最大的黄酮类化合物是() A.黄酮 B.黄酮醇C.二氢黄酮D.查耳酮 E.异黄酮 正确答案:C 6.酸性最强的黄酮类化合物是() A.5-羟基黄酮 B.4’-羟基黄酮 C.3-羟基黄酮 D.3’-羟基黄酮 E.4’-羟基二氢黄酮
正确答案:B 7.酸性最弱的黄酮类化合物是() A.5一羟基黄酮 B.7-羟基黄酮 C.4’-羟基黄酮 D.3’-羟基黄酮 E.6一羟基黄酮 正确答案:A 10.黄酮类化合物色谱检识常用的显色剂是()A.盐酸-镁粉试剂B.FeCl3试剂C.Gibb’s试剂 D.2%NaBH4甲醇溶液 E.l%AlCl3甲醇溶液 正确答案:E 11.在碱液中能很快产生红或紫红色的黄酮类化合物是() A.二氢黄酮B.查耳酮 C.黄酮醇D.黄酮 E.异黄酮 正确答案:B 13.将总黄酮溶于乙醚,用 5%NaHCO3萃取可得到() A.5,7-二羟基黄酮B.5-羟基黄酮C.3’,4’-二羟基黄酮 D.5,8-二羟基黄酮 E.7,4’-二羟基黄酮正确答案:E 15.当药材中含有较多粘液质、果胶时,如用碱液提取黄酮类化合物时宜选用()
A.5%Na2CO3 B.l%NaOH C.5%NaOH D.饱和石灰水 E.氨水 正确答案:D 17.下列化合物进行聚酰胺柱色谱分离,以浓度从低 到高的乙醇洗脱,最先被洗脱的是() A.2’,4’-二羟基黄酮B.4’-OH黄酮醇C.3’,4’-二羟基黄酮 D.4’-羟基异黄酮 E.4’-羟基二氢黄酮醇 正确答案:A 18.黄芩苷可溶于() A.水 B.乙醇C.甲醇 D.丙酮 E.热乙酸 正确答案:E 19.下列化合物属于黄酮碳苷的是 A、芦荟苷 B、葛根素 C、大豆苷 D、芦荟大黄素苷 E、橙皮苷 正确答案:B 20.与查耳酮互为异构体的是 A、黄酮 B、二氢黄酮 C、异黄酮 D、橙酮 E、花色 素 正确答案:B
黄酮含量的测定
黄酮含量的测定 1.提取(以麦苗粉为例) 根据仿生学原理,人体胃、小肠、大肠的体液酸度最佳pH分别为2.0,7.5,8.3。称取1g麦苗粉末,选用乙醇-水作为浸取剂,模拟胃肠道的pH,分别调pH值2.0,7.5,8.3,在60℃下超声50min,合并3次提取剂,,定容。 工艺流程:1g麦苗粉末→一次提取(加入10ml70﹪的乙醇,乙醇pH2.0)→抽滤→留渣继续二次提取,滤液保存→二次提取(加10ml70﹪的乙醇,提取剂pH7.5)→抽滤→留渣继续三次提取,滤液保存→三次提取(加入10ml70﹪的乙醇,乙醇pH8.3)→合并三次滤液→定容至30mL→黄酮类化合物含量的测定分光光度法测吸光值。 麦苗汁的提取 直接从榨汁后定容至100ml的麦苗汁中取36.5ml,加入85.2ml无水乙醇,60℃超声提取150min。 2.试剂配置 芦丁标准液:准确称取芦丁标准品7.5mg,用50%乙醇溶解并定容至25mL,得到浓度为300mg/mL的芦丁标准溶液。 10% Al(NO3)3溶液:称取5g Al(NO3)3,用蒸馏水溶解并定容至50mL。 5% NaOH 溶液:称取2.5g NaOH,用蒸馏水溶解并定容至50mL。 5% NaNO2 溶液:称取2.5g NaNO2,用蒸馏水溶解并定容至50mL。 0.05mol/L Tris-HCl缓冲液(pH=8.2):0.1mol/L Tris 50mL,加入0.1mol/L HCl 22.9mL,混匀,稀释定容至100mL。 3 mmol/L 邻苯三酚-HCl溶液:准确称取0.0189g邻苯三酚,用10 mmol/L HCl溶解并定容至100mL。 9mmol/L水杨酸-乙醇:准确称取1.2430g水杨酸,用95%乙醇溶解并定容到1000mL 容量瓶中。 9mmol/L FeSO4:准确称取1.3680g FeSO4,定容到1000mL容量瓶中。 10mmol/L HCl:准确量取83.3mL分析纯HCl,定容到100mL容量瓶中。 8.8 mmol/L H2O2 溶液:吸取0.109mL 30% H2O2,用蒸馏水溶解并定容至500mL。 3.标准曲线的绘制 准确称取芦丁标准品15mg,用50%乙醇溶解并定容至50mL,得到浓度为0.3mg/mL的芦丁标准溶液。取7支试管编号,分别按表1中所给的量加入各种试剂,并测定其吸光值。 表6 芦丁标准曲线的绘制 试剂0(mL) 1(mL) 2(mL) 3(mL) 4(mL) 5(mL) 6(mL) 芦丁标准溶液0 0.5 1.0 1.5 2.0 2.5 3.0 50%乙醇 3.0 2.5 2.0 1.5 1.0 0.5 0 5% NaNO2 溶液0.4 0.4 0.4 0.4 0.4 0.4 0.4 10% Al(NO3)3 溶液0.4 0.4 0.4 0.4 0.4 0.4 0.4 5% NaOH 溶液 4.0 4.0 4.0 4.0 4.0 4.0 4.0 蒸馏水 2.2 2.2 2.2 2.2 2.2 2.2 2.2 加入5% NaNO2 溶液0.4 mL后,摇匀,放置6min ;加入10% Al(NO3)3 溶液0.4 mL
黄酮类化合物
黄酮类化合物 黄酮类化合物泛指两个具有酚羟基的苯环(A-与B-环)通过中央三碳原子相互连结而成的一系列化合物黄酮类化 合物结构中常连接有酚羟基、甲氧基、甲基、异戊烯基等官能团。此外,它还常与糖结合成苷。多数科学家认为黄酮的基本骨架是由三个丙二酰辅酶A和一个桂皮酰辅酶A生物合成而产生的。经同位素标记实验证明了A环来自于三个丙二酰辅酶A,而B环则来自于桂皮酰辅酶A[1]。1、分类:根据中央三碳链的氧化程度、B-环连接位置(2-或3-位)以及三碳链是否构成环状等特点,可将主要的天然黄酮类化合物分类:黄酮类(flavones)、黄酮醇(flavonol)、二氢黄酮类(flavonones)、二氢黄酮醇类(flavanonol)、花色素类(anthocyanidins)、黄烷-3,4二醇类(flavan-3,4-diols)、双苯吡酮类(xanthones)、查尔酮(chalcones)和双黄酮类(biflavonoids)等十五种。另外,还有一些黄酮类化合物的结构很复杂,其中包括榕碱及异榕碱等生物碱型黄酮。2、理化性质:天然黄酮类化合物多以苷类形式存在,并且由于糖的种类、数量、联接位置及联接方式不同可以组成各种各样黄酮苷类。组成黄酮苷的糖类包括单糖、双糖、三糖和酰化糖。黄酮苷固体为无定形粉末,其余黄酮类化合物多为结晶性固体。黄酮类化合物不同的颜色为天然色素家族添加
了更多色彩。这是由于其母核内形成交叉共轭体系,并通过电子转移、重排,使共轭链延长,因而显现出颜色。黄酮苷一般易溶于水、乙醇、甲醇等级性强的溶剂中;但难溶于或不溶于苯、氯仿等有机溶剂中。糖链越长则水溶度越大。黄酮类化合物因分子中多具有酚羟基,故显酸性。酸性强弱因酚羟基数目、位置而异。3、显色:1.盐酸-镁粉(或锌粉) 反应为鉴定黄酮类化合物最常用的颜色反应,反应机理现在认为是因为生成了阳碳离子缘故[1]。2.四氢硼钠(NaBH4)是对二氢黄酮类化合物专属性较高的一种还原剂,产生红~紫色。而与其它黄酮类化合物均不显色。3. 黄酮类化合分子中常含有下列结构单元,故常可与铝盐、铅盐、锆盐、镁盐、锶盐、铁盐等试剂反应,生成有色络合物。与1%三氯化铝 或硝酸铝溶液反应,生成的络合物多为黄色(λmax=415nm),并有荧光,可用于定性及定量分析。4、黄酮对身体的好处黄酮广泛存在自然界的某些植物和浆果中,总数大约有4千 多种,其分子结构不尽相同,如芸香苷、橘皮苷、栎素、绿茶 多酚、花色糖苷、花色苷酸等都属黄酮。不同分子结构的黄酮可作用于身体不同的器官,如山楂--心血管系统,兰梅-- 眼睛,酸果--尿路系统,葡萄--淋巴、肝脏,接骨木果--免疫系统,平时我们可以通过多食葡萄、洋葱、花椰莱、喝红酒、多饮绿茶等方式来获得黄酮,作为身体的一种补充。 黄酮的功效是多方面的,它是一种很强的抗氧剂,可有效清
黄酮类化合物
第五章黄酮类化合物 一、选择题 (一)单项选择题(在每小题的五个备选答案中,选出一个正确答案,并将正确答案的序号填在题干的括号内) 1.构成黄酮类化合物的基本骨架是() A. 6C-6C-6C B. 3C-6C-3C C. 6C-3C D. 6C-3C-6C E. 6C-3C-3C 2.黄酮类化合物的颜色与下列哪项因素有关() A. 具有色原酮 B. 具有色原酮和助色团 C. 具有2-苯基色原酮 D. 具有2-苯基色原酮和助色团 E.结构中具有邻二酚羟基 3.引入哪类基团可使黄酮类化合物脂溶性增加() A. -OCH3 B. -CH2OH C. -OH D. 邻二羟基 E. 单糖 4.黄酮类化合物的颜色加深,与助色团取代位置与数目有关,尤其在()位置上。 A. 6,7位引入助色团 B. 7,4/-位引入助色团 C. 3/,4/位引入助色团 D. 5-位引入羟基 E. 引入甲基 5.黄酮类化合物的酸性是因为其分子结构中含有() A. 糖 B. 羰基 C. 酚羟基 D. 氧原子 E. 双键 6.下列黄酮中酸性最强的是() A. 3-OH黄酮 B. 5-OH黄酮 C. 5,7-二OH黄酮
D. 7,4/-二OH黄酮 E. 3/,4/-二OH黄酮 7.下列黄酮中水溶性性最大的是() A. 异黄酮 B. 黄酮 C. 二氢黄酮 D. 查耳酮 E. 花色素 8.下列黄酮中水溶性最小的是() A. 黄酮 B. 二氢黄酮 C. 黄酮苷 D. 异黄酮 E. 花色素 9.下列黄酮类化合物酸性强弱的顺序为() (1)5,7-二OH黄酮(2)7,4/-二OH黄酮(3)6,4/-二OH黄酮A.(1)>(2)>(3) B.(2)>(3)>(1) C.(3)>(2)>(1)D.(2)>(1)>(3) E.(1)>(3)>(2) 10.下列黄酮类化合物酸性最弱的是() A. 6-OH黄酮 B. 5-OH黄酮 C. 7-OH黄酮 D. 4/-OH黄酮-二OH黄酮 11.某中药提取液只加盐酸不加镁粉,即产生红色的是() A. 黄酮 B. 黄酮醇 C. 二氢黄酮 D. 异黄酮 E. 花色素 12.可用于区别3-OH黄酮和5-OH黄酮的反应试剂是() A. 盐酸-镁粉试剂 B. NaBH4试剂 C.α-萘酚-浓硫酸试剂 D. 锆-枸橼酸试剂 E .三氯化铝试剂 13.四氢硼钠试剂反应用于鉴别() A. 黄酮醇 B. 二氢黄酮 C. 异黄酮
第5章-黄酮类化合物-习题
第五章 黄酮类化合物 一、名词解释 1. 黄酮类化合物 2. 盐酸-镁粉反应 3. 锆-枸椽酸反应 二、指出下列化合物属于何种黄酮类型 H O O (1)黄芩甙 H Glu (2)甘草甙 H 3CO O OH O O H O OH O OCH 3OH (3)红花甙 O H OH O H O O OH (4)银杏素 H 23 O H O O OH Glu O H O OH O OH OH OH 三、填空 1. 黄酮类化合物结构中有一个带_____性的氧原子,能与_____形成yang 盐。yang 盐极不稳定,_____即可分解。 2. 黄酮类化合物就整个分子而言,由于具有多个_____基,故呈__ _性,能溶于____性水液中。 3. 用聚酰胺柱层析分离黄酮类成分时,用醇由稀到浓洗脱时,查耳酮往往比相应的二氢黄酮____被洗脱;苷元比其相应的苷____被洗脱;单糖苷比相应的三糖苷___被洗脱。 4.黄酮类化合物的酸性来源于_____,其酸性强弱顺序依次为____>____>____ >____>____。 5.黄酮类化合物的基本骨架为___,其主要结构类型是依据___、_ __及___某特点而分类。 6. 黄酮类化合物的颜色与分子中是否存在__________及__________有关。
7. 30%乙醇、95%乙醇、NaOH 水溶液、尿素水溶液、水,五种溶剂在聚酰胺柱上对黄酮类化合物的洗脱能力由强到弱的顺序为________________________。 8.花色素类化合物的颜色随着____不同而改变,___呈红色,___呈紫色,__呈蓝色。 9.黄酮类化合物分子结构中,凡有______或______时,都可与多种金属试剂生成有色络合物或有色沉淀,有的还产生荧光。 10.黄酮类化合物在240-400nm 区域有两个主要吸收带,带Ⅰ在______区间,由______所引起;带Ⅱ在______之间,起因于_____引起的吸收。 四、选择题 1. 四氢硼钠是一种专属性较高的还原剂,只作用于: A. 黄酮 B. 二氢黄酮 C. 二氢黄酮醇 D. 查耳酮 2.下列化合物在聚酰胺TLC 上,以氯仿-甲醇-丁酮-丙酮(40:20:5:1)展开时,Rf 值的大小应为: O O OH OH OH O O OH OH OH O O OH OH O glc (1) (2) (3) HO rha A. ①②③ B. ③②① C. ②①③ D. ②③① 3. 下列化合物在聚酰胺柱上,用醇作溶剂洗脱时,其先后顺序应为: glcO O OH O O O O O OCH 3 OH OH glcO glcO OH O O O O O O OH OH glcO (1) (2) (3) (4) A. ①②③④ B. ③①②④ C. ①②④③ D. ②①③④ 4.下列化合物用pH 梯度法进行分离时,从EtOAc 中,用5%NaHCO 3、0.2%NaOH 、4%NaOH 的水溶液依次萃取,先后萃取出的顺序应为:
银杏叶中黄酮类化合物的含量测定
江苏畜牧兽医职业技术学院 毕业论文(设计) 专业药品质量检测技术班级药检071 学号200703123124 论文 (设计) 题目:银杏叶中黄酮类化合物的含量测定 学生姓名:刘江南 设计地点:江苏畜牧业兽医职业技术学院 指导教师:赵丽职称讲师 论文完成时间: 2010年5月20日
银杏叶中黄酮类化合物的含量测定 刘江南 药品质量检测技术 摘要:黄酮类化合物是银杏叶的主要药用成分,其黄酮含量在很大程度上决定着银杏叶的利用价值。以十二烷基硫酸钠(SDS)一正丁醇一正庚烷一水 微乳系统为流动相,预制聚酰胺薄层板为固定相,通过调节微乳系统的 极性,较好地分离出十几种银杏叶黄酮。与传统的流动相系统—有机溶 液系统相比,微乳系统显示出较强的分离优势。通过对大龄银杏叶不同 生长时期黄酮含量的测定与比较,分析银杏叶中黄酮含量随生长期的变 化规律,揭示出大龄银杏树采摘叶片的最佳时期。试验结果表明:不同 生长时期的银杏叶黄酮含量变化幅度较大,在1年中黄酮含量出现2次峰 值,8月份出现第1个峰值,黄酮含量为0.884%, 以后下降较快,10月叶 色发黄后又上升到最高值 0.977%。 关键词:银杏叶黄酮含量薄层色谱生长时期高效液相色谱 Title:In Gingko leaf flavonoid content determination Liujiangnan Drug quality testing technology Abstract:Flavonoids are the main medicinal components of ginkgo biloba,its flavonoid content to a large extent determines the value of ginkgo biloba use. Sodium dodecyl sulfate (SDS) 1-butanol 1-heptane microemulsion system of water as the mobile phase, pre-polyamide thin-layer plate as the stationary phase, by adjusting the polarity of the microemulsion system, well separated a dozen of flavonoids. Mobile phase with the traditional system - the organic solution systems, the microemulsion system showed strong separation advantage.Leaves of Ginkgo biloba on older growth and flavonoids content during the comparison, analysis of flavonoids of Ginkgo biloba in the variation with growth phase, revealing the older leaves of ginkgo trees picking the best time. The results showed that: different growth stages of the content of flavonoids in a significant reduction in 1 year in the flavonoid content of 2 times the
黄酮类化合物的生理功能
黄酮类化合物的生理功能 黄酮类化合物广泛存在于植物中,实际上存在于植物的所有部分,包括根、心材、树皮、叶、果实和花中,光全作用中约有2%的碳源被转化成类黄酮。早在30年代人们就发现了黄酮类化合物具有维生素C样的活性,曾一度被视为是维生素P。至今法国与俄罗斯仍继续称黄酮类化合物为维生素P。Pratt等人研究了黄酮类化合物的抗氧化性质,认为黄酮是作为一级抗氧化剂而起作用的,它们具有显著的抗氧化性能。黄酮抗油脂过氧化的作用早在60年代就已经被证实了。80年代以来,对黄酮类化合物的研究逐渐转向其清除自由基的能力、抗衰老及对老年病的防治功效上。 黄酮类化合物中含有消炎、抑制异常的毛细血管通透性增加及阻力下降、扩张冠状动脉、增加冠脉流量、影响血压、改变体内酶活性、改善微循环、解痉、抑菌、抗肝炎病毒、抗肿瘤具有重要生物活性的化合物,有很高的药用价值。中草药含黄酮类化合物的很多,已经证明类黄酮是许多中草药的有效成份。例如满山红中的杜鹃素、小叶枇杷中的小叶枇杷素、矮地茶中的槲皮苷、铁包金中的芦丁、白毛夏枯草和青兰中的木犀草素、红管药中的槲皮素、葛根中的黄豆苷与葛根素、毛冬青与银杏叶中的黄酮醇苷、黄芩中的抗菌成分黄芩素和解热有效成分黄芩苷等。此外,还有很多中草药富含黄酮类成分,如槐米、陈皮、射干、红花、甘草、蒲黄、枳实、芫花、金银花、菊花、山楂、淫羊藿、桎木和地锦等。除了药用价值外,其中的部分黄酮类化合物(特别是来源自药食两用的中草药)显然可应用在功能性食品。 黄酮和黄酮醇是植物界分布最广的黄酮类化合物,广泛存在于食用蔬菜及水果中,在沙棘、山楂、洋葱等中含量较高,茶叶、蜂蜜、果汁、葡萄酒中含量丰富。椐估计人体每天从食物中摄入这类物质可达1g,产生有益的生理作用。黄酮类化合物无显著毒性,大鼠对槲皮素的经口LD50为10~50g/kg ,小鼠一次口服15g/kg,观察7d无一死亡。临床病人摄取芦丁2.25g持续7d或60mg/d连续5年,均无任何副反应。在其他一系列大剂量、长时间的动物试验中,均未发现有致癌性。显性致死试验、细胞姐妹染色体试验、微核试验证明槲皮素类衍生物无致突变作用。 黄酮类化合物的生理功能可概括为: ⑴调节毛细血管的脆性与渗透性。 ⑵是一种有效的自由基清除剂,其作用仅次于维生素E。 ⑶具有金属螯合的能力,可影响酶与膜的活性。 ⑷对维生素C有增效作用,似乎有稳定人体组织内维生素C的作用。 ⑸具有抑制细菌和抗生素的作用,这种作用使普通食物抵抗传染病的能力相当高。 ⑹在两方面表现有抗癌作用,一方面是对恶性细胞的抑制(即停止或抑制细胞的增长),另一方面是从生化方面保护细胞免受致癌物的损害。 尽管对黄酮类化合物的看法尚有矛盾的方面,但它目前仍被应用来防治下列一些疾病: ⑴毛细血管的脆性和出血。 ⑵牙龈出血。 ⑶眼的视网膜内出血。
第六章-黄酮类化合物
一、填空题: 1.黄酮类化合物是泛指()的一系列化合物,其基本母核为()。 2.酮类化合物的颜色与分子中是否存在()和()有关,如色原酮本身无色,但当2位引入(),即形成()而显现出颜色。 3.一般黄酮、黄酮醇及其苷类显();查耳酮为();而二氢黄酮为()。 4.黄酮、黄酮醇分子中,如果在()位或()位引入()或()等供电子基团,能促使电子移位和重排而使化合物颜色()。 5.花色素及其苷的颜色特点是(),pH﹤7时显(),pH为8.5时显(),pH﹥8.5时显()。 6.游离黄酮类化合物一般难溶或不溶于水,易溶于()、()、()、()等有机溶剂。 7.黄芩根中的主要有效成分是(),其水解后生成的苷元是(),分子中具有()的结构,性质不稳定,易被氧化成()衍生物而显()色。 8.不同类型黄酮苷元中水溶性最大的是(),原因是();二氢黄酮的水溶性比黄酮(),原因是()。 9.黄酮类化合物结构中大多具有(),故显一定的酸
性,不同羟基取代的黄酮其酸性由强至弱的顺序为()、()、()、()。 10.黄酮类化合物γ-吡喃酮环上的()因有未共享电子对,故表现出微弱的碱性,可与强无机酸生成()。 11.具有()、()或()结构的黄酮类化合物,可与多种金属盐试剂反应生成络合物。 12.锆盐-枸橼酸反应常用于区别()和()黄酮,加入2%二氯氧锆甲醇溶液,两者均可生成黄色锆络合物,再加入2%枸橼酸甲醇溶液后,如果黄色不减褪,示有()或()黄酮;如果黄色减褪,示有()黄酮。 13.用pH梯度萃取法分离游离黄酮时,先将样品溶于乙醚,依次用碱性由()至()的碱液萃取,5%NaHCO3可萃取出(),5%Na2CO3可萃取出(),0.2%NaOH可萃取出(),4%NaOH 可萃取出()。 14.聚酰胺的吸附作用是通过聚酰胺分子上的()和黄酮类化合物分子上的()形成()而产生的。不同类型黄酮类化合物与聚酰胺的吸附力由强至弱的顺序为()、()、()、()。
黄酮类化合物提取分离纯化及其活性的研究进展
黄酮类化合物提取分离纯化及其活性的研究进展姓名常姣专业微生物学 摘要文章综述了黄酮类化合物的结构特征及提取、分离纯化技术介绍了黄酮类化合物的生物活性,并对其开发利用进行了展望。旨在为黄酮类化合物的研究、开发以及应用提供参考。 关键词黄酮;提取;分离纯化;生物活性 民以黄酮类化合物也称黄碱素, 是广泛存在于自然界的一大类化合物, 在植物体内大多与糖结合成甙的形式存在, 也有部分以游离状态的甙元存在。由于最先发现的黄酮类化合物都具有一个酮式羰基 结构, 又呈黄色或淡黄色, 故称黄酮[ 1]。 目前对天然黄酮类化合物的提取方法较多,如溶剂提取法、微波提取法、超声波提取法、酶解法、超临界流体萃取法、双水相萃取分离法及半仿生提取法等, 每种方法都有它各自的优点和点。用上述方法提取的黄酮类化合物仍然是一个混合物, 不仅是含有其它杂质的粗品, 而且是几种黄酮类成分的混合物, 需进一步分离纯化, 常用的方法有柱层析法、重结晶法、铅盐沉淀法和高效液相色谱法等。 黄酮类化合物具有降低血管脆性及异常的通透性、降血脂、降血压、抑制血小板聚集及血栓形成、抗肝脏病毒、抗炎、抗菌、解栓、抗氧化、清除自由基、抗衰老、抗癌、防癌、降血糖、镇痛和免疫等生理活性[ 2-5]。这些生理活性已被关注,对该类化合物的研究成为医药界的热门课题。人体自身不能合成黄酮类化合物而只能从食物中摄取,因此多年来科学家都在积极研究探讨从植物体中分离 纯度高、活性强的黄酮类化合物[6]。 1黄酮类化合物的理化性质 黄酮类化合物是以2-苯基色原酮为母核而衍生的一类通过三碳链相互连接而成的大多具有基本碳 架的一系列化合物,且母核上常有羟基、甲氧基、甲基、异戊烯基等助色取代基团。黄酮类化合物多为晶体固体,多数具有颜色,少数(如黄酮苷类)为无定形粉末,除二氢黄酮、二氢黄酮醇、黄烷及黄烷醇有旋光性外,其余则无旋光性) 黄酮类化合物的溶解度因结构及存在状态(苷或苷元、单糖苷、双糖苷或三糖苷)不同而有很大差异) 一般游离态苷元难溶于水,易溶于甲醇、乙醇、乙酸乙酯、乙醚等有机溶剂) 其中,黄酮、黄酮醇、查儿酮等平面型分子,因堆砌较紧密,分子间引力较大,故更难溶于水;而二氢黄酮及二氢黄酮醇等,因系非平面型分子,故排列不紧密,分子间引力降低,有利于水分子进入,水中溶解度稍大。 2黄酮类化合物的提取分离及纯化 黄酮类化合物在花、叶、果等组织中多以苷元的形式存在,而在根部坚硬组织中,则多以游离苷元形式存在。因此,不同来源、部位、种类黄酮提取所采取的方法不同[6]。分离黄酮类化合物的方法很多,根据黄酮类化合物与混入其他化合物的极性不同可采用溶剂萃取法,根据黄酮化合物在酸性水中难溶、碱性水中易溶的特点可采用碱提酸沉法等。 2.1溶剂法 2.1.1 热水提取法
(整理)黄酮类化合物-
第七章 黄酮类化合物 黄酮类化合物(flavonoids )是广泛存在于自然界的一大类化合物,大多具有颜色。这一类化合物主要存在于双子叶植物和裸子植物中,在菌类、藻类、地衣类等低等植物中较少见。此类化合物在植物体中大部分与糖结合成苷,一部分以游离状态存在。 黄酮类化合物有多方面的生物活性。例如在心血管系统方面,槐米中的芸香苷和陈皮中的橙皮苷等成分有调节血管通透性和维生素P 样作用,可用作防治高血压及动脉硬化的辅助药物;银杏中的银杏黄酮、葛根中的葛根素等成分有明显的扩张冠状动脉作用。在抗肝脏毒方面,水飞蓟素有护肝的作用,可用作治疗急慢性肝炎、肝硬化及多种中毒性肝损伤。在抗菌作用方面,黄芩中的黄芩苷、黄芩素等成分有一定程度的抗菌作用。此外,黄酮类化合物在镇咳、祛痰、解痉等方面也有一定治疗作用。因此黄酮类化合物是天然药物中的一类重要的有效成分。 第一节 黄酮类化合物的结构与分类 以前,黄酮类化合物主要是指基本母核为2-苯基色原酮类化合物,现在则是泛指两个苯环(A 环与B 环)通过中央三碳链相互连接而成,具有6C-3C-6C 基本骨架的一系列化合物。 O O O O H 1 234 5 6 78A B C 1 / 2/ 3/4/ 5/ 6/ 根据中央三碳链的氧化程度、三碳链是否成环及B 环连接位置等特点,可将黄酮类化合物进行分类(表7-1)。 色原酮(苯并-γ-吡喃酮) 2-苯基色原酮(黄酮)
黄酮类化合物多为上述基本母核的衍生物,在A环和B环上常有羟基、甲氧基、异戊烯基等取代基。组成苷的糖类常有D-葡萄糖、D-半乳糖、L-鼠李糖、L-阿拉伯糖、D-木糖及D-葡萄糖醛酸等。也有双糖和三糖,如芸香糖、龙胆二糖、龙胆三糖等。糖多结合在C3、C5、C7位,其它位置也有连接。 下面将黄酮类化合物的主要类型举例如下: 一、黄酮和黄酮醇类 基本结构: O R O R=H 黄酮R=OH 黄酮醇
黄酮类化合物
黄酮类化合物 黄酮类化合物是自然界存在的最大类别的酚类化合物之一,它广泛存在于植物的各个部位,尤其是花叶部位,主要存在于芸香科、唇形科、豆科、伞形科、银杏科、与菊科等。有文献记载约有20%药中含有黄酮类化合物,可见其资源之丰富。许多研究已表明黄酮类化合物具有多种生物活性,除利用其抗菌、消炎、抗突变、降压、清热解毒、镇静、利尿等f乍佣外,在抗氧化、抗癌、防癌、抑制脂肪氧化酶等方面也有显著效果。他是大多数氧自由基的清除剂,因而能提高SOD(过氧化物歧化酶)的活力,减少MDA(脂质过氧化物丙二醛)及OX —LDL(氧化低密度脂蛋白)的生成。他可以增加冠脉流量:对实验性心肌梗塞有对抗作用,对急性心肌缺血有保护作用,对治疗冠心病、心绞痛、高血压等有显著效果,对降低舒张压,防治心律失常、心血管病和活血化瘀也起重要作用。由于黄酮类化合物的这些生物活性使他的研究进入了—个新的阶段,掀起了黄酮类化合物研究、开发;f0用热潮,促使其在化妆品、医药、食品等工业中有广泛的应用。目前发现的黄酮类化合物已达5000多种,但研究亦发现,在这众多的黄酮类化合物中却因其结构的不同,有的表现出生物活性,有的却没有生物活性,而且生物活性亦因其结构的差异而不同。所以提取分离出具有较高生物活性的黄酮类化合物对医药及食品工业是十分重要的。 一、国内外研究现状 邢秀芳研究了纤维素酶在葛根总黄酮提取中的应用,结果显示在纤维素的作用下,葛根总黄酮的收率提高了130/0。廖亮研究了银杏叶中总黄酮提取方法结果表明乙醇提取较好。方桂珍正交实验研究仙鹤草中总黄酮的提取工艺,考察浸提液浓度、浸提温度、浸提时间、浸提次数、液科比等5个因素对f山鹤草总黄酮含量的影响,确立了仙鹤草总黄酮最佳提取条件为:浸提液体积分数40%,液料比10:1,浸提温度7d℃,回流提取3次,每次0.5h。 高红宁采用紫外分光光度法测定苦参中总黄酮的含量,研究大孔树脂AB一8对苦参总黄酮的吸附性能及原液浓度、pH、流速、洗脱剂的种类对树脂吸附性的影响,结果表明原液浓度为0285mg/ml,pH值为4,流速为3BVm洗脱剂用50%乙醇时,AB一8树脂,吸效果较好。康纯研究了微乳薄层色谱对黄酮类层分分离鉴定,以6种SDS一正丁醇一正庚烷一水徽乳液作为展开剂,通过聚酰胺薄层层析,分离和检测14种中药材、饮片及中成
黄酮类化合物练习题答案
黄酮类化合物练习题 参考答案 一、选择题 (一)单项选择题 1.D 2.D 3.A 4.B 5.C 6.D 7.D 8.A 9.B 10.B 11.E 12.D 13.B 14.E 15.E 16.D 17.B 18.C 19.A 20.B 21.B 22.E 23.C 24.B 25.C 26.A 27.B 28.A 29.A 30.C (二)多项选择题 1.BDE 2.ABCDE 3.ABDE 4.ABD 5.AE 6.ABD 二、名词解释 1.黄酮类化合物:指两个苯环(A环和B环)通过中间三碳链相互联结而成的(6C-3C-6C)一系列化合物。 2.碱提取酸沉淀法:利用某些具有一定酸性的亲脂性成分,在碱液中能够溶解,加酸后又沉淀析出的性质,进行此类成分的提取和分离。 三、填空题 1.2-苯基色原酮;三碳链;6C-3C-6C。 2.2位引入苯基;灰黄色至黄色;黄色至橙黄色;交叉共轭体系。 3.交叉共轭体系;助色团;助色团;加深;7以下;8.5左右;>8.5。 4.甲醇;乙醇;醋酸乙酯;乙醚;亲水性(水溶性);亲水性;亲脂性;酚羟基。 5.7,4/-二羟基;7或4/ 羟基-;一般酚羟基;C5-OH;C4位羰基;ρ~π共轭效应;分子内氢键。 6.橙红色至紫红;异黄酮;查耳酮;四氢硼钠(钾);紫色至紫红色。 7.C3 、、C5-羟基;邻二酚羟基;配合物;沉淀。 8.C3;C5;鲜黄色;C5-OH黄酮;C3-OH黄酮。 9.花;叶;果实;苷;苷元。 10.溶剂提取;碱提取酸沉淀;叶绿素;油脂;色素;蛋白质;多糖。 11.活性炭吸附;pH梯度萃取;聚酰胺色谱。 12.酰胺基;游离酚羟基;氢键缔合;羟基数目和位置;水和醇;异黄酮;二氢黄酮;黄酮;黄酮醇。 13.芦丁;槲皮素;芸香糖;1:10000;1:200;1:300;1:30。 14.离子型,非平面。 四、鉴别题 1. 颜色不褪颜色减褪
常见食用豆类中黄酮类化合物含量的测定
2009年7月 第24卷第7期 中国粮油学报 JournaloftheChineseCerealsandOilsAssociation V01.24.No.7 Jul.2009 常见食用豆类中黄酮类化合物含量的测定 任顺成王鹏王国良马宇翔陈丽兰 (河南工业大学粮油食品学院,郑州450052) 摘要以芦丁为标样应用氯化铝显色法、硝酸铝显色法分别测定15种常见食用豆类中的黄酮类化合物总含量,以染料木素做为标样应用直接比色法测定其中食用豆类样品中异黄酮的总含量,利用高压液相色谱法测定常见食用豆类中的4种大豆异黄酮单体成分的含量。结果表明:使用氯化铝显色法进行测定,赤豆、绿豆等7种食用豆类显示合有黄酮类化合物,并且含量最多的赤豆为0.501mg/g。硝酸铝显色法测定豆类样品黄酮类总合量为0.297~8.844mg/g。直接比色法测定食用豆类中异黄酮总含量为1.994—8.840mg/g。高压液相色谱法测定4种大豆异黄酮单体成分的总含量为0.031~3.345mg/g。 关键词食用豆类黄酮类异黄酮比色法高压液相色谱 中图分类号:TS214文献标识码:A文章编号:1003—0174(2009)07—0132—06 食用豆类是以收获籽粒兼做蔬菜供人类食用的豆科作物的统称。食用豆类不仅是重要的粮食资源之一,而且具有很高的营养价值。食用豆类中除含有丰富的油脂和优质蛋白以外,还含有多种生物活性物质,其中含有多种维生素,矿物质以及黄酮类化合物[1|。 黄酮类又称生物类黄酮,为植物多酚类的代谢物,是广泛存在于自然界的一大类化合物,大多有颜色。黄酮类化合物具有抗炎、抗菌、抗病毒、抗氧化、抗衰老、抗骨质疏松、抗肿瘤等多种生物活性,是重要的食品添加剂和营养强化剂…2。其中大豆异黄酮作为黄酮类化合物中的异黄酮成分,其分子结构骨架是3一苯色原酮,目前发现的大豆异黄酮主要有12种,分为三大类,即大豆苷类(DaidzinGroups)、染料木苷类(GenistinGroups)、大豆黄素苷类(GlycitinGroups),以游离型、葡萄糖苷型、乙酰基葡萄糖苷型、丙二酰基葡萄糖苷型等4种形式存在,其中游离型占总量的2%一3%[31。大豆异黄酮具有明显的抗氧化作用,药理学研究表明大豆异黄酮可作为雌性激素治疗替代品,能改善妇女更年期综合症,并有效降低血胆固醉含量,防止骨质疏松及抑制癌细胞增长等[4|。 采用氯化铝显色法、硝酸铝显色法分别测定了 收稿日期:2008—07—08 作者简介:任顺成,男,1963年出生,副教授,博士,硕士生导师,天然活性成分及其功能评价15种常见食用豆类中的黄酮类化合物总含量,应用直接测定法测定食用豆类中异黄酮的总含量,利用高压液相色谱法对样品中的4种大豆异黄酮单体含量进行了测定。为评价食用豆类的保健功能以及为优良品种的选育、栽培提供参考。 1材料与方法 1.1材料与仪器 大豆、黑小豆、绿大豆、黑大豆、蚕豆、绿豆、红小豆、刀豆、芸豆、饭豆、麻豇豆、豌豆、花豇豆、小扁豆和鹰嘴豆:市售。’ 芦丁标样:分析纯,上海华硕精细化学品有限公司;大豆苷、大豆苷元、染料木苷、染料木素:标样,纯度i>98%,美国signa公司。 WFZUV一2000型紫外分光光度仪:尤尼卡(上海)仪器有限公司;LC卜10At、,p型高效液相色谱仪、sP卜10Avvp型紫外检测器、scL_10A、rp型系统控制器、CTO--10Asvp型柱温箱:日本岛津公司。 1.2试验方法 1.2.1食用豆类中黄酮类化合物的提取 将食用豆类样品粉碎,过40目筛,以石油醚在65℃温度下回流脱脂1h,抽滤后放在50℃左右的烘箱里干燥,备用。准确称取脱酯豆粉5.0g,用75%的乙醇,以1 g 5mL的料液比,在60℃温度下,浸提2h,冷却后,用循环水式真空泵进行抽滤,最后再用中速滤纸过滤,得到澄清的提取液,定容在 万方数据
