2.2芳香烃学案

第二章第二节芳香烃
学习目标:
1、掌握苯的分子结构特点。
2、了解芳香烃、芳香族化合物的概念。
3、掌握苯的物理性质和化学性质。
4、掌握苯的同系物与苯在结构和性质上的异同点。
一、苯的结构与性质
3、化学性质
(1)氧化反应(燃烧)
苯燃烧时的现象是。
化学方程式:。
(2)氧化反应
苯(填能或不能)使溴水和酸性高锰酸钾溶液褪色。
(3)取代反应
苯可以发生取代反应,苯环上的H原子被其他原子(如卤素原子)、原子团(如硝基)所取代,类似于甲烷。苯与溴的取代反应,需要在催化剂三溴化铁作用下进行,生成了苯的一溴取代物——溴苯,还有溴化氢。
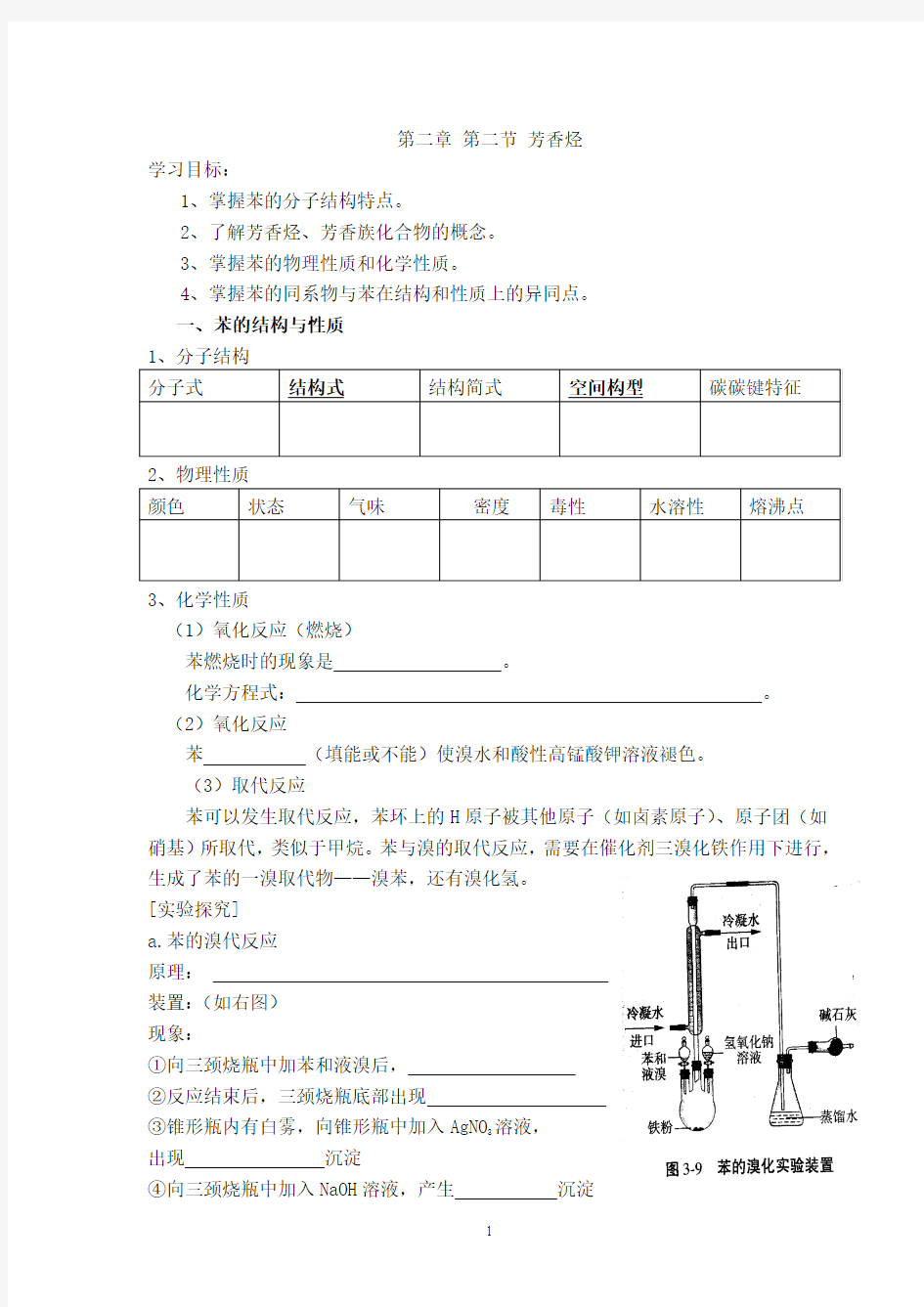
[实验探究]
a.苯的溴代反应
原理:
装置:(如右图)
现象:
①向三颈烧瓶中加苯和液溴后,
②反应结束后,三颈烧瓶底部出现
溶液,
③锥形瓶内有白雾,向锥形瓶中加入AgNO
3
出现沉淀
④向三颈烧瓶中加入NaOH溶液,产生沉淀
注意:
①直型冷凝管的作用:
(HBr 和少量溴蒸气能通过)。
②锥形瓶的作用:
③锥形瓶内导管为什么不伸入水面以下:
④碱石灰的作用: 。
⑤纯净的溴苯应为无色,为什么反应制得的溴苯为褐色: ⑥NaOH 溶液的作用: ⑦最后产生的红褐色沉淀是什么: ,反应中真正起催化作用的是 b.苯的硝化反应:
原理:
装置:(如右图)
现象:加热一段时间后,反应完毕,将混合物倒入盛
有水的烧杯中,在烧杯底部出现
注意:
①硝基苯 溶于水,密度比水 ,有 味
②长导管的作用:
③为什么要水浴加热:
(1) ;
(2) ; ④温度计如何放置:
(4)苯的加成反应
在比较苛刻的条件下,苯也可以发生加成反应。例如,在镍催化剂、加热条件下,苯可以加氢生成环己烷。
化学方程式:
二、苯的同系物
(1)概念
苯的同系物只有一个苯环,它们可以看成是由苯环上的H 被 代替而得到的。 例如:
甲苯 乙苯
苯的同系物的通式:
概念辩析:请用圆形图方式表示芳香化合物、芳香烃、笨的同系物三者的包含关系。
(2)性质 CH 3 CH 2CH 3
①相似性:
A.都能燃烧,产生明亮火焰、冒浓黑烟。
B.都能和X
2、HNO
3
等发生反应。
甲苯与浓硝酸的反应:
2,4,6---三硝基甲苯(TNT)是一种溶于水的色针状晶体,烈性炸药。
C.都能与H
2
发生加成反应。
D.苯及其同系物一般不与溴水反应,但能对溴水进行而令溴水层褪色。
②不同点:
A.侧链对苯环的影响
使苯环侧链位上的氢原子容易被取代,如甲苯发生硝化反应生成三硝基甲苯,而苯一般只生成一硝基苯。
B.苯环对侧链的影响
实验:甲苯中加入酸性KMnO
4
溶液,现象
乙苯中加入酸性KMnO
4
溶液,现象
结论:由于苯环和烷基的相互作用,导致苯的同系物性质比苯更加。若与苯
环直接相连的碳原子上连有氢原子,则该苯的同系物就能够使酸性KMnO
4
溶液,与苯环直接相连的烷基通常被氧化为;若发生
取代反应,则苯环侧链位上的氢原子容易被取代。
三、芳香烃的来源和用途
芳香烃,包括苯、甲苯、乙苯、二甲苯等含有一个苯环的有机物,也包括含有多个苯环的联苯、萘、蒽、菲等稠环芳香烃,一些常见的稠环芳香烃的分子结构见下图:
苯萘分子蒽分子菲分子
1、芳香烃的来源
苯等芳香烃最早是从中发现,当时几乎是芳香烃的唯一来源,直到人们发现了石油化学工业中的工艺。现在,石油来源的芳香烃,占了芳香烃产量的绝大部分。
2、芳香烃的用途
芳香烃被广泛用来做有机原料,可用来
(包括合成纤维)等。家庭装修时涂墙的涂料,经常含有苯、甲醛等有害物,需要通风至这些有害物完全挥发之后,方可入住。
〖课后练习〗
一、选择题(每小题只有1个选项符合题意)
1.下列事实不能说明苯分子中不存在单双键交替出现的结构的是()
A.苯分子中的6个碳碳双键的键长均相同,且长度介于单键和双键之间
B.苯的二氯代物只有三种同分异构
C.苯不能使溴的CCl
4
溶液褪色
D.苯的1H核磁共振谱图中只有一个峰
2.下列对于苯的叙述正确的是()
A.易被强氧化剂KMnO
4
等氧化
B.属于不饱和烃易发生加成反应
C.属于不饱和烃但比较易发生取代反应
D.苯是一种重要的有机溶剂可广泛应用于生产绿色油漆等
3.下列关于苯及其同系物的说法中,正确的是()
A.苯及其同系物可以含有1个苯环,也可以含有多个苯环
B.苯及其同系物都能溴水发生取代反应
C.苯及其同系物都能氯气发生取代反应
D.苯及其同系物都能被酸性KMnO
4
溶液氧化
4.要鉴别己烯中是否混有少量甲苯,最恰当的实验方法是()
A.先加足量的酸性高锰酸钾溶液,然后再加入溴水
B.先加适量溴水,然后再加入酸性高锰酸钾溶液
C.点燃这种液体,然后再观察火焰是否有浓烟
D.加入浓硫酸与浓硝酸后加热
5.下列各组物质互为同系物的是()
A.苯和乙炔 B.甲苯和二甲苯 C.硝基苯和三硝基甲苯 D.乙烯和丁二烯
6.某芳香族化合物的分子式为C
8H
6
O
2
,它的分子(除苯环外不含其它环)中不可能有
()
A.两个羟基 B.一个醛基 C.两个醛基 D.一个羧基
7.用相对分子子质量为43的烷基取代甲苯苯环上的一个氢原子最多可得到取代产物()
A.3种 B.4种 C.5种 D.6种
8.将112mL乙炔溶于2mol苯中,再加入30g苯乙烯,所得混合物的含碳的质量分数 A、75% B、66.75 C、92.3% D、不能确定
9.用分液漏斗可以分离的一组液体混合物是()
A.溴和苯 B.苯和溴苯 C.水和硝基苯 D.苯和汽油
二、选择题(每小题有2个选项符合题意)
10.下列物质中,既能与氢气在一定条件下加成,又能使酸性高锰酸钾溶液褪色,且属于芳香烃的是()
A.苯 B.甲苯 C.苯乙烯 D.2—甲基—1,3—丁二烯11.有关 CHF
2
≡C-CH
3
分子结构的下列叙述中,正确的是()A.除苯环外的其余碳原子有可能共直线; B.12个碳原子不可能共平面;
C.除苯环外的其余碳原子不可能共直线; D.12个碳原子有可能共平面。三、非选择题
12.下列物质中,属于芳香族化合物的是,属于芳香烃的
是,属于苯的同系物的是。(填编号)
E F G
13.“立方烷”是一种新合成的烃,其分子为正立方体结构,其碳架结构如右图所示(碳、氢原子未画出,每个折点代表一个碳原子)。请回答:
(1)该“立方烷”的分子式为
(2)该“立方烷”的二氯取代物有种同分异构体;芳香
烃中有一种化合物与“立方烷”互为同分异构体,则该芳香烃的结构简式为
(3)“立方烷”可能发生的反应或变化有(从A、B、C、D中选择)
A.可使Br
2
水褪色,但不反应 B.不能使Br
2
的CCl
4
溶液褪色C.能发生取代反应 D.能发生加成反应
14.乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成不同的化合物,如图所示。
完成下列各题:
(1)正四面体烷的分子式为____________,其二氯取代产物有_________种。
(2)关于乙烯基乙炔分子的说法错误的是
A.能使KMnO4酸性溶液褪色
正四面体烷
乙烯基乙炔
苯
CH≡C-CH=CH2
OH CH CH2CH
3
CH2CH3
CH3
A B C D
CH CH3
CH3
B.1 mol 乙烯基乙炔能与3 mol Br2 发生加成反应
C.乙烯基乙炔分子内含有两种官能团
D.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式________。(4)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例)。
芳香烃时
第二章第一节芳香烃(第二课时) 高二姓名日期:2014-1-8编号:编制人:王志省审核人 一、【教学目标】掌握苯的同系物的化学性质尤其为取代和加成反应。 二、【学法指导】1、内容:课本P38-P39 2、学法:参考课本及相关资 料。 三、【展示课导学】 合作 探究 环节 展示提 升质疑 评价环节 总结归纳环节 互动 策 展示方 案 随堂笔记 (成果记录·知识生成·同步演练) 一、苯的同系物 1、概念:苯环上的氢原子被取代后的产物 2、结构特点:分子中只有个苯环,侧链都是(即碳碳键全部是 单键) 3.通式:;物理性质与苯相似 4、苯的同系物的同分异构现象 书写苯的同系物的同分异构体时,苯环不变,变换取代基的位置及取代基碳链的长短。 例如C 8 H 10 对应的苯的同系物有4个同分异构体,分别为、、、 二、苯的同系物化学性质 1、氧化反应 ①苯不能被KMnO 4 酸性溶液氧化,甲苯、二甲苯等苯的同系物(填“能”或“不能”) 被KMnO 4 酸性溶液氧化。可利用此性质区分苯和苯的同系物。故含有结构的物质,可使酸性溶液褪色,被氧化成。 ②苯的同系物均能燃烧,现象是,反应的化学方程式为: 2、取代反应 甲苯与浓硝酸和浓硫酸的混合物在一定条件下发生反应生成三硝基甲苯的化学方程式为:。 三硝基甲苯的系统命名为,又叫(TNT), 色,溶于水,是一种烈性炸药 —C— | H |
R COOH COOH 通过这个反应可以说明_______(基团)受_______(基团)的影响,使其某些位置变得更加活泼。 (拓展)苯的同系物发生取代反应的位置与反应条件有很大的关系,联系前面所学的知识判断下列两个反应的发生各需要什么条件: ─CH 3 + Br 2 ①─CH 2 Br + HBr ①:________ ─CH 3 + Br 2 ②─CH 3 + HBr ②:________ 3、加成反应 甲苯在一定条件下也可与氢气发生苯环的加成反应:_________________________ (思考)受甲基的影响,苯环是不是可以像烯、炔烃一样可与溴水发生加成反应呢观察甲苯和溴水混合时的现象。 三、芳香烃的来源及应用 1、芳香烃 房子内含有一个或多个的烃,由2个或2个以上的苯环而成的芳香烃称为稠环芳香烃,如萘:蒽: 2、来源:1845年至20世纪40年代是芳香烃的主要来源,自20世纪40年代后,随着石油化工的发展,通过获得芳香烃。 【训练课导学】“日清过关”巩固提升三级达标训练题 书写等级得分批阅日期 1.下列物质中属于苯的同系物的是( ) 2.下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是( ) A.甲苯与硝酸反应生成三硝基甲苯 B.甲苯能使酸性高锰酸钾溶液褪色 C.甲苯燃烧产生带浓烟的火焰 D.1 mol甲苯与3 mol H 2 发生加成反应 3.在苯的同系物中加入少量的酸性KMnO 4 溶液,振荡后褪色,正确的解释为( ) A.苯的同系物分子中的碳原子数比苯分子中的碳原子数多 B.苯环受侧链影响易被氧化 C.侧链受苯环影响易被氧化 D.由于苯环和侧链的相互影响均易被氧化 4.在下列有机物中,能跟溴水发生加成反应,又能被酸性高锰酸钾溶液氧化的是()A.乙烯 B.苯 C.乙烷 D.甲苯 5.烷基取代苯可以被酸性高锰酸钾溶液氧化生成,但若烷基R中直接与苯环连接的碳原子没 有C-H键,则不容易被氧化得到现有分子式是C 11 H 16 的烷基取代苯。已知它可以被氧化成为
专题3常见的烃芳香烃第1课时练习答案
O 专题3常见的烃第二单元芳香烃 1苯的结构与性质1 1 .下列说法正确的是 A .芳香烃就是指苯和苯的同系物 C .含有一个苯环的化合物一定属于芳香烃 [参考答案]D 2 .下列烃完全燃烧后的产物 CO 2和H 2O 的物质的量之比为2 : 1的是 A .乙烷 B .乙烯 C .乙炔 D .苯 [参考答案]C 、D 3 .以下叙述中,科学家与其重大发现相符合的是 A .凯库勤提出苯分子结构学说 B .拉瓦锡发现氮气 C .道尔顿首先提出分子的概念 D .阿伏加德罗提出近代原子学说 [参考答案]A 4.苯环结构中,不存在单双键交替结构,可以作为证据的事实是 ①苯不能使KMnO 4 ( H + )溶液褪色②苯中碳碳键的键长均相等③苯能在加热和催化剂存 在的条件下跟 H 2加成生成环己烷④经实验测得邻二甲苯仅一种结构⑤苯在 FeBr 3存在的 条件下同液溴可发生取代反应,但不因化学变化而使溴水褪色 A .②③④⑤ B .①③④⑤ C .①②④⑤ [参考答案]C 5 .下列事实中,能说明苯与一般烯烃在性质上有很大差别的是 A .苯不跟溴水反应 B .苯不跟酸性 KMnO 4溶液反应 C . 1mol 苯能与3mol H 2进行加成反应 D .苯是非极性分子 [参考答案]A 、B 6. ( 2004年?上海高考? 28)人们对苯的认识有一个不断深化的过程。 (1) 1834年德国科学家米希尔里希,通过蒸馏安息香酸( 液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式 (2)由于苯的含碳量与乙炔相同, 人们认为它是一种不饱和烃, 写出C 6H 6的一种含三键且无 。苯不能使溴水褪色,性质类 似烷烃,任写一个苯发生取代反应的化学方程式 (3)烷烃中脱去2 mol 氢原子形成I mol 双键要吸热。但1, 3 一环己二烯( 氢原子变成苯却放热,可推断苯比 1, 3 一环己二烯 _______ (填"稳定”或"不稳定” (4) 1866年凯库勒(下图)提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分 性质,但还有一些问题尚未解决,它不能解释下列 _________________ 事实(填入编号)。 a .苯不能使溴水褪色 b .苯能与H 2发生加成反应 c .溴苯没有同分异构体 d .邻二溴苯只有一种 B .芳香烃的通式是 C n H 2n -6(n 》6) D .苯是结构最简单的芳香烃 D .①②③④ 支链链烃的结构简式 00H )和石灰的混合物得到 脱去2 mol
高考化学 总复习学案45 芳香烃煤
[考纲要求] 1.以苯为例,了解芳香烃的基本结构。2.掌握芳香烃中各种碳碳键、碳氢键的性质和主要化学反应。3.了解煤、石油、天然气等资源的综合利用。 知识点一 苯的结构和性质 1.苯的结构和芳香烃 苯的分子式为C 6H 6,结构简式为____________或____________,苯分子具有__结构,键与键的夹角为________;苯分子中不存在一般的碳碳双键,6个碳原子之间的键长、键能相等,是一种介于单键和双键之间的独特的键,分子里含有一个或多个苯环的碳氢化合物,属于芳香烃,苯是最简单的芳香烃。 2.苯的性质 (1)物理性质 苯为无色、有____________的液体,有毒,________溶于水,密度比水________,熔点仅为5.5℃。 (2)苯分子的特殊结构决定了苯兼有烷烃和烯烃的化学性质,即易取代,能加成,难氧化。 ①取代反应 卤代反应: _____________________________________________________________; 硝化反应:______________________________________________________________ ________________________________________________________________________; 磺化反应:_____________________________________________________________。 ②加成反应:___________________________________________________________。 ③氧化反应:C 6H 6+152 O 2――→点燃6CO 2+3H 2O ,苯不能使酸性KMnO 4溶液褪色。 3.苯的同系物的性质 由于苯环受烃基的影响,使苯与苯的同系物有所不同。 (1)氧化反应:燃烧通式:_____________________________________,苯的同系物分子中的烃基一般可以被酸性KMnO 4溶液氧化为羧基。 (2)取代反应 知识点二 煤、石油、天然气的综合利用 1.煤的综合利用 煤是由________和少量________组成的____________,主要含有________元素,还含有少量__________、________、________、________等元素。
芳香烃练习题含答案
第二单元芳香烃 基础题组 1.已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如图: , 则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为( ) A .2种种 C. 4种 D. 6种 答案.C 解析:要推算硼氮苯的二氯取代物数目,其方法是将二个Cl原子“定一、移一”,首先将一个Cl原子定在B原子上,移动另一个Cl原子,得3种结构;再将一个Cl原子定在N原子上,移动另一个Cl原子,也得3种结构,其中有两种(另一个Cl原子在B上的)与前面重复,故只有4种。 故可用酸性高锰酸钾溶液或溴水鉴别这3种液体。 2.要鉴别己烯中是否混有少量甲苯,正确的实验方法是 () A.先加足量的酸性高锰酸钾溶液,然后再加入溴水 B.先加足量溴水,然后再加入酸性高锰酸钾溶液
C.点燃这种液体,然后再观察火焰的颜色 D.加入浓硫酸与浓硝酸后加热 答案B 解析:先将己烯加成,再氧化甲苯进行检验,防止己烯被氧化造成干扰。 3.(双选)可用来鉴别己烯、四氯化碳、苯的方法是() A.酸性高锰酸钾溶液 B.溴水 C.液溴溶液 答案.AB 解析:使酸性高锰酸钾溶液褪色的是己烯;不褪色,分层后无色油状物在上层的是苯,分层后无色油状物在下层的是四氯化碳。使溴水褪色的是己烯;分层后下层有色的是四氯化碳,分层后上层有色的是苯。 4.(双选)在实验室中,下列除去杂质的方法正确的是() A.溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出溴 B.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷 C.硝基苯中混有浓HNO3和H2SO4,将其倒入NaOH溶液中,振荡、静置、分液 D.乙烯中混有SO2,将其通入NaOH溶液中洗气 答案.CD 解析:选项A中生成了新杂质碘,选项A错误;用乙烯和氢气加成
高二化学《芳香烃》教案
高二化学《芳香烃》教案 教学目标 使学生掌握苯的重要化学性质; 使学生了解苯的同系物在组成、结构、性质上的异同,理解共价单键的可旋转性。 以甲苯为例,让学生了解苯的同系物的某些化学性质。 教学重点 苯的化学性质 教学难点 苯的化学性质 课时安排 课时 教学用具 黑板、粉笔、多媒体 教学方法 师生互动、探究学习 教学过程 [复习]: 填写下表: 苯的分子式 结构式
结构简式 空间构型 键参数 苯分子有怎样的结构特点? 苯分子里6个碳原子之间的键完全相同,是一种介于单键和双键之间的独特的键。苯分子是平面结构,键与键之间夹角为120°,常用结构式芳香烃教学设计来表示苯分子。苯是非极性分子。 [过渡]:分子里含有一个或多个苯环的碳氢化合物叫做芳香烃,简称芳烃。苯是最简单、最基本的芳烃。我们已经了解了苯的分子结构,那它的性质又如何呢? [实验1]:展示苯的实物,让学生直接观察苯的颜色和状态。将苯与水混合于试管,振荡、静置后观察现象,认识苯的溶解性. 一.苯的物理性质: 无色、有特殊气味的液体,比水轻,不溶于水,沸点80.1℃,熔点5.5℃。 二.苯的化学性质。 苯既不能使酸性高锰酸钾溶液褪色,也不能使溴水褪色。说明苯的化学性质比较稳定,但在一定条件下苯也能发生化学反应。 [实验2]:纸上蘸取少量苯溶液,点燃.观察实验现象.
氧化反应 c6H6+15o2芳香烃教学设计12co2+6H2o火焰明亮,有黑烟. 常用的氧化剂如no4、2cr2o7、稀硝酸等都不能使苯氧化。这说明苯环是相当稳定的。 取代反应 苯跟卤素的反应。 [实验3]:苯与溴的反应。 ①.原料:苯、液溴、铁粉。 ②.反应原理: 芳香烃教学设计芳香烃教学设计Br +Br2芳香烃教学设计+HBr 芳香烃教学设计③.装置原理: a.长导管的作用是什么?。 芳香烃教学设计b.锥形瓶中水的作用是什么?。 c.为什么导管末端不能插入液面以下?。 ④.操作顺序:圆底烧瓶中先加入少量苯、液溴,然后加入铁粉,塞紧橡皮塞。反应结束后向锥形瓶中滴入硝酸银溶液,并将烧瓶中的液体倒入盛有水的烧杯中。 ⑤.实验现象: a.烧瓶中混合物沸腾; b.导管口出现白雾;
人教版高二化学选修五 22 芳香烃导学案
高二化学导学案:编号:使用时间: 班级:小组:姓名:组内评价:教师评价: 第二章第2节芳香烃 编制人:李百禄审核人:领导签字: 【学习目标】1.了解苯的结构和性质。 2.掌握苯及苯的同系物的结构特点和化学性质。 3.简单了解芳香烃的来源及其应用。 【重点难点】苯的同系物的结构特点和化学性质。 自主学习 一、芳香烃的来源及应用 1.什么是芳香烃:最简单的是: 例举见过的芳香烃:(阅读39页资料卡片) 2.芳香烃的来源和应用(阅读课本39页三) 来源: 应用: 思考:稠环芳香烃萘、蒽是否是苯的同系物? 二、苯的结构和性质 1.苯的分子结构
物理性质2. 3.化学性质 三、苯的同系物
1.苯的同系物的组成和结构 苯的同系物是苯环上的氢原子被取代的产物,其分子中只有一个苯环,侧 链都是烷基。 2.苯的同系物的化学性质 合作探究 烃的检验一、1.苯能否使溴水褪色?原因是什么?烯烃和炔烃能使溴水褪色,其原理是什么? 2.如何鉴别苯和甲苯? 4
溴、溴水、溴的四氯化碳溶液、光照、催化剂等)对反应的影响。 二、根据苯与溴、浓硝酸反应发生的条件,请设计制备溴苯和硝基苯实验方案实验仪器: 实验药品: 实验步骤: 反应装置: 反应现象: 探究: (一)关于制备溴苯的实验 1、铁粉的作用? 2、长导管的作用 3、为什么导管的末端不插入液面下? 4、哪些现象说明发生了取代反应而不是加成反应? 5、纯净的溴苯是无色的液体,为什么反应生成所看到的是褐色的?如何恢复其本来的面目? (二)关于制备硝基苯的实验 1.配制浓硫酸与浓硝酸混和酸时,是否可以将浓硝酸加入到浓硫酸中?为什么? 2.为了使反应在50-60℃下进行,常用的方法是什么? 3洗涤、分离粗硝基苯使用的主要仪器是什么?
2019 2020年苏教版选修5 专题3第二单元 芳香烃 作业
第二单元芳香烃 一、选择题 1.下列叙述中,错误的是 ( ) A.苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯 B.苯乙烯在合适条件下催化加氢可生成乙基环己烷 C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 【解析】选D。苯与浓硝酸、浓硫酸共热并保持55~60℃水浴加热发生取代反应生成硝基苯,其中浓硫酸起催化剂和吸水剂的作用,A项正确;苯乙烯中的碳碳双键和苯环都可以和氢气发生加成反应,故在合适条件下催化加氢可生成乙基环己烷,B项正确;乙烯可以与溴的四氯化碳溶液发生加成反应,碳碳双键断开分别加溴原子,生成1,2-二溴乙烷,C项正确;甲苯与氯气在光照下应该发生甲基上的取代反应,不是生成2,4-二氯甲苯,D项错误。 2.(双选)下列各组物质中,能用酸性高锰酸钾溶液鉴别的是 ( ) A.乙烯,乙炔 B.甲烷,苯 D. 苯,溴苯乙烯,苯C. 【解析】选C、D。A项,均使酸性高锰酸钾溶液褪色,现象相同,不能鉴别,错误;B项,均不与酸性高锰酸钾反应,现象相同,不能鉴别,错误;C项,乙烯使酸性高锰酸钾溶液褪色,而苯不能,现象不同,可鉴别,正确;D项,均不与酸性高锰酸钾溶液反应,均出现分层,但苯的密度比水小,溴苯的密度比水大,现象不同,可鉴别,正确。 乙苯的结构简式为3.,它的侧链具有烷烃的性质。下列关于它的性质的叙述) ( 中不正确的是 在光照条件下,它可以与氯气发生取代反应A. 它可以和溴水发生加成反应而使溴水褪色B. H 它的分子式为CC.108 H发生加成反应D.在一定条件下,它可以与2选项正确;ACHCH上的氢原子可以被氯气中的氯原子取代,B【解析】选。光照时,侧链—32 但是可以和溴水发生萃取而不能与溴水发生加成反应,≡C—,C乙苯分子中不含和—乙苯中相当于有1 mol选项错误;B使溴水层褪色, 发生加成反应生成,D选项正确。 3 mol,最多可以和3 mol H2【互动探究】(1)乙苯的一氯代物有几种? 提示:乙苯分子中含有5种不同化学环境的氢原子(如下图所示),所以其一氯代物有5种。
芳香烃导学案
第二节 芳香烃(导学案) 学习目标:1.掌握苯和苯的同系物的结构及化学性质; 2.了解芳香烃的来源及其使用 3.归纳、比较法:归纳比较苯和脂肪烃及苯的同系物的结构和性质 学习重难点:苯和苯的同系物的结构、性质差异 一、 苯的结构和性质 1、苯的结构:分子式 探究一: 苯分子的结构是怎样的呢? ① 苯分子结构的确定经历了漫长的历史过程,1866年,德国化学家凯库勒提出苯环结构, 称为凯库勒式: 那么凯库勒式能完全真实的反应苯分子的结构吗? 根据以下信息,谈谈你对苯分子结构的认识? ② 苯的一取代物只有一种,邻位二取代物只有一种 和 是同一种物质 ③ 苯不能使溴水腿色,不能使酸性高锰酸钾溶液腿色 说明苯环中 存在单双键交替的结构,因此凯库勒式不能全面的反应苯的结构,只是习 惯上沿用至今。 苯分子中碳碳键的键长 ,介于 和 之间 这说明碳原子之间形成的一种 的特殊共价键。所以苯的结构简式可 以表示为 或 ,空间结构:苯分子中6个碳原子和6个氢原子 ,形 成 ,键角 为120° 。 2、苯的物理性质 苯是 色,带有 气味的有 的液体,密度比水 3、苯的化学性质 (1)取代反应 ①苯和溴的反应 反应的化学方程式为: 1.长直导管b 的作用——使 冷凝回流和 (HBr 和少量溴蒸气能通过)。 Cl Cl Cl
2 锥形瓶的作用——吸收,所以加入AgNO3溶液,出现浅黄色沉淀(AgBr) 3 锥形瓶内导管为什么不伸入水面以下——防止 4 碱石灰的作用——吸收、蒸气、蒸汽。 5 纯净的溴苯应为无色,为什么反应制得的溴苯为褐色——溴苯中溶解的 6 NaOH溶液的作用——除去溴苯中的,然后过滤、再用分离,可制得较为纯净的溴苯 7 反应中真正起催化作用的是 ②苯的硝化反应 苯和和的混合物共热至50℃——60℃反应的化学方程式为: 注意:1 硝基苯溶于水,密度比水,有味 2 长导管的作用—— 3 为什么要水浴加热?(1)(2)便于控制温度,防止生成副产物(因为加热到100~110℃时就会有间二硝基苯生成;) (2)苯的加成反应 在特定的条件下,苯和氢气发生加成反应的化学方程式为: (3)苯的氧化反应 苯在空气中燃烧产生,说明苯的含碳量很高,燃烧的化学方程式为:;苯(填“能”或“不能”)使KmnO4酸性溶液褪色。 二、苯的同系物 1、概念:苯环上的氢原子被取代后的产物 2、结构特点:分子中只有个苯环,侧链都是(即碳碳键全部是单键) 3.通式:;物理性质和苯相似 4、苯的同系物的同分异构现象 书写苯的同系物的同分异构体时,苯环不变,变换取代基的位置及取代基碳链的长短。 例如C8H10对应的苯的同系物有4个同分异构体,分别为、、、 5、苯的同系物的化学性质 (1)氧化反应
(含3套新高考模拟卷)高中化学芳香烃(第2课时)导学案选修5
芳香烃 自学导航 【学习目标】 1.掌握苯和苯的同系物的结构特点、化学性质; 2.理解苯的同系物结构中苯环和侧链烃基的相互影响; 3.了解芳香烃的来源。 【重点难点】 苯和苯的同系物的结构特点、化学性质 学习过程 【基础知识扫描】 二、芳香烃的来源与应用 1.来源:(1)煤 煤焦油 芳香烃(即最初来源于 ) (2)石油化工 催化重整、裂化(现代来源) 在芳香烃中,作为基本有机原料应用的最多的是 、 和 2.苯的同系物 (1)概念 苯的同系物只有一个苯环,它们可以看成是由苯环上的H 被 代替而得到的。 例如: 甲苯 乙苯 苯的同系物的通式: (2)性质 ①相似性: A .都能燃烧,产生明亮火焰、冒浓黑烟。 B .都能和X 2、HNO 3等发生氧化反应。 甲苯与浓硝酸的反应: 2,4,6---三硝基甲苯(TNT )是一种 溶于水的 色针状晶体,烈性炸药。 C .都能与H 2发生加成反应 ②不同点: A .侧链对苯环的影响 使苯环侧链 位上的氢原子容易被取代,如甲苯发生硝化反应生成三硝基甲苯,而苯一般只生成一硝基苯。 B .苯环对侧链的影响 实验:甲苯中加入酸性KMnO 4溶液→KMnO 4溶液,现象 乙苯中加入酸性KMnO 4溶液→KMnO 4溶液,现象 色 结论:若与苯环直接相连的碳原子上连有氢原子,则该苯的同系物就能够使酸性KMnO 4溶 液 ,与苯环直接相连的烷基通常被氧化为 。 (3)乙苯的制备 原理(反应方程式): 干馏 分馏 CH 3 CH 2CH 3
3.多环芳烃 A .多苯代脂烃:苯环通过 连接在一起。 B .联苯或联多苯:苯环之间通过 直接相连。 C .稠环芳烃:由共用苯环的若干条 形成的。 【典型例析】 〖例1〗下列关于苯及其同系物的说法中,正确的是 ( ) A .苯及其同系物可以含有1个苯环,也可以含有多个苯环 B .苯及其同系物都能溴水发生取代反应 C .苯及其同系物都能氯气发生取代反应 D .苯及其同系物都能被酸性KMnO 4溶液氧化 〖例2〗某芳香族化合物的分子式为C 8H 6O 2,它的分子(除苯环外不含其它环)中不可能有 A .两个羟基 B .一个醛基 C .两个醛基 D .一个羧基 ( ) 〖例3〗烷基取代基R 可被酸性高锰酸钾溶液氧化为COOH (苯甲酸),但若烷基R 中直接与苯环相连接的碳原子上没有C -H 键,则不容易被氧化得到苯甲酸。现有分子式为C 11H 16的一烷基取代苯,已知它可以被氧化称为苯甲酸的异构体有7种,其中3种是: CH 2CH 2CH 2CH 2CH 3、CHCH 2CH 2CH 3CH 3、CH 2CHCH 2CH 3CH 3 请写出其它4种的结构简式_____________________________。 【反馈训练】 1.从煤焦油中获得芳香烃的方法是 A .干馏 B .裂化 C .催化重整 D .分馏 2.要鉴别己烯中是否混有少量甲苯,最恰当的实验方法是 A .先加足量的酸性高锰酸钾溶液,然后再加入溴水 B .先加适量溴水,然后再加入酸性高锰酸钾溶液 C .点燃这种液体,然后再观察火焰是否有浓烟 D .加入浓硫酸与浓硝酸后加热 3.联苯的结构简式如右图,下列有关联苯的说法中正确的是 A .分子中含有6个碳碳双键 B .1mol 联苯最多可以和6molH 2发生加成反应 C .它容易发生加成反应、取代反应,也容量被强氧化剂氧化 D .它和蒽( )同属于芳香烃,两者互为同系物 4.甲苯与浓硝酸、浓硫酸的混合酸在300C 发生反应获得的产物主要是 A .间硝基甲苯 B .2、4、6—三硝基甲苯 C .邻硝基甲苯和对硝基甲苯 D .三硝基甲苯 5.下列有关反应和反应类型不相符的是 蒽 联苯 联苯 2
2021新人教版高中化学选修5第二章第二节《芳香烃》word学案
第二节芳香烃 [学习目标定位] 1.认识苯的分子结构和化学性质,学会溴苯、硝基苯的实验室制取。2.知道苯的同系物的结构与性质的关系,知道芳香烃的来源及其应用。 1.苯是无色、有特殊气味的液体,把苯倒入盛碘水的试管中,振荡,静置,发现液体分层,上层呈紫红色,下层呈无色,说明苯的密度比水小,而且不溶于水。加几滴植物油于盛苯的试管中,振荡,发现植物油溶于苯,说明苯是很好的有机溶剂。将盛有苯的两个试管分别插入沸水和冰水中,将会发现前者沸腾,后者凝结成无色晶体。 2.苯的分子式是C6H6,结构简式是,其分子结构特点: (1)苯分子为平面正六边形结构; (2)分子中6个碳原子和6个氢原子都在同一平面内; (3)6个碳碳键键长完全相同,是一种介于碳碳单键和碳碳双键之间的特殊化学键。 3.苯易发生取代反应,能发生加成反应,难被氧化,其化学性质不同于烷烃和烯烃。(1)苯不能使酸性高锰酸钾溶液褪色,在空气中能够燃烧,燃烧时产生明亮的火焰并有浓烟 产生,燃烧的化学方程式为 (2)①苯不与溴水反应,但在催化剂作用下能与液溴发生取代反应,反应方程式为 ②苯与浓硝酸反应的化学方程式为 (3)一定条件下,苯能与H2发生加成反应,反应方程式为 探究点一溴苯和硝基苯的实验室制取 1.溴苯的实验室制取
(1)实验装置如下图所示。装置中的导管具有导气、冷凝回流作用。 (2)将苯和少量液溴放入烧瓶中,同时加入少量铁屑作催化剂,用带导管的塞子塞紧。观察实验现象: ①常温下,整个烧瓶内充满红棕色气体,在导管口有白雾(HBr遇水蒸气形成); ②反应完毕后,向锥形瓶中滴加AgNO3溶液,有淡黄色的AgBr沉淀生成; ③把烧瓶里的液体倒入盛有冷水的烧杯里,烧杯底部有褐色不溶于水的液体生成。 2.实验室制备硝基苯的实验装置如右图所示,主要步骤如下: ①配制一定比例的浓硫酸与浓硝酸混合酸,加入反应器中。 ②向室温下的混合酸中逐滴加入一定质量的苯,充分振荡,混合均匀。 ③在50~60 ℃下发生反应,直至反应结束。 ④除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤。 ⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。 填写下列空白: (1)配制一定比例的浓硫酸与浓硝酸混合酸时,操作注意事项是。 (2)步骤③中,为了使反应在50~60 ℃下进行,常用的方法是。 (3)步骤④中洗涤和分离粗硝基苯应使用的仪器是。 (4)步骤④中粗产品用5%NaOH溶液洗涤的目的是。 (5)纯硝基苯是无色、密度比水 (填“小”或“大”)、具有味的油状液体。答案(1)先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却(2)将反应器放在50~60 ℃的水浴中加热 (3)分液漏斗(4)除去粗产品中残留的酸(5)大苦杏仁 特别提醒①浓硫酸与浓硝酸混合时,应先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却。如果先注入浓硫酸,再注入浓硝酸,会造成浓硝酸受热迸溅、挥发。②反应温度是50~60 ℃,为方便控制,所以用水浴加热。 [归纳总结] (1)苯与溴的反应中应注意的问题
认识有机化合物导学案
. 第一章《认识有机化合物》 第一节有机化合物基础第1课时有机化合物的分类 【学习目标】掌握有机化合物分类的一般方法 【学习重点】有机物的常见类别 【学习难点】官能团分类法 【基础扫描】全员参与巩固基础 一、有机化合物的基本特征 1、有机物的定义:组成中含有元素的化合物统称有机物 【注意】⑴有机化合物的组成中必须含有碳元素,但是组成中含有碳元素的化合物,却不一定都是有机物。例如:、、、、 这几类物质组成中都含有碳元素,但是都不是有机化合物 ⑵有机化合物通常又被简称为有机物,它们均为化合物,即有机物中不存在单质 2、有机物的组称元素:有机物的组成元素,除外,通常还含有 等非金属元素 3、有机物的结构特点 ⑴有机物分子中碳原子间均以结合形成或,这是有机物结构的基础 ⑵有机物分子之间均通过结合形成 4、有机物的数量特点 有机物种类繁多,达上千万种。其原因是: ⑴碳原子有个价电子,能与其它原子形成个 ⑵有机物分子中碳原子之间能以、、 三种不同的方式形成共价键,且碳原子之间又能以或的方式结合,形成有机物的基本骨架结构 ⑶有机物中普遍存在现象 5、有机物的性质特点 ⑴溶解性:大多数有机物难溶于,易溶于(如、、等) ⑵可燃性:绝大多数有机物 ⑶耐热性:多数有机物较低,受热易 ⑷导电性:绝大多数有机物为,不能,不易 ⑸化学反应:有机化学反应都比较,一般反应速率,多数需要使用,并常伴有发生【练习1】下列叙述正确的是() A、有机物一定来自有机体内 B、有机物与无机物可以相互转化 C、CO属于有机物 D、AB + CD ==AC +BD 一定属于复分解反应【练习2】下列物质中不属于有机物的是() A、NaCN B、CH3COOH C、甲烷 D、SiC 【练习3】决定有机物种类繁多的原因,不正确的是() A、碳原子间可以有多种排列方式 B、碳原子有4个价电子,可与其他原子形成4个共价键 C、碳原子之间的成键方式较多 D、有机物分子中,碳原子间只能排列成链状 【练习4】人类已知的化合物种类最多的是() A、第I A族元素的化合物 B、第III A族元素的化合物 C、第IV A族元素的化合物 D、第VII A族元素的化合物 【练习5】有机化学主要研究有机化合物所发生的反应,下列化合物中不是有机物的是() A、CO2 B、C2H6 C、HCHO D、CH3OH 【练习6】自然界中化合物的种类最多的是() A、无机化合物 B、有机化合物 C、铁的化合物 D、碳水化合物【练习7】下列物质属于有机物的是() A、Na2CO3 B、CaC2 C、CO(NH2)2 D、CO 【练习8】目前已知化合物中数量、品种最多的是IVA碳的化合物(有机化合物),下列关于其原因的叙述中不正确的是() A、碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键 B、碳原子性质活泼,可以跟多数元素原子形成共价键 C、碳原子之间既可以形成稳定的单键,又可以形成稳定的双键和三键 D、多个碳原子可以形成长度不同的链、支链及环,且链、环之间又可以相互结合 【练习9】下列物质属于有机物的是() A、氰化钾(KCN) B、氰酸铵(NH4CNO) C、尿素(NH2CONH2) D、碳化硅(SiC) 【练习10】第一位人工合成有机物的化学家是() A、门捷列夫 B、维勒 C、拉瓦锡 D、牛顿 【练习11】有机化学的研究领域是() ①有机物的组成②有机物的结构、性质③有机合成④有机物应用
芳香烃 学案 2014 - 修
第二章第2节芳香烃课前预习学案 2014.2.24 一、预习目标 1、了解苯及其同系物的结构和性质等知识 2、简单了解芳香烃的来源及应用 二、预习内容 (一)、苯的结构和性质 1、苯的结构(1)分子式(2)结构简式(3)最简式(4)空间结构:苯分子中6个碳原子和6个氢原子共平面,形成,键角为120°,碳碳键长介于______和之间 2、苯的物理性质苯是___ 色,带有______ 气味的有_____ 的液体,密度比水 练习:苯环结构中,不存在单双键交替结构,可以作为证据的事实是() ①苯不能使KMnO4(H+)溶液褪色②苯分子中碳原子之间的距离均相等③苯能在一定条件下跟H2加成生成环己烷④经实验测得邻二甲苯仅一种结构⑤苯在FeBr3存在的条件下同液溴可以发生取代反应,但不因化学变化而使溴水褪色 A.②③④⑤B.①③④⑤C.①②④⑤D.①②③④ 【思考】可以从哪几个方面来证实苯分子中不存在单双键交替结构? 3、苯的化学性质(1)取代反应 ①苯与溴的反应反应的化学方程式为: ②苯的硝化反应 苯与和_________的混合物共热至50℃——60℃反应的化学方程式为: (2)苯的加成反应 在特定的条件下,苯与氢气发生加成反应的化学方程式为: (3)苯的氧化反应 苯在空气中燃烧产生,说明苯的含碳量很高,燃烧的化学方程式为:;苯(填“能”或“不能”)使KmnO4酸性溶液褪色 新课课内探究学案 实验探究: 根据苯与溴、浓硝酸发生反应的条件,请你设计制备溴苯和硝基苯的实验方案 提示:沸点:苯80.1℃Br2 58.78℃溴苯156.43℃硝基苯210.9℃ 实验设计的基本要求:①科学性②安全性③可行性④简约性 实验设计: 1、溴苯的制备 实验步骤:
芳香烃
第二单元芳香烃 双基再现 1.下列物质中,一定能因发生化学反应而使溴的CCl4溶液和酸性高锰酸钾溶液褪色的是()A.甲苯B.C3H6C.C5H12D.C2H4 2.可用来鉴别乙烯、四氯化碳、苯的方法是() A.酸性高锰酸钾B.溴水C.液溴D.硝化反应 3. 都属于萘的同系物。萘和萘的同系物分子组成通式是()A.C n H2n-6(n≥11)B.C n H2n-8(n>10) C.C n H2n-10(n≥10)D.C n H2n-12(n≥10) 4.间-二甲苯苯环上的三溴代物的同分异构体数目为()A.1 B.2 C.3D.4 5.下列各物质中,互为同系物的是() A 和B.HCOOCH3和CH3COOH C.油酸和软脂酸 6.某种物质A苯环上的二溴代物有9种同分异构体,由此推断A苯环上的四氯代物的同分异构体数目有()A.9种B.10种C.11种D.12种 7.化合物A的分子式为C9H8,存在于煤焦油中,它能迅速使Br2的CCl4溶液和酸性高锰酸钾溶液褪色,在一定条件下也能结合1分子的氢而生成B,分子式为C9H10,而在剧烈条件可以氢化生成C,分子式为C9H16。A剧烈氧化时生成邻苯二甲酸。试推测A、B、C的结构简式。 A:;B:;C:。 变式活学 8.1999年,在欧洲一些国家发现饲料被污染,导致畜禽类制品及乳制品不能食用,经测定饲料中含有剧毒物质 二恶英,其结构为,已知它的二氯代物有10种,则其六氯代物有() A.15种B.11种C.10种D.5种 9.已知1,2,3-三苯基环丙烷的3个苯基可分布在环丙烷环平面的上下,因此有如下2个异构体。 据此,可判断1,2,3,4,5-五氯环戊烷的异构体数是() A.4 B.5 C.6 D.7 10.下列物质中既能使溴水褪色又能使酸性的KMnO4溶液褪色的是() A、甲苯 B、己烯 C、苯 D、己烷 11.下面是某些稠环芳烃的结构简式()
高考化学总复习 第九章 第三节芳香烃学案
第三节芳香烃 1.了解苯的组成、结构、性质及在化 工生产中的重要作用。 2.了解苯的同系物的组成、结构和性 质。 3.了解天然气、石油液化气和汽油的 主要成分及其应用。
梳理基础 一、苯 1.苯的结构。 分子式:_______ 结构简式:_______或_______ 成键特点:介于_______和 之间特殊的键 空间构型:_______形,所有 原子在_______上答案:1.C6H6碳碳单键碳碳双键平面正六边同一平面 2.物理性质。 苯是____色具有________气味的____体,密度比水____,____溶于水,沸点80.1 ℃,熔点5.5 ℃,苯____毒,是一种重要的有机溶剂。 答案:2.无特殊液小不有 3.化学性质。
有关反应的化学方程式为: ①____________________________。 ②____________________________, 其中浓H 2SO 4的作用是____和_____。 ③____________________________。 ④____________________________。 答案:3.取代 取代 加成 火焰明亮、有浓烟 不能 ①+Br 2――→Fe +HBr ② +HNO 3―――――→浓H 2SO 4 50~60 ℃+H 2O 催化剂 脱水剂 ③+3H 2―――→催化剂 ④2+15O 2――→点燃 12CO 2+6H 2O ①与液溴和Fe 属于反应 ②与浓HNO 3 属于____反应 ③与H 2 属于____反应 ④与O 2 现象:____________ ⑤与KMnO 4(酸性)溶液 使KMnO 4(酸性)溶液褪色
芳香烃导学案(精品)
【学习目标】 1、了解苯的结构特征,掌握苯的主要化学性质。 2、了解芳香烃、苯的同系物的概念 ,了解甲苯的某些化学性质。 3、掌握苯与苯的同系物的相似性和鉴别方法 【自主预习】 1、芳香烃:分子里含有一个或多个________的化合物 2、苯的分子结构:分子式_______ ;结构简式_______ 或_______ ;空间结构:分子中的6个碳原子和6个氢原子都在_______ 内,形成____________,碳碳键是介于__________ 和_________之间的________的化学键,键角为_______ 。 3、苯的物理性质 :苯是 色,带有 气味的 体,密度比水 。 4、苯的化学性质:苯分子中特殊化学键决定了其化学性质的独特性:兼有 烃和 烃的性质,即能发生 反应和 反应。 5、苯的同系物:苯环上的氢原子被 取代后的产物。通式: ; 6、苯的同系物的结构特点:分子中只有 个苯环,侧链都是 。 7、甲苯与浓硝酸反应的方程式: 。 三硝基甲苯的系统命名为 又叫(TNT ), 溶于水,是一种烈性炸药。 8、芳香烃的来源: 和 。 【预习自测】 1、下列关于苯的叙述正确的是( ) A .苯的分子式为C 6H 6,它不能使酸性KMnO 4溶液褪色,属于饱和烃 B .从苯的凯库勒式看,苯分子中含有碳碳双键,应属于烯烃 C .在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应 D .苯分子为平面正六边形结构,6个碳原子之间的价键完全相同 2、下列事实能说明苯是一种不饱和烃的是( ) A 、苯不能使酸性KMnO 4溶液褪色 B 、苯在一定条件下可与液溴发生取代反应。 C 、苯在一定条件下可与H 2发生加成反应 D 、苯的核磁共振氢谱图中只有一种峰。 3、、、它们都有一个 ,侧链为 基,分子组 成上相差一个或两个CH 2原子团,它们和苯是 【合作探究】 探究一:你能区分芳香族化合物、芳香烃、苯的同系物吗尝试用图像把这三者的关系表示出来。 Ⅰ、制备溴苯(如右图):现象:1 向烧瓶中加入苯和液溴再加入铁屑后, 反应迅速进行,溶液几乎“沸腾”,一段时间后反应停止。 2 反应结束后,烧瓶底部出现红褐色(因溶有Br 2)油状液体(溴苯)。 3 锥形瓶内有白雾,向锥形瓶中加入AgNO 3溶液,出现浅黄色沉淀。 CH 2—CH 3 CH 3 CH 3 CH 3 ) )
上海高二下化学第07讲 苯和芳香烃(教学案)汇总
高二下化学第07讲苯和芳香烃 ——芳香族化合物的母体 教学目标:1、了解苯的组成和结构特征2、掌握苯及其同系物的化学性质 3、了解芳香烃的概念及甲苯、二甲苯的某些性质 4、通过苯的溴代或硝化反应与甲苯与酸性高锰酸钾溶液反应的比较,理解有机分子中基团 之间的相互影响 教学重点:苯的结构特征、苯及其同系物的化学性质 教学难点:苯及其同系物的化学性质 知识网络: 教学内容: 一、苯 1、物理性质: 颜色状态溶解性:无色液体、易挥发,难溶于水、密度比水小,是重要的有机溶剂。 特性:有特殊气味、有毒(易使人至再生障碍性贫血)。是一种重要的化工原料。 2、分子结构: (凯库勒结构式) 分子式:C6H6 、结构式: 结构特点: (1)平面正六形结构,12个原子均在同一平面内,键角均为120° (2)苯分子中没有单、双键交替的结构,6个碳碳键键长完全相同,键能和键长是介于单键和双键之间的特殊的化学键(共轭大π键)。苯的性质即是体现了饱和烃和不饱和烃的性质。 3、化学性质: (1)氧化反应: 燃烧:2C6H6+15O2→12CO2+6H2O,火焰明亮且伴有浓烟。 (不能被KMnO4所氧化,不能使酸性KMnO4溶液褪色。) (2)取代反应—体现了饱和烃的性质
①卤代反应 与液溴的取代反应: 实验现象: a 、试管A 中及双球U 形管中的左则充满红棕 色气体(反应放热使液溴变为蒸气) b 、双球U 形管中的无色CCl 4变成呈红色(溶解了Br 2) c 、试管B 中有浅黄色沉淀生成 [HBr+AgNO 3→AgBr ↓(浅黄色)] 问题: a 、双球U 形管中CCl 4作用:除去因放热产生的Br 2蒸气和苯蒸气,以防干扰B 试管中的AgNO 3溶液与HBr 的反应。 b 、反应中铁丝所起作用:催化剂。 c 、怎样得到比较纯净的溴苯:把A 试管中反应后的物质倒入盛有NaOH 的烧杯中以除去没反应的溴,再除去铁丝,分液取下层液体即得溴苯(溴苯密度比较大且不溶于水)。 ②硝化反应 硝基苯:苦杏仁味的油状液体,难溶于水比水重。 浓H 2SO 4的作用:催化剂和吸水剂。 试管上的长导管:冷凝和回流的作用,防止苯的挥发。 硝基(-NO 2)取代了苯中的-H 原子,该反应叫又叫硝化反应。 实验操作: a 、先混合酸(把2mL 浓硫酸慢慢加入到1.5mL 浓硝酸中) b 、再把1mL 苯慢慢加到混酸中并摇匀。 c 、放入60℃水浴中加热10min ,以防局部温度过高而发生更多的副反应 d 、把混合液倒入另一盛有水的烧杯中 实验现象: a 、试管底部有黄色油状物质生成,可能是HNO 3分解产生的NO 2溶解在硝基苯中所致。 b 、倒入烧杯后,底部呈无色油状液体,NO 2及硝酸、硫酸溶解在水中。 ③磺化反应:苯分子里的氢原子被硫酸分子里的磺酸基(-SO 3H)所取代的反应叫磺化反应 C 6O 6+HO-SO 3H △ C 6H 5-SO 3H+H 2O 浓硫酸的作用:反应物 (3)加成反应—体现了不饱和烃的性质 C 6H 6+3H 2 催化剂 C 6H 12(环已烷) C 6H 6+3Cl 2 催化剂 C 6H 6Cl 6(六氯环已烷,一种杀虫剂)
高二化学HXXX508第二章第二节芳香烃导学案(精品文档)
高二化学 编号:HX-XX5-08 《第二章 第二节 芳香烃》导学案 编写: 王伟 备课组审核:王伟 教研组审核:王福 班级: 组别: 姓名: 【学习目标】 1、掌握苯的分子结构特点。 2、了解芳香烃、芳香族化合物的概念。 3、掌握苯的物理性质和化学性质。 4、掌握苯的同系物与苯在结构和性质上的异同点。 【学习过程】 一、苯的分子结构 1、分子式: 最简式(实验式): 2、空间构型:苯分子为 结构,键角为 。 3、结构特点:苯分子中碳碳键键长为40×10 -10m , 是介于 的特 殊的化学键。 4、 结构式 : 5、 结构简式(凯库勒式): 二、苯的物理性质 苯是 色,带有 气味的液体,苯 毒, 溶于水, 溶于有机溶剂,密 度比水 ,熔沸点 ,易 ,用冰冷却,苯凝结成无色的晶体。 三、苯的化学性质 1、氧化反应: 苯较稳定, 能使酸性KMnO 4溶液褪色,能燃烧,但由于其含碳量过 ,而出现明显 的 。 2、取代反应 a.卤代:方程式: 溴代反应注意事项: 1、实验现象:烧瓶内:液体微沸,烧瓶内充满有大量 色气体。 锥形瓶内:管口有 出现,往溶液中滴加AgNO 3 溶液会出现 色沉淀。 2、加入Fe 粉是 ,但实质起作用的是 教师 批阅 定等
3、加入的必须是,不能用溴水,苯不与溴水发生化学反应,只能是萃取作用。 4、长直导管的作用是:导出气体和 5、纯净的溴苯为色油状液体,溶于水,密度比水。新制得的粗溴苯往往为褐色,是因为溶解了未反应的。欲除去杂质,应用溶液洗液后再分液。 [思考与交流]1、锥形瓶中导管末端为什么不插入液面以下? 2、如何证明反应是取代反应,而不是加成反应? 3、HBr可以用什么来检验? b.硝化:方程式 硝基苯:色,油状液体,味,毒,密度水,溶于水,溶于有机溶剂 [思考与交流] ?硝基苯不纯显黄色(溶有NO2)如何除杂? 3、苯的加成反应 在比较苛刻的条件下,苯也可以发生加成反应。例如,在镍催化剂、加热条件下,苯可以加氢生成环己烷。 化学方程式: 四、苯的同系物 1.概念:通式: [自主探究]概念辩析:请用圆形图方式表示芳香化合物、芳香烃、苯的同系物三者的包含关系。 2
芳香烃
芳香烃 第二单元芳香烃第一课时要点:1芳香族化合物及芳香烃的概念 2苯的分子结构特点及物理性质:(1)分子式、结构简式(2)分 子空间构型(3)苯分子中C原子成键特点3苯的化学性质:(1) 苯的溴代实验(2)苯的硝化实验(3)苯的加氢加成反应【问】根 据有机物的分类,我们知道有机物中有一类物质称为芳香族化合物,最初发现的这类物质绝大部分都是具有香味的,它们是从各种天然 的香树脂、香精油中提取出来的。目前,已知的很多芳香族化合物 其实并不具有芳香气味,所以,“芳香族化合物”这一名称已经失去 了原先的意义,只是一直沿用至今,那么现在我们所定义的芳香族 化合物是一类怎样的物质呢?它们在结构上有什么共同的特点呢? 芳香族化合物——分子结构中含有苯环的有机物。【问】什么是烃 类物质?只含有C、H元素的一类有机物。把这两类物质合并起来,取个交集,就是我们今天要研究的一类有机物——芳香烃。芳香烃——芳香族碳氢化合物,简称芳香烃或芳烃。一苯的结构与性质1 苯的结构(1)分子式:C6H6(2)结构式:【交流与讨论】那么苯 分子的结构是怎样的呢?①苯的1H核磁共振谱图(教材P48)苯分 子中6个H所处的化学环境完全相同苯分子结构的确定经历了漫长 的历史过程,1866年,德国化学家凯库勒提出苯环结构,称为凯库 勒式:那么凯库勒式能完全真实的反应苯分子的结构吗?根据以下 信息,谈谈你对苯分子结构的认识?②苯的一取代物只有一种,邻 位二取代物只有一种和是同一种物质③苯不能使溴水腿色,不能使 酸性高锰酸钾溶液腿色④碳碳双键加氢时总要放出热量,并且放出 的热量与碳碳双键的数目大致成正比。苯在镍等催化下可与氢气发 生加成反应生成环己烷,所放出的热量比环己二烯与氢气加成生成 环己烷的还要少。说明苯环中并不存在单双键交替的结构,因此凯 库勒式不能全面的反应苯的结构,只是习惯上沿用至今。【过渡】 那么苯分子的结构到底是怎样的?拓展视野:苯环中的碳原子都是 采用的sp2杂化,碳原子之间形成σ(sp2-sp2)键,六个C原子的 p轨道重叠形成一个大π键。苯分子中碳碳键的键长都是一样长的
