有机化学笔记整理(网上找的)

基础有机化学
(邢其毅版)
2011年上海医工院考研笔记整理姓名:庄守群
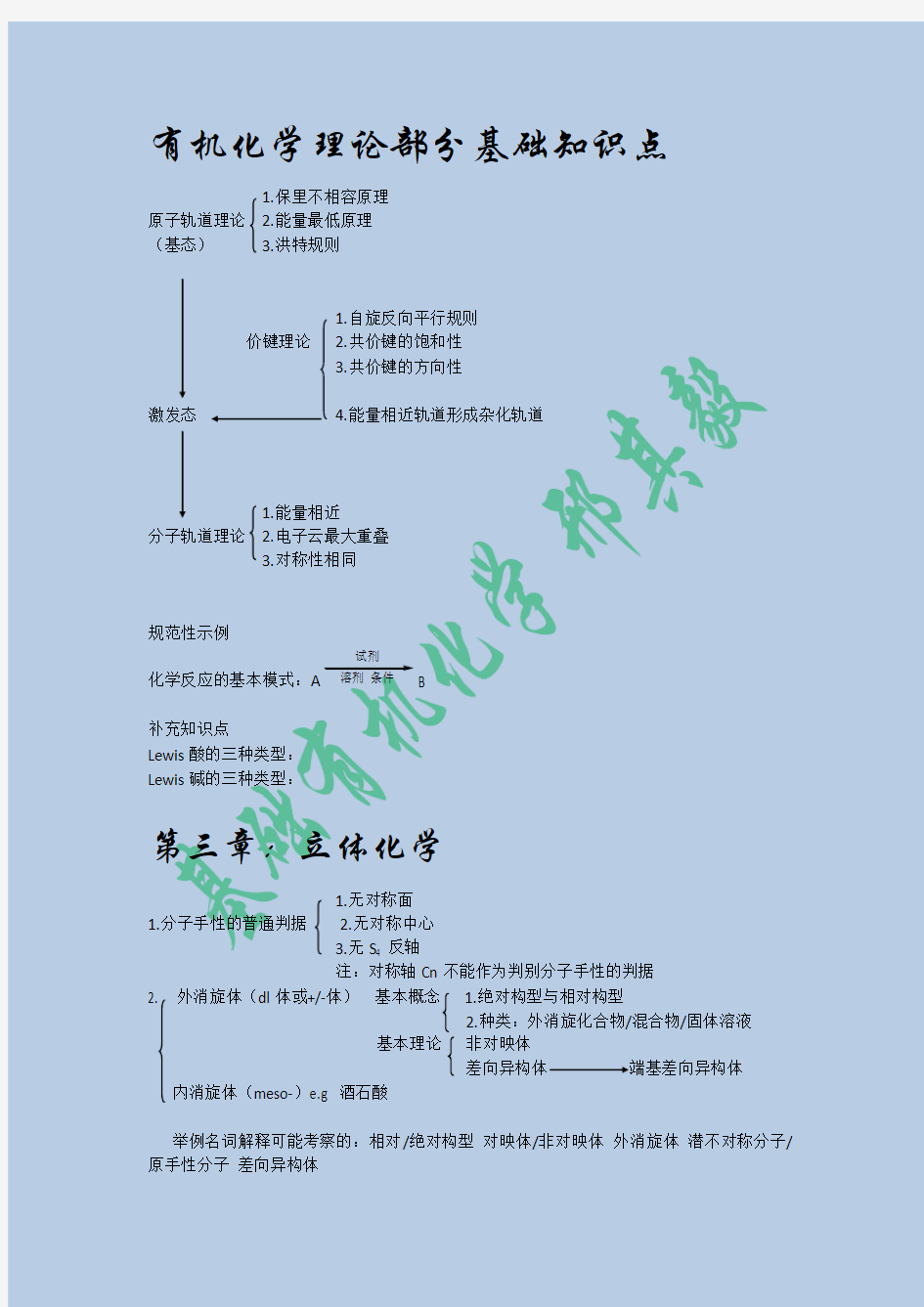
有机化学理论部分基础知识点
1.保里不相容原理
原子轨道理论 2.能量最低原理
(基态) 3.洪特规则
1.自旋反向平行规则
价键理论 2.共价键的饱和性
3.共价键的方向性
激发态 4.能量相近轨道形成杂化轨道
1.能量相近
分子轨道理论 2.电子云最大重叠
3.对称性相同
规范性示例
化学反应的基本模式:A
试剂
溶剂条件 B
补充知识点
Lewis酸的三种类型:
Lewis碱的三种类型:
第三章:立体化学
1.无对称面
1.分子手性的普通判据
2.无对称中心
3.无S4 反轴
注:对称轴Cn不能作为判别分子手性的判据
2. 外消旋体(dl体或+/-体)基本概念 1.绝对构型与相对构型
2.种类:外消旋化合物/混合物/固体溶液
基本理论非对映体
差向异构体端基差向异构体内消旋体(meso-)e.g 酒石酸
举例名词解释可能考察的:相对/绝对构型对映体/非对映体外消旋体潜不对称分子/原手性分子差向异构体
3.立体异构部分
⑴含手性碳的单环化合物:
判别条件:一般判据 无S 1 S 2 S 4 相关:构象异构体ee
aa ea
ae
构象对映体 主要考查:S 1=对称面的有无
相关实例:1.1,2-二甲基环己烷 1,3二甲基环己烷 1,4二甲基环己烷 ⑵含不对称原子的光活性化合物 N 稳定形式 S P 三个不同的基团 ⑶含手性碳的旋光异构体
丙二烯型旋光异构体 1.狭义
c c c
条件:a b 两基团不能相同
2.广义:将双键看成环,可扩展一个或两个
c
c c
联苯型旋光异构体 (阻转异构现象- 少有的由于单键旋转受阻而产生的异构体)
B
A a
b
构型命名方法:选定一环,大基团为1,小基团为2.另一环,大集团为3,将其小基团转到环后最远处。
⑷含手性面的旋光异构体
分子内存在扭曲的面而产生的旋光异构体,e.g 六螺苯
4.外消旋化的条件
⑴若手性碳易成碳正离子、碳负离子、碳自由基等活性中间体,该化合物极易外消旋化。 ⑵若不对称碳原子的氢是羰基的-H ,则在酸或碱的作用下极易外消旋化。
含多个不对称碳原子时,若只有其中一个碳原子易外消旋化,称差向异构化。
5.外消旋化的拆分
化学法 酶解法 晶种结晶法 柱色谱法
不对称合成法:
1.Prelog 规则—一个分子得构象决定了某一试剂接近分子的方向,这二者的关联成为Prelog 规则.
2.立体专一性:即高度的立体选择性
6.构象中重要作用力
非键连的相互作用:不直接相连的原子间的作用力。(由于受别的相连原子之间相互连接而造成空间上的限制而引起的范德华力)
扭转张力:偏离最稳定形式而存在,具有恢复构象的能力----源于范德华力
转动能垒:稳定构象变成不稳定构象所需要的能量。
7.典型有机化合物的构象分析
0°极限构象I 重叠型构象
乙烷0-60°扭曲型构象
60°极限构象II 交叉型构象
伞形式锯架式纽曼式
环形有机化合物
角张力:由键角的屈饶引起。
大环化合物易稳定(原因):非平面结构
环丙烷:键角香蕉键H-C-H 115°>109°C-C-C 105°<109°
键长151pm < 154pm
分析保持轨道109°(电子云重叠很差)六个氢呈重叠型且均等保持电子云最大重叠(电子排斥大)
环丁烷:
环戊烷:信封型
半椅型减小了平面型的扭转张力
第四章烷烃自由基取代反应
1.基本理论
⑴①沸点
影响因素:分子质量分子间作用力
烷烃:有瞬时偶极距
作用力:色散力分子间范德华力
结论:分子接触面越大,相互作用力越大,沸点升高。叉链分子有叉链位阻作用。分子间作用力小,沸点降低。
分子接触面升高用于分析正烷烃的沸点,随分子质量而升高的原因
②熔点
影响因素:分子质量分子间作用力晶格中排列情况---分分子对称性高,排列比较整齐,分子间引力大,熔点高。
结论:双数碳原子彼此靠近,熔点升高值(2n+2,2n )较单数(2n+1,2n-1)碳链升高值大一些。
同碳原子数,环烷烃较链烷烃熔点、沸点、密度均高一些。
⑵.有机反应
A .自由基反应:
均裂 产生:自由基或游离基 实质:电中性 多数仅有瞬时寿命 活性中间体 离子型反应:
异裂 产生:正负离子 实质:电性 仅有瞬时寿命 活性中间体 协同反应
环状过渡态基元反应 B .热力学和动力学分析
过渡态:极不稳定 反应中间阶段
反应能势图
中间体:处于势能谷底 为稳定物种 有一定寿命 C .过渡态假说 Hammond 假说
针对过渡态,为解决过渡态的相关问题提出来的。
内容:在简单的一步反应中(基元反应),该步过渡态的结构能量与更接近的那边类似。 结论:放热反应,过渡态的结构与反应物相似。 吸热反应,过渡态的结构与生成物相似。
根据多步反应中反应物、中间体和生成物来讨论过渡态的结构。 2.烷烃
⑴结构与反应性:C (2.5)--H(2.2) 电负性差别很小,不易偏向于某一原子,整个分子电子分布较均匀—可用于偶极矩的分析
烷烃—亲电亲核无效(无特殊亲和力,即没有电子云密度很大或很小的部位)
--主要反应:加热或光照条件下发生自由基反应(须有引发剂)
引发自由基的几种方式:
1. 有些化合物十分活泼,极易产生自由基,称引发剂,如过氧化乙酰,过氧化苯甲酰。
烃基过氧化物ROOH 或其他有-O-O-H 键,这是一个弱键,适当温度下易分解,产生自由
基,引发链反应。
促使反应很快进行(大量放热,过氧化物易爆原因)
o o
o
o
55-85℃
PhH
o
o
2. 有时也通过单电子的转移氧化还原反应来产生自由基。如:
H 2O 2+Fe 2+ HO +HO -+Fe 3+ RCOO -
RCOO
诱导期的产生:
1.氧气或者捕获自由基的杂质可与自由基结合生成稳定的自由基。
-e -
电解
CH 3
O 2+CH 3OO
抑制剂的加入…待氧气消耗殆尽,自由基链反应立即开始。
断键,自由基反应原则:最弱的键较易断裂,最稳定的自由基较易形成。 2.自由基反应加入I 2,可是反应终止。
3.碘自由基又容易自相结合成键,碘自由基与双键加成需要较大的活化能。见325页
自由基反应和协同反应:都没有明显的溶剂效应,酸碱等催化剂对反应没有明显的影响。
应用:烷烃的卤代
基本概念:反应速率的快慢 活化能的大小 过渡态势能/结构 与形成的活性中间体有关 (如自由基更稳定,键解离能下降,活化能也就越小。反应也就越快)
如果一个反应可以生成几种生成物,则每一种生成物通过不同的过渡态生成,则最主要的生成物,通过势能/活化能最低的过渡态形成。
自由基的稳定性:是指与它的母体化合物的稳定性相比较,比母体化合物能量高得多的叫不稳定,高的较少的较稳定。
⑵自由基反应共性
链引发 链转移 链终止
链引发:需引发剂 极易产生活性质点的自由基 若体系中有氧气(抑制剂),会有诱导期。只要有少量抑制剂存在,就能使反应变慢或终止。自由基反应中加入碘单质,可是反应终止。
大分子在中间断裂的稳定性更强,在中间断裂的机会是比较多的,如正丁烷。原因:产物自由基稳定性较高。
链转移:一个自由基变成另一个自由基
特点:没有明显的溶剂化效应,酸碱催化剂无明显影响。
链终止:自由基两相成键。
产生自由基反应(始)的三个条件:
1. 光照或加热
2.引发剂:如过氧化乙酰
3.单电子转移
应用:甲烷的卤化
1.不可用氟单质、碘单质卤化
用氟单质:大量放热,难以移走,破坏生成的氟甲烷,生成碳单质和氟化氢。 用碘单质:+
CH 3I
HI
CH 4
+
I 2
(易)
卤化反映逆反应容易进行。自由基链反应中加入碘单质,使反应终止。
R 3C
+
+
I
I 2
R 3CI
注:碘自由基活性差。
2. 氯 溴反应区别:
氯自由基活泼,过渡态的反应势能与反应物接近,中间体自由基的活性影响小,过渡态结构类似于反应物。 结论:产物受中间体影响小。
溴自由基次活泼,过渡态来得晚,过渡态的势能与中间体接近,活性中间体稳定。 结论:产物受中间体影响大。 活性中间体稳定,过渡态势能低,活化能降低,反应速率加快。
谨防:高温时该理论无效。如温度大于450℃,有足够的能量,反应结果仅与氢原子的个数有关。 反应类型:
⑴烷烃的热裂 热作用的自由基反应
热裂:自由基之间的相互结合。
如用催化剂可以降低温度,但反应机理就非自由基反应,而是离子型反应。 ⑵烷烃的氧化:又叫老化 自由基反应
R 3C
+
OO O 2
R 3C R 3CH R 3C
+O 2+
OOH
OO
R 3C R 3CH +
OOH
R 3C R 3C
+
烃基过氧化氢ROOH 或其他过氧化物有-O-O-键适当温度易分解产生自由基,引发链反应,产生大量自由基,很快进行,大量放热------可用于解释:过氧化物易产生爆炸。 可与氧气发生自由基类型:1.烷烃的三级氢 2.醛上氢 3.醚的 ⑶气相硝化,磺化:高温自由基反应
与卤化反应不同的是,气相硝化,磺化要-C-C-键的断裂。(主要用于工业合成,实验室有很大的局限性)
3. 小环烷烃
a 与氢气反应(限三四元环)
反应原则:催化氢化在空阻小的位置发生
+H 2
Pt/C,50℃
(书上讲,叉链化合物比较稳定)
b 与X 2反应(限三元环)
+
Br
2
Br
Br
C 与HI 反应(限三四元环)
原则:反应类型--离子型反应:极性大的键先断裂
+HI
I
d 自由基反应(导致的手性R S 各占50%,无立体选择性)
+Cl
2
Cl
hr
+Br
2
Br
hr
本章小结:
SN2
反应分子数 与动力学上的级数往往相同
动力学上的技术与反应分子数并不总一致。
Nu -即为溶剂:溶剂解反应 溶剂大量 前后基本不变
一般速率较慢,用于研究反应机理,非常重要用于合成生产上则很少
Sn 最初达到的活化能有谁提供?
溶剂与过渡态有偶极—偶极相互作用,底物在形成过渡态时需要能量,此能量可由偶极—偶极相互作用时所释放的能量提供。
Sn1重排机理:
推动力:一个较稳定的分子/离子去代替一个叫较不稳定的分子/离子。
第六章 脂肪族饱和碳的亲核取代反应和消除反应
一.电子效应
1.诱导效应(一般以氢为比较标准)
也可以通过测量酸或碱的Ka 获得或者通过测量偶极矩(强弱)获得。
a . 带带正电荷的基团具有吸电子的诱导效应,带负电荷的基团具有给电子的诱导效应。(一
般只考虑三根键的影响) b . 烷基有给电子的诱导效应和给电子的超共轭效应。
吸电子能力强弱比较: NO 2>CN>F>Cl>Br>I>C >OR>OH>Ph>C=C
2.共轭效应
a.有吸电子共轭效应的:NO
CN COOH CHO COR
2
(R) NHCOR OH OR OCOR
b. 有给电子共轭效应的:NH
2
c.同时有共轭效应和诱导效应的,且异向的:
(R) 综合给电子效应给电子的共轭>吸电子的诱导
NH
2
X 综合吸电子效应给电子的共轭<吸电子的诱导
3.超共轭效应
a.产生原因:烷基碳与极性小的氢相结合,对于电子云屏蔽效应很小,烷基上C-H的
一对电子,受核的作用相互吸引,到一定距离时,烷基上几个C-H键电子云又相互排斥,可离域到邻近的π轨道上或者p轨道上(碳正离子或自由基)
b.超共轭效应大小影响因素:由p轨道或π轨道相邻碳上的-C-H键的多少有关:正相
关
4.场效应静电作用原子链起作用:诱导效应
空间传递:场效应
吸电子基团使附近的带正电荷的基团不易离去。
应用:影响电子云密度如:影响酸性。
二.活性中间体
1.键解离能:烷基形成自由基所需能量。
电离能:自由基形成碳正离子所需能量。
2.碳正离子:3° >2°,烯丙基>1°
a有关烷基的给电子作用的实现:sp3-c s轨道成分少,离核远;sp2-c s轨道成分多,离核近。诱导效应也是sp2d的电负性强的原因。
b超共轭效应
3.手性碳构型保持与构型翻转(Walden转化)
构型保持:新键在旧键断裂的方向形成的情况
构型翻转:新键在旧键断裂相反的方向形成的情况
4.SN2 SN1
SN2 反应通式:(自己补充)
a 亲核试剂是溶剂,即溶剂解。
b 基本过程的描述:
c 过渡态时 SN2 SN1中心碳均为sp2-c
d 成环的 SN2
合适的位置,成环的难易:
五元环最易,其次是六元环。
三元环最有张力,但两个基团处于相邻位置,也较易。
(七八元环)大环:大环化合物对然没有张力,但更易分子间SN2。
降低反应物分子间距离,避免分子间接触,可分子内SN2:高稀溶液中进行。
SN1
机理通式:
基本特征:1.中心碳手性,产物外消旋。2.常常生成重排产物。
Winserin机理:
RX
R +X
-R +||X
-R +X -+内返
紧密离子对
离子对外返
溶剂分离子对
离子外返
自由离子
注:非极性溶剂,倾向于生成紧密离子对和溶剂分离子对。
强极性溶剂,倾向 于生成自由离子。
亲核试剂进攻紧密离子对,生成构型翻转的产物 溶剂分离子对,消旋产物占多数
自由离子,完全消旋。
结果:构型转化的产物多于构型保持的产物,最终没有得到外消旋体。
小结
SN2:SN2机理—walden 转化 SN1: SN1机理
Winstein 机理
离子对机理:ion-pair 非极性溶剂:
RX
R +X -R +||X -内返
紧密离子对
离子对外返
溶剂分离子对(中间有溶剂分子渗入)
强极性溶剂:
RX
R +X -+离子外返
自由离子
(离子周围被溶剂分子包
围)
Nu-试剂进攻产物完全消旋
SN1机理
应用离子对内返机理,如:ROH+SOCl 2 RCl
RCOOH+SOCl 2 RCOOCl
I-的碱性 I-的原子半径大,负电荷比较分散,负电荷越分散,越稳定,越不易和质子反应。 F-原子半径小,负电荷比较集中,负电荷越集中,越易结合质子,碱性越强。 磺酸的结构式要记住: 磺酸根负离子和硫酸根负离子是好的离去基团,更易离去的原因: 离去后,产物磺酸根,硫酸根较稳定,产物的稳定性促成了离去的动力。 碱性:试剂对质子的亲和能力。 亲核性:一个试剂在形成过渡态时对碳原子亲核能力。 影响亲和取代反应的因素: 烷基的结构 SN2:空间效应(空阻大,会使进入基团与碳原 子碰撞机会很少) SN1:空间+电子效应(超共轭效应 空助效应) R 3C +最易形成1.电子效应:R 3C + 超共轭效应最 大,正电荷更以分散2空阻下降:.空助效应 三个基团拥挤的力量提供了形成平面三角形的活 能 注:1.BnX CH 2 CHCH 2X 可进行SN1和SN2 2.二苯卤代烷 三苯卤代烷进行SN1 3.X 连在双键上,-X 不易离去。n 电子与π键的共 轭 离去基团的离去能力 好的离去基团 碱性小 键能小 不好的离去基团加催化剂,如-OH 卤化 为使SN 易于进行,常设法将一个不好的离去基团转变成 一个好的离去基团。如用ZnCl2或硫酸使其形成 ROH 2R-O-ZnCl 2 H 或即:使离去基团碱性变弱,易于 接受一对电子离去。 (小结:离去基团键能越小,键越容易断裂;碱性越弱,形 成的负离子越稳定) 试剂的亲核性:取决于 可极化性+碱性 对SN1:不影响 碳正离子反应性很高,不管试剂 的亲核能力是大还是小,均能发生反应。比较起来,电子云密度高的亲核试剂,SN1产率高。 对SN2:试剂亲核性越强,反应越快。 高极化性类型:1.分子质量越大,原子核对外层电子的约束力越大,可极化性越高。 2.孤对电子(未成键电子),只受一核影响,可极化性升高。 3.弱键电子结合松散,可极化性升高。 4.离域状态电子比定域状态电子,可极化性要 高。 小结:试剂亲核能力影响 1. R 3C -R 2N - RO - F - 碱性下降可极化性下降 亲核性下降 2.若二者相反,在偶极溶剂中,与碱性顺序一致; 在质子溶剂中,与可极化顺序一致。 可极化性受溶剂影响不大,碱性受溶剂影 响很大。可极化性高,碱性弱的溶剂,质 子溶剂中,碱性弱,溶剂化很少。偶极溶 剂中,也很少溶剂化,这些试剂在质子和 偶极溶剂中亲核性均很高。碱性很强,可 极化性低的试剂,质子溶剂中,成氢键能 力特别强(其随负电荷的密度的增加而增 加),即溶剂化作用大,在反应时需要去 溶剂化的能量大,故反应性能低。 综合--一般规律: CH3O-CH3CH2O-(CH3)2CHO-(CH3)3CO-OH-ArO-C2H5COO- 亲核性依次递减 质子溶剂中的一般亲核顺序: RS- ArS- CN- I- NH3/RNH2 RO- OH- Br- PhO- Cl- H2O F- 亲核性逐渐降低 I-的亲核性:好的离去基团+好的亲核试剂 应用:反应时常考虑用较便宜的溴 代烷或氯代烷为原料,反应中加入 少量碘化钠,与亲核试剂反应,以 提高反应产率。 两位负离子:-O-N=O 遇酸—HO-N=O 遇AgONO---SN2-- RCH2NO2(N 亲核性强) 遇R2CHBr--SN1-- R2CHONO R2CHX可进行SN1或SN2,这 种情况下,Ag+将X-先拉下来,促 进了SN1反应的进行。由于静电 吸引,R2C+就与NO2-中负电荷密集 的O结合了。 RCH2X +NaCN SN2RCH CN 2 遇到AgCN,使Ag+与X-作用,RCH2+有正电性质:类SN1 RCH2X +AgCN RCH2N C 溶剂: 质子溶剂:能与负离子形成强的氢键。如水,醇,酸,氨 / 胺。 偶极溶剂:(偶极非质子溶剂)分子中氢和分子内原子结 合牢固,不易给出质子。 结构特征:偶极负端露于分子外部,偶极正端 藏于分子内部。如DMSO,二甲亚砜,乙腈,DMF, 丙酮,Py,硝基甲烷。 非极性溶剂:这类溶剂不给出质子,与溶剂作用力弱。如 二氯甲烷,THF,乙酸乙酯,乙醚,四氯甲烷, 二氧六环,环己烷。 分析:质子溶剂对SN1有利--质子溶剂中的质子, 可以和反应中产生的负离子,特别是由氧和氮 产生的负离子,通过氢键溶剂化,这样使负电 荷分散,负离子稳定。(稳定离去基团,加速 SN1反应进行)(溶剂与过渡态通过偶极-偶极 相互作用时释放的能量提供活化能---增大溶剂 极性,溶剂极性大,溶剂化力量也大,提供的 能量也大,解离就很快进行即SN1) 偶极溶剂减小极性,对SN2反应有利。(溶剂化)(过渡 态的极性小于亲核试剂的极性,增加了溶剂极 性,使极性大的亲核试剂溶剂化不利于SN2) 极 性分子在非极性溶剂中,以分子缔合态而存在 (不溶解,不能均匀分散,反应时要克服这种 力量) 影响反应速度的一般有:空间+电子效应 如CN-+RCH2X或R2CX的SN反应与R3CX发生的消除反应 注意:非极性溶剂,倾向于生成紧密离子对和溶剂分离子对; 强极性溶剂,倾向于生成自由离子。 亲核试剂进攻紧密离子对,生成构型翻转的产物; 溶剂分离子对,消旋产物占多数; 自由离子,完全消旋。 结果:构型转化的产物多于构型保持的产物,最终没有得到外消旋体。 6. 机理:反式消除单分子E1机理 双分子E2消除 单分子共轭碱消除Elcb E2机理通式如下: 当连有醇羟基的碳原子与3°C或2°C相连时,酸催化脱水时,会发生E2消除反应成 烯。 ●卤原子离去快慢对反应有影响 RI>RBr>RCl ●必须条件:碳氢键和离去基团(被消除的基团)必须处于反式共平面 分子去对交叉构象,反式消除(被消除的β-H C-H键必须与α-C的p轨道平行,才能形成π键) 分子取重叠构象,顺式消除 ●区域选择性:遵循Zaitsev规则增加碱的强度及体积,得到反Zaitsev产物。 (增大后,空阻较大的β-H不易进攻,进攻酸性强的β-H) E2与SN2反应的并存与竞争: 区别:E2进攻β-H,SN2进攻α-C 试剂亲核性强,碱性弱,体积小时,利于SN2 试剂碱性强,浓度大,体积大,反应温度高时,利于E2. E1消除反应(三级卤代烷在无碱存在时,的消除为E1) E1机理通式如下: ●特征:1.遵循Zaitsev规则 2.E式产物 3.伴有重排产物(用氧化铝或硅酸盐表面脱水, 此反应产物不重排)。 E1与SN1反应的并存与竞争: 离去基团的离去能力,只影响反应速率,而不影响产物比例。 试剂亲核性越强,空阻小,对SN1有利 试剂碱性强,空阻大,对E1有利。 在极性溶剂及没有强碱存在时,主要的取代产物。 机理应用:Wagner-Meerwein重排。机理如下: E2与E1的竞争实质:取决于C-X与C-H的断裂相对速率 若V C-X >V C-H,, 则E1 若 V C-X C-H, 则E2. Elcb单分子共轭碱消除 邻二卤代烷在锌或镁作用下,可失去卤原子生成烯烃。(共平面的反式消除) Zn: C C X X C C X Zn 2+X -碳负离子中间体 C C Mg C C X MgX 中间产物(这种Grignard 试剂很不稳定,很快分解成烯烃) C C Rr Br C C I -:(提供电子) 碘化物与邻二卤代烷的反应(若环状,要求反式共平面)I -应用: 保护双键,或者提纯烯烃 先用Br 2加成,再和碘化物反应,使双键重新出现 总结: 一级卤代烷:一般SN2,强碱存在E2. 二级卤代烷+β位有侧链的一级卤代烷(空阻增大,β-H 增多),减小极性(溶剂) 强亲核试剂存在:SN2 强碱存在:E2 三级卤代烷:无碱存在时 一般情况下 SN1产物增多, 强碱或弱碱存在 E2 取代基空间体积大 E1 有机化学常用网址 作者: llljjj999 发布日期: 2006-4-02 查看数: 99 出自: https://www.360docs.net/doc/f05886277.html, 有机合成: Organic Syntheses(有机合成手册), John Wiley & Sons (免费) https://www.360docs.net/doc/f05886277.html,/ Named Organic Reactions Collection from the University of Oxford (有机合成中的命名反应库) (免费) https://www.360docs.net/doc/f05886277.html,/thirdyearcomputing/NamedOrganicReac... 有机化学资源导航Organic Chemistry Resources Worldwide https://www.360docs.net/doc/f05886277.html,/ 有机合成文献综述数据库Synthesis Reviews (免费) https://www.360docs.net/doc/f05886277.html,/srev/srev.htm CAMEO (预测有机化学反应产物的软件) https://www.360docs.net/doc/f05886277.html,/products/cameo/index.shtml Carbohydrate Letters (免费,摘要) https://www.360docs.net/doc/f05886277.html,/Carbohydrate_Letters/ Carbohydrate Research (免费,摘要) https://www.360docs.net/doc/f05886277.html,/locate/carres Current Organic Chemistry (免费,摘要) https://www.360docs.net/doc/f05886277.html,/coc/index.html Electronic Encyclopedia of Reagents for Organic Synthesis (有机合成试剂百科全书e-EROS) https://www.360docs.net/doc/f05886277.html,/eros/ European Journal of Organic Chemistry (免费,摘要) https://www.360docs.net/doc/f05886277.html,/jpages/1434-193X/ Methods in Organic Synthesis (MOS,有机合成方法) https://www.360docs.net/doc/f05886277.html,/is/database/mosabou.htm Organic Letters (免费,目录) https://www.360docs.net/doc/f05886277.html,/journals/orlef7/index.html Organometallics (免费,目录) https://www.360docs.net/doc/f05886277.html,/journals/orgnd7/index.html Russian Journal of Bioorganic Chemistry (Bioorganicheskaya Khimiya) (免费,摘要) 辽宁大学 英语语言文学考研经验 说起考研很多人在自习室强迫自己从早坐到晚,其实不见得学进去了多少,其实学习的关键还是抓住技巧,要多交流,我刚开始复习的时候high研APP上的师哥师姐给了我很多的帮助。 第一门依然是政治,只能说今年政治我的大题拯救了我,也是比较幸运,背的大题基本都用到了。但是选择题就呵呵哒了,也没有对答案,但是感觉很差。所以政治真的要想拿高分,选择题还是要多刷几遍。而我因为复习的有点晚,在大纲出来后才开始看政治,看得比较慢,看一章做一章的练习,政治新时器最后只有刷一遍的时间,只做一遍题目的话肯定基本就没啥印象,所以基础就没打好。后来导致肖秀荣8套4套卷做的很差,一般选择只有20几分。所以政治有时间还是要多看几遍。当然选择题只刷肖秀荣8套4套是不够的,因为就考试来看肖秀荣老师压中的选择题基本很少,很多都是只压中了题目,我当时还做了考虫的押题4套卷包括大题很多都是背的考虫的押题,可以说压中的还是比较多的。总结政治用到的资料:政治大纲、肖秀荣1000题、肖秀荣8套4套卷。 政治当时我是从红宝书面试后才开始看的,以前从未看过一点。所以政治开始过早只会拖垮其他方面的复习。等红宝书,向今年红宝书快10月份才出,不过依然不晚,前面无需买什么任一、精讲精练之类的书,纯属浪费钱。对于肖的精讲精练我并不推荐,因为在我经过我无数次的对比我发现没人任何书可以取代大纲解析也就是红宝书,任一我扫过一眼,条例确实清晰,但很多内容都没能涉及,看红宝书是让你能全面了解知识,不一定要记住,我是前后看了快4遍,但是什么也没记住,不过会让你不会对每一道题感到陌生。 红宝书出版后要尽快用1个月时间看完一遍,认真看,不过也不必太纠结其中,该理解的理解了就可以。期间用肖1000题来巩固,这时候看完一遍就到11月份了,每天都看政治但不必过多1到1.5个小时就够了,一个小时看40页红宝书,半个小时做第二遍肖1000,期间配合真题,虽然考试内容有很大调整,但是真题的价值远远高于任何资料,这是我的感受,哲学,是靠做真题理解了几乎课本上全部的知识点,毛邓三考真题也记住了大体重点内容。 这个时候看完时间会在11月20号左右。不用急一本巨好无比的资料出现了,不过你无须购买,到论坛里就可以下到《风中劲草核心考点》,不过大家切记,考研政治的风中劲草习题并不推荐,《风中劲草核心考点》200多页,当时我的 第一章绪论 1.价键的形成是原子轨道的重叠(从电子云的角度讲也可以说是电子云相互交盖的结果)或电子配对的结果,如果两个原子都有未成键电子,并且自旋方向相反,就能配对形成共价键。 1.1)共价键形成的基本要点1.成键电子自旋方向必需相反; 2.) 共价键的饱和性,形成八隅体稳定结构;3.)共价键的方向性——成键时,两个电子的原子的轨道发生重叠,而P电子的原子轨道具有一定的空间取向,只有当它从某一方向互相接近时才能使原子轨道得到最大的重叠,生成的分子的能量得到最大程度的降低,才能形成稳定的分子。 2.由于电子云不完全对称而呈极性的共价键叫做极性共价键,可 用箭头表示这种极性键,也可以用δ+、δ-标出极性共价键的带电情况。例 3.★诱导效应产生的原因:成键原子的电负性不同。 4.★诱导效应的传递:逐渐减弱,传递不超过五个原子。 5.★诱导效应的相对强度:一般以电负性的大小作比较 同族元素来说 F > Cl > Br > I 同周期元素来说 - F > -OR > -NR2 不同杂化状态的碳原子来说 –C≡CR >–CR=CR2 > -CR2-CR3 (CH3) 3C– > (CH3)2CH– > CH3CH2– > CH3– 7.以I表示诱导效应, -I吸电子诱导效应,+I推电子诱导效应(具有+I效应的原子团主要是烷基,其相对强度如下: 第二章饱和烃烷烃和环烷烃 1.构造异构体(Constitutional isomerism):分子式相同,分子中原子互相连接的方式和次序不同的异构体。这种构造异构体是由于碳架不同引起的,故又称碳架异构。P25表2-1 构象异构体:分子组成相同,构造式相同,因构象不同而产生的异构体。(构象:指分子中原子或原子团由于围绕s单键的旋转而产生的分子中原子在空间的不同排列. ) 2.普通命名法:用甲乙丙丁戊己庚辛壬癸,数目表示碳原子数目,正/异/新来区别, 甲烷 衍生命名法: 以甲烷为母体,把其他烷烃都看作甲烷的烷基衍生物,一般选择连接烷基最多的碳原子作为母体甲烷 系统命名法;支链烷烃的命名与普通命名法相同,支链看作是直链烷烃的烷基衍生物 3.★系统命名法:若主链上有几种取代基时,应按“次序规则”,较优基团后列出。 常见有机化学方程式归纳 物质类别性质反应方程式 一、烷烃 1、燃烧 CH4 + 2O2CO2 + 2H2O 2、取代反应 CH4 + Cl2CH3Cl + HCl CH3Cl + Cl2CH2Cl2 + HCl(或CH4 + 2Cl2CH2Cl2 + 2HCl) CH2Cl2 + Cl2CHCl3 + HCl(或CH4 + 3Cl2CHCl3 + 3HCl) CHCl3 + Cl2CCl4 + HCl(或CH4 + 4Cl2CCl4 + 4HCl) CH3CH3 + Br2CH3CH2Br + HBr 3、高温分解CH4 C + 2H2↑ 二、烯烃 1、燃烧 C2H4 + 3O22CO2 + 2H2O 2、加成反应 3、加聚反应 4、氧化反应 三、炔烃 1、燃烧 2C2H2 + 5O24CO2 + 2H2O 2、加成反应 四、芳香烃 1、卤代 2、硝化 3、加成 4、氧化 五、醇 1、与活泼金属反应2CH3CH2OH +2 Na2CH3CH2ONa + H2↑ 2、消去反应 3、脱水成醚 4、取代反应 5、氧化 6、酯化反应 六、醛1、氧化 2C2H4O + 5O24CO2 + 4H2O 2、还原 七、酮1、加氢还原 八、羧酸 1、酸性 2CH3COOH + 2Na = 2CH3COONa + H2↑ CH3COOH + NaOH = CHCOONa + H2O 2CH3COOH + Na2CO3 = 2CH3COONa + H2O + CO2↑ CH3COOH + NaHCO3 = CH3COONa + H2O + CO2↑ 2、酯化反应参考醇的性质 九、酯1、水解 十一、卤代烃 1、水解反应 2、消去反应 十二、酚1、弱酸性 重视Wert auf A legen 或多或少mehr oder weniger ……被……(公认为)有……特性etwas gilt jm als etw ……为某人充当/用作……etwas dient jm als etw 打听……sich über A orientieren # Ich habe mich über die Sache orientiert. 遵循……sich an A orientieren # Wir orientieren uns an die Wünsche der Masse. 贯彻,实施sich durchsetzen # Er konnte sich bei seinen Schülern nicht durchsetzen. 视……为……A als A ansehen 某物被视为…… etwas wird als etwas an ge sehen 来自江苏东南部的苏州aus Suzhou im Südosten von Jiangsu kommen 大约Pi und Daumen 转入……auf A übergehen 使……置于……(某种状态)A in A versetzen ……出现/产生etwas stellt sich ein 某人忘记某事etwas entf?llt jm ……从……中得出etwas ergibt sich aus D 以及其他u.a.= und andere 在……期间im Laufe + G (im Laufe des Gespr?chs) 拨错号码sich verw?hlen 通过……表明它的特征etwas ist durch etwas gekennzeichnet/charakterisiert 使某人觉得……jm Adj vorkommen 能胜任某事/匹敌某人D/jm gewachsen sein / in der Lage sein /k?nnen 不仅仅是……;甚至……nicht nur ebenso..., ...sogar... 比某人有……的优势jm an D überlegen sein/ besser als jd sein 按照事实的an der Sache orientiert 来自……;(由……)得知,表明aus D hervorgehen(vi.—sein) 高中化学有机物重要知识笔记 在高中化学课本中,有机化学的特点是知识点较多,有机分子结构复杂,这也是很多学生觉得有机化学难学好的原因。下面是的小编为你们整理的文章,希望你们能够喜欢 高中化学有机物知识 乙炔的制取和性质 1. 反应方程式CaC2 + 2H2OCa(OH)2 + C2H2 2. 此实验能否用启普发生器,为何? 不能. 因为1)CaC2吸水性强,与水反应剧烈,若用启普发生器,不易控制它与水的反应. 2)反应放热,而启普发生器是不能承受热量的.3)反应生成的Ca(OH)2 微溶于水,会堵塞球形漏斗的下端口。 3. 能否用长颈漏斗? 不能. 用它不易控制CaC2与水的反应. 4. 用饱和食盐水代替水,这是为何? 用以得到平稳的乙炔气流(食盐与CaC2不反应) 5. 简易装置中在试管口附近放一团棉花,其作用如何? 防止生成的泡沫从导管中喷出. 6. 点燃纯净的甲烷、乙烯和乙炔,其燃烧现象有何区别? 甲烷淡蓝色火焰; 乙烯: 明亮火焰,有黑烟乙炔: 明亮的火焰,有浓烟. 7. 实验中先将乙炔通入溴水,再通入KMnO4(H+)溶液中,最后点燃,为何? 乙炔与空气(或O2)的混合气点燃会爆炸,这样做可使收集到的乙炔气纯净,防止点爆. 8. 乙炔使溴水或KMnO4(H+)溶液褪色的速度比较乙烯,是快还是慢,为何? 乙炔慢,因为乙炔分子中叁键的键能比乙烯分子中双键键能大,断键难. 高中化学有机物重要知识 一、煤的干馏 1. 为何要隔绝空气?干馏是物理变化还是化学变化?煤的干馏和木材的干馏各可得哪些物质? 有空气氧存在,煤将燃烧.干馏是化学变化. 煤焦油粗氨水木焦油 煤的干馏可得焦炉气木材的干馏可得木煤气焦碳木炭 2. 点燃收集到的气体,有何现象?取少许直试管中凝结的液体,滴入到紫色的石蕊试液中,有何现象,为什么? 此气体能安静地燃烧,产生淡蓝色火焰.能使石蕊试液变蓝,因为此液体是粗氨水,溶有氨,在水中电离呈碱性. 二、乙酸乙酯的制取 1. 反应方程式CH3COOH + CH3CH2OH --浓H2SO4,加热CH3COOCH2CH3 + H2O 2. 盛装反应液的试管为何应向上倾斜45角? 液体受热面积最大. 有机化学常用网址整理 http://www.chem.ucalgary.ca/courses/351/Carey5th/Carey.html https://www.360docs.net/doc/f05886277.html,/iupac/nomenclature/ On-Line Learning Center "Organic Chemistry" 5th ed. by Francis A. Carey IUPAC Nomenclature of Organic Chemistry 有机合成: Organic Syntheses(有机合成手册), John Wiley & Sons (免费) https://www.360docs.net/doc/f05886277.html,/ Named Organic Reactions Collection from the University of Oxford (有机合成中的命名反应库) (免费) https://www.360docs.net/doc/f05886277.html,/thirdyearcomputing/NamedOrganicReac... 有机化学资源导航Organic Chemistry Resources Worldwide https://www.360docs.net/doc/f05886277.html,/ 有机合成文献综述数据库Synthesis Reviews (免费) https://www.360docs.net/doc/f05886277.html,/srev/srev.htm CAMEO (预测有机化学反应产物的软件) https://www.360docs.net/doc/f05886277.html,/products/cameo/index.shtml Carbohydrate Letters (免费,摘要) https://www.360docs.net/doc/f05886277.html,/Carbohydrate_Letters/ Carbohydrate Research (免费,摘要) https://www.360docs.net/doc/f05886277.html,/locate/carres Current Organic Chemistry (免费,摘要) https://www.360docs.net/doc/f05886277.html,/coc/index.html Electronic Encyclopedia of Reagents for Organic Synthesis (有机合成试剂百科全书e-EROS) https://www.360docs.net/doc/f05886277.html,/eros/ European Journal of Organic Chemistry (免费,摘要) https://www.360docs.net/doc/f05886277.html,/jpages/1434-193X/ Methods in Organic Synthesis (MOS,有机合成方法) https://www.360docs.net/doc/f05886277.html,/is/database/mosabou.htm Organic Letters (免费,目录) https://www.360docs.net/doc/f05886277.html,/journals/orlef7/index.html Organometallics (免费,目录) https://www.360docs.net/doc/f05886277.html,/journals/orgnd7/index.html Russian Journal of Bioorganic Chemistry (Bioorganicheskaya Khimiya) (免费,摘要) http://www.wkap.nl/journalhome.htm/1068-1620 Russian Journal of Organic Chemistry (Zhurnal Organicheskoi Khimii) (免费,摘要) http://www.maik.rssi.ru/journals/orgchem.htm 同济大学 英语语言文学考研经验 考研的日子是我大学四年过的最充实,最像个大学学生的时光。记得准备复试的时候,和别人说,不想回忆这段日子,因为我经历了什么,只有我自己知道。这一路走来非常感谢high研APP里同学们的支持和帮助,谢谢大家了。 备考的时候,走了不少弯路,如今写出来,希望能成为一盏小小路灯,有些许用处。 首先,政治。 8月下旬出大纲之后,买了政治新时器,边看边做笔记,配套1000题,风中劲草出来后,加上风中劲草。政治新时器看了三遍,很细到细到粗。同样的,1000题和真题做了3遍。风中劲草大概是10月才出来,那时候开始背专业课了,主要背诵的时间也用在专业课上了,所以2遍没背完。不过我看政治新时器时做的笔记很有用,练习的时候小题基本上38+。11月,时事政治小册子出来,每天抽时间看看,我没花时间去特意记忆。不得不说,今年肖四肖八很给力,押题押的挺神。记得要看,大题要背。熟记。 今年考试顺也不顺,第一天考试,前天晚上失眠。哦,准确的说,我失眠了两个多月,花了半个月调整,也没调整过来。睡了3个小时后去考试,政治和德语,觉得没发挥出应有水平。很失望,但考试就是这样,不论原因。毕竟,心态也是其中一部分。 其二: 二外,德语。 德语,是很难的。。同济的德语,更难。考新编大学德语四本书。本人觉得,123很重要,4是属于鸡肋。也有人说3也没必要看,但是,3里面有很多语法,个人觉得需要看。234属于自学,大三下因为意外,在家待了一学期,德语2没办法上课,只能自己看。刚开始看,抱着词典一点点查,每天基本会花一下午的时间看德语。而且进度很慢。我还买了外研社的黄皮书,德语语法,仔细做一遍还挺有用,34的配套练习,大四大六的习题册。大六的习题册中句型改写感觉很好,要把握好。习题册中的句型改写和翻译,记得好好写,很有用。我还背了大六的作文范文,虽然没考到,但也用到了一些句子。哦,我还买了圣才的德语二外真题,里面的小题一定要细看,最好把考到的,或者是你经常错的知识点和表达记下来,错题本还是挺有用的。 第三: 综合英语。 Chap 11 醛、酮、醌 一、命名 ● 普通命名法:醛:烷基命名+醛 酮:按羰基所连接两个羟基命名 Eg : ● 系统命名法: 醛酮:以醛为母体,将酮的羰基氧原子作为取代基,用“氧代”表示。也 可以醛酮为母体,但要注明酮的位次。 二、结构:C :sp 2 三、醛酮制法: ● 伯醇及仲醇氧化脱氢:(P382) RCH 2OH RCHO RCOOH 及时蒸出 1 醇 醛 酸 。[O]:KMnO 4K 2Cr 2O 7+H 2SO 4CrO 3+吡啶CrO 3+醋酐 丙酮-异丙醇铝等 、 、、、。2 醇 酮 R --?OH R -C -R'? O 氧化到醛、酮,不破坏双键 氧化到醛、酮 通用,氧化性强, 须将生成的醛及时蒸出 ● 羰基合成:合成多一个碳的醛 CH 2=CH 2 + CO CH 3CH 2CHO ]CH 2-CH 2C O 2 ● 同碳二卤化物水解:制备芳香族醛、酮 甲乙酮 CH 3CCH 2CH 3O CH 3CH 2CH 2CHO CH 3CHCH 2CHO CH 3CH 3-C-CH=CH 2O 正丁醛异戊醛 甲基乙烯基酮 CHO 苯甲醛C-CH 3O 苯乙酮 C-O 二苯甲酮 CH 3CHCH 2CHO 3 CH 3CH 2-C-CH-CH 3 O CH 34 3-甲基丁醛2-甲基-3-戊酮β-甲基丁醛 12 3 4 5 苯基丙烯醛3-CH=CH-CHO (肉桂醛)3 2 1 32 1 CH 3CH=CHCHO CH-CHO CH 32-丁烯醛苯基丙醛2-CH 3C-CH 2-CCH 3O O β-戊二酮 戊二酮 2,4-(巴豆醛) 1234苯基丙醛 α- 8大高考状元化学复习笔记分享 王龙(北京大学计算机科学技术系学生,江西省高考理科状元): 化学被称为理科中的文科。题目量较多,单题分较少,因此波动性不大,比之数、理较为稳定。它需要识记许多内容,包括基本知识、元素及其单质、化合物性质、基本解题方法等,皆具有某些文科的特点。但它也具有相当的灵活性,如物质推断题中,你好像看到一个摩术师在向你展示其技艺而你不知其所以然。我的化学老师说,学习化学要首先对各物质性质非常熟悉,因为一些题(如物质推断题)并不能用逻辑推理方式,由果推因,只能由一些特征现象“猜”出物质或元素,这就需要对知识很熟悉。在熟悉的基础上要分门别类,列出知识框表,当然这就要求能深刻理解各个概念,否则分类就没有明确标准。就这样一个框套一个框,许多小体系组成若干中体系,再结合,直至整个体系。如我通常用元素周期表来形成最基本框架,下面细分,哪些族氧化能力强,哪些物质可作半导体……同时记住一些特殊现象,如CuSO4 和H2S可生成H2SO4,用弱酸H2S产生强酸。这方面内 容一般老师都会讲,而且比我清楚得多,最好能向老师讲教。胡湛智(北京大学生命科学学院学生,贵州省高考理科状元): 化学大概是大家感觉比较好的科目,它和数学、物理一样,页 1 第 要把听课、钻研课本、做习题有机地结合起来。化学中有几个板块:基本理论、元素化合物、电化学、有机化学等。我认为学好化学要注意多记、多用、多理解,化学题重复出现的概率比较大,重要题型最好能在理解的基础上记住,许多化学反应的特征比较明显,记牢之对于解推断题将会有很大帮助。在平时多做题时要注意总结很多有用的小结论,并经常用一用,这在高考时对提高速度有很大帮助。高考化学试题中选择题占87分之多,因此多解、快解选择题是取得好分数的致胜因素。如何才能做得快呢?这就需要你从大量解题的训练中找出一些小窍门来。举一个简单的例子:45克水蒸气和4.4克二氧化碳混合后气体的平均分子量为多少?①45.1,②17.2,③9,④19。如果拿到题马上开始算,大约要2~3分钟,如果你用上自己的小窍门,注意到该混和气体的平均分子量只能在18~44之间,那你可只用二秒钟时间就选出正确答案。类似这样的小窍门还很多,希望大家多留心,注意寻找用熟,迅速提高模考分数。 另外,学好复习好化学并在考试中取胜的一个经验是学会“猜”。这种“猜”实际上是一种层次较高的推断,要有一定的基础,做的题多了熟能生巧,自然会获得一种“灵感”,自己可以创造“猜”法,因为它是你勤劳学习的结晶,不是 常用的有机化学网站 2008-06-01 19:10 | (分类:默认分类) 有机合成: Organic Syntheses(有机合成手册), John Wiley & Sons (免费) https://www.360docs.net/doc/f05886277.html,/ Named Organic Reactions Collection from the University of Oxford (有机合成中的命名反应库) (免费) https://www.360docs.net/doc/f05886277.html,/thirdyearcomputing/NamedOrganicReac... 有机化学资源导航Organic Chemistry Resources Worldwide https://www.360docs.net/doc/f05886277.html,/ 有机合成文献综述数据库Synthesis Reviews (免费) https://www.360docs.net/doc/f05886277.html,/srev/srev.htm CAMEO (预测有机化学反应产物的软件) https://www.360docs.net/doc/f05886277.html,/products/cameo/index.shtml Carbohydrate Letters (免费,摘要) https://www.360docs.net/doc/f05886277.html,/Carbohydrate_Letters/ Carbohydrate Research (免费,摘要) https://www.360docs.net/doc/f05886277.html,/locate/carres Current Organic Chemistry (免费,摘要) https://www.360docs.net/doc/f05886277.html,/coc/index.html Electronic Encyclopedia of Reagents for Organic Synthesis (有机合成试剂百科全书e-EROS) https://www.360docs.net/doc/f05886277.html,/eros/ European Journal of Organic Chemistry (免费,摘要) https://www.360docs.net/doc/f05886277.html,/jpages/1434-193X/ Methods in Organic Synthesis (MOS,有机合成方法) https://www.360docs.net/doc/f05886277.html,/is/database/mosabou.htm Organic Letters (免费,目录) https://www.360docs.net/doc/f05886277.html,/journals/orlef7/index.html Organometallics (免费,目录) https://www.360docs.net/doc/f05886277.html,/journals/orgnd7/index.html Russian Journal of Bioorganic Chemistry (Bioorganicheskaya Khimiya) (免费,摘要) http://www.wkap.nl/journalhome.htm/1068-1620 Russian Journal of Organic Chemistry (Zhurnal Organicheskoi Khimii) (免费,摘要) http://www.maik.rssi.ru/journals/orgchem.htm Science of Synthesis: Houben-Weyl Methods of Molecular Transformation https://www.360docs.net/doc/f05886277.html,/ Solid-Phase Synthesis database (固相有机合成) https://www.360docs.net/doc/f05886277.html,/chem_db/sps.html Synthetic Communications (免费,摘要) https://www.360docs.net/doc/f05886277.html,/servlet/product/productid/SCC SyntheticPages (合成化学数据库) (免费) 基础有机化学 (邢其毅版) 2011年上海医工院考研笔记整理姓名:庄守群 有机化学理论部分基础知识点 1.保里不相容原理 原子轨道理论 2.能量最低原理 (基态) 3.洪特规则 1.自旋反向平行规则 价键理论 2.共价键的饱和性 3.共价键的方向性 激发态 4.能量相近轨道形成杂化轨道 1.能量相近 分子轨道理论 2.电子云最大重叠 3.对称性相同 规范性示例 化学反应的基本模式:A 试剂 溶剂条件B 补充知识点 Lewis酸的三种类型: Lewis碱的三种类型: 第三章:立体化学 1.无对称面 1.分子手性的普通判据 2.无对称中心 3.无S4 反轴 注:对称轴Cn不能作为判别分子手性的判据 2. 外消旋体(dl体或+/-体)基本概念 1.绝对构型与相对构型 2.种类:外消旋化合物/混合物/固体溶液 基本理论非对映体 差向异构体端基差向异构体内消旋体(meso-)e.g 酒石酸 举例名词解释可能考察的:相对/绝对构型对映体/非对映体外消旋体潜不对称分子/原手性分子差向异构体 3.立体异构部分 ⑴含手性碳的单环化合物: 判别条件:一般判据 无S 1 S 2 S 4 相关:构象异构体ee aa ea ae 构象对映体 主要考查:S 1=对称面的有无 相关实例:1.1,2-二甲基环己烷 1,3二甲基环己烷 1,4二甲基环己烷 ⑵含不对称原子的光活性化合物 N 稳定形式 S P 三个不同的基团 ⑶含手性碳的旋光异构体 丙二烯型旋光异构体 1.狭义c c c 条件:a b 两基团不能相同 2.广义:将双键看成环,可扩展一个或两个c c c 联苯型旋光异构体 (阻转异构现象- 少有的由于单键旋转受阻而产生的异构体) B A a b 构型命名方法:选定一环,大基团为1,小基团为2.另一环,大集团为3,将其小基团转到环后最远处。 ⑷含手性面的旋光异构体 分子内存在扭曲的面而产生的旋光异构体,e.g 六螺苯 4.外消旋化的条件 ⑴若手性碳易成碳正离子、碳负离子、碳自由基等活性中间体,该化合物极易外消旋化。 ⑵若不对称碳原子的氢是羰基的-H ,则在酸或碱的作用下极易外消旋化。 含多个不对称碳原子时,若只有其中一个碳原子易外消旋化,称差向异构化。 5.外消旋化的拆分 化学法 酶解法 晶种结晶法 柱色谱法 不对称合成法: 1.Prelog 规则—一个分子得构象决定了某一试剂接近分子的方向,这二者的关联成为Prelog 规则. 2.立体专一性:即高度的立体选择性 《有机化学基础》知识点整理 一、重要的物理性质 1.有机物的溶解性 (1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。 (2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。(它们都能与水形成氢键)。 (3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。④有的淀粉、蛋白质可溶于水形成胶体 ..。蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。 2.有机物的密度 (1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂) (2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯 3.有机物的状态[常温常压(1个大气压、20℃左右)] (1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态 ②衍生物类:一氯甲烷( ...2.F.2.,.沸点为 ...-.29.8 .. ....CCl ....℃) .....CH..3.Cl..,.沸点为 ...-.24.2 ....℃) ..氟里昂( 氯乙烯( ....,.沸点为 ...HCHO ...-.21..℃) .. ...-.13.9 ....CH..2.==CHCl ..甲醛( ......,.沸点为 ....℃) 氯乙烷( ..一溴甲烷(CH3Br,沸点为3.6℃) ....℃) ...12.3 ....CH..3.CH..2.Cl..,.沸点为 四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃) 甲乙醚(CH3OC2H5,沸点为10.8℃)环氧乙烷( ,沸点为13.5℃) (2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。如,己烷CH3(CH2)4CH3环己烷甲醇CH3OH 甲酸HCOOH 溴乙烷C2H5Br 乙醛CH3CHO 溴苯C6H5Br 硝基苯C6H5NO2 ★特殊:不饱和程度高的高级脂肪酸甘油酯,如植物油脂等在常温下也为液态 (3)固态:一般N(C)在17或17以上的链烃及高级衍生物。如,石蜡、C17以上的烃 饱和程度高的高级脂肪酸甘油酯,如动物油脂在常温下为固态 ★特殊:苯酚(C6H5OH)、苯甲酸(C6H5COOH)、氨基酸等在常温下亦为固态 4.有机物的颜色 ☆绝大多数有机物为无色气体或无色液体或无色晶体,少数有特殊颜色,常见的如下所示: ☆三硝基甲苯(俗称梯恩梯TNT)为淡黄色晶体; ☆部分被空气中氧气所氧化变质的苯酚为粉红色; ☆ 2,4,6—三溴苯酚为白色、难溶于水的固体(但易溶于苯等有机溶剂); ☆苯酚溶液与Fe3+(aq)作用形成紫色[H3Fe(OC6H5)6]溶液; ☆多羟基有机物如甘油、葡萄糖等能使新制的氢氧化铜悬浊液溶解生成绛蓝色溶液; ☆淀粉溶液(胶)遇碘(I2)变蓝色溶液; 2016中国矿业大学英语语言文学考研经验 今天收拾东西,清理考研战场,看着那一摞摞的“书山”,想起几个月前的拼搏,终于还是决定要写点什么,希望能给由于各种原因选择考矿大英语语言文学专业的朋友们提供一点帮助,使他们少走一点弯路。顺便,为我们专业刷点存在感。 首先晒晒初试分:政治72,德语(二外)95,基础英语112,专业英语(英美文学)132,总分411 下面先说说择校,再谈初试经验,复试嘛,个人认为,只要初试考好了,基本没有问题。 一、择校相关 报考矿大的挑战性 可能许多朋友选择矿大是因为感觉它比较好考,确实,从报录比上看竞争是没有一些文科强势的高校激烈。但从试卷上看,真的没有大多数人以为的那样容易,有些地方甚至非常有挑战性。 比如,基础英语题型是:一篇改错,四篇阅读选择题,20题英美文化选择和判断正误(某年出过填空),几题判断修辞题,还有4-5题翻译理论简答题,然后是英汉互译,每篇三四百字,最后还有一篇五六百字的作文。简答、翻译、写作都是要大量写字的,耗时都不低,但考试时间只有两个小时,写得慢的话光简答就差不多半小时下去了,更别提前面还有阅读理解。 我是第二次考研。之前看过大多数高校能找到的试卷,除了矿大,就没有把翻译和写作弄到一张试卷上折磨人的。(写作是500字哦。) 再比如,专业英语(文学)最主要的题目是选段评论,做过这种题型的朋友们都知道吧,它是非常考基础考水平的。好在选段下面会给出作者和出处。 拿我自己来说,去年我曾经历过一次考研失败,考的是魔都某校,调剂很辛酸,当然也失败了。在继续考研和稳定下来工作之间犹豫良久,最终还是因为不甘心坚持了。现在想想,那一年虽然失败,确实让我积累了许多经验教训,专业上也打下了基础,不然今年初试,尤其是文学肯定考不了这么好。 所以如果选择矿大,消减了一些心理负担的同时,也必须做好准备,踏踏实实的学习,否则,是绝不可能考上的。(除非英语基础文学基础二外基础都非常非常好,不过如果那样的话,您确定不考上外么?) 难度问题讲完了,下面说说报考矿大的优势吧。 第一,基础英语除了10分的改错,没有其他语法、搭配、词汇等基础题,主考能力和参考书上的内容。非常适合英语基础不好,但强于阅读翻译,或者有决心有毅力拼搏几个月的朋友。反观某些文科强势的高校(以上外为例),其基础英语对语法搭配词汇等等的考查深度,真心不是半年的突击所能搞定的。 第二,复试非常公平,非常良心,良心到基本不改变初试排名。老师们都特别和蔼可亲。刷的人也很少。我是那种经常面试崩的人,口语也不太好,本以为总分排名肯定会下滑的,没想到保持原样了。 第三,同学们都很优秀。这次统考进入复试12人,考到四百分以上或略低于四百的就有四五个。 第四,所有的自主出题的试卷都能买到。在矿大文昌校区研究生院后面的小山坡上(先到研究生院上二楼,从后门出去就到了)有一家打印社。 第五,徐州消费水平低算不算? 总之,欢迎优秀学子踊跃报考矿大哦。 高中有机化学知识点归纳和总结(完整版) 一、同系物 结构相似,在分子组成上相差一个或若干个CH 2原子团的物质物质。 同系物的判断要点: 1、通式相同,但通式相同不一定是同系物。 2、组成元素种类必须相同 3、结构相似指具有相似的原子连接方式,相同的官能团类别和数目。结构相似不一定完全相同, 如CH 3CH 2CH 3和(CH 3)4C ,前者无支链,后者有支链仍为同系物。 4、在分子组成上必须相差一个或几个CH 2原子团,但通式相同组成上相差一个或几个CH 2原子 团不一定是同系物,如CH 3CH 2Br 和CH 3CH 2CH 2Cl 都是卤代烃,且组成相差一个CH 2原子团,但不是同系物。 5、同分异构体之间不是同系物。 二、同分异构体 化合物具有相同的分子式,但具有不同结构的现象叫做同分异构现象。具有同分异构现象的化合物互称同分异构体。 1、同分异构体的种类: ⑴ 碳链异构:指碳原子之间连接成不同的链状或环状结构而造成的异构。如C 5H 12有三种同分异 构体,即正戊烷、异戊烷和新戊烷。 ⑵ 位置异构:指官能团或取代基在在碳链上的位置不同而造成的异构。如1—丁烯与2—丁烯、 1—丙醇与2—丙醇、邻二甲苯与间二甲苯及对二甲苯。 ⑶ 异类异构:指官能团不同而造成的异构,也叫官能团异构。如1—丁炔与1,3—丁二烯、丙 烯与环丙烷、乙醇与甲醚、丙醛与丙酮、乙酸与甲酸甲酯、葡萄糖与果糖、蔗糖与麦芽糖等。 ⑷ 其他异构方式:如顺反异构、对映异构(也叫做镜像异构或手性异构)等,在中学阶段的信 息题中屡有涉及。 各类有机物异构体情况: ⑴ C n H 2n +2:只能是烷烃,而且只有碳链异构。如CH 3(CH 2)3CH 3、CH 3CH(CH 3)CH 2CH 3、C(CH 3)4 ⑵ C n H 2n :单烯烃、环烷烃。如CH 2=CHCH 2CH 3、 CH 3CH=CHCH 3、CH 2=C(CH 3)2、 、 ⑶ C n H 2n -2:炔烃、二烯烃。如:CH ≡CCH 2CH 3、CH 3C ≡CCH 3、CH 2=CHCH=CH 2 ⑷ C n H 2n -6:芳香烃(苯及其同系物) 、 ⑸ C n H 2n +2O :饱和脂肪醇、醚。如:CH 3CH 2CH 2OH 、CH 3CH(OH)CH 3、CH 3OCH 2CH 3 CH 2—CH 2 CH 2—CH 2 CH 2 CH 2—CH —CH 3 CH 3 CH 3 CH 3 3 CH 3 CH 3 催化剂 加热、加压 有机化学知识点归纳 一、有机物的结构与性质 1、官能团的定义:决定有机化合物主要化学性质的原子、原子团或化学键。 2、常见的各类有机物的官能团,结构特点及主要化学性质 (1)烷烃 A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4 B) 结构特点:键角为109°28′,空间正四面体分子。烷烃分子中的每个C 原子的四个价键也都如此。 C) 物理性质:1.常温下,它们的状态由气态、液态到固态,且无论是气体还是液体,均为无色。 一般地,C1~C4气态,C5~C16液态,C17以上固态。 2.它们的熔沸点由低到高。 3.烷烃的密度由小到大,但都小于1g/cm^3,即都小于水的密度。 4.烷烃都不溶于水,易溶于有机溶剂 D) 化学性质: ①取代反应(与卤素单质、在光照条件下) , ,……。 ②燃烧 ③热裂解 C 16H 34 C 8H 18 + C 8H 16 ④烃类燃烧通式: O H 2 CO O )4(H C 222y x y x t x +++????→?点燃 ⑤烃的含氧衍生物燃烧通式: O H 2 CO O )24(O H C 222y x z y x z y x +-+ +????→?点燃 E) 实验室制法:甲烷:3423CH COONa NaOH CH Na CO +→↑+ 注:1.醋酸钠:碱石灰=1:3 2.固固加热 3.无水(不能用NaAc 晶体) 4.CaO :吸水、稀释NaOH 、不是催化剂 (2)烯烃: A) 官能团: ;通式:C n H 2n (n ≥2);代表物:H 2C=CH 2 B) 结构特点:键角为120°。双键碳原子与其所连接的四个原子共平面。 C) 化学性质: CH 4 + Cl 2CH 3Cl + HCl 光 CH 3Cl + Cl 2 CH 2Cl 2 + HCl 光 CH 4 + 2O 2 CO 2 + 2H 2O 点燃 CH 4 C + 2H 2 高温 隔绝空气 C=C 原子:—X 原子团(基):—OH 、—CHO (醛基)、—COOH (羧基)、C 6H 5— 等 化学键: 、 —C ≡C — C=C 官能团 CaO △ 中国矿业大学 ——英语语言文学 考研心路 本人报考的是中国矿业大学英语语言文学,下面先说说择校,再谈初试经验,复试嘛,个人认为,只要初试考好了,基本没有问题。 一、择校相关 可能许多朋友选择矿大是因为感觉它比较好考,确实,从报录比上看竞争是没有一些文科强势的高校激烈。但从试卷上看,真的没有大多数人以为的那样容易,有些地方甚至非常有挑战性。 比如,基础英语题型是:一篇改错,四篇阅读选择题,20题英美文化选择和判断正误(某年出过填空),几题判断修辞题,还有4-5题翻译理论简答题,然后是英汉互译,每篇三四百字,最后还有一篇五六百字的作文。简答、翻译、写作都是要大量写字的,耗时都不低,但考试时间只有两个小时,写得慢的话光简答就差不多半小时下去了,更别提前面还有阅读理解。 我是第二次考研。之前看过大多数高校能找到的试卷,除了矿大,就没有把翻译和写作弄到一张试卷上折磨人的。(写作是500字哦。) 再比如,专业英语(文学)最主要的题目是选段评论,做过这种题型的朋友们都知道吧,它是非常考基础考水平的。好在选段下面会给出作者和出处。 拿我自己来说,去年我曾经历过一次考研失败,调剂很辛酸,当然也失败了。在继续考研和稳定下来工作之间犹豫良久,最终还是因为不甘心坚持了。现在想想,那一年虽然失败,确实让我积累了许多经验教训,专业上也打下了基础,不然今年初试,尤其是文学肯定考不了这么好。 所以如果选择矿大,消减了一些心理负担的同时,也必须做好准备,踏踏实实的学习,否则,是绝不可能考上的。(除非英语基础文学基础二外基础都非常非常好,不过如果那样的话,您确定不考上外么?) 难度问题讲完了,下面说说报考矿大的优势吧。 第一,基础英语除了10分的改错,没有其他语法、搭配、词汇等基础题,主考能力和参考书上的内容。非常适合英语基础不好,但强于阅读翻译,或者有决心有毅力拼搏几个月的朋友。反观某些文科强势的高校(以上外为例),其基础英语对语法搭配词汇等等的考查深度,真心不是半年的突击所能搞定的。 第二,复试非常公平,非常良心,良心到基本不改变初试排名。老师们都特有机化学常用网址
2021辽宁大学英语语言文学考研参考书真题经验
江南大学有机化学期末考试复习笔记
常见有机化学方程式归纳
德语笔记
高中化学有机物重要知识笔记
有机化学网站大集锦
2021同济大学英语语言文学考研参考书真题经验
大学有机化学2笔记整理
8大高考状元化学复习笔记分享
有机化学常用网站
有机化学笔记整理
(完整版)有机化学基础知识点整理打印版
2016中国矿业大学英语语言文学考研经验
高中有机化学知识归纳和总结(完整版)
有机化学知识点总结归纳(全)
2021中国矿业大学英语语言文学考研参考书真题经验
