2019华南师范化学与环境学院硕士研究生复试及拟录取情况汇总表
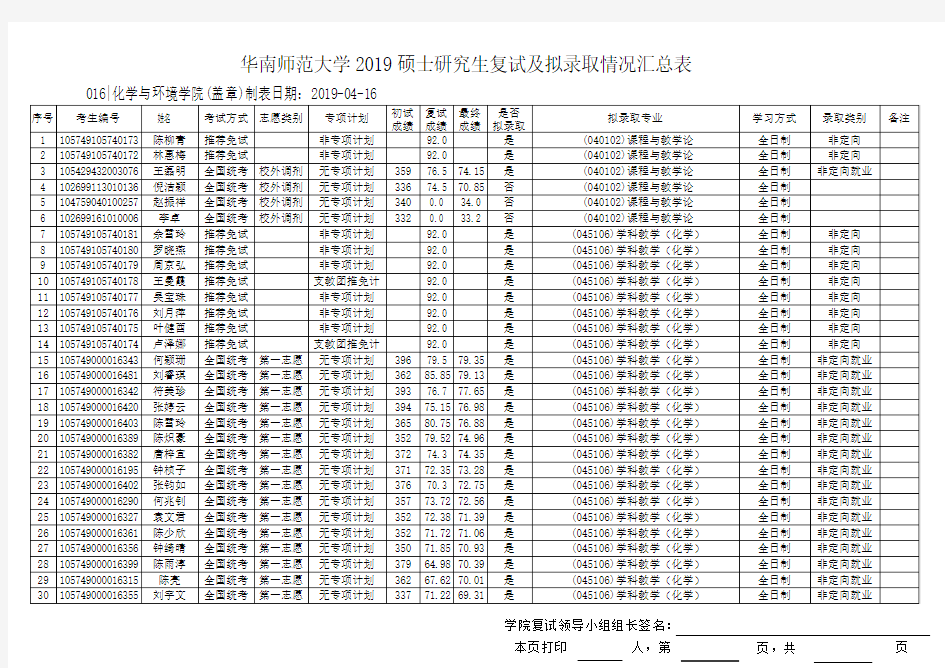
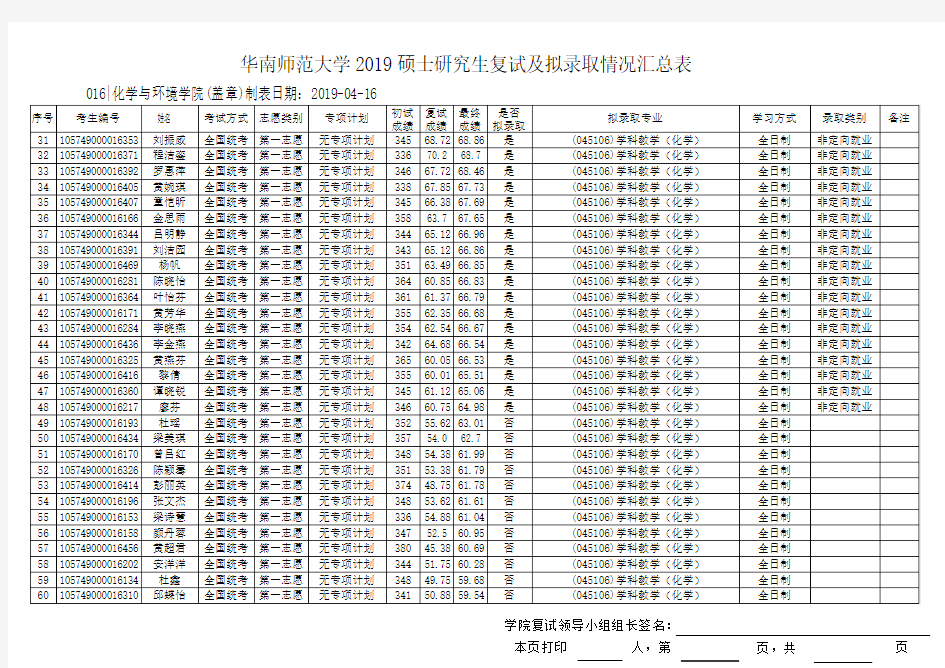
学院复试领导小组组长签名:
学院复试领导小组组长签名:
学院复试领导小组组长签名:
学院复试领导小组组长签名:
学院复试领导小组组长签名:
学院复试领导小组组长签名:
学院复试领导小组组长签名:
学院复试领导小组组长签名:
2017年华南理工大学 951有机化学、无机化学基础 硕士研究生考试大纲及参考书目
951有机化学、无机化学基础知识考试大纲 一、 考试目的 《有机化学、无机化学基础知识》作为全日制生物医学工程专业硕士学位入学考试的专业课考试,其目的是考察考生是否具备进行生物医学工程硕士学习所要求的化学知识。 二、考试的性质与范围 该考试是一种测试应试者单项能力的考试,考试范围包括考生应具备的有机化学和无机化学等方面的技能。 三、考试基本要求 1. 具有化学方面的基础知识 2. 熟悉化学问题的分析,以及实验的设计 四、考试形式 该考试为闭卷考试 五、考试内容(或知识点) 有机化学 1.有机化合物的命名、顺反及对映异构体命名、个别重要化合物的俗名和英文缩写。 2.有机化合物的结构、共振杂化体及芳香性,同分异构与构象。 3.诱导效应、共轭效应、超共轭效应、空间效应、小环张力效应、邻基效应、氢键的概念及上述效应对化合物物理与化学性质的影响。 4.主要官能团(烯键、炔键、卤素、硝基、氨基、羟基、醚键、醛基、酮羰基、羧基、酯基、氰基、磺酸基等)的化学性质及他们之间相互转化的规律。 5.烷烃、脂环烃、烯烃、炔烃、卤代烃、醇、酚、醚、醛、酮、不饱和醛酮、羧酸、羧酸及其衍生物、丙二酸酯、β-丙酮酸酯、氨基酸、硝基化合物、胺、腈、偶氮化合物、磺酸、简单杂环化合物、单糖等的制备、分离、鉴定、物理性质、化学性质及在合成上的应用。 6.常见有机化合物的波谱(红外、核磁) 7.饱和碳原子上的自由基取代,亲核取代,芳环上的亲电与亲核取代,碳碳重键的亲电、自由基及亲核加成,消除反应,氧化反应(烷烃、烯烃、炔烃、醇、醛、芳烃侧链的氧化、烯炔臭氧化及Cannizzaro反应),还原反应(不饱和烃、芳烃、醛、酮、羧酸、羧酸衍生物、硝基化合物、腈的氢化还原及选择性还原反应),缩合反应(羟醛缩合、Claisen缩合、Caisen-Schmidt缩合、Perkin缩合),降级反应(Hofmann 降解,脱羧),重氮化反应,偶合反应,重排反应(频那醇重排、Beckmann重排、Hofmann 重排)的历程及在有机合成中的应用。 8.碳正离子、碳负离子、自由基、苯炔的生成与稳定性及其有关反应的规律。能够从中间体稳定性来判断产物结构。 无机化学
北京师范大学、华中师范大学、南京师范大学无机化学教研室《无机化学》笔记和课后习题详解(下册)卤 素【
第14章卤素 一、选择题 1.下述氟化物溶解度由小变大规律正确的是()。 【答案】A 2.下列氟化物中,属于非离子型的化合物是()。 【答案】A 3.将离子氧化成应选用的氧化剂为()。 【答案】C 4.下列各组物质相互作用,溶液出现蓝色现象的是()。A.将Cl2气通入淀粉与KI的混合溶液中 B.淀粉溶液与饱和氯水混合 C.淀粉溶液与KI溶液混合 D .淀粉溶液与浓混合 【答案】A 5.下列性质递变规律不正确的是()。 A .离子半径 B.电子亲和能F>Cl>Br>I
C.电负性F>Cl>Br>I D .离子的水合热(绝对值) 【答案】B 6.氯气中毒时,可吸入的解毒剂是()。 A.乙醚与乙醇的混合蒸气 B.水蒸气与乙醇的混合蒸气 C.乙醚与氧气的混合气体 D.乙醚蒸气 【答案】A 7 .在常温下,与NaOH作用生成产物正确的是()。A.Cl2生成NaClO和NaCl B.Cl2生成NaClO3和NaCl C.Br2生成NaBr和NaBrO D.I2生成NaI和NaIO 【答案】A 8.下列含氧酸酸根在酸性条件下,氧化性强弱顺序正确的是()。 【答案】C 9.下列酸的酸性强弱顺序正确的是()。
【答案】A 10.氢氟酸可以贮存于铜、铅等金属制造的容器中,其原因是()。A.氢氟酸在金属表面上形成了一层致密的氟化物薄膜,可防止金属进一步腐蚀B.在金属表面上形成了一层氧化物薄膜,可保护金属免受腐蚀 C.氢氟酸本身是弱酸,对金属无腐蚀性 D.氢氟酸不与以上金属发生反应 【答案】A 11.实验室中制取少量HBr,不能采用的方法是()。 A.KBr固体与浓硫酸作用 B.KBr固体与浓磷酸作用 C.作用 D.红磷与混合后滴加 【答案】A 12.主要用于火柴、焰火的是()。 【答案】C 13.下列反应中不属于氧化还原反应的是()。
2019年华南师范大学文学院708 +808真题回忆
2019年华南师范大学文学院708 +808真题回忆808文学史: 一、简答题.(40分) 1.《诗经》中关于战争描写的特点 2. 3.曹禺的戏剧创作艺术特色 4.你对鲁迅的小说有什么分析(大概意思) 二、论述题(40分) 1.结合具体作品分析曹植的写作风格及其原因 2.分析张爱玲的创作,并说明她对海内外作家创作的影响(大概意思) 三、古文阅读(35分) 一、《左忠毅公逸事》 1.断句:5分 一日使史更敝衣草屦背筐手长镵为除不洁者引入微指左公处 2.翻译:8分 久之,闻左公被炮烙,旦夕且死;持五十金,涕泣谋于禁卒,卒感焉。 3.分析古文中的人物形象,8分还是10分。 还有一题忘记了 三、诗歌阅读 《浣溪沙·簌簌衣巾落枣花》 宋·苏轼 簌簌衣巾落枣花, 村南村北响缲车。 牛衣古柳卖黄瓜。 酒困路长惟欲睡, 日高人渴漫思茶。 敲门试问野人家。 1.诗中描绘了什么?(大概意思) 2.谈谈你对“日高人渴漫思茶”的理解(大概) 3.为什么“敲门试问野人家‘’?(大概) 四、现代文阅读(35分) 《断章》 卞之琳 你站在桥上看风景, 看风景的人在楼上看你。 明月装饰了你的窗子, 你装饰了别人的梦。
1.分析写作特点(大概) 2.忘了,和第一题差不多,反正就是鉴赏 3.请你根据诗中的描绘设计一幅图画或者小话剧,或者微电影(10分) (我的内心os:这道题真的好坑(?︿?)) 708汉语基础 古代汉语 一、写出下列字的小篆或者其他古字形,并指出其属于六书中的哪一种(12分)亦,叔,朝,面,(还有两个忘记了) 二、名词解释 1.《说文解字》 2.使动用法 3.平水韵 4.破读 三、给出一些句子 分析“以” 的性质,用法或者含义 分析“是‘’的性质,用法或者含义。 指出下面的押韵,如果有合韵,指出合韵。 《诗经·静女》 自牧归荑,洵美且异。匪女之为美,美人之贻。 四、古文阅读(等我想起来再补充) 无非就是宾语前置,翻译这些,通论都有 现代汉语 一、分析下面发音,指出错误并且分析原因 zing jǚ chuen 二、分析词性 持续,继续突然,猛然 三、分析构词法(写出小类) 改革健儿 四、指出下面句子修辞手法(每句有两种) 五、指出下面复句的类型 1.要么……要么…… 2.读好写好,他的作文就会写好(大概) 六、分析借喻和借代的异同
物理化学试验-华南理工大学
物理化学实验Ⅰ 课程名称:物理化学实验Ⅰ 英文名称:Experiments in Physical Chemistry 课程代码:147012 学分:0.5 课程总学时:16 实验学时:16 (其中,上机学时:0) 课程性质:?必修□选修 是否独立设课:?是□否 课程类别:?基础实验□专业基础实验□专业领域实验 含有综合性、设计性实验:?是□否 面向专业:高分子材料科学与工程、材料科学与工程(无机非金属材料科学与工程、材料化学) 先修课程:物理、物理化学、无机化学实验、有机化学实验、分析化学实验等课程。 大纲编制人:课程负责人张震实验室负责人刘仕文 一、教学信息 教学的目标与任务: 该课程是本专业的一门重要的基础课程,物理化学实验的特点是利用物理方法来研究化学系统变化规律,是从事本专业相关工作必须掌握的基本技术课程。其任务是通过本课程的学习,使学生达到以下三方面的训练: (1)通过实验加深学生对物理化学原理的认识,培养学生理论联系实际的能力; (2)使学生学会常用的物理化学实验方法和测试技术,提高学生的实验操作能力和独立工作能力; (3)培养学生查阅手册、处理实验数据和撰写实验报告的能力,使学生受到初步的物理性质研究方法的训练。 教学基本要求: 物理化学实验的特点是利用物理方法来研究化学系统变化规律,实验中常用多种物理测量仪器。因此在物理化学实验教学中,应注意基本测量技术的训练及初步培养学生选择和配套仪器进行实验研究工作的能力。 物理化学实验包括下列内容: (1)热力学部分量热、相平衡和化学平衡实验是这部分的基本内容。还可以选择稀溶液的依数性、溶液组分的活度系数或热分析等方面的实验。
2019华南师范大学学科教学(语文)考研333教育综合与902语文课程与教学论测验真题试卷与真题答案
2019华南师范大学学科教学(语文)考研333教育综合与902语文课程与教学论测验真题试卷与真题答案
————————————————————————————————作者:————————————————————————————————日期:
2019华南师范大学学科教学(语文)考研333教育综合与902语文课程与教学论考试真题试卷与真题答案 《华南师范大学902语文课程与教学论考研真题(2011-2018年)》 2018年华南师范大学902语文课程与教学论考研真题(回忆版) 2017年华南师范大学902语文课程与教学论考研真题(回忆版) 2016年华南师范大学902语文课程与教学论考研真题(回忆版) 2015年华南师范大学902语文课程与教学论考研真题(回忆版) 2014年华南师范大学902语文课程与教学论考研真题(回忆版) 2013年华南师范大学902语文课程与教学论考研真题(回忆版) 2012年华南师范大学902语文课程与教学论考研真题(回忆版) 2011年华南师范大学902语文课程与教学论考研真题(回忆版)《2019华师考研333教育综合复习全析(含历年真题答案,共
九册)》 《2019华南师范大学考研333教育综合复习全析(含历年真题答案,共九册)》由鸿知华师考研网依托多年丰富的教学与辅导经验,与该专业课优秀研究生合作汇编而成。全书内容紧凑权威细致,编排结构科学合理,为参加2019华南师范大学考研的考生量身定做的必备专业课资料。 《2019华南师范大学考研333教育综合复习全析(含历年真题答案)》全书编排根据: 《教育学(王道俊)》 《当代教育心理学(修订版)(陈琦、刘儒德)》 《中国教育史(孙培青)》 《简明中国教育史(王炳照)》 《外国教育史(张斌贤)》 《外国教育史教程(吴式颖)》 《教育心理学(张大均)》 结合提供的往年华师考研真题内容及答案解析,帮助报考华南师范大学硕士研究
北京师范大学、华中师范大学、南京师范大学无机化学教研室《无机化学》(第4版)-模拟试题(上册)
第四部分模拟试题 说明:参照北京师范大学、华中师范大学、南京师范大学无机化学教研室主编的《无机化学》(第4版)教材,根据各高校历年考研真题的命题规律及热门考点精心编写了1套考前模拟试题,并提供详尽、标准解答。通过模拟试题的练习,学员既可以用来检测学习该考试科目的效果,又可以用来评估对自己的应试能力。 北京师范大学、华中师范大学、南京师范大学无机化学教研室《无机化学》(第4版)配套 模拟试题及详解 一、选择题(每题3分,共30分) 1.下列说法正确的是()。 A.玻尔半径指的是电子离氢原子核的距离 B.玻尔半径指氢原子半径 C.玻尔半径是指电子云密度最大处离核的距离 D.玻尔半径是指电子出现几率最大处离核的距离 【答案】D 【解析】电子轨道不是固定的、机械的。电子出现几率最大处离核的距离称作玻尔半径。 2.关于氢原子的4s和4p轨道能量的高低,正确的是()。 A. B.
C. D.不能确定 【答案】C 【解析】H原子中只有一个电子,在4s和4p轨道上没有电子,就没有核内质子对4s 和4p的作用,不存在能量大小;若H原子的电子跃迁,将不存在屏蔽作用,能量大小由主量子数n决定。n相同的轨道的能量相同,因而4s和4p轨道的能量相等。 3.下列关于化学键的说法正确的是()。 A.原子之间的相互作用都是化学键 B.只有在相邻的两个原子之间才能形成化学键 C.化学键就是原子间的吸引作用 D.化学键包括原子间相互吸引和相互排斥两方面的强烈作用 【答案】D 【解析】原子之间有各种作用,只有这种作用导致形成分子时才是化学键;金属键、离子键均不一定是由相邻的两个原子间形成的,整体是一个大化学键,不相邻的原子间也可形成化学键;化学键是原子核内质子对其他原子核外电子的吸引及两核内质子、各自的核外电子相互排斥的强烈作用的总和。 4.下列关于离子键的说法正确的是()。 A.当两种元素的电负性差值大于1.7时,形成化合物的化学键是离子键 B.离子晶体中的离子键就是一个正离子和一个负离子之间的静电引力 C.离子键键能的大小与离子半径、离子电荷有关
华南理工大学 本科物理化学复习笔记
本科物理化学复习提纲(I) (华南理工大学物理化学教研室葛华才,2004年6月) 第一章气体 一.一.重要概念 理想气体,分压,分体积,临界参数,压缩因子,对比状态 二.二.重要关系式 (1) 理想气体:pV=nRT , n = m/M (2) 分压或分体积:p B=c B RT=p y B (3) 压缩因子:Z = pV/RT 第二章热力学第一定律与热化学 一、重要概念 系统与环境,隔离系统,封闭系统,(敞开系统),广延量(加和性:V,U,H,S,A,G),强度量(摩尔量,T,p),功,热,内能,焓,热容,状态与状态函数,平衡态,过程函数(Q,W),可逆过程,节流过程,真空膨胀过程,标准态,标准反应焓,标准生成焓,标准燃烧焓 二、重要公式与定义式 1. 体积功:δW= -p外dV 2. 热力学第一定律:?U = Q+W,d U =δQ +δW 3.焓的定义:H=U + pV 4.热容:定容摩尔热容C V,m = δQ V /dT = (?U m/?T )V 定压摩尔热容C p,m = δQ p /dT = (?H m/?T )P 理性气体:C p,m- C V,m=R;凝聚态:C p,m- C V,m≈0 理想单原子气体C V,m =3R/2,C p,m= C V,m+R=5R/2 5. 标准摩尔反应焓:由标准生成焓?f H Bθ (T)或标准燃烧焓?c H Bθ (T)计算 ?r H mθ = ∑v B?f H Bθ (T) = -∑v B?c H Bθ (T) 6. 基希霍夫公式(适用于相变和化学反应过程) ?r H mθ(T2)= ?r H mθ(T1)+?2 1 T T?r C p,m d T 7. 恒压摩尔反应热与恒容摩尔反应热的关系式
华南理工大学《物理化学》48学时试卷(B)参考答案
《物理化学》48学时试卷(B)参考答案 2012.6 一、选择题(10题,每题2分,共20分) 1.A 2.B 3.C 4. B 5. B 6.C 7.B 8.B 9.B 10. D 10.初始浓度降低,半衰期增加,可否定为0,1级反应。假设为2级反应,则有k=1/(c A,0t1/2),实验结果符合这个关系式,故为2级 二、计算题(6题,共60分) 1.解:(1)ΔU=ΔH=0 (2分) Q R=W R=nRT ln(p1/p2)=228.9 J (2分) ΔS=nR ln(p1/p2)=0.763 J·K-1(2分) ΔA=ΔG= -nRT ln(p1/p2)= -228.9 J (2分) (2)状态函数的变化同(1) ΔU=ΔH=0 (1分) ΔA=ΔG= -228.9 J (2分) ΔS=0.763 J·K-1(1分) Q IR=W IR=p2(V2-V1)=nRT(1-p2/p1)=149.9 J (2分) 2. 解:解:△H= △H1+ △H2+ △H3= nC p,m,l(T2-T1) + n△H凝固+ nC p,m,s(T1-T2) = 5×[(75.3-37.6) (273.15-268.15) -6009 ] J = -5820.5 J (4分) △S= △S 1+ △S 2+ △S 3= nC p,m,l ln(T2/T1) + n(△H2/T2) + nC p,m,s ln(T1/T2) = n[(C p,m,l-C p,m,s) ln(T2/T1) + (△H2/T2) ] = 5×[(75.3-37.6) ln(273.15/268.15) +(-6009/273.15) ] J·K-1 = -21.3 J·K-1 (4 分) △G= △H- T△S = -5820.5J-268.15K×(-21.3 J·K-1) = -108.36 J (2 分) 3. 解:设苯、甲苯分别记为A、B。 (1)苯在85℃时的饱和蒸气压p A*,利用克-克方程 ln(p A*/101.325kPa)= -(30770/8.315)(1/358.15-1/353.25) (4分) p A*=116.9kPa (1分)
【华南理工大学2012年考研专业课真题】无机化学2012
866 华南理工大学 2012年攻读硕士学位研究生入学考试试卷(请在答题纸上做答,试卷上做答无效,试后本卷必须与答题纸一同交回) 科目名称:无机化学 适用专业:无机化学;物理化学
9. 在BF 3分子中,B 采取 杂化,其几何构型为 ;在离子中,B 采取 4BF ? 杂化,其几何构型为 。 10. 在氢原子的激发态中,4s 和3d 状态的能量高低为E 4s E 3d ;在Ca 原子中,能量高低为E 4s E 3d ;在Cr 原子中,能量高低为E 4s E 3d 。 三、完成并配平下列化学反应方程式(每题2 分,共12 分。过程不写) (1)Na 2S 2O 3 + I 2 ?→? (2)HgCl 2 + SnCl 2 (过量) ?→? (3)PbO 2 + HCl ?→? (4)BCl 3 + H 2O ?→? (5) + 4MnO ? 23 SO ? + H + ?→?(6)NaCrO 2 + H 2O 2 + NaOH ?→? 四、问答题 1. (6 分)已知:E \ (Hg 2+/Hg ) = 0.92 V ,E +22\ (Hg /Hg) = 0.80 V ,E + 22\ (Ag +/Ag) = 0.79 V 。 (1) 写出Hg 的歧化反应,以及由该反应组成的原电池的符号; + 22 (2) 写出Hg 2+ 与Ag 作用的反应方程式。 2. (8 分)试用四种试剂,把含有BaCO 3、AgCl 、SnS 和CuS 四种固体混合物一一溶解分离,每一种试剂只可溶解一种固体物质,并指明溶解次序。 3. (4分)AlF 3的沸点高达1563K ,AlCl 3在456K 就开始升化。试加以解释。 4. (6 分)实验测得[Co(NH 3)6]Cl 3具有反磁性,试用价键理论推断该配合物中心离子的杂化类型、空间构型和配合物类型(内轨型或外轨型);并用晶体场理论说明其中心离子d 电子的排布方式。
华南理工大学物理化学物理化学复习纲要(完整整理版)
物理化学复习提纲 (华南理工大学物理化学教研室葛华才) 第一章气体 一.重要概念 理想气体,分压,分体积,临界参数,压缩因子,对比状态 二.重要关系式 (1) 理想气体:pV=nRT , n = m/M (2) 分压或分体积:p B=c B RT=p y B (3) 压缩因子:Z = pV/RT 第二章热力学第一定律与热化学 一、重要概念 系统与环境,隔离系统,封闭系统,(敞开系统),广延量(加和性:V,U,H,S,A,G),强度量(摩尔量,T,p),功,热,内能,焓,热容,状态与状态函数,平衡态,过程函数(Q,W),可逆过程,节流过程,真空膨胀过程,标准态,标准反应焓,标准生成焓,标准燃烧焓 二、重要公式与定义式 1. 体积功:W= -p外dV 2. 热力学第一定律:U = Q+W,d U =Q +W 3.焓的定义:H=U + pV 4.热容:定容摩尔热容 C v ,m = Q V /dT = (U m/T )V 定压摩尔热容 C p ,m = Q p /dT = (H m/T )P 理性气体:C p,m- C v,m=R;凝聚态:C p,m- C v,m≈0 理想单原子气体C v,m =3R/2,C p,m= C v,m+R=5R/2 5. 标准摩尔反应焓:由标准生成焓 f H B (T)或标准燃烧焓 c H B (T)计算 r H m = v B f H B (T) = -v B c H B (T) 6. 基希霍夫公式(适用于相变和化学反应过程) ?r r r=?r r r r(r1)+∫?r r r,r r2 r1 rr 7. 恒压摩尔反应热与恒容摩尔反应热的关系式 Q p -Q v = r H m(T) -r U m(T) =v B(g)RT 8. 理想气体的可逆绝热过程方程: p 1V 1 ?= p 2 V 2 ?,p 1 V 1 /T1 = p2V2/T2,?=C p,m/C v,m 三、各种过程Q、W、U、H的计算1.解题时可能要用到的内容 (1) 对于气体,题目没有特别声明,一般可认为是理想气体,如N 2,O 2 ,H 2 等。 恒温过程d T=0,U=H=0,Q=W 非恒温过程,U = n C v,m T,H = n C p,m T 单原子气体C v ,m =3R/2,C p,m = C v,m+R = 5R/2 (2) 对于凝聚相,状态函数通常近似认为只与温度有关,而与压力或体积无关,即 U≈H= n C p,m T
华南理工大学期末考试《 物理化学》下学期考试试卷B卷
《 》试卷第 1 页 共 4 页 华南理工大学期末考试 《 物理化学》试卷 1. 考前请将密封线内填写清楚; 所有答案请直接答在试卷上(或答题纸上); .考试形式:闭卷; 选择题(每题2分,共20分) 原电池是指: ( ) (A)将电能转换成化学能的装置 (B) 将化学能转换成电能的装置 (C) 可以对外作电功的装置 (D)对外作电功同时从环境吸热的装置 电解金属盐的水溶液时, 在阴极上 : ( ) (A) 还原电势愈正的粒子愈容易析出 (B) 还原电势与其超电势之代数和愈正的粒子愈容易析出 (C) 还原电势愈负的粒子愈容易析出 (D) 还原电势与其超电势之和愈负的粒子愈容易析出 LiCl 的无限稀释摩尔电导率为 115.03×10-4 S ·m 2·mol -1,在 298 K 时,测得 LiCl 稀溶液中 Li + 的迁移数为 0.3364,则 Cl - 离子的摩尔电导率 λm (Cl -)为: ( ) (A) 76.33×10-4 S ·m 2·mol -1 (B) 113.03×10-4 S ·m 2·mol -1 (C) 38.70×10-4 S ·m 2·mol -1 (D) 76.33×102 S ·m 2·mol -1 有一ZnCl 2水溶液,m =0.002 mol ·kg -1 ,γ±=0.83,则a ±为: ( ) (A) 1.66×10-3 (B) 2.35×10-3 (C) 2.64×10-3 (D) 2.09×10-4 对于反应 2NO 2= 2NO + O 2,当选用不同的反应物和产物来表示反应速率时,其 ( ) (A) -2d[NO 2]/d t = 2d[NO]/d t = d[O 2]/d t (B) - d[NO 2]/2d t = d[NO]/2d t = d[O 2]/d t = d ξ /d t (C) - d[NO 2]/d t = d[NO]/d t = d[O 2]/d t
华南师范大学2019-2020学期大学城互选课程安排表.doc
华南师范大学2019-2020(1)学期大学城互选课程安排表 课程介绍: 1、 课程名称:营养与健康 开课学院:体育科学学院 任课教师: 朱玲,女,运动人体科学激光运动医学方向博士、华南师范大学体育科学学院运动人体科学副教授。2002年于华南师范大学生命科学学院获生
物教育学学士学位;2002-2003年在第四军医大学全军重点实验室学习;2005年于华南师范大学生命科学学院获得生理学硕士学位;2008年于华南师范大学体育科学学院获得运动人体科学博士学位。自2008年起在华南师范大学任教。 主讲全日制本科生专业课程《运动生物化学与运动营养学》、《健康教育与健康促进》,曾担任《运动生理学》、《运动生物化学》、《运动解剖学》、《体育保健学》等课程的教学工作。开设有网络课程《营养与健康》,每学期选修学生300人。获华南师范大学2010“为了明天”中青年教师课堂教学比赛三等奖;2012年获学生选为体育科学学院最喜爱的理论课老师之一。 科研方面,在激光生物医学研究方面具有良好的研究经验,利用物理、化学、生物、医学等方面的跨学科学习,参与研究低强度激光对猪和人中性粒细胞呼吸爆发的影响、对PC12细胞凋亡的抑制作用,AD光疗,细胞增殖内稳态等研究工作。在国内外杂志上发表科研论文若干,参加国内国际会议多次做口头报告并获奖。 学分/学时:2/34 课程简介: 课程定位:本课程是一门理论性和实用性较强的课程,通过本课程的学习,使学生增强健康教育学与营养学方面的理论知识,学会运用这些知识改善人群健康的技能。 课程目标:营养与健康是营养学的一个分支,是研究营养与人体健康关系的学科,本课程要求学生系统地学习和掌握营养学的基础知识和基本理论,熟悉食品营养价值和人群营养的评价方法,认识和了解我国居民的膳食特点和营养状况,会运用营养学理论解决实际营养与健康问题。 教学内容和学时安排:
华南理工大学攻读硕士学位研究生入学无机化学试卷
866 华南理工大学 2008年攻读硕士学位研究生入学考试试卷 (请在答题纸上做答,试卷上做答无效,试后本卷必须与答题纸一同交回) 科目名称:无机化学 适用专业:无机化学,物理化学,应用化学
(B) 在恒容条件下,通入一定量的氮气 (C) 在恒压条件下,通入一定量的氮气 (D) 在恒压条件下,通入一定量的水蒸气 6. 二氧化氮溶解在NaOH 溶液中可得到( ) (A) NaNO 2和H 2O (B) NaNO 2,O 2和H 2O (C) NaNO 3,N 2O 5和H 2O (D) NaNO 3,NaNO 2和H 2O 7. 下列反应不可能按下式进行的是( ) (A) 2NaNO 3 + H 2SO 4(浓)Na ?→?2SO 4 + 2HNO 3 (B) 2NaI + H 2SO 4(浓)Na ?→?2SO 4 + 2HI (C) CaF 2 + H 2SO 4(浓)CaSO ?→?4 + 2HF (D) 2NH 3 + H 2SO 4?→?(NH 4)2SO 4 8. 在K[CoCl 4(NH 3)2]中,Co 的氧化数和配位数分别是( ) (A) +2和4 (B) +2和6 (C) +3和6 (D) +3和4 9. 按酸碱质子理论,在水溶液中既可作酸亦可作碱的物质是( ) (A) (B)NH (C) Cl HCO 3? 4+ ? (D) H 3O + 10. Cr(VI)在碱性介质中的存在形成是( ) (A) 橙色的227Cr O ? (B) 黄色的227Cr O ? (C) 橙色的 (D) 黄色的 CrO 42?CrO 42? 11. K sp \ (AgCl) = 1.8 × 10 ?10,K sp \ (Ag 2CrO 4) = 2.0 × 10 ?12。在含Cl ? 和浓度均 为0.3 mol·L CrO 42??1的溶液中,加AgNO 3应是( ) (A) AgCl 先沉淀,Cl ? 和CrO 能完全分离开 42? (B) AgCl 先沉淀,Cl ? 和不能完全分离开 CrO 42?
无机化学》习题解析和答案
1、教材 《无机化学》北京师范大学、华中师范大学、南京师范大学无机化学教研室编,高等教育出版社,2002年8月第4版。 2、参考书 《无机化学》北京师范大学、华中师范大学、南京师范大学无机化学教研室编,高等教育出版社,1992年5月第3版。 《无机化学》邵学俊等编,武汉大学出版社,2003年4月第2版。《无机化学》武汉大学、吉林大学等校编,高等教育出版社,1994年4月第3版。 《无机化学例题与习题》徐家宁等编,高等教育出版社,2000年7月第1版。 《无机化学习题精解》竺际舜主编,科学出版社,2001年9月第1版 《无机化学》电子教案 绪论(2学时) 第一章原子结构和元素周期系(8学时) 第二章分子结构(8学时) 第三章晶体结构(4学时) 第四章配合物(4学时) 第五章化学热力学基础(8学时) 第六章化学平衡常数(4学时)
第七章化学动力学基础(6学时) 第八章水溶液(4学时) 第九章酸碱平衡(6学时) 第十章沉淀溶解平衡(4学时) 第十一章电化学基础(8学时) 第十二章配位平衡(4学时) 第十三章氢和稀有气体(2学时) 第十四章卤素(6学时) 第十五章氧族元素(5学时) 第十六章氮、磷、砷(5学时) 第十七章碳、硅、硼(6学时) 第十八章非金属元素小结(4学时) 第十九章金属通论(2学时) 第二十章s区元素(4学时) 第二十一章p区金属(4学时) 第二十二章ds区元素(6学时) 第二十三章d区元素(一)第四周期d区元素(6学时) 第二十四章d区元素(二)第五、六周期d区金属(4学时) 第二十五章核化学(2学时) 1.化学的研究对象 什么是化学 ●化学是研究物质的组成、结构、性质与变化的一门自然科学。(太宽泛)●化学研究的是化学物质(chemicals)。 ●化学研究分子的组成、结构、性质与变化。
华南理工大物理化学学期末考试
,考试作弊将带来严重后果! 华南理工大学期末考试 《物理化学》(48、56、64学时)试卷(B) 1. 考前请将密封线内填写清楚; 2. 所有答案请直接答在试卷上; 3.考试形式:闭卷; 选择题.(每题2分,10题共20分) 1. 已知反应CO(g)+1/2O2(g) →CO2(g) 的焓变为△H,下列说法中何者是不正确? A. △H是CO2(g) 的生成焓 B. △H是CO(g)的燃烧焓 C. △H是负值 D. △H与反应△U的数值不等 2. 室温下,10 p O-的理想气体绝热节流膨胀至5p O-的过程有: (1) W < 0 ;(2) T1> T2;(3) Q = 0 ;(4) △S > 0 A. (3)、(4) B. (2)、(3) C. (1)、(3) D. (1)、(2) 3. 反应N2(g) + 3H2(g) = 2NH3(g) 可视为理想气体间反应,在反应达平衡后,若维持系 A. K pθ不变,平衡时N2和H2的量将增加,而NH3的量减少 B. K pθ不变,且N2,H2,NH3的量均不变 C. K pθ不变,平衡时N2和H2的量将减少,而NH3的量增加 D. K pθ 增加,平衡时N2和H2的量将减少,NH3的量增加 4. 298K时A和B两种气体在某一溶剂中溶解的享利系数分别为k A和k B,且知k A>k B,A和B压力相同时,在该溶剂中所溶解的量是( ) A. A的量大于B的量 B. A的量小于B的量 C. A的量等于B的量 C. A的量与B的量无法比较 5. NH4HS(s) 和任意量的NH3(g) 及H2S(g) 达平衡时有( ) A. C = 2,P = 2,F = 2; B. C = 1,P = 2,F = 1;
华南师范国际文化学院2019硕士研究生复试及拟录取情况汇总表
华南师范大学 2019 硕士研究生复试及拟录取情况汇总表
序号
1 2 3 4 5 6 7 8 9
10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31
022|国际文化学院(盖章)制表日期:2019-04-013
考生编号
姓名
考试方式 志愿类别
专项计划
初试 复试 最终 成绩 成绩 成绩
105749000001741
郜然 全国统考 第一志愿 无专项计划 328 67.35 66.48
101419321507021
刘晨 全国统考 校外调剂 无专项计划 326 81.0 73.1
103199411921269 王晨旭 全国统考 校外调剂 无专项计划 337 73.0 70.2
100279218041275
郑娜 全国统考 校外调剂 无专项计划 335 70.625 68.81
105749000007445 周俊伶 全国统考 第一志愿 无专项计划 390 83.85 80.925
105749000007212 黄小宛 全国统考 第一志愿 无专项计划 411 76.0 79.1
105749000007288 朱柏帆 全国统考 第一志愿 无专项计划 382 81.55 78.98
105749000007294
张静 全国统考 第一志愿 无专项计划 378 81.55 78.58
105749000007458 李文洁 全国统考 第一志愿 无专项计划 405 74.85 77.925
105749000007287 张延杰 全国统考 第一志愿 无专项计划 387 78.05 77.73
105749000007318
张莉 全国统考 第一志愿 无专项计划 383 78.05 77.33
105749000007229 熊雅雯 全国统考 第一志愿 无专项计划 365 81.35 77.18
105749000007248 孙悦青 全国统考 第一志愿 无专项计划 383 77.75 77.18
105749000007336 卢雪怡 全国统考 第一志愿 无专项计划 376 79.15 77.18
105749000007314
向茜 全国统考 第一志愿 无专项计划 373 79.65 77.13
105749000007319
王蝶 全国统考 第一志愿 无专项计划 379 78.0 76.9
105749000007416 王丽萍 全国统考 第一志愿 无专项计划 364 80.45 76.63
105749000007380 邬艳丽 全国统考 第一志愿 无专项计划 380 76.55 76.28
105749000007432 牛婉琳 全国统考 第一志愿 无专项计划 373 77.9 76.25
105749000007333 庄嘉宁 全国统考 第一志愿 无专项计划 366 79.25 76.23
105749000007359
何蕾 全国统考 第一志愿 无专项计划 366 79.25 76.23
105749000007277 禹文杰 全国统考 第一志愿 无专项计划 364 79.1 75.95
105749000007227 甘佳美 全国统考 第一志愿 无专项计划 373 76.45 75.53
105749000007299
潘越 全国统考 第一志愿 无专项计划 368 77.4 75.5
105749000007309
陈卓 全国统考 第一志愿 无专项计划 377 75.2 75.3
105749000007222 张锶皓 全国统考 第一志愿 无专项计划 370 76.35 75.18
105749000007255 王晨希 全国统考 第一志愿 无专项计划 363 76.9 74.75
105749000007272 李秋月 全国统考 第一志愿 无专项计划 367 76.0 74.7
105749000007305 李婷婷 全国统考 第一志愿 无专项计划 358 77.75 74.68
105749000007235 静铭铭 全国统考 第一志愿 无专项计划 384 72.05 74.43
105749000007285
李培 全国统考 第一志愿 无专项计划 366 75.45 74.33
是否 拟录取
是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是 是
拟录取专业
(040102)课程与教学论 (040102)课程与教学论 (040102)课程与教学论 (040102)课程与教学论 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育 (045300)汉语国际教育
学院复试领导小组组长签名:
本页打印
人,第
学习方式
全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制 全日制
录取类别 备注
非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 加 10 分 非定向就业 非定向就业 非定向就业 非定向就业 加 10 分 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 加 10 分 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业 非定向就业
页,共
页
2018年华南理工大学研究生入学考试专业课真题866_无机化学
. \ 866 华南理工大学 2018 年攻读硕士学位研究生入学考试试卷 ( 试卷上做答无效 ,请在答题纸上做答 ,试后本卷必须与答题纸一同交回) I ./ 8.一·般同族元素的金属性随着原子序数的增加而增强 ,下列各族中例外的是 ( (A) IVA (B) IA (C) IB (D) VIA 9.与波函数视为同义语的是( 科目名称 :无机化学 适用专业 :无机化学 :物理化学 共 5 页 (A ) 概率密度 (B ) 电子云 (C ) 原子轨道 (D ) 原子轨道的角度分布图 10.首先对原子结构提出核模型的科学家是 ( )。 一、选择题 ( 每题 2 分 ,共 60 分) 1.在同一容器中充入下列气体各 1.0 克,其中分压最大的物质是 ( )。 (A ) 汤姆生 ( Thomson ) (C) 莫塞莱 ( Mosely ) (B ) 卢瑟福 ( Rutherford ) (D ) 查德威克 ( Chadwick ) (A) C02 . (B) 02 (C) Ne (D) N2 2.平衡系统 :2Cl2(g ) 十 2H20(g ) 件 4HCl(g) + 02(g )中 。保持温度和体积不变 ,通入惰 1 1.·F 列各元素的原子排列中 ,电负性减少顺序正确的是( (A) K>Na>Li (B) O>Cl>H (C) As>P>H (D) Cr>N>Hg 性气体 ,则 HCI 的量( )。 (A ) 增加 (B )不变 (C) 减少 (D )不能确定 3.某基元反应 A + B →D 的 Ea C 正) = 600 KJ·mor1 , Ea ( 逆) =150 ,则反应的 L'l,H8m 12.一基态原子的第五电子层只有 2 个电子 ,贝IJ 亥i 为( )。 原子的第四电子层上的电子数可能 (A) 8 (B) 18 (C) 8-18 (D) 18-32 是( 13.某元素 X 的逐级电离能 ( KJ·mor1 ) 分别为 740 、1500、7700 、10500、13000、18000、 (A) 450 KJ·mor ' (B) -450 KJ·mor1 (C) 750 KJ·mor' (D) 375 KJ·mor' 4月HAc C K8α l.75x l0-5 ) 和 NaAc 溶液配制 pH=4.50 的缓冲溶液 ,c(HAc)/c(NaAc)= 21700 。当它们与氯反应时最可能生成的阳离子是 ( (A) X+ (B) X2+ (C) x3+ (D) X 4+ (A) 1.55 (B) 0.089 (C) 1.80 (D) 0.89 14.下列物质极化率最大的是 ( (A) F2 (C) Br2 5.将 AgCl 和 Ag !的饱和恪浓的清液混合 ,在其中加入 AgN03 固体,将会( (A ) 只有 AgCI 沉淀 (8) 只有 Ag !沉淀 (C) AgCI. Agl 都沉淀 ,以AgCI 为主 (D) AgCI. Ag !都沉淀 ,以 A g !为主 6. 己知 25°C 时,E\Cu2+/Cu+) = 0.159 Y, E8(Cu+/Cu) = 0.515 V ,则反应 2Cu + 件 Cu2+ 十 Cu 的标准平衡常数 Ke = ( )。 (A) 2.02×106 (8) 1.06×1012 (C) 9.69x 10-7 (D) 1.03×106 15. r 司核双原子分子中 ,两个原子的能级相近的 p 轨道可能组成的分子轨道数是 (A) 2 (8) 3 (C) 4 (D) 6 16.ABm 分子中有 p-p π 键存在 ,则原子 A 必定不能采取下列杂化中的是( (A) sp3 (8) sp2 (C ) sp (D ) 不等性 sp2 17.S 凹的几何形状为( )。 7.某元素的原子最外层只有两个 l=O 的电子,该元素在周期表中必定不属于( (A ) 正四面体 (B ) 四1J 锥 (C) 平面正方形 (D ) 变形四面体 (A) s 区元素 (8) ds 区元素 (C) d 区元素 (D) p 区元素 18.下列离子晶体中 ,正、负离子的配位数都是 8 的是( 第 l 页 第 2 页 、、、,/ D 、,L C ‘、 ,,,, R U /,、、、
华南理工大学物理化学考研心得
华南理工大学物理化学考研心得 考研心得总结1 准备考研是一个比较艰难的阶段,因为一方面这是一个打持久战的过程,另一方面这又是一个锻炼自己毅力和心态的时刻.对于准备考研的人来说,确定考研方向很重要。先确定考研的方向,对自己的能力,自己未来的出路要有清楚的认识.确定一个适合自己的院校,千万不要目标过高,这样很容易导致考研失败。一旦确定了方向,就可以利用网络资料,从该方向全国排名以及每年的录取比例等方面做一个全面的了解。根据自己的实际情况确定报考的学校和专业,此阶段大家都比较迷茫,不用盲目确定报考学校,因为确定方向后,大体所考的专业科目差不多。如果你还没有定下考研方向,那么可以先从基础课开始复习,一边复习基础课一边确定报考方向;如果你已经确定考试方向,就可以给自己列一个大体计划按照计划完成任务即可。 考研复习过程中要始终保持一种积极乐观的心态,不要给自己太大的压力,更不要和别人比,也切忌和自己比。每天给自己制定一个小计划,不断地鼓励自己,每天进步一点点。考研的战线拉的太长的话,那么在后面的时间里,就会松懈掉,没有当初的斗志.所以不用那么早就开始准备.战线过长是会影响毅力,但是只要你在准备的过程中合理安排,就不会出现这个情况.我认为复习时一定要讲究效率和方法,不要打疲劳的时间战和死记硬背,这样
不但使自己很累,而且长此以往让自己失去了学习的乐趣。每天保证6个小时高效率的学习。学习累了,可以去锻炼一下身体,打一下乒乓球,缓解一下紧张的思维,再回去开始学习,这样效率很高。复习的环境也很重要,尽量避开人多的地方,让自己全心身地投入到复习中。同时也可以找一个志同道合的考研同伴,一起互相监督鼓励。要注意身体,考研是持久战,好身体才是革命的本钱,要注意及时补充能量,保证良好的睡眠,才能保证第二天有很好的学习效率。 我参加了考研政治辅导课程,对于政治的复习有很大的帮助。辅导班的老师可以很系统的把整个教材熟悉一遍,让你捋清楚政治的大体框架,同时分清重点难点。让你大体上对政治考试心里有个数。还有辅导老师所讲解一些解题技巧答题方法也是比较受用的。今年押题部分五道大题全部命中,所以只要好好复习,成功是很容易的。平时复习政治的时候,单选题范围大,灵活,所以要多做所选题练兵,通过做题掌握理解政治方面的知识点。大题的话只要平时熟悉那些基本知识点,学会用政治语言答题,政治一般不会有太大问题。同时注意每年发生的热点问题,结合政治理论分析。所以政治报了班,只要把课上的内容学习好,要塌实全面掌握基础知识,学会学活,这样无论遇到怎样的题都能应付自如。 考研心得总结2
