由废铝箔制备硫酸铝

由废铝箔制备硫酸铝
一、目的要求
1. 了解用铝制备硫酸铝的方法。
2. 掌握沉淀与溶液分离的几种操作方法。
3. 进行废物利用。 二、实验原理
2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2 ↑
2Na[Al(OH)4]+H2SO4=2Al(OH)3 ↓+Na2SO4 +2H2O 2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O 三、仪器和试剂
仪器:抽滤瓶、布氏漏斗、烧杯、蒸发皿、比色管
试剂:废铝箔H2SO4溶液NaOH
HNO3溶液Fe 标准溶液NH4SCN 溶液 四、实验步骤
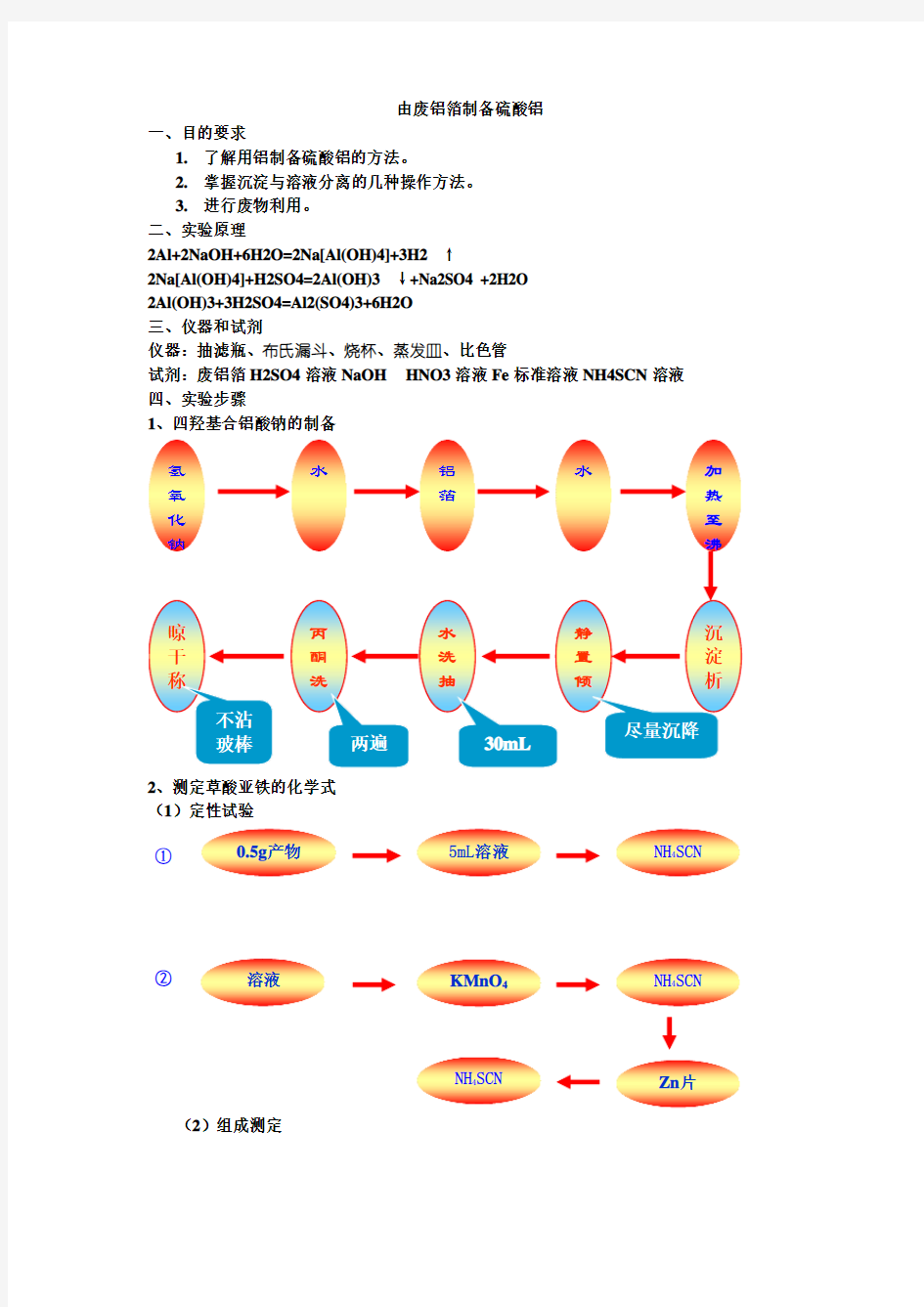
1、四羟基合铝酸钠的制备
2、测定草酸亚铁的化学式 (1)定性试验
(2)组成测定
0.5g 产物 5mL 溶液 NH 4SCN
①
溶液
KMnO 4
NH 4SCN
Zn 片
NH 4SCN
②
注意事项
在制备过程中,要不断搅拌,以免爆沸.
要用丙酮洗涤晶体.
要用电子天平称取草酸亚铁晶体.
需将溶液加热至40-50 C,然后用标准高锰酸钾溶液滴定.
五、思考题
1. 使Fe3+ 还原为Fe2+ 时,用什么作还原剂?过量的还原剂怎样除去?还原反应完成的标志是什么?
2. 用KMnO4滴定Fe2+ 时,溶液中能否带有草酸盐沉淀?
聚合硫酸铝(新型絮凝剂)
新型絮凝剂聚合硫酸铝的研究及应用 杨叶毅卢建业梁伟杰冯蔚龙广东奇力士石油化工有限公司 摘要:以硫酸铝为原料,采用中和法研制新型絮凝剂聚合硫酸铝,进行了最佳碱化剂的选择,并确定了最佳碱化度、最佳聚合反应时间及最佳PH值,并针对聚合硫酸铝稳定性相对较差的缺点,进行了聚合硫酸铝稳定剂的筛选。通过对其性能研究表明,聚合硫酸铝在无论在絮凝性能上还是在投加量上都比传统的硫酸铝有更大的优越性,并且具有更宽广的对原水PH值的使用范围。同时,在相同条件下,聚合硫酸铝的除浊效果明显优于硫酸铝,比聚合氯化铝略好。 关键词:聚合硫酸铝絮凝剂水处理 1 前言 随着工业生产的发展,用水量急剧增加,工业废水也相应增加,不论饮用水、工业用水,还是废水都必须经过处理才能使用或排放。水处理方法很多,如絮凝沉淀法、生化法、离子交换法等等。但应用最广泛、成本最低的处理方法还是絮凝沉淀法。 絮凝沉淀法的关键是絮凝剂,作为水处理方面的絮凝剂主要是无机絮凝剂和有机絮凝剂,无机絮凝剂主要有铁盐和铝盐两大类[1,2]。由于有机絮凝剂可能存在的毒性,加之其价格昂贵等原因,很少在净水处理上应用[3]。铁盐絮凝剂,其絮凝效果不错,但由于铁离子对饮用水及各种工业用水有着不良影响及其使用时对设备的强烈腐蚀性,在水处理上没有得到广泛应用[4]。在水处理方面,应用最广泛的还是铝盐絮凝剂,它主要有硫酸铝、聚合氯化铝等,但随着水处理工业的发展,对它们提出了更高的要求,为改善铝盐的絮凝效果和减少铝盐药剂的投加量,我们进行了聚合硫酸铝絮凝剂的研究。聚合硫酸铝絮凝剂在国外已有报道,但在国内,这方面的工作还相对较落后,因此积极研究和开发聚合硫酸铝絮凝剂具有重要的现实意义。 2 基本原理 2.1 以氢氧化钙为碱化剂 反应方程式为: nAl2(SO4)3·14H2O+(n×m/2)Ca(OH)2+xH2O 磷酸 [Al2(OH)m(SO4)3-m/2]n+( n×m/2)CaSO4↓
福州市高考理综-化学模拟考试试卷(I)卷(模拟)
福州市高考理综-化学模拟考试试卷(I)卷 姓名:________ 班级:________ 成绩:________ 一、单选题 (共7题;共14分) 1. (2分) (2019高一上·温州期中) 下列分散系中,能产生“丁达尔效应”的是() A . 食盐水 B . 豆浆 C . 石灰乳 D . 硫酸铜溶液 2. (2分) (2016高一下·淮安期中) 设 NA为阿伏加德罗常数,下列说法中错误的是() A . 在标准状况下,22.4LSO3所含的硫原子数目为NA B . 常温常压下,7.8g过氧化钠含有的离子数为0.3NA C . 18 g 水所含的电子数目为10 NA D . 3.2g O2、O3混合物中所含氧原子一定是0.2NA 3. (2分)下列化学用语的书写,正确的是() A . 氮气的电子式: B . 次氯酸的化学式:HClO C . 溴化钠的电子式: D . 乙烷的结构式:C2H6 4. (2分)高铁酸钾(K2FeO4)具有强氧化性,是一种新型多功能水处理剂,其生产工艺流程如下:
已知:K2FeO4在水溶液中易发生反应:4FeO42﹣+10H2O?4Fe(OH)3+8OH﹣+3O2↑,下列说法不正确的是() A . 步骤③中氧化剂与还原剂的物质的量之比为3:2 B . 步骤④中Na2FeO4转变为湿产品是因为K2FeO4溶解度更小 C . 步骤⑤中的洗涤剂可用CH3COOK和异丙醇来配制 D . 配制90%Fe(NO3)3溶液必需的玻璃仪器有容量瓶、烧杯、量筒、玻璃棒 5. (2分) (2016高二上·上饶期末) 一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2﹣.下列对该燃料电池说法不正确的是() A . 在熔融电解质中,O2﹣移向负极 B . 电池的总反应是:2C4H10+13O2=8CO2+10H2O C . 通入空气的一极是正极,电极反应为:O2+4e﹣=2O2﹣ D . 通入丁烷的一极是正极,电极反应为:C4H10+26e﹣+13O2﹣=4CO2↑+5H2O 6. (2分) (2018高三上·烟台期末) 短周期主族元素W、X、Y、Z的原子序数依次增加。K、L、M、N均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是固体,乙是气体,K是主要的大气污染物之一,0.05mol·L-1丙溶液的pH为1,上述物质的转化关系如下图所示。下列说法正确的是() A . 原子半径:W 我国硫酸铝生产技术及发展趋势 摘要:综述了硫酸铝生产技术、除铁技术及节能技术,指出开发新技术、新工艺、新材料,并使其工业化,是硫酸铝行业今后的研究和发展方向。 关键词:硫酸铝生产技术除铁节能 硫酸铝是无机盐基本品种之一,主要用于造纸和净水工业,就其生产规模而言,在我国仅次于芒硝、硅酸钠居于第三位。鉴于硫酸铝生产工艺成熟定型,有关该方面的报道近年来不多,在此仅将硫酸铝的生产方法及最新进展作以简要论述。 一、硫酸铝生产技术 目前工业硫酸铝产品按性状一般分为液体硫酸铝和固体硫酸铝,生产工艺也按此分类。 1.液体硫酸铝的生产工艺简介 液体硫酸铝的生产工艺主要有两种:氢氧化铝法和铝土矿酸浸取法。 氢氧化铝法[1]:氢氧化铝和硫酸在加热条件下反应即得到液体硫酸铝。该方法生产过程简单,不需要高温高压等苛刻条件和沉降、除铁等过程,相对能耗较低,而且生产的液体硫酸铝品质纯净,性能优良。缺点是成本高,价格贵。 铝土矿酸浸取法[2]:铝土矿生产液体硫酸铝的过程相对较复杂,首先需要将铝土矿粉碎到合适的粒度,在压力反应釜中和工业硫酸在加压、加热的条件下,经过几个小时的酸解,使铝土矿中的铝转移到酸解液中,生成硫酸铝溶液,进而生产出硫酸铝产品。铝土矿法生产的硫酸铝产品杂质含量较高,但是原料易得,虽然增加了许多工序,成本仍然较低,因此较便宜。 2..固体硫酸铝的生产工艺简介 2.1 铝矾土硫酸常压浸取Dorr法(常压反应法)[3] 常压浸取Dorr法硫酸铝生产流程为将铝土矿磨细至80%过200目,送入料仓,将98%的硫酸打入高位槽,二者以化学计量首先连续进入1号反应器。1号反应器,2号反应器,3号反应器串连,内衬铅并用蒸汽加热。在近沸点温度下反应,并以此进入2号反应器,3号反应器,使反应趋于完全。由反应器中出来的混合物送入几个串联逆流操作的增稠器中,除去不溶残渣,同时得到充分洗涤,澄清后的硫酸铝液进出蒸发器进行浓缩,然后冷却结晶。 2.2铝土矿硫酸加压反应法[1] 陕西省高二上学期期中化学试卷(理科)D卷 姓名:________ 班级:________ 成绩:________ 一、选择题 (共16题;共32分) 1. (2分) (2019高一上·广东月考) 下列实验操作中叙述正确的是() A . 可用量筒量取7.50 mL NaOH溶液 B . 分液时,应从分液漏斗下口依次放出下层液体和上层液体 C . 容量瓶用蒸馏水洗涤后不烘干就使用 D . 为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行 2. (2分)(2017·嘉兴模拟) 下列说法正确的是() A . 煤、石油、沼气属于人类利用的主要化石燃料 B . 煤干馏是复杂的物理化学变化,可得到焦炭、煤焦油和焦炉煤气等 C . 氢气是一种清洁能源 D . 需要加热才能发生的反应一定是吸热反应 3. (2分) (2016高二下·攀枝花期中) 已知C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 ,某有机物的结构简式如下:Na、NaOH、NaHCO3分别与等物质的量的该物质恰好反应时,Na、NaOH、NaHCO3的物质的量之比为() A . 3:3:2 B . 3:2:1 C . 1:1:1 D . 3:2:2 4. (2分)(2020·江苏模拟) 反应CH3CH2CH2OH CH3CH=CH2↑+H2O可用于制备丙烯。下列表示反应中相关微粒的化学用语正确的是() A . 中子数为10的氧原子: B . 硫原子的结构示意图: C . 聚丙烯的结构简式: D . H2O的电子式: 5. (2分) (2015高二上·宁波开学考) 下列除去杂质(括号的物质为杂质)的方法中,错误的是() A . FeCl3溶液(FeCl2):通入适量Cl2 B . CO(CO2):通过NaOH溶液洗气后干燥 C . MnO2(KCl):加水溶解后过滤、洗涤、烘干 D . SO2(HCl):通过饱和Na2CO3溶液洗气后干燥 6. (2分) NA 代表阿伏加德罗常数的值.下列说法正确的是() A . C2H4 和C3H6的混合物的质量为a g,所含碳氢键数目为 B . 标准状况下,2.24 L 2H35Cl 中所含中子数为1.8NA C . 50 mL 12 mol?L﹣1 盐酸与足量MnO2 共热,转移的电子数为0.3NA D . 1 L O.lmol?L﹣1的NaHCO3 溶液中HCO3﹣和CO32﹣的离子数之和为0.1NA 7. (2分)(2017·银川模拟) 下列关于有机化合物的说法正确的是() A . 的名称为2﹣甲基﹣1﹣丙醇 B . 氯乙烯和聚乙烯均能发生加成反应 C . C3H2Cl6 有4种同分异构体 硫酸生产酸洗废酸减排及降低硫酸铝生产成本的实现 发表时间:2016-11-08T14:48:58.497Z 来源:《低碳地产》2016年7月第14期作者:廖波 [导读] 随着社会经济和科学技术的快速发展,节能减排、清洁生产是企业稳定快速发展的根本之路。 广东广业云硫矿业有限公司广东云浮 527300 【摘要】随着社会经济和科学技术的快速发展,节能减排、清洁生产是企业稳定快速发展的根本之路。文章介绍了一种硫酸铝的清洁生产技术方案,不仅可以稳定生产出合格的硫酸铝产品,并且实现了硫酸生产酸洗废酸的减排,降低了硫酸铝的生产成本,总体上基本实现节能减排、清洁生产,获得了较好的经济效益和社会效益,可为硫酸铝行业今后发展提出参考。 【关键词】无机盐;硫酸铝;酸洗废酸;生产工艺;清洁型生产 硫酸铝是无机盐基本品种之一,主要用于造纸及净水工业 ,就其生产规模而言 ,在我国仅次于芒硝、硅酸钠而居第三位。特别是近年来,随着改革开放的深入发展和市场竞争的优胜劣汰 ,我国硫酸铝产业有了长足的发展,全国硫酸铝行业出现了发展迅速、生产水平提高、技改成果显著等可喜局面,基本满足我国相关工业部门发展的需要。为响应国家节能环保号召,促进企业的健康可持续发展,有必要加大对硫酸铝生产技术的研究,促其生产清洁化。 1 实验过程 1.1 主要原料 硫酸铝生产原料:铝土矿,酸洗废酸,成品工业硫酸。其中,铝土矿:外购,其中Al2O3的质量分数均不小于45%;硫酸:本公司产品,工业品(质量分数为93%)。 在实际生产中,先将来自硫酸车间逐级沉降后的稀酸加入到调浆罐中,之后将调浆罐中的浆液与成品硫酸一起加入到反应釜中进行反应。对原料的各种要求见表1,对稀酸的要求见表2。 1.2 仪器及设备 雷蒙机(4R-3216型),某重工机器制造有限公司提供;反应工序反应釜(有效容积为6m3),博山压力容器厂提供;沉降工序沉降槽(有效容积为12.5m3),公司自制;蒸发器(单效盘管式,面积为50m2,容积为12m3),公司自制;钢带结晶机(总长为25m,宽度为1m,有效冷却面积为22m2);BMJ100/1000-400板框压滤机(过滤面积为82m2,压力≤14MPa),某化工机械厂提供;稀酸沉降池(5m×5m×4m),公司自制;耐腐耐磨砂浆泵(65UHB-ZK-30-50,流量为30m3,扬程为50m),某泵业有限公司提供;稀酸储液槽(Φ3m×3m),公司自制。 1.3 制备工艺 硫酸铝的制备工艺流程如图1所示。来自硫酸车间净化岗位的稀酸经稀酸循环泵打入稀酸沉淀池,经3次沉淀后,用稀酸泵打入板框压滤岗位,用板框压滤机将稀酸挤压过滤后,送至硫酸铝车间稀酸贮槽,然后进入调浆罐与计量后的铝土矿粉混合,进行调浆。合格的矿粉浆液用泵送入反应釜中,与质量分数为93%的硫酸在压力为(0.31±0.02)MPa的条件下反应,生成硫酸铝浆液。反应生成的混合浆液,用蒸汽压入干扰式重力沉降槽中稀释,加入絮凝剂,促使残渣沉降分离。清液(即头遍溶液)经自由管放入中和槽,用硫酸中和成合格的溶液,送入蒸发工序。残渣倒槽后经3次逆流增浓洗涤后用泥浆泵送入渣池。 合格的清液经常压单效排管(或盘管)式蒸发器浓缩到铝含量大于15.60%(质量分数),放入浓缩液贮槽,供钢带结晶机冷凝结晶。冷凝结晶的片状硫酸铝,经锤式粉碎机粉碎至合格粒度,用斗式提升机提至料仓进行计量包装,码垛后入库。 2 结果与讨论 2.1 矿渣洗涤次数 该公司采用的铝土矿溶出率较高,其氧化铝的质量分数均超过45%。在处理过程中,沉降矿渣用水洗涤的次数影响了铝元素的溶出率,如表3所示。将沉降矿渣用水反复洗涤4次,以充分回收硫酸浸出的硫酸铝,提高了铝土矿中铝的利用率。 硫酸铝钠的制备 目录 摘要 Abstract 第一章文献综述 1.1硫酸铝钠的简介 1.2硫酸铝钠的用途 1.3硫酸铝钠的生产方法 1.4硫酸铝钠的制备 1.4.1制备方法 1.4.2工艺条件 1.5 硫酸铝钠的产品分析 第二章实验部分 2.1实验药品与仪器 2.1.1药品 2.1.2仪器 2.2实验方法及步骤 2.2.1试验方法 2.2.2实验步骤 2.3数据结果处理与分析 2.3.1数据结果处理 2.3.2数据结果分析 2.3.2.1温度的选择 2.3.2.2 原料硫酸铝与硫酸钠摩尔比的影响 2.3.2.3溶液浓缩度的影响 第三章结论参考文献 致谢 摘要 以硫酸铝和硫酸钠为原料制备净水剂硫酸铝钠,考察了温度、原料硫酸钠与硫酸铝的摩尔比以及溶液浓缩度对制备硫酸铝钠的影响。结果表明,硫酸铝钠在温度80~90℃,原料硫酸铝与硫酸钠摩尔比1:1~1:1.1,反应时间45~60min时,产品色泽良好。 关键词:硫酸铝硫酸钠硫酸铝钠 Abstract Alumina and sodium sulfate as raw material to the sparsity of alumina preparation sodium, a visit to the raw materials of alumina and sodium temperature and solution concentration degree the mole ratio of alumina preparation sodium results show that, the effect of sodium in temperature of 80 ~ of alumina, the raw material with sodium 90 aluminium mole ratio of 1:1 ~ 1:1. 1, and the reaction time 45 to 60 min, good color products. 实验十七聚合硫酸铝的制备及性能测定 一、实验目的: 1、学习聚合硫酸铁的制备及净化水的知识; 2、学习和了解絮凝沉降法处理工业废水的有关知识; 3、掌握含锌废水浮选处理技术; 4、巩固分光光度法和原子吸收法测定方法。 二、实验原理 聚合硫酸铁是一种铁系无机高分子混凝剂,与硫酸亚铁、三氯化铁、硫酸铝以及碱式氯化铝等相比,具有无毒、适用pH 范围广、矾花大、沉降快等优点,对COD、色度以及重金属离子等都有较好的去除效果,因此,被广泛地应用于给排水工业和废水处理等行业。 生产聚合硫酸铁的原料来源很多,如硫酸亚铁、钢铁酸洗废液、铁泥和铁矿石等,其中以硫酸亚铁为原料的生产工艺简单,条件温和,成品杂质少,品质高。本实验以钛白粉厂的副产品硫酸亚铁为原料,在常温常压下采用双氧水直接氧化法合成聚合硫酸铁。 按照氧化方式的不同,聚合硫酸铁的生产方法可分为直接氧化法和催化氧化法两大类。直接氧化法是直接通过强氧化剂(如NaClO、KClO3、H2O2等) 将亚铁离子氧化为铁离子,经水解和聚合获得聚合硫酸铁; 催化氧化法是在催化剂( 如NaNO2、HNO3等) 的作用下,利用空气或氧气将亚铁离子氧化为铁离子,经水解和聚合获得聚合硫酸铁。催化氧化法一般以空气为氧化剂,生产成本相对较低,在实际生产中应用较广,但需在较高的温度(80 ℃) 和反应压力(0. 3 MPa) 下进行,反应时间较长(NaNO2法为17 h ,HNO3法为5 h) ,需要安装废气净化装置,以脱去反应过程中产生的大量氮氧化物气体,工艺流程复杂,对设备要求较高,投资较大。 二价铁被双氧水氧化形成三价铁离子。在一定pH下,铁离子水解生成聚合硫酸铁,当稀释时进一步发生水解,形成Fe(OH)3 胶体,通过沉淀、吸附、絮凝等作用,使水相中的悬浮物、染料、Zn2+被转入固相。固相的物质可通过过滤或上浮法除去。 Fe(H2O)33++OH- →Fe(OH)3↓+3H++H2O Zn2++OH- →Zn(OH)2↓ 再通过浮上法,将氢氧化铁胶体浮上,使水中锌除去。 三、试剂与仪器 试剂:硫酸亚铁、硫酸、双氧水、酞青蓝或酞青绿、松节油。 标准锌溶液:称取 0.4399g(保证试剂)ZnSO 4?7H 2 O溶于水中,并稀释到1升, 此溶液为1.00μg/ml 的锌。 1.0%十二烷基硫酸钠。 1.0%油酸钠。 其它:1.0%NaOH、1%Fe 2(SO 4 ) 3 溶液。 仪器:78HW-1恒温加热磁力搅拌器、锥形瓶(250ml,6个)、容量瓶(100ml)、722型可见光分光光度计、移液管。 四、实验步骤与现象: 1、聚合硫酸铁的制备 称取10.99g磨细后的硫酸亚铁于250 mL 锥形瓶中,加水25 mL,此时溶液 呈现蓝绿色,浓硫酸0.64 mL ,开启搅拌器,用滴管缓慢加入H 2O 2 2.7mL(用滴管 加入),每隔三秒加一滴。加完后,溶液呈现深褐色静置,冷却,即得聚合硫酸铁成品溶液。 2、产品的性能检测(去浊率测定) 取200 mL 高浊度原水样(6份),其中五份加入1∶100 稀释后的聚合硫酸铁5 mL ,剧烈搅拌3min ,慢速搅拌10min,然后静置相同长的时间后取上层清液(液面以下2~3cm 处) ,测定其在420nm的吸光度,比较处理前后之吸光度,则得到去浊率。用不同用量的聚合硫酸铁进行实验,测水样的吸光度,得去浊率。作用量与去浊率的关系图,找出最佳用量。 江苏省2020-2021版高三上学期化学开学考试试卷 姓名:________ 班级:________ 成绩:________ 一、单选题 (共21题;共42分) 1. (2分)下列物质中属于天然高分子化合物的是() A . 纤维素 B . 蔗糖 C . 油脂 D . 聚乙烯 2. (2分)石油的减压分馏可以获得() A . 石油气 B . 汽油 C . 乙烯、丙烯、丁二烯 D . 重柴油 3. (2分) (2015高一上·海南期末) 在某无色透明的酸性溶液中,能大量共存的离子组是() A . Na+、K+、SO42﹣、HCO3﹣ B . Na+、K+、Cl、SO42﹣ C . Cu2+、K+、SO42﹣、NO3﹣ D . Fe2+、K+、NO3﹣、Cl 4. (2分)用NA表示阿伏加德罗常数的值,下列叙述中正确的是() A . 0.1mol·L-1稀硫酸中含有SO42-离子个数为0.1NA B . 电解饱和食盐水,当阳极产生2.24L的氢气时,转移的电子数为0.2 NA C . 常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA D . 标准状况下,22.4LSO3所含的分子数为NA 5. (2分) (2018高二上·常州期末) 下列物质既含离子键又含共价键的是() A . CaCl2 B . H2O2 C . MgF2 D . NH4Cl 6. (2分) (2016高一下·沙市月考) 136C﹣NMR(核磁共振)可用于含碳化合物的结构分析,136C表示的含义正确的是() A . 质量数是13,原子序数是6,核内有6个中子 B . 与金刚石、石墨、C60等互为同素异形体 C . 碳元素的相对原子质量为13 D . 碳的一种核素,与126C互为同位素 7. (2分) (2017高一上·咸阳期末) 下列试剂能贮存在磨口玻璃塞的试剂瓶里的是() A . HF溶液 B . KOH溶液 C . 盐酸 D . 水玻璃 8. (2分) (2017高一上·浦东期末) 分析如图的能量变化示意图,确定下列选项中正确的是() 明矾的制备、组分含量测定及其晶体的培养 一. 实验目的 1. 熟练掌握无机物的提取、提纯、制备、分析等方法的操作及方案设计。 2. 学习设计综合利用废旧物的化学方法。 3. 学习从溶液中培养晶体的原理和方法。 4. 自行设计鉴定产品的组成、纯度和产率的方法,并鉴定之。 仪器和试剂 (1)仪器:100cm3烧杯,布氏漏斗,抽滤瓶,表面皿,玻璃棒,试管,电子天平,容量瓶(250 mL、100mL),移液管,锥形瓶(两个),烘箱。 (2)试剂废铝(易拉罐),NH3 · H2O(6mol·dm-3),H2SO4(9mol·dm -3),KAl(SO4)2·12H2O 晶种,EDTA溶液(0.02599mol·L-1),二甲酚橙(XO,2g·L-1)水溶液,HCl(6mol·L-1,3mol·L-1),NH3·H2O(1+1),六次甲基四胺溶液(200g·L-1),Zn2+(0.02581 mol·L-1);NH4F溶液:200 g·L-1,贮于塑料瓶中; KOH溶液:1.5mol/L 取8.416g KOH定容于100ml容量瓶中; 氯化钡溶液:0.25g/mL ,取25.45克氯化钡溶于100mL蒸馏水中; 硫酸根标准贮备溶液:550u g/mL,准确称取1.3522g已烘干的基准硫酸钾定容于100mL容量瓶中。 二. 实验提要 目前使用的铝制品的包装和用具较多,因此废旧饮料罐、盒,铝质导线等废 铝很多,设计简便的方法由铝制的易拉罐制备明矾(KAl(SO 4) 2 ·12H 2 O),并培 养明矾的单晶,计算产率和鉴定产品的质量。 1、实验原理 (1)明矾的制备 将铝溶于稀氢氧化钾溶液制得偏铝酸钾: 2Al+2KOH+2H2O=2KAlO2+3H2 往偏铝酸钾溶液中加入一定量的硫酸,能生成溶解度较小的复盐KAl(SO4)2·12H2O] 反应式为: KAlO2+2H2SO4+10H2O=KAl(SO4)2.12H2O 不同温度下明矾、硫酸铝、硫酸钾的溶解度(100gH2O 中)如下表所示:温度T/K 物质种类273 283 293 303 313 333 353 363 KAl(SO4)2·12H2O/g 3.00 3.99 5.90 8.39 11.7 24.8 71.0 109 Al2(SO4)3 /g 31.2 33.5 36.4 40.4 45.8 59.2 73.0 80.8 K2SO4/g 7.4 9.3 11.1 13.0 14.8 18.2 21.4 22.9 单晶的培养 要使晶体从溶液中析出,从原理上来说有两 种方法。以图1的溶解度曲线的过溶解度曲线 为例,为溶解度曲线,在曲线的下方为不 饱和区域。若从处于不饱和区域的 A 点状态的 溶液出发,要使晶体析出,其中一种方法是采 用的过程,即保持浓度一定,降低温 废铝箔之硫酸铝钾大晶体及碱式碳酸铜制 备 实验题目:由废铝箔制备硫酸铝钾大晶体 一、实验目的 1、巩固对铝和氢氧化铝两性的认识,掌握复盐晶体的制备方法; 2、了解从水溶液中培养大晶体的方法,制备硫酸铝钾大晶体。 3、掌握沉淀与溶液分离的几种操作方法。 二、实验原理 1、明矾的性状 明矾又称白矾、钾矾、钾铝矾、钾明矾、十二水硫酸铝钾。是含有结晶水的硫酸钾和硫酸铝的复盐。化学式KAl(SO4)2·12H2O,式量474.39,正八面体晶形,有玻璃光泽,密度1.757g/cm3,熔点92.5℃。64.5℃时失去9分子结晶水,200℃时失去12分子结晶水,溶于水,不溶于乙醇。在20度,1个标准大气压下,明矾在水中的溶解度约为5.90g。 表1 溶解度的参照表 2、明矾晶体的实验制备原理 铝屑溶于浓氢氧化钾溶液,可生成可溶性的四羟基合铝(Ⅲ)酸钾K[Al(OH)4],用稀H 2SO 4调节溶液的pH 值,将其转化为氢氧化铝,使氢氧化铝溶于硫酸,溶液浓缩后经冷却有较小的同晶复盐,此复盐称为明矾 [KAl(SO 4)2·12H 2O ]。小晶体经过数天的培养,明矾则以大块晶体结晶出来。制备中的化学反应如下: 2Al + 2KOH + 6H 2O ══ 2K[Al(OH)4] + 3H 2↑ 2 K[Al(OH)4] + H 2SO 4 ══ 2Al(OH)3↓+ K 2SO 4 + 2H 2O 2Al(OH)3 + 3H 2SO 4 ══ Al 2(SO 4)3 + 6 H 2O Al 2 (SO 4)3 + K 2SO 4 + 24H 2O ══2KAl(SO 4)2·12H 2O 三、实验步骤 1、工艺流程图 废铝→溶解→过滤→酸化→浓缩→结晶→过滤 单晶培养→明矾单晶 2、明矾晶体的实验制备 取50mL2mol·L -1 KOH 溶液,分多次加入2g 废铝制品(铝质牙膏壳、铝合金易拉罐等),反应完毕后用布氏漏斗抽滤,取清液稀释到l00mL ,在不断搅拌下,滴加3 mol·L -1 H 2SO 4溶液,调ph6-7(按化学反应式计量,约41mL)。加热至沉淀完全溶解,并按计量数加入 ,适当浓缩溶液,然后用自来水冷却结晶,抽滤,所得晶体即为KAl(SO 4)2·12H 2O 。 3、明矾透明单晶的培养 KAl(SO 4)2·12H 2O 为正八面体晶形。为获得棱角完整、透明的单晶,应让籽晶(晶种)有足够的时间长大,而晶籽能够成长的前提是溶液的浓度处于适当 KOH ↘ H 2SO 4 ↘ K 2SO 4 ↘ K 2SO 年产万吨硫酸铝车间工艺设计设计 年产1万吨硫酸铝车间工艺设计 摘要 我国硫酸铝的生产现状,年产量万吨以上的企业已达29个,3000t至10000t的企业达85个。全国硫酸铝生产能力已达115万t,产量突破95万t,仅次于美国和日本,而居世界第三位[1];硫酸铝生产中存在的问题是,设计不合理,设备不配套,产量质量都无法达到初衷要求以及部分生产厂家规模较小,经济效益差导致产品积压严重、投资无法收回,使部分企业背上沉重的经济包袱;生产工艺主要有铝灰、铝渣法、活性氢氧化铝法、铝矾土常压法、煤矸石加压法等,对各个工艺的优缺点进行对比,发现以高岭土为原料生产硫酸铝,具有原料成本低,产量高,产品质量好,过程易控制等优点,制备过程中产生的废渣可作为高活性的高硅材料,也可作为优良的涂料及板材制品填料,从而实现了综合利用和无废渣排放,具有积极的环保意义;采用高岭土为原料生产硫酸铝,符合设计的目的和指导思想。 高岭土生产硫酸铝,使高岭土经过预处理过程,排除高岭土中的粗石英砂、杂质,用于生产水泥玻璃,得到高岭土精矿,经过煅烧活化,粉碎,过筛送致生产车间,与55%的硫酸容易混合送至反应釜,经过反应的酸浸,沉降,分离和中和处理,得到合格的硫酸铝容易,送至浓缩结晶槽中,进行浓缩结晶,并通过成品粉碎机将硫酸铝晶体粉碎,包装。 关键词:硫酸铝;现状;生产工艺;高岭土 Abstract The plants having 10,000 tons of annual output of aluminum sulfate in China hav being upto 29, and the plants having 3000 t to 10000 t, being upto 85. The aluminum sulfate production capacity has reached 1.15 million t, yield breakthroughs 950,000 t, after the United States and Japan, the third in the world live;Aluminum sulfate production in the problem is that the unreasonable design, equipment is not supporting, yield and quality are unable to meet its mind and requested some smaller manufacturers, leading to poor economic returns serious backlog of products, investment is not possible, so that some enterprises back heavy The economic burden of production of a major Al Grey, Al Jardine, of aluminum hydroxide, bauxite atmospheric pressure, such as coal gangue compression method, all of the advantages and disadvantages compared to that of raw materials for the production of kaolin Aluminum sulfate, a low-cost raw materials, high yield, good quality products, process-control advantages, in the course of preparation of the high-activity waste residue can be used as the high-silicon material, but also as a fine of paint and sheet metal products fill, so as to achieve a comprehensive Use and no waste residue emissions, have a positive environmental significance of raw materials used for the production of kaolin aluminum sulfate, with the design of purpose and guiding ideology. Kaolin production of aluminum sulfate, kaolin After pretreatment process, rule out the possibility of kaolin in the rough quartz sand, impurities, the glass used in the production of cement, by Kaolin concentrate, after calcination activated, crushing, screening sent to the production workshop, with 55 percent of the sulfuric acid Mixed 硫酸铝的生产现状及应用前景 摘要硫酸铝是近几年山东铝业公司开发的一个产品品种,属于化学品氧化铝的范畴,硫酸铝广泛应用于国民经济各个领域,本文通过研究硫酸铝的主要特性以及硫酸铝的主要应用领域,讨论了硫酸铝的主要应用趋势,并提出了铝盐发展的建议。 关键词硫酸铝碱式聚氯化铝氢氧化铝碳分母液碳分分解率浆内施胶剂水处理ASA AKD 前言: 山东铝业公司自2001年开始生产硫酸铝产品,经过氧化铝厂服务公司作了大量的前期准备工作,试生产成功,并在山东省市场具有了一定的占有率。2003年3月正式成立氧化铝厂铝盐车间,使用质量较差的废品氢氧化铝生产硫酸铝,2004年由氧化铝厂出资对生产线进行了扩产改造,新上生产线一条,达到了万吨生产规模,2004年共生产硫酸铝产品1.3万t,全国估计总产量在300万t以上,普通型的产品在全国范围内基本上是处于供大于求的现状,低铁和高氧化铝含量的产品市场形势较好。2005年6月开始利用氧化铝厂正品白色氢铝生产低铁产品,并推向国内市场。 1.硫酸铝的产品性能及用途 1.1分子式: AL2(SO4)3xH2O 分子量342.15(无水) 1.2性能: 硫酸铝为白色结晶体,比重为1.69,在空气中长期存放易吸潮结块。易溶于水,水溶液成酸性,难容于醇。过保和溶液在常温下结晶为无色单斜晶体13水和物(理论是18水合物,经过生产实践及化验分析确定为13水合物),8.8℃下结晶为27水合物。在86.5℃ 下到250℃失去结晶水。无水硫酸铝加热到300℃开始分解,860℃时分解为γ-AL2O3、SO3、SO2等。 1.3用途: 主要用作造纸施胶剂和饮用水、工业用水及废水处理的絮凝剂,还用于生产人造宝石和其他铝盐,氨明矾,钾明矾,精制硫酸铝的原料。另外,还广泛用作优质澄清剂,石油除臭脱色剂、混凝土防水剂和防雨布原料,高级纸张锻白,钛白粉后薄膜处理和催化剂载体的生产。 1.4化学方程式: 2AL(OH)3+3H2SO4+nH2O=AL2(SO4)3.xH2O+Q 1.5工艺流程图: 反应釜 粉碎 包装 冷却结晶 熟化 蒸汽 成品入库 创作编号: GB8878185555334563BT9125XW 创作者:凤呜大王* 实验题目:由废铝箔制备硫酸铝钾大晶体 一、实验目的 1、巩固对铝和氢氧化铝两性的认识,掌握复盐晶体的制备方法; 2、了解从水溶液中培养大晶体的方法,制备硫酸铝钾大晶体。 3、掌握沉淀与溶液分离的几种操作方法。 二、实验原理 1、明矾的性状 明矾又称白矾、钾矾、钾铝矾、钾明矾、十二水硫酸铝钾。是含有结晶水的硫酸钾和硫酸铝的复盐。化学式KAl(SO4)2·12H2O,式量474.39,正八面体晶形,有玻璃光泽,密度1.757g/cm3,熔点92.5℃。64.5℃时失去9分子结晶水,200℃时失去12分子结晶水,溶于水,不溶于乙醇。在20度,1个标准大气压下,明矾在水中的溶解度约为5.90g。 表1 溶解度的参照表 O 0 0 作编号:GB8878185555334563BT9125XW 作者: 凤呜大王* 154.0 2、明矾晶体的实验制备原理 铝屑溶于浓氢氧化钾溶液,可生成可溶性的四羟基合铝(Ⅲ)酸钾K[Al(OH)4],用稀H 2SO 4调节溶液的pH 值,将其转化为氢氧化铝,使氢氧化铝溶于硫酸,溶液浓缩后经冷却有较小的同晶复盐,此复盐称为明矾[KAl(SO 4)2·12H 2O ]。小晶体经过数天的培养,明矾则以大块晶体结晶出来。制备中的化学反应如下: 2Al + 2KOH + 6H 2O ══ 2K[Al(OH)4] + 3H 2↑ 2 K[Al(OH)4] + H 2SO 4 ══ 2Al(OH)3↓+ K 2SO 4 + 2H 2O 2Al(OH)3 + 3H 2SO 4 ══ Al 2(SO 4)3 + 6 H 2O Al 2 (SO 4)3 + K 2SO 4 + 24H 2O ══2KAl(SO 4)2·12H 2O 三、实验步骤 1、工艺流程图 废铝→溶解→过滤→酸化→浓缩→结晶→过滤单晶培养→明矾单 晶 KOH ↘ H 2SO 4 ↘ K 2SO 4 ↘ 安徽建筑工业学院 大作业 题目:年产10万吨硫酸铝工艺设计学院:材料与化学工程学院 专业:08化学工程与工艺 姓名:李小磊 学号:08206040213 指导教师:葛业军 完成日期:2011年3月25号 目录 摘要 (3) 前言 (3) 1 设计概述 (3) 1.1设计的目的和意义 (3) 1.2 生产能力 (3) 1.3 设计指导思想 (3) 1.4 设计原则 (4) 1.5 设计重点 (4) 2.生产工艺的选择 (4) 2.1原料 (4) 2.2生产工艺:高岭土常压反应法 (4) 3. 工艺计算 (6) 3.1生产流程 (6) 3.1.1工艺流程方块图 (7) 3.1.2预处理 (7) 3.2物料衡算 (7) 3.2.1设计生产能力 (7) 3.2.2原料组成 (7) 3.2.3酸浸段 (8) 3.2.4加热浓缩段 (8) 3.3 能量衡算 (9) 3.3.1吸热 (9) 3.3.2放热 (9) 4.三废处理及副产品的综合利用 (10) 5. 总结 (10) 参考文献 (11) 摘要 我国硫酸铝的生产现状,年产量万吨以上的企业已达29个,3000t至10000t 的企业达85个。全国硫酸铝生产能力已达115万t,产量突破95万t,仅次于美国和日本,而居世界第三位[1]以高岭土为原料生产硫酸铝,具有原料成本低,产量高,产品质量好,过程易控制等优点,制备过程中产生的废渣可作为高活性的高硅材料,也可作为优良的涂料及板材制品填料,从而实现了综合利用和无废渣排放,具有积极的环保意义;采用高岭土为原料生产硫酸铝,符合设计的目的和指导思想。 关键词:硫酸铝;生产工艺;高岭土 前言 硫酸铝化学名(Aluminium sulfate)Al2(SO4)3,无色单斜结晶,在空气中长期存放易吸潮结块。易溶于水,水溶液显酸性,难溶于醇,是无机盐基本品种之一,应用十分广泛。加热至770度是开始分解为氧化铝、三氧化铝、二氧化铝、二氧化硫和水蒸气。水解后生成氢氧化铝。工业品为白色或灰白色粉立状晶体。主要用于净水与造纸[2]。在造纸工业中可作纸的填料和处理造纸工业废水。在净水方面,作为城市用水和废水处理的絮凝剂,可以除去水中的磷酸盐、锌、铬等杂质,以及除菌、控制水的颜色和气味。硫酸铝还可以用来生产其他铝盐、硫酸铝衍生物,无机高分子絮凝剂及铵明矾、钾明矾等。 本设计以高岭土为原料,拟设计一套年产10万吨硫酸铝的生产车间。 1.设计概述 1.1设计的目的和意义 通过具体的年产10万吨硫酸铝的工艺设计,我们可以很大程度上将在大学中所学的基础化学以及化工专业基础课程应用到实践中。这样不仅对我们的理论知识是一次深化,更能陪样我们理论联系实际, 将理论应用到实践中去的能力, 更重要的是可以通过此工艺的设计对现有硫酸铝生产工艺进行全面深入的调查研究,对比不同工艺,取各工艺技术之优点融合为一合理先进的工艺设计。通过完成本设计,基本掌握过年产10万吨硫酸铝车间的工艺流程设计、基本工艺计算等设计理论和设计技能;对通用工程设计有一个系统的了解和整体的把握,达到大学工科本科生应具备的专业设计能力。 1.2生产能力 生产能力:年产10万吨硫酸铝 原料:高岭土(含硫酸铝39.50 %)、98%硫酸 成品质量标准:GB2942-92标准 年生产日:300天(全天候) 日产硫酸铝 100000/300=333.33吨 每小时生产 333.33/8=41.666吨/小时 1.3 设计指导思想 为适应我国硫酸铝生产工业发展的需要,在硫酸铝工艺设计中巩固和应用所学的基础理 聚合硫酸铝的制备及形态特征* 秦建昌1,2 冯雪冬2,3 栾兆坤2** 马艳飞3 (1 中国科学院生态环境研究中心,环境水质学国家重点实验室,北京,100085;2 中国石化胜利油田 纯梁采油厂,东营,257000;3 山东理工大学,资源与环境工程学院,淄博,255049) 摘 要 以Al 2(SO 4)3 18H 2O 为原料,采用一次加碱法,高速剪切合成聚合硫酸铝(PAS),研究碱化度(B )对铝离子形态的影响.采用混凝实验比较AS,PAC,PAS 的混凝效果,测定处理后水中残留铝的含量.结果表明:相同B 值条件下,PAS 的Al a 少于PAC 的Al a 含量,Al b 含量与PAC 基本持平,Al c 含量大于PAC 的Al c 含量;PAS 的p H 适用范围宽,絮体沉降性能强,残留铝量低. 关键词 聚合硫酸铝,形态,混凝. 聚合硫酸铝(PAS)为铝盐类无机高分子絮凝剂(IPF)[1].目前,制备PAS 的最大问题在于产品缺乏一定的稳定性,文献所报道PAS 的制备多为聚合氯化铝(PAC)中引入适量SO 2-4,或硫酸铝(AS)中引入聚硅酸合成聚硅硫酸铝,而以阴离子SO 2- 4为主的产品所见报道不多[2]. 本文在高速剪切条件下,以一次加碱法合成不同碱化度的PAS,通过选用不同碱化剂,比较B 值、AS 浓度及乳化反应时间,确定了合成高Al b 和Al c 含量的PAS 的最佳合成条件.以Ferron 络合逐时比色法研究了PAS 的铝形态特征分布,对PAS 的混凝特性与AS 和PAC 进行了比较研究. 1 实验部分 1 1 聚合硫酸铝的制备及测定 称取一定重量硫酸铝(Al 2(SO 4)3 18H 2O)溶于去离子水中,使Al( )浓度为1 5mol l -1,测定其准确浓度后存储备用.量取一定体积的铝储备液,稀释至预定浓度,加入适当的稳定剂,在高速剪切的条件下,一次加入碱化剂,乳化15min,制取不同B 值的PAS.反应产物常温熟化一天至两天,最后转化为半透明状液体,pH 值3 0 3 8,Al 2O 3%质量分数8% 10%. Al( )浓度及B 值的测定方法参照国家标准水处理剂 降合氯化铝标准[3].Ferron 逐时络合比色法采用合加比色 缓冲溶液法[4] . 1 2 混凝实验 2003年10月18日收稿. *基金项目:国家自然科学基金资助项目(50178067).**通信联系人. 第23卷 第5期2004年 9月 环 境 化 学 ENVIRONMENTAL CHEMISTRY Vol.23,No.5 September 2004 聚合氯化铝(PA C)混凝剂研究的进展Ξ 王亚芝1,曹培锋2,任毅斌2 (1.河北省环境科学研究院;2.河北省环境工程评估中心;31石家庄市环境监测中心,河北石家庄 050021) 摘 要:本文概括和评论了PA C的基本形态、作用机理、生产工艺、产品标准和应用的研究的主要内容、取得的进展。 关键词:聚合氯化铝;水解;沉淀;絮凝 聚合氯化铝(PA C)是30年代发展起来的一种高效的无机高分子絮凝剂,60年代后期正式投入工业生产和应用,被广泛应用于上下水、循环用水、工业废水处理及污泥脱水等过程中,关于PA C的基本形态、作用机理、生产工艺、产品标准和应用的研究也活跃起来。 1 基本形态 水解PA C形态一直是分析、催化、土壤、地球化学、新材料、环境科学和生物毒理学等众多领域研究的前沿和热点。由于制备途径、反应条件和溶液化学组成等诸多因素的影响,铝水解聚合反应过程及其形态分布极其复杂,水解产物不稳定,因此现有的实验方法、仪器性能及分析和测试手段均制约了对铝水解溶液中各种形态的结构特征、相对含量及其形成机理的研究进展。现代PA C的研究已从形态学上确定了PA C中起最佳絮凝做用的铝化学状态为A l13聚合态[1]。 近年来通常采用A l-Ferron逐时络合比色法和27A l核磁共振法(NM R)进行形态的检测,其中A l -Ferron逐时络合比色法由Sm ith在1971年改进提出的逐时络合比色法,利用A l( )的各种水解聚合形态与Ferron解离——络合反应速度不同区分其相对形态,将铝的水解状态定量为A la、A l b和A lc 三种形态;27A l核磁共振法(NM R)由A k itt等在70年代后期提出的,可以定量检测出水解液中A l单质、A l13O4(OH)247+聚合物和其它不可测得的形态。汤鸿宵等研究结果表明A l-Ferron比色法所测得A lb形态的含量与A l核磁共振法(NM R)所测得A l13形态的含量十分吻合,两种方法在定量测定PA C溶液的形态分布上有很好的相关关系[2]。王东升等人采用A l-Ferron法研究了悬浮体系中PA C 的形态分布表征,结果表明混合方式对A l-Ferron 法的应用具有一定的影响作用,颗粒物的存在对反应的影响主要取决于其浓度与粒度分布,A l-Ferron法完全适用于颗粒物悬浮体系中的形态分布表征[3]。其它形态检测方法包括A llouche等采用高分辨率的原位27A l-NM R方法检测法[4]、容量滴定法[5]、透光率脉动检测法[6]。 除此之外,人们还用计算模型或模式来量化形态分布。栾兆坤应用‘M I N EQL’化学平衡模式对采用不同反应途径制得的聚合铝(PA C)溶液中的化学形态分布硅铝进行了定量模拟研究[7];卢建杭等人考察了A l-Ferron逐时络合比色反应假一级反应动力学特征,结果表明当碱铝比处于2.0~2.5之间,A l b的初始浓度和假一级速率常数随碱铝比的变化情况在一定程度上可以反映PA C溶液的形态分布和转化特征[8]。王趁义等人应用ExpA ssoc分布对A l-Ferron逐时络合动力学曲线进行了定量模拟[9],并依据A l( )盐强制水解聚合过程的电位滴定实验结果,给出了通过电位滴定实验计算PA C含量的定量公式[10]。 2 作用机理 水解后的带有正电荷的PA C在静电库仑力、分子间范德华力、憎水斥力以及羟基与表面的键合力等的作用下,吸附在水中悬浮的胶体上。PA C在颗粒物表面结合后,颗粒物所带负电荷转化为正电荷, PA C则在颗粒物表面发生进一步的水解,在高浓度、高pH条件下单核络合物缩聚为一系列多核络合物,最后形成表面无限聚合度氢氧化铝沉淀,此时的凝聚作用转化为絮凝作用为主,电中和作用转化为粘附卷扫作用为主。絮凝法处理可以分为凝聚阶段、絮凝阶段和沉降阶段。 凝聚几乎是瞬时发生的,因此絮凝剂必须以尽快的速度(<0.1s)在水解反应完成之前就分散到水 31 2009年第10期 内蒙古石油化工Ξ收稿日期:2008-12- 作者简介:王亚芝(1972-),女,硕士。我国硫酸铝生产技术及发展趋势
陕西省高二上学期期中化学试卷(理科)D卷
硫酸生产酸洗废酸减排及降低硫酸铝生产成本的实现
硫酸铝钠的制备
实验十七 聚合硫酸铝的制备及性能测定
江苏省2020-2021版高三上学期化学开学考试试卷
明矾的制备实验报告
废铝箔之硫酸铝钾大晶体及碱式碳酸铜制备培训资料
最新年产万吨硫酸铝车间工艺设计设计
我国硫酸铝发展现状
废铝箔之硫酸铝钾大晶体及碱式碳酸铜制备
化工设计:年产10万吨硫酸铝
聚合硫酸铝的制备及形态特征_秦建昌
聚合氯化铝_PAC_混凝剂研究的进展
